文章信息
- 张子川, 杨平, 仝川
- ZHANG Zichuan, YANG Ping, TONG Chuan
- 盐分对河口淡水、微咸水沼泽湿地土壤甲烷产生潜力的影响
- Effects of seawater and NaCl solution pulses on methane production potential from laboratory-incubated tidal freshwater and brackish marsh soil
- 生态学报, 2015, 35(24): 8075-8084
- Acta Ecologica Sinica, 2015, 35(24): 8075-8084
- http://dx.doi.org/10.5846/stxb201406201275
-
文章历史
- 收稿日期: 2014-06-20
- 网络出版日期: 2015-05-21
2. 福建师范大学地理科学学院, 福州 350007;
3. 福建师范大学地理研究所, 福州 350007;
4. 福建师范大学亚热带湿地研究中心, 福州 350007
2. School of Geographical Sciences, Fujian Normal University, Fuzhou 350007, China;
3. Institute of Geography, Fujian Normal University, Fuzhou 350007, China;
4. Research Centre of Wetlands in Subtropical Region, Fujian Normal University, Fuzhou 350007, China
全球变暖引起的海平面上升已成为全球变化研究的一个重要领域。政府间气候变化专业委员会(IPCC)第四次评估报告指出,20世纪全球海平面上升约0.17 m,全球沿海地区盐水入侵(saltwater intrusion)加剧[1]。海平面上升和河流淡水径流减少的综合效应导致一些河口的咸水-淡水混合区上溯,形成明显的盐水入侵,对河口潮汐淡水湿地和微咸水湿地生态系统产生潜在的、巨大的影响[2]。
潮汐湿地位于河流与海洋交汇处,受河流径流和海洋潮汐作用共同影响。潮汐湿地按照盐度可分为潮汐淡水湿地(盐度<0.5‰)、潮汐寡盐水湿地(0.5‰<盐度<5.0‰,oligohaline)、潮汐中盐水湿地(5.0‰<盐度< 18.0‰,mesohaline)和潮汐咸水湿地(18.0‰<盐度<35.0‰)[3, 4]。寡盐和中盐水潮汐湿地也被统称为微咸水(或半咸水)(brackish)湿地[5]。河口区盐度梯度下的潮汐沼泽湿地甲烷排放已有报道[6, 7]。在海平面上升、盐水入侵加剧的背景下,研究河口潮汐湿地碳、氮生物地球化学循环、温室气体产生和排放等过程显得尤为重要。近年来,盐水入侵对于河口潮汐淡水沼泽湿地碳、氮生物地球化学循环的影响,日益引起科学家的关注[8, 9, 10, 11],伴随着盐水入侵带来大量的硫酸根(SO42-)。作为一个重要的电子受体,硫酸根可使河口区潮汐淡水沼泽湿地土壤产甲烷过程向硫酸盐还原过程转变,湿地土壤甲烷产生量和排放量短期内明显减少,这一现象已被一些研究证明[8, 10]。盐水入侵同时也伴随着大量氯离子(Cl-)输入,进而存在氯离子胁迫作用(电导率增加而引发渗透势的变化)。氯离子引发的离子胁迫可通过改变土壤-水体系电导率而影响土壤微生物种群[12]。Baldwin等[13]采用小型生态系方法,向淡水湿地添加不同盐度NaCl溶液,结果显示甲烷产生速率明显减少。然而关于盐水入侵对河口潮汐淡水、微咸水沼泽湿地甲烷气体产生的影响及机制的了解仍相对较少,伴随着盐水入侵而增强的氯离子胁迫作用是否同样也对于河口区微咸水沼泽湿地甲烷的产生造成影响,还鲜见报道。本文以闽江河口区分布的潮汐淡水、微咸水短叶茳芏沼泽湿地土壤为研究对象,室内模拟海水和纯NaCl盐水入侵,以期揭示海水和NaCl盐水对河口淡水、微咸水沼泽湿地土壤甲烷产生潜力的影响,辨识伴随着海水入侵而增强的硫酸盐还原和氯离子胁迫在抑制河口淡水、微咸水沼泽湿地甲烷产生潜力方面的作用和贡献。
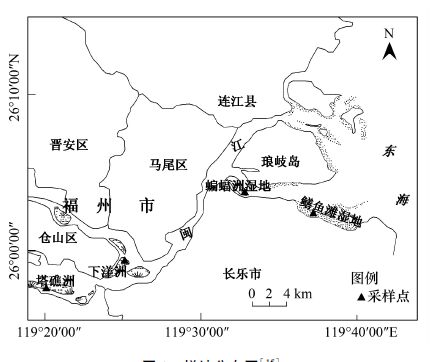
1 材料与方法 1.1 研究区和样地概况闽江河口区从河口海滨段向上游方向依次分布有鳝鱼滩湿地、蝙蝠洲湿地、下洋洲湿地和塔礁洲湿地(图 1)。鳝鱼滩湿地是闽江河口区面积最大潮汐湿地,短叶茳芏(Cyperus malaccensis Lam. var. brevifolius Bocklr.)和芦苇(Phragmites australis)是鳝鱼滩湿地主要土著优势种,其中短叶茳芏沼泽集中分布于鳝鱼滩湿地中西部,并较接近堤岸一侧,表层土壤电导率为1.68—7.65 mS/cm(2011年10月至2012年6月,下同)。蝙蝠洲湿地受潮汐影响也较大,表层土壤电导率为1.26—3.27 mS/cm,同样短叶茳芏和芦苇是其主要优势植物。下洋洲湿地位于闽江北港河道与南港交汇处,地势低平,主要分布有短叶茳芏沼泽,表层土壤电导率为0.31—0.42 mS/cm。塔礁洲湿地的地势低洼处和边缘同样分布有短叶茳芏沼泽,表层土壤电导率为0.16—0.52 mS/cm。下洋洲和塔礁洲均为典型淡水潮汐湿地,分布在鳝鱼滩湿地近堤岸侧和蝙蝠洲湿地的短叶茳芏沼泽为微咸水潮汐沼泽。闽江河口区气候暖热湿润,年均降水日数153 d,年均降水量1346 mm,降水多发生在3—9月。闽江河口段潮汐特征表现为口外正规半日潮,口内非正规半日浅海潮[14]。
1.2 土样采集在以上4个湿地分布的短叶茳芏沼泽采集土样,时间均在落潮后时段,2012年6月29日采集鳝鱼滩和蝙蝠洲,6月30日采集下洋洲和塔礁洲。在4个湿地分布的短叶茳芏群落典型地段,分别在与海岸线或河岸线平行的方向随机布设3个取样点(样点间约5 m间距),在每个取样点用不锈钢采样器随机采集数个表层(0—10 cm)土样并混合,混合后的土样放入塑料自封袋密封立刻运回实验室,4℃冷藏,以供开展甲烷产生潜力测定的厌氧培养实验和各项土壤理化指标的测定。土壤间隙水通过对土壤样品离心获得。
1.3 土壤和间隙水理化指标的测定原位用IQ150便携式pH/温度计(IQ Scientific Instruments,USA)测定土钻旁土壤(10 cm深度)的pH值,原位用2265FS便携式电导计(Spectrum Technologies Inc.,USA)测定土壤电导率,并以此表征土壤盐度[16]。
土壤含水量和容重用烘干法测定,土壤质地采用激光粒度仪(Mastersizer-2000,英国)测定,土壤水溶性有机碳(DOC)采用去离子水浸提并用TOC分析仪(TOC Vcph,Shimadzu,日本)测定,土壤微生物量碳(MBC)采用氯仿熏蒸培养法[17],土壤有机质采用重铬酸钾外加热法测定[18]。
采用离心法获得土壤间隙水样,间隙水用针头式过滤器过滤,并分装保存。间隙水中NH4+、NO3-和NO2-浓度采用连续流动分析仪(SKALAR San++,荷兰)测定,SO42-和Cl-浓度采用离子色谱仪(ICS-2100,美国戴安公司)测定。
1.4 不同盐度的海水和NaCl盐水的配置利用热带海水礁盐(Cnsic Marine Biotechnology CO.,LTD)及去离子水配置出不同盐度(5,10,15和21 g/L)的“人造海水”[19],分别称为H5、H10、H15和H21;另外,用分析纯NaCl和去离子水配置出盐度分别为5,10,15和21 g/L的纯NaCl盐水,分别称Y5、Y10、Y15和Y21,不同盐度“人造海水”和NaCl纯盐水中SO42-和Cl-浓度见表 1。不添加任何物质的去离子水作为对照,记为CK。
| 组成 Component | H5 | H10 | H15 | H21 | Y5 | Y10 | Y15 | Y21 |
| Cl-/(mmol/L) | 71.36 | 165.87 | 215.00 | 362.89 | 83.85 | 173.90 | 261.65 | 375.33 |
| SO42-/(mmol/L) | 3.28 | 7.00 | 9.22 | 16.10 | BD | BD | BD | BD |
| BD: 低于检测水平 |
实验室厌氧培养法是目前最为普遍的甲烷产生潜力测定方法,厌氧环境主要通过氮气置换实现,土样用干土或鲜土配置成为泥浆[20, 21],本研究采用鲜土进行厌氧培养试验。对于鲜土样挑除根等杂物,过2 mm土筛,充分混合均匀,并分别取鲜土样30 g,各放入125 mL培养瓶,分别加入以上4个盐度梯度的海水和纯盐水及对照去离子水,保持水土体积为1 ∶ 1,振荡形成泥浆。硅胶密封培养瓶并放入30℃(采样原位温度)生化培养箱2 d恢复活性,然后进行无光照厌氧培养。培养瓶用氮气冲洗3—5 min[20],使培养瓶内保持厌氧环境,30℃下连续培养12 d,每3 d为1个甲烷产生潜力计算时间段,分别记为1—3 d,4—6 d,7—9 d和10—12 d,各时段每天用微型注射器抽取气样2 mL,用气相色谱仪测定甲烷浓度,计算1个甲烷产生潜力。为保证培养瓶中气压稳定,每次抽取后补充等量氮气。为了防止培养瓶中积累甲烷过多而抑制甲烷产生,每培养3 d后洗气1次。
甲烷浓度采用气相色谱仪(岛津GC-2010,日本)测定,检测器为离子火焰化检测器(FID),载气为氮气,流速20 mL/min; 氢气为燃气,流速为47 mL/min;空气为助燃气,流速为400 mL/min,检测器温度为130 ℃,分离柱温度为60℃。培养瓶内土壤甲烷产生潜力计算公式[20]:
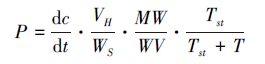
式中,P(μg g-1 d-1)为甲烷产生潜力;dc/dt(μL L-1 d-1)为培养期间培养气室上部气相甲烷浓度变化率;VH(L)为培养气室上部气体体积;WS(g)为干土重;MW(g/mol)为甲烷摩尔质量;MV为标准状态下气体摩尔体积(22.4 L/mol);Tst(K)为标准温度;T(℃)为培养温度。
1.6 数据处理用SPSS17.0软件中多重方差分析(Least significant difference test of One-way ANOVA,LSD) 统计分析不同湿地各土壤理化指标以及不同盐度处理间甲烷产生潜力的差异显著性,显著性水平为P<0.05。用Pearson分析盐度等环境因子与甲烷产生潜力的相关性。
2 结果 2.1 土壤和间隙水的理化特征4 个短叶茳芏湿地表层土壤容重和DOC浓度无显著差异,鳝鱼滩短叶茳芏湿地SOC含量显著低于其它3个湿地,然而土壤微生物量碳(MBC)含量显著高于其它3个湿地。粒径分布具有明显规律,沿着淡水至微咸水的盐度梯度,粉粒、粘粒逐渐增加,而砂粒含量却不断减少。pH也是鳝鱼滩短叶茳芏湿地土壤最高(表 1)。4个短叶茳芏湿地表层土壤间隙水NH4+和NO2-浓度无显著性差异,鳝鱼滩和蝙蝠洲短叶茳芏湿地土壤间隙水Cl-显著高于其它2个湿地。
| 采样点 Sampling site | 容重 Bulk density/ (g/cm3) | DOC/ (mg/kg) | SOC/ (g/kg) | MBC/ (mg/kg) | 粘粒 Clay/% | 粉粒 Silt/% | 砂粒 Sand/% | 电导率 Conductivity/ (mS/cm) | pH |
| 鳝鱼滩 | 0.74±0.07a | 72.1±28.4 a | 25.8±0.3c | 406.0±69.1 a | 13.4±1.80 ab | 70.2±1.86 a | 16.4±3.06 c | 1.97±0.54 a | 6.68±0.03 a |
| 蝙蝠洲 | 0.78±0.04 a | 47.0±3.4a | 53.4±4.1a | 213.0±5.3b | 15.0±0.45 a | 67.0±0.57 a | 18.0±1.00 c | 1.29±0.39 ab | 5.58±0.06 b |
| 下洋洲 | 0.78±0.01 a | 69.9±20.1 a | 37.2±1.9b | 209.1±10.5 b | 12.3±0.08 a | 63.0±0.63 b | 24.7±0.70b | 0.42±0.03 b | 4.51±0.03 b |
| 塔礁洲 | 0.66±0.03 a | 46.0±6.3a | 51.7±4.5a | 280.2±17.4 b | 10.6±0.24 b | 49.4±0.74c | 40.0±0.70 a | 0.46±0.01 b | 5.87±0.06 c |
| 数据为平均值±标准误,同一列数据标注不同字母表示差异性显著,P<0.05,n = 3 | |||||||||
| 采样点 Sampling site | NH4+/ (mmol/L) | NO2-/ (mmol/L) | NO3-/ (mmol/L) | SO42-/ (mmol/L) | Cl-/ (mmol/L) |
| 鳝鱼滩 | 0.18±0.07 a | 3.36±0. 60×10-4a | 4.40±0. 83×10-4b | 3.28±1.42a | 45.87±18.13 a |
| 蝙蝠洲 | 0.12±0.00 a | 2.89±0. 04×10-4a | 6.60±0. 14×10-4ab | 0.42±0.10 a | 9.83±1.06b |
| 下洋洲 | 0.18±0.04 a | 3.03±0. 06×10-4a | 10.74±0. 82×10-4a | 0.06±0.00 a | 1.70±0.23 c |
| 塔礁洲 | 0.20±0.03 a | 1.95±0. 38×10-4a | 8.19±2.40×10-4ab | 0.04±0.02 a | 1.64±0.19 c |
| 数据为平均值±标准误,同一列数据标注不同字母表示差异性显著,P<0.05,n = 3 | |||||
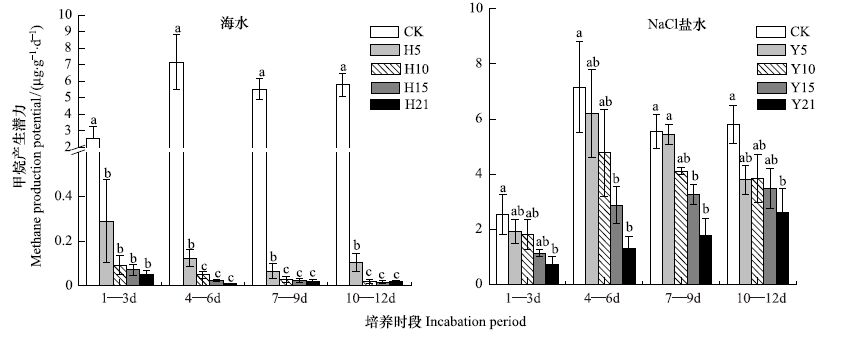
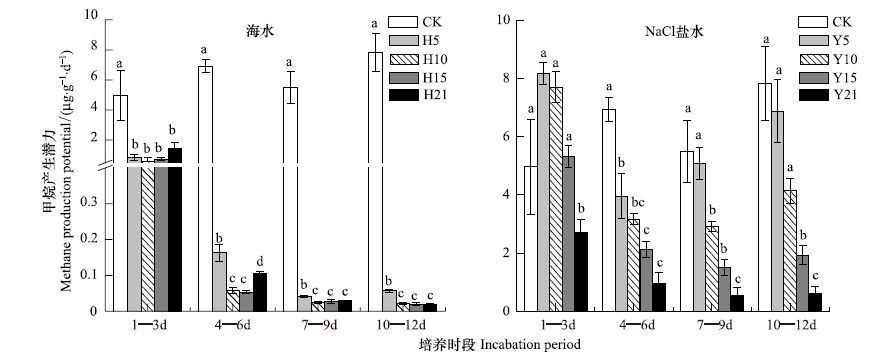
与对照相比,4个盐度海水处理在1—12 d内均对鳝鱼滩微咸水短叶茳芏湿地土壤甲烷产生潜力产生显著的抑制作用(P<0.05),在第4—6天,7—9天 和10—12天,盐度5 g/L海水处理的土壤甲烷产生潜力显著高于其它3个盐度海水处理的土壤甲烷产生潜力,但其它3个盐度海水处理下的土壤甲烷产生潜力无显著差异著(P>0.05)(图 2)。与对照比较,盐度21 g/L的NaCl溶液在1—12 d内对甲烷产生潜力造成显著的抑制作用,盐度15 g/L的NaCl溶液在第4—6天,7—9天对甲烷产生潜力造成显著的抑制作用,盐度5,10 g/L的NaCl溶液在1—12 d 对甲烷产生潜力均没有显著地抑制甲烷产生潜力(图 2)。
|
| 图2 海水和NaCl盐水添加对鳝鱼滩短叶茳芏湿地甲烷产生潜力的影响 (平均值±标准误) Fig.2 Effect of addition of seawater and NaCl solution on soil methane production potential of C. malaccensis marsh in the Shanyutan (Mean±SE) |
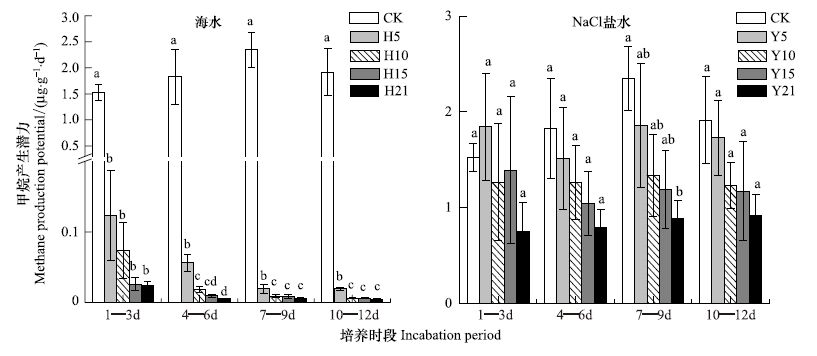
对于蝙蝠州微咸水短叶茳芏湿地,与对照比较,4个盐度的海水处理在1—12 d内均对甲烷产生潜力产生显著的抑制作用(P<0.05),在第4—6天,7—9天 和10—12天,盐度5 g/L海水处理的土壤甲烷产生潜力显著高于其它3个盐度海水处理的土壤甲烷产生潜力,而其它3个盐度海水处理下的土壤甲烷产生潜力多无显著差异(P>0.05)。除了在第7—9天,盐度21 g/L的NaCl溶液显著地抑制甲烷产生潜力,其余培养时段,各盐度NaCl溶液均没有显著地抑制甲烷产生潜力(图 3)。
|
| 图3 海水和NaCl盐水添加对蝙蝠洲短叶茳芏湿地甲烷产生潜力的影响 (平均值±标准误) Fig.3 Effect of addition of seawater and NaCl solution on soil methane production potential of C. malaccensis marsh in the Bianfuzhou (Mean±SE) |
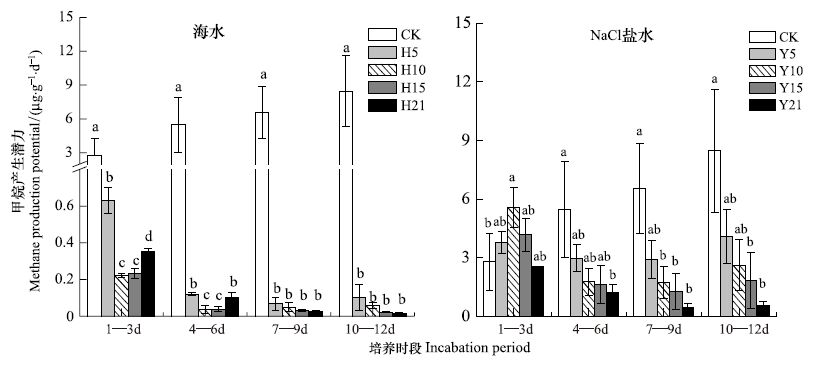
对于下洋洲淡水短叶茳芏湿地,与对照比较,4个盐度的海水处理在1—12 d内均对甲烷产生潜力产生显著的抑制作用(P<0.05),在第4—6天,7—9天 和10—12天,盐度5 g/L海水处理的土壤甲烷产生潜力显著高于其它3个盐度海水处理的土壤甲烷产生潜力,而其它3个盐度海水处理的土壤甲烷产生潜力多无显著性差异著(P>0.05)。与对照比较,盐度21 g/L的NaCl溶液在1—12 d内对甲烷产生潜力均造成显著的抑制作用,盐度15 g/L的NaCl溶液在第4—6天,7—9天 和10—12天对甲烷产生潜力造成显著的抑制作用,盐度10 g/L NaCl溶液在第4—6天,7—9天显著抑制甲烷产生潜力,盐度5 g/L NaCl溶液只在第4—6天显著地抑制甲烷产生潜力(图 4)。
|
| 图4 海水和NaCl盐水添加对下洋洲短叶茳芏湿地甲烷产生潜力的影响 (平均值±标准误) Fig.4 Effect of addition of seawater and NaCl solution on soil methane production potential of C. malaccensis marsh in the Xiayangzhou (Mean±SE) |
对于塔礁洲淡水短叶茳芏湿地,与对照比较,4个盐度海水处理1—12 d内均对甲烷产生潜力产生显著的抑制作用(P<0.05),在第1—3天,4—6天,盐度5 g/L海水处理下的土壤甲烷产生潜力显著高于其它3个盐度海水处理下的土壤甲烷产生潜力,在第1—3天,4—6天,盐度21 g/L海水处理的土壤甲烷产生潜力反而显著高于盐度10和15 g/L的海水处理(P<0.05)。与对照比较,盐度21 g/L NaCl溶液在第4—6天、7—9天和10—12天对甲烷产生潜力均造成显著的抑制作用,盐度15 g/L NaCl溶液只在第7—9天和10—12天对甲烷产生潜力造成显著的抑制作用,盐度10 g/L NaCl溶液在第7—9天显著抑制甲烷产生潜力,盐度5 g/L NaCl溶液在1—12 d内对甲烷产生潜力均未造成显著的抑制作用(图 5)。
|
| 图5 海水和NaCl盐水添加对塔礁洲短叶茳芏湿地甲烷产生潜力的影响 (平均值±标准误) Fig.5 Effect of addition of seawater and NaCl solution on soil methane production potential of C. malaccensis marsh in the Tajiaozhou (Mean±SE) |
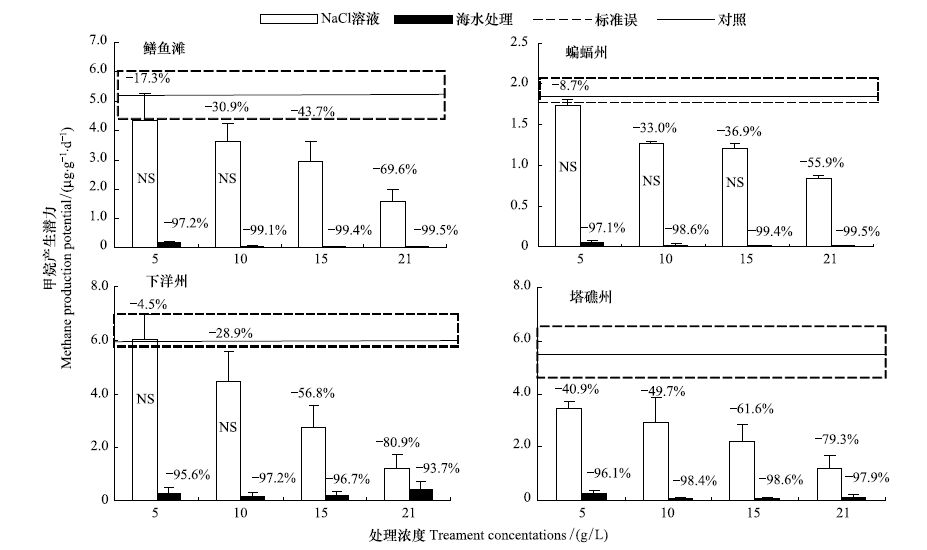
相对海水处理,纯NaCl溶液对于潮汐淡水、微咸水沼泽湿地甲烷产生潜力的影响要小的多(图 6)。与对照组相比,鳝鱼滩短叶茳芏湿地只有盐度15,21 g/L NaCl溶液显著抑制甲烷产生潜力,抑制率分别为69.6%和43.7%,而盐度5、10 g/L NaCl盐水对甲烷产生潜力无显著抑制效应,抑制率仅分别为17.3%和30.9%;对于蝙蝠州短叶茳芏湿地,只有盐度为21 g/L NaCl溶液显著抑制了甲烷产生潜力,而盐度5,10,15 g/L NaCl溶液对甲烷产生潜力均无显著抑制效应,盐度5 g/L NaCl溶液对甲烷产生潜力的抑制率仅为8.7%;对于下洋州短叶茳芏湿地,同样只有盐度15,21 g/L NaCl溶液显著抑制了甲烷产生潜力,而盐度5,10 g/L NaCl溶液对甲烷产生潜力无显著抑制效应;对于塔礁州短叶茳芏湿地,4个盐度的NaCl溶液对于甲烷产生潜力均具有显著的抑制作用(图 6)。
|
| 图6 海水和NaCl溶液添加处理12d培养期短叶茳芏湿地土壤甲烷产生潜力均值 (%代表与对照相比的下降百分比,各盐度处理显著减少的比例(P < 0.05),NS代表无显著性差异) Fig.6 Mean methane production potential of C. malaccensis marshes in the 12 days incubation period by the addition of seawater and NaCl solution (Percentages represent differences in mean methane production potential compared with the freshwater control (P< 0.05),NS = not significant) |
硫酸盐还原与甲烷产生是有机底物厌氧矿化的2个重要终端氧化过程[22]。湿地土壤产甲烷菌可利用底物醋酸产生甲烷,而硫酸盐还原菌可利用醋酸产生二氧化碳和硫化氢,并抑制湿地甲烷产生[23]。醋酸发酵产甲烷及硫酸盐还原的化学反应式如下[24]:

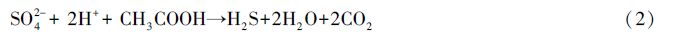
本研究12 d厌氧培养期间内,与对照组相比,4个盐度的海水添加对于淡水、微咸水短叶茳芏湿地土壤甲烷产生潜力均具有显著的抑制作用,抑制率最高值(99.5%)发生在鳝鱼滩和蝙蝠州短叶茳芏湿地土壤遭受盐度为21 g/L模拟海水入侵,最低值(93.7%)发生在在下洋州湿地土壤遭受盐度为21 g/L模拟海水的入侵(图 6)。海水中的主要阴离子成分为氯离子和硫酸根离子(表 1)。Weston等[8]和Chambers[11]的研究表明,湿地土壤厌氧环境中的硫酸盐还原菌对于底物的竞争能力远远超过产甲烷菌,伴随着海水入侵,可供硫酸盐还原菌利用的SO42-浓度也随之升高,使潮汐淡水、微咸水沼泽湿地土壤产甲烷过程向硫酸盐还原作用过程转变,甲烷产生速率明显降低。Pattnaik等[25]向热带水稻田土样施加 NaCl,CaCl2和MgSO4当量比为3 ∶ 2 ∶ 1,电导率分别为4,8,16 and 20 mS/cm溶液,室内厌氧培养试验的结果表明,随着电导率的上升,对于非盐性水稻土甲烷产生的抑制效果也在持续增加,在培养试验的第35 d,盐度为20 mS/cm的处理几乎完全抑制了甲烷的产生,盐度为4 mS/cm的处理对于甲烷产生的抑制率也超过55%。
综合分析图 2—5表明,海水盐度只要达到5 g/L便可显著地抑制河口淡水、微咸水沼泽湿地的甲烷产生过程。此外,从第4 d开始,除塔礁州短叶茳芏湿地以外,盐度10、15和21 g/L的海水处理对于其它3个湿地土壤甲烷产生潜力的抑制效应显著高于盐度5的海水处理,这表明在盐度为5—21 g/L这一区间,盐度10 g/L是海水入侵并影响淡水、微咸水沼泽湿地甲烷产生的一个重要的“拐点”,盐度超过10 g/L的海水的入侵对于河口淡水、微咸水沼泽湿地甲烷产生的抑制效用显著高于盐度不足10 g/L的海水的入侵,而盐度范围在10—21 g/L之间的海水入侵对于河口淡水、微咸水沼泽湿地甲烷产生的抑制效果并无差异。
盐度5 g/L NaCl溶液并没有显著抑制甲烷产生潜力,甚至盐度10 g/L NaCl溶液也不显著抑制甲烷产生潜力(塔礁州除外),只有盐度达到15 g/L以上,NaCl溶液才显著抑制甲烷产生潜力(蝙蝠州除外),以上结果表明,Cl-对于湿地土壤甲烷产生的抑制作用只在高的NaCl浓度时才发生。Chambers等[19]在3周的淡水湿地土样室内泥浆培养并模拟盐水入侵试验中,也发现添加NaCl 计量分别为5 g/kg和14 g/kg处理与对照组比较差异并不显著,只有35 g/kg处理时才显著降低甲烷产生潜力。Baldwin等[13]研究也表明,高浓度的NaCl溶液抑制淡水湿地土壤中醋酸发酵型产甲烷菌,这也有助于解释本研究中只有盐度15,21 g/L NaCl溶液才显著抑制甲烷产生潜力的实验结果。因此可以推测,相对于Cl-胁迫过程,SO42-还原作用对于甲烷产生过程的抑制作用明显。
本研究中4个盐度的模拟海水入侵对于微咸水和淡水潮汐湿地甲烷产生潜力的抑制效应十分接近,抑制效率保持在一个很高的范围(93.7%—99.5%)。但是,NaCl溶液对潮汐微咸水和淡水湿地甲烷产生潜力的抑制效应并不完全相同,当盐度为10 g/L时,NaCl溶液对塔礁州淡水潮汐湿地土壤甲烷产生潜力的抑制效应大于微咸水潮汐湿地(鳝鱼滩和蝙蝠州);当盐度为15和21g/L时,NaCl溶液对淡水潮汐湿地(下洋州和塔礁州)土壤甲烷产生潜力的抑制效应大于微咸水潮汐湿地(鳝鱼滩和蝙蝠州)。淡水潮汐沼泽湿地甲烷产生潜力对于NaCl溶液添加的响应更敏感,微咸水潮汐湿地(鳝鱼滩和蝙蝠州)土壤间隙水中Cl-离子浓度显著高于2个淡水潮汐湿地(表 2),可以推测其已遭受一定的氯离子胁迫影响,因而对于NaCl溶液添加而造成的氯离子胁迫作用具有一定的适应性。
对于模拟海水入侵处理,由图 2—图 5可以看出,与对照比较,各时段不同盐度处理的土壤甲烷产生潜力均有所下降,与最初1—3 d培养期相比,之后3个时段(9 d)甲烷产生潜力下降的更明显,且各时段间没有明显差异。这一结果与Chambers等[19]连续3周(每周测定一个甲烷产生速率)的模拟海水入侵淡水湿地的结果一致。在模拟海水入侵事件发生的前几天,即培养实验初期,泥浆中硫酸盐和甲烷产生底物(乙酸)含量均较高,硫酸盐还原对于土壤甲烷产生潜力表现出明显的抑制作用,然后随着时间的推移,后3个时段土壤甲烷产生潜力进一步下降且相近,推测可能是由于硫酸盐还原过程的抑制作用在最初1—3 d培养期已将土样中甲烷产生底物(乙酸等)大部分消耗掉,因此,后3个时段甲烷产生潜力明显下降,且无显著差异;或是由于随着培养时间的推移,硫酸盐还原抑制效应逐渐增强,并具有一定的持续性,这样虽然土样中仍有足够的甲烷产生底物,但基本是被硫酸盐还原过程所利用,甲烷产生受到程度更大的抑制,进而造成后3个时段土壤甲烷产生潜力显著下降,且无显著差异。
本研究应用土样泥浆厌氧培养试验,评价了不同盐度的海水和NaCl溶液对土壤电导率低于2 mS/cm的闽江河口区微咸水、淡水短叶茳芏沼泽湿地甲烷产生潜力影响的短期效应,研究发现:
(1)盐度5 g/L海水添加处理即可显著地抑制闽江河口淡水、微咸水沼泽湿地甲烷产生潜力,抑制率在93%以上。
(2)NaCl溶液只有盐度达到15和21 g/L才可显著抑制闽江河口淡水、微咸水沼泽湿地甲烷产生潜力,且抑制率最多为80.9%,盐度为5和10 g/L NaCl溶液不显著抑制闽江河口淡水、微咸水沼泽湿地甲烷产生潜力,抑制率多小于30%。
(3)伴随着海水入侵而发生的硫酸盐还原作用及Cl-离子胁迫作用对河口淡水、微咸水沼泽湿地甲烷产生具有显著的抑制效应。
本研究是在实验室运用厌氧培养实验,并模拟海水入侵开展盐分对河口潮汐淡水和微咸水沼泽湿地土壤甲烷产生潜力影响的研究,今后应加强原位模拟试验,把室内培养实验与野外原位实验相结合,更科学和全面地评估海水入侵对于河口潮汐淡水沼泽湿地土壤甲烷产生和排放的影响。
致谢: 本研究在野外采样中得到福建师范大学章文龙、徐辉和万斯昂等同学大力协助,特此致谢。
| [1] | IPCC. Climate Change: The Physical Science Basis Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge-New York: Cambridge University Press, 2007. |
| [2] | Knowles N. Natural and management influences on freshwater inflows and salinity in the San Francisco Estuary at monthly to interannual scales. Water Resources Research, 2002, 38(12): 25-1-25-11,. |
| [3] | Odum W E. Comparative ecology of tidal freshwater and salt marshes. Annual Review of Ecology and Systematics, 1988, 19(1): 147-176. |
| [4] | McLusky D S. Marine and estuarine gradients-an overview. Netherland Journal of Aquatic Ecology, 1993, 27(2-4): 489-493. |
| [5] | Barendregt A, Whigham D F, Meire P, Baldwin A H, van Damme S. Wetlands in the tidal freshwater zone. Wetlands: Functioning, Biodiversity Conservation, and Restoration. Berlin, Heidelberg: Springer, 2006, 191: 117-148. |
| [6] | DeLaune R D, Smith C J, Patrick Jr W H. Methane release from Gulf coast wetlands. Tellus B, 1983, 35(1): 8-15. |
| [7] | Bartlett K B, Bartlett D S, Harriss R C, Sebacher D I. Methane emissions along a salt marsh salinity gradient. Biogeochemistry, 1987, 4(3): 183-202. |
| [8] | Weston N B, Dixon R E, Joye S B. Ramifications of increased salinity in tidal freshwater sediments: Geochemistry and microbial pathways of organic matter mineralization. Journal of Geophysical Research: Biogeosciences (2005-2012), 2006, 111(G1): G01009, doi: 10.1029/2005JG000071. |
| [9] | Weston N B, Vile M A, Neubauer S C, Velinsky D J. Accelerated microbial organic matter mineralization following salt-water intrusion into tidal freshwater marsh soils. Biogeochemistry, 2011, 102(1-3): 135-151. |
| [10] | Neubauer S C. Ecosystem responses of a tidal freshwater marsh experiencing saltwater intrusion and altered hydrology. Estuaries and Coasts, 2013, 36(3): 491-507. |
| [11] | Chambers L G, Osborne T Z, Reddy K R. Effect of salinity-altering pulsing events on soil organic carbon loss along an intertidal wetland gradient: a laboratory experiment. Biogeochemistry, 2013, 115(1-3): 363-383. |
| [12] | Frankenberger W T, Bingham F T. Influence of salinity on soil enzyme activities. Soil Science Society of America Journal, 1982, 46(6): 1173-1177. |
| [13] | Baldwin D S, Rees G N, Mitchell A M, Watson G, Williams J. The short-term effects of salinization on anaerobic nutrient cycling and microbial community structure in sediment from a freshwater wetland. Wetlands, 2006, 26(2): 455-464. |
| [14] | 刘剑秋, 曾从盛, 陈宁. 闽江河口湿地研究. 北京: 科学出版社, 2006. |
| [15] | 仝川, 闫宗平, 王维奇,曾从盛. 闽江河口感潮湿地入侵种互花米草甲烷通量及影响因子. 地理科学, 2008, 28(6):826-832 |
| [16] | 王玲玲, 孙志高, 牟晓杰, 孙万龙, 宋红丽, 姜欢欢. 黄河口滨岸潮滩湿地CO2, CH4和N2O通量特征初步研究. 草业学报, 2011, 20(3): 51-61. |
| [17] | Vance E D, Brookes P C, Jenkinson D S. An extraction method for measuring soil microbial biomass C. Soil Biology and Biochemistry, 1987, 19(6): 703-707. |
| [18] | 鲁如坤. 土壤农业化学分析方法. 北京: 中国农业科技出版社, 1999. |
| [19] | Chambers L G, Reddy K R, Osborne T Z. Short-term response of carbon cycling to salinity pulses in a freshwater wetland. Soil Science Society of America Journal, 2011, 75(5): 2000-2007. |
| [20] | Wassmann R, Neue H U, Bueno C, Lantin R S, Alberto M C R, Buendia L V, Bronson K, Papen H, Rennenberg H. Methane production capacities of different rice soils derived from inherent and exogenous substrates. Plant and Soil, 1998, 203(2): 227-237. |
| [21] | Bergman I, Klarqvist M, Nilsson M. Seasonal variation in rates of methane production from peat of various botanical origins: effects of temperature and substrate quality. FEMS Microbiology Ecology, 2000, 33(3): 181-189. |
| [22] | Struchtemeyer C G, Elshahed M S, Duncan K E, McInerney M J. Evidence for aceticlastic methanogenesis in the presence of sulfate in a gas condensate-contaminated aquifer. Applied and Environmental Microbiology, 2005, 71(9): 5348-5353. |
| [23] | Oremland R S, Polcin S. Methanogenesis and sulfate reduction: competitive and noncompetitive substrates in estuarine sediments. Applied and Environmental Microbiology, 1982, 44(6): 1270-1276. |
| [24] | van der Gon H A D, van Bodegom P M, Wassmann R, Lantin R S, Metra-Corton T M. Sulfate-containing amendments to reduce methane emissions from rice fields: mechanisms, effectiveness and costs. Mitigation and Adaptation Strategies for Global Change, 2001, 6(1): 71-89. |
| [25] | Pattnaik P, Mishra S R, Bharati K, Mohanty S R, Sethunathan N, Adhya T K. Influence of salinity on methanogenesis and associated microflora in tropical rice soils. Microbiological Research, 2000, 155(3): 215-220. |
 2015, Vol. 35
2015, Vol. 35