文章信息
- 卞方圆, 苏建荣, 刘万德, 李帅锋, 郎学东
- BIAN Fangyuan, SU Jianrong, LIU Wande, LI Shuaifeng, LANG Xuedong
- 云南红豆杉新采收种子的形态与离体胚的萌发特性
- Morphology of fresh seeds and germination of in vitro embryos for Taxus yunnanensis
- 生态学报, 2015, 35(24): 8211-8220
- Acta Ecologica Sinica, 2015, 35(24): 8211-8220
- http://dx.doi.org/10.5846/stxb201406081180
-
文章历史
- 收稿日期: 2014-06-08
- 网络出版日期: 2015-05-21
云南红豆杉(Taxus yunnanensis)又名紫金杉、紫杉,被国际松杉类专家组(CSG)确定为3级渐危种,也是国家一级保护植物[1]。云南红豆杉还是一种重要的药用植物,富含天然抗癌药物紫杉醇(Taxol)[2],被广泛用于滇、川、渝、藏等地的药用原料林基地建设[3, 4]。红豆杉植物种子在自然条件下需两冬一夏才能萌发,萌发率很低[5, 6, 7]。为缩短种子萌发时间,提高萌发率,规模化培育原料林和保育所需优质实生苗,国内外学者围绕红豆杉种子生物学、生理生态学、种苗培育方面开展了大量的研究,但在种皮透水性的强弱,是否为萌发的主要障碍[7, 8, 9, 10, 11];胚乳对种胚萌发有抑制作用,还是促进作用[12, 13];新采收种子离体胚培养的萌发率是高(82%),还是低(8.5%)[13, 14, 15]这3个关键问题上仍未形成一致观点和结论。
种子休眠(Seed Dormancy)是指在一定的时间内,具有活力的种子在任何正常的物理环境因子组合下不能萌发的现象[16, 17]。Baskin和Baskin[16, 18]依据物种的成熟新鲜种子是否在持续四周的最佳萌发条件下萌发与否作为划分种子休眠与否的时间界限,并结合种子的其它特性划分出生理休眠(Physiological Dormancy,PD)、形态休眠(Morphological Dormancy,MD)、形态生理休眠(Morphophysiological Dormancy,MPD)、物理休眠(Physical Dormancy,PY)和复合休眠(Combinational dormancy,PY+PD)5 种类型。PD广泛存在于裸子植物和大多数被子植物的种子中,主要以离体胚能否正常生长,萌发是否需要释放休眠的预处理确定并划分亚类;MD型种子的胚已分化,但小、发育不完全,胚生长至足够体积后就能萌发;MPD 的种子具有未发育完全和生理休眠的胚;PY则是由种皮或者果皮的不透水所引起;PY+PD的种皮(果皮)不透水,而且胚具有生理休眠[19]。红豆杉种子的休眠机理迄今仍不清楚,快速解除休眠的技术也尚未发现[7, 20],而澄清种胚的萌发特性、种皮透水性等争议较大的问题是深入研究种子休眠类型与机理及开发休眠解除技术提高发芽率的重要基础。
本研究以新采收的云南红豆杉种子为对象,通过对种子的形态特征、种胚大小与萌发的关系、种皮透水性及离体胚萌发特性等方面的研究,探讨种皮的透水特性、胚乳对离体胚萌发的影响及离体胚培养萌发率变异巨大的成因,为揭示云南红豆杉的休眠机理及休眠解除机理累积基础数据,同时为推动种群恢复和实生苗的规模化培育提供科学依据。
1 材料与方法 1.1 材料试验所用云南红豆杉种子采自中国林业科学研究院资源昆虫研究所景东试验站栽培的同一种源。采样地海拔1200m,位于E 100°18′,N 23°52′。该区属亚热带季风气候,年平均气温(18.3±0.5)℃,极端最高温(37±1.5)℃,极端最低温(-2±1)℃;年平均降雨量1100±50mm,多集中于7—8月;年平均日照天数(205±5)d;年均太阳辐射总量(131.7±2.5)×4.184kJ/cm2。2013年12月5日采摘假种皮变红的种子用于试验。采种后带回实验室立即用水浸泡并搓洗除去假种皮,将洗净的种子阴干后备用。经国家标准《林木种子检验规程》(GB 2772—1999)[21]TTC法测定,种子生活力为78%。
1.2 方法 1.2.1 试验种子抽样方法各试验均采用《林木种子检验规程》(GB 2772—1999)[21]四分法按所需用量从2000粒左右种子中随机抽取各项试验种子。
1.2.2 种子和种胚的形态与大小观察种子与胚的形态,测量种子大小、千粒重、胚大小,称量种皮、种仁、胚重量。种子大小以长轴、横径和纵径表示,随机抽取30粒种子,3次重复,用精确到0.01mm的游标卡尺测量。云南红豆杉种子外观近似于椭球体,因此根据椭球体的计算公式计算种子体积。胚形态用VHX-1000超景深三维显微镜观察与测量,随机抽取30粒种子,3次重复。由于种胚形状呈酒瓶形,上半部近似圆锥体,下半部近似圆柱体,采用圆锥和圆柱体积公式计来计算种胚的体积。种子千粒重按《林木种子检验规程》(GB 2772—1999)[21]测定。种皮、种仁、胚的重量为鲜重,随机取30粒种子,3次重复,用解剖刀将种子分离成种皮和种仁(包括胚乳、胚)两部分,再分别用电子天平称量;用解剖刀沿种仁中线切除部分胚乳后用解剖针挑出完整的种胚,取10粒种胚用电子天平称量,重复20次。
1.2.3 种子的含水量由于红豆杉种子较坚硬,所以先将种皮夹破,再置于103±2℃的恒温干燥箱中烘17h,然后取出在干燥器中冷却至室温。每次取约3g种子,3次重复。用烘干前后的重量差值除以干重计算种子含水量[22]。
1.2.4 种子透水性的测定实验设完整种子、夹破种子、酸蚀40min种子、酸蚀20min种子4个处理,其中夹破处理为切去约十分之一的种皮,酸蚀所用试剂为98%的浓硫酸。取完整种子、夹破种子各30粒分别称质量,然后放入烧杯中,加蒸馏水浸泡,在室温条件下吸胀。另取酸蚀20min种子和酸蚀40min种子各30粒分别称质量,先流水冲洗24h,再继续浸泡水中。流水冲洗每2h称量1次,24h之后每6h称量1次,36h后每12h称量1次,直至恒重[23]。4个处理,每个处理3次重复,以浸种前后的质量差除以浸种前质量计算种子吸水率。
1.2.5 不同大小种子的离体胚培养随机抽取150粒种子,用0.01mm的游标卡尺测量种子的长轴、横径和纵径,计算体积。做频率分布图,对种子大小进行分组。然后进行萌发试验,每组随机取40颗,重复3次,去外种皮,经70%酒精和0.1%升汞常规表面消毒后,在无菌条件下切除种皮和部分胚乳后接种于MS基本培养基上。培养基的pH值为5.8,添加3%蔗糖、0.8%琼脂。培养温度控制在(25±1)℃,每天光照16h,光照度为2000lx[13]。接种时间为2013年12月19日。离体胚萌发指具有子叶和胚轴的胚,每天观察记录种子的萌发情况,做动态曲线图。发芽率(Gp)为发芽总数除以培养总数,发芽指数(Gi)为在时间t日的发芽数除以相应的发芽日数的总和。
1.2.6 带全胚乳和带部分胚乳胚的培养用带全胚乳及带1/3、1/2、2/3胚乳和不带胚乳的胚进行离体培养,每组处理40颗,重复3次。去外种皮,经70%酒精和0.1%升汞常规表面消毒后,在无菌条件下切除种皮和1/3、1/2、2/3或全部胚乳。将5个处理的种子分别接种于MS培养基上。培养方法同上,接种时间是2013年12月24日。按前述离体胚萌发标准,记录种子萌发日进程,绘制动态曲线。计算发芽率(Gp)和发芽指数(Gi)。
1.2.7 数据统计与分析采用SPSS 18.0进行处理数据,计算种子与种胚各性状之间的相关系数;用单因素方差分析,检验不同的种皮处理对种子吸水的差异性和不同种胚大小的萌发率、发芽指数间的差异性,并进行LSD多重比较。采用SigmaPlot 12.5制图。
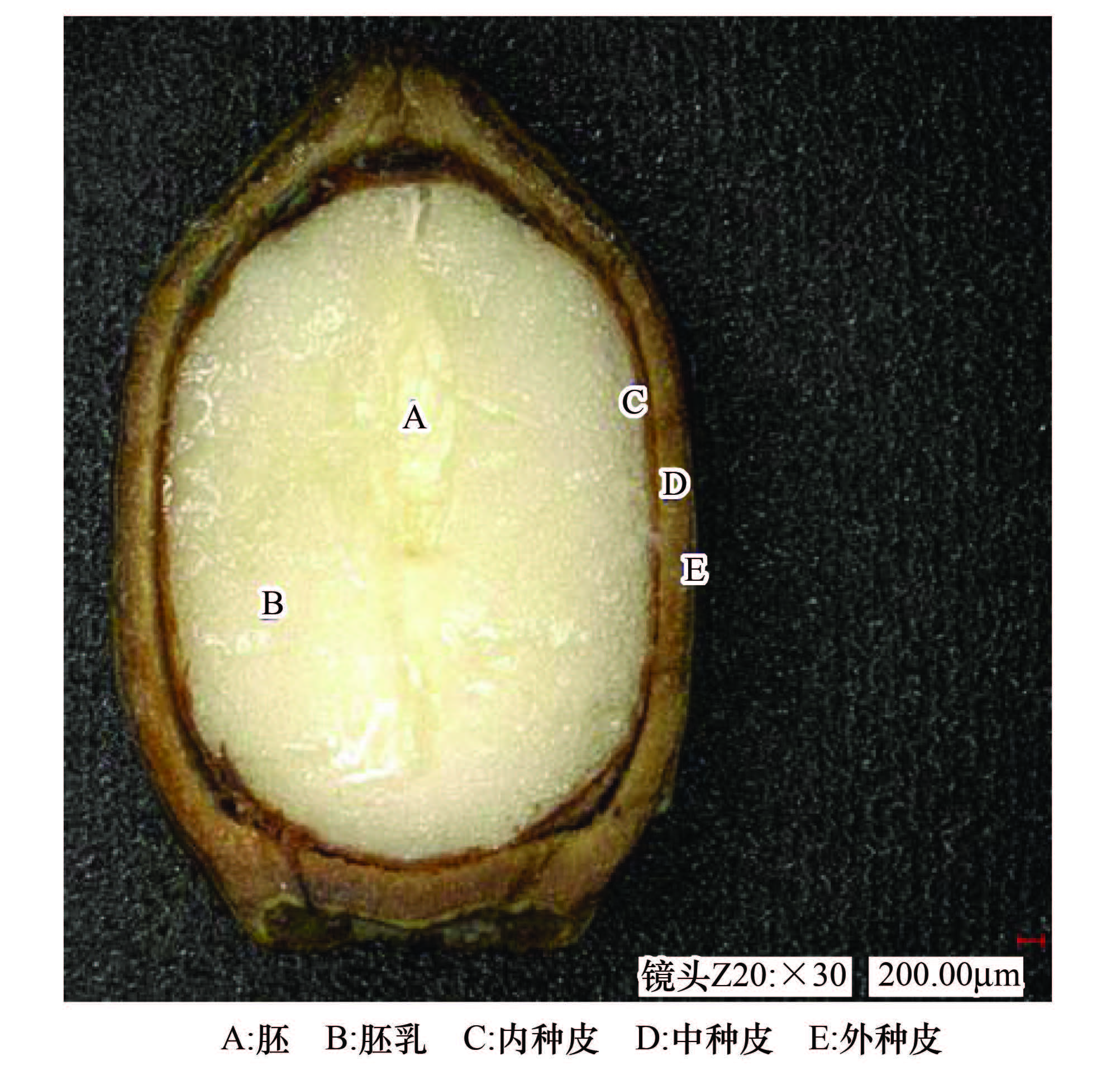
2 结果与分析 2.1 种胚的形态与大小 2.1.1 种胚的主要性状特征云南红豆杉种子倒卵形,少数三棱形(图 1),种子有鲜红色杯状肉质假种皮包于种子下半部,顶端有小突尖,基部圆形。种子由种皮、胚及胚乳3部分组成(图 2)。种皮坚硬,褐色,平滑,在高倍显微镜下可见密布排列整齐的小椭圆形突起,包括外、中、内种皮。胚呈酒瓶形,白色,光滑(图 3)。胚乳淡黄色,油质。

|
| 图1 云南红豆杉种子形态 Fig.1 Seed morphology of Taxus yunnanensis |
|
| 图2 南红豆杉种子纵切面 Fig.2 Seeds longitudinal section of Taxus yunnanensis |

|
| 图3 云南红豆杉种胚形态 Fig.3 Embryo morphology of Taxus yunnanensis |
云南红豆杉种子特征数据见表 1。种子平均千粒重为72.934g、平均含水率为32%;种子的长轴长、横径长和纵径长分别是6.905、4.876mm和4.403mm;平均每粒种子的种皮重、种仁重和种胚重为0.045、0.036g和0.0036g,分别占单粒种子重量的50.56%、40.45%和8.99%。
| 指标 Index | 平均值±标准差 Mean±SD | 最小值 Minimum | 最大值 Maximum |
| 千粒重 1000 seed weight/g | 72.934±1.429 | — | — |
| 种皮重 Seed coat weight/g | 0.045±0.008 | 0.026 | 0.057 |
| 种仁重 Seed kernel weight/g | 0.036±0.006 | 0.024 | 0.049 |
| 种胚重 Embryo weight/g | 0.008±0.002 | 0.005 | 0.011 |
| 种子长轴 Seed long axis/mm | 6.905±0.436 | 6.02 | 7.92 |
| 种子横径 Seed transverse diameter/mm | 4.876±0.240 | 4.27 | 5.46 |
| 种子纵径 Seed longitudinal diameter/mm | 4.403±0.332 | 3.78 | 5.25 |
| 种胚长 Embryo length/mm | 2.437±0.238 | 1.817 | 3.233 |
| 含水量 Seed moisture content/% | 32.000±1.250 | — | — |
| 种皮、种仁为单个质量,种胚为每10个质量。 | |||
云南红豆杉种胚性状之间的相关分析(表 2)表明,种子的千粒重与种皮重、种胚长,种皮重与种仁重,种仁重与种子纵径长之间存在显著的相关性(P< 0.05);种子的长轴长分别与种子的横径长、种子纵径长和种胚长存在极显著正相关(P< 0.01);种子的横径长与种子纵径长和种胚长也呈极显著正相关(P< 0.01);种子纵径长与种胚长的相关性也达到极显著(P< 0.01)。
| 指标 Index | 千粒重 1000 seed weight | 种皮重 Seed coat weight | 种仁重 Seed kernel weight | 种胚重 Embryo weight | 种子长轴 Seed long axis | 种子横径 Seed transverse diameter | 种子纵径 Seed longitudinal diameter | 种胚长 Embryo length | 含水量 Seed moisture content |
| 千粒重1000 seed weight | 1.000 | ||||||||
| 种皮重Seed coat weight | 0.859* | 1.000 | |||||||
| 种仁重Seed kernel weight | 0.709 | 0.236* | 1.000 | ||||||
| 种胚重Embryo weight | 0.701 | 0.202 | 0.404 | 1.000 | |||||
| 种子长轴Seed long axis | 0.619 | 0.092 | 0.202 | 0.304 | 1.000 | ||||
| 种子横径Seed transverse | 0.150 | 0.168 | 0.114 | 0.174 | 0.631* * | 1.000 | |||
| 种子纵径Seed longitudinal | 0.645 | 0.279 | 0.296* | 0.190 | 0.773* * | 0.681* * | 1.000 | ||
| 种胚长Embryo length | 0.769* | 0.085 | 0.262 | 0.174 | 0.865* * | 0.546* * | 0.725* * | 1.000 | |
| 含水量Seed moisture content | 0.450 | 0.483 | 0.178 | 0.102 | 0.575 | 0.902 | 0.925 | 0.296 | 1.000 |
| *P< 0.05; * *P< 0.01 | |||||||||
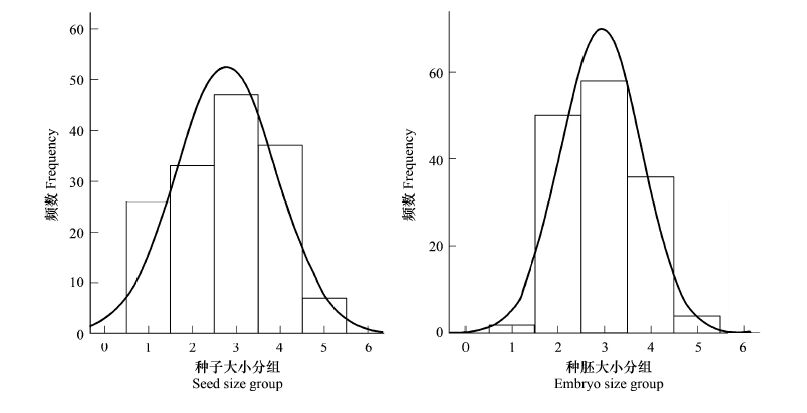
云南红豆杉种子和种胚体积大小呈明显的正态分布(图 4)。
|
| 图4 种子与种胚大小的频数分布图 Fig.4 Distribution of Seed and embryo size frequency |
种子的体积大小在51.658—109.649mm3之间,全距57.991,以11.598为组距可将种子分成特小、小、中等、大、特大5个组,对应的体积范围分别为51.658—63.256mm3、63.257—74.854mm3、74.855—86.452 mm3、86.453—98.050mm3和98.051—109.649mm3。云南红豆杉种胚的体积分布范围为0.156—1.012mm3,按体积大小可分为特小、小、中等、大、特大5个组,体积范围分别为0.156—0.327 mm3、0.328—0.498 mm3、0.499—0.669 mm3、0.670—0.840 mm3和0.841—1.012 mm3。
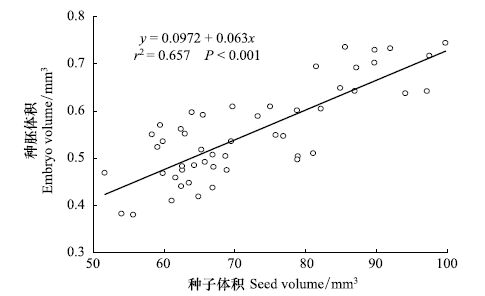
散点图(图 5)显示种子与种胚的体积之间存在明显的线性相关关系。进一步分析表明,云南红豆杉种胚的体积与种子的体积之间的回归方程为y=0.0972+0.063x(r2=0.657,P<0.001)。种胚体积大小变异的65.7%可用种子体积的大小来解释,因此生产上可用种子的大小来判断种胚的大小。云南红豆杉种胚与种子体积大小的比值(E ∶ S)为0.074。
|
| 图5 种子-种胚体积散点图 Fig.5 Scatter diagram of seed and embryo volume |
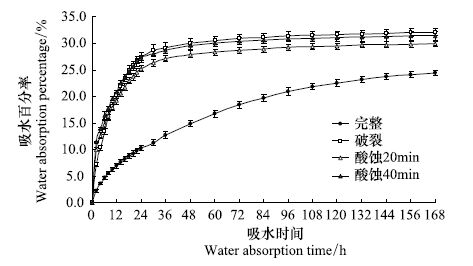
在整个实验过程中,完整种子的吸水率明显低于破裂种皮、酸蚀40min、酸蚀20min的处理种子的吸水率,但随着浸泡时间的增加吸水率的差异逐渐缩小(图 6)。
|
| 图6 不同处理云南红豆杉种子的吸水动态 Fig.6 Water absorption dynamics of different processing Taxus yunnanensis seeds |
从吸水速度看,完整种子的吸水速度最慢;而破裂种子与酸蚀种子吸水速度在18h内基本一致,快速吸水,18h后酸蚀20min种子的吸水速度稍慢于破裂种子和酸蚀40min种子。酸蚀40min 种子率先达到20%的吸水率,只需10h,其次破裂种子需12h,酸蚀20min种子需14h,而完整种子最慢,达到20%吸水率需要87h。到第30小时时,破裂种子的吸水率为28.7%,酸蚀20min为26.3%,酸蚀40min为28.0%,之后破皮种子与酸蚀种子的吸水量逐渐趋于饱和,而完整种子仍保持较快的吸水趋势。破皮种子与酸蚀种子在48h后达到饱和含水量,吸水率在28%左右;完整种子含水量达到饱和需要144h,吸水率为23.7%。
方差分析表明,不同的时间处理(P<0.001)与种皮处理(P<0.001)对云南红豆杉种子的吸水率都有极显著影响。对不同种皮处理间的LSD多重比较表明,完整种子的含水率与破皮种皮、酸蚀40min、酸蚀20min处理种子的含水率差异达极显著水平(P<0.001);而后三者种子含水率的差异则不显著。所以,在培育实生苗过程中可采用98%的浓硫酸处理种子20 min,以增加种皮的透水性和种子含水量,提高种子萌发率。
2.3 种子大小对种胚萌发的影响试验将不同大小的种子接种在MS培养上,培养12d左右可以明显观察到部分种胚生长出2片绿色子叶,同时胚轴伸长(图 7)。

|
| 图7 云南红豆杉种子的离体培养 Fig.7 In vitro culture of Taxus yunnanensis seeds |
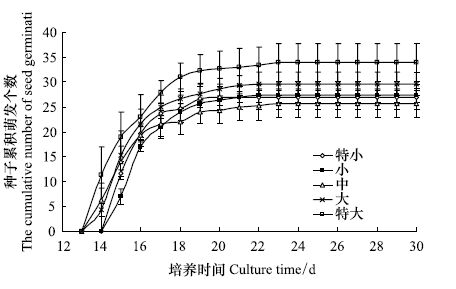
云南红豆杉离体胚培养的萌发进程(图 8)表明,不同大小种子的萌发趋势较为一致,初期萌发率有随时间快速增长的特点。特大、大和中等大小种子的离体胚最先开始萌发,小种子和特小种子开始萌发的时间稍晚。离体培养到12—18d左右,大量种胚同时萌发,萌发率较高,萌发率增长速度较快。随时间的推移,每天种胚的新增萌发量减少,萌发速度开始减慢。在接种之后的23d左右就观测不到种子萌发现象,种胚萌发基本停止,萌发率也不再增加。
|
| 图8 不同大小种子萌发动态 Fig.8 Seed germination dynamic of different sizes |
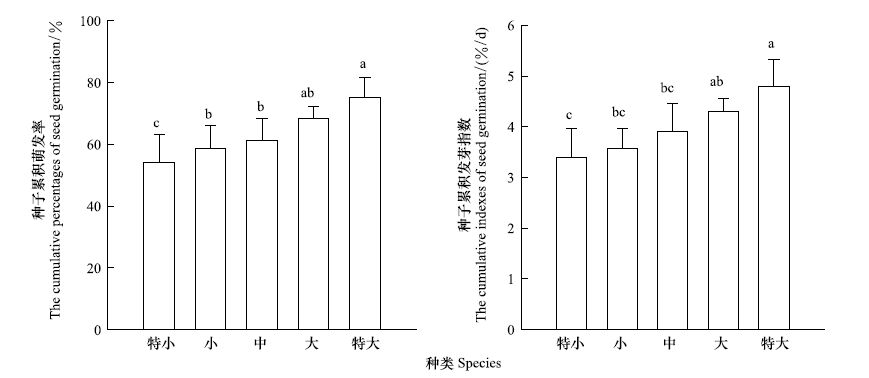
云南红豆杉离体胚的平均萌发率和发芽指数随种子大小的增大而增加(图 8)。离体胚的萌发率在44%—80%之间,特大种子的萌发率为80%,大、中、小和特小种子的萌发率分别为77.8%、67.5%、62.0%和44.0%。方差分析表明,不同大小种子离体胚的萌发率(Gp)和发芽指数(Gi)的差异均达到显著水平(FGp= 4.194 > F0.05=3.480;FGi= 4.260 > F0.05=3.480)。LSD检验表明:特大种子的萌发率显著高于特小种子(P<0.001),显著高于小种子和中种子(P<0.05);大种子的萌发率显著高于特小种子(P<0.05);其余种子之间差异不显著。可见,在离体胚培养过程中,选择个大、饱满的种子,尤其是选用体积在98 mm3以上的特大种子可显著提高胚的萌发率。该结果也说明,在实生苗培育的制种环节中应考虑对种子进行分级,以提高种子的萌发率,降低育苗成本。
|
| 图9 不同大小种子萌发率与发芽指数 Fig.9 Seed germination rate and germination index of different sizes |
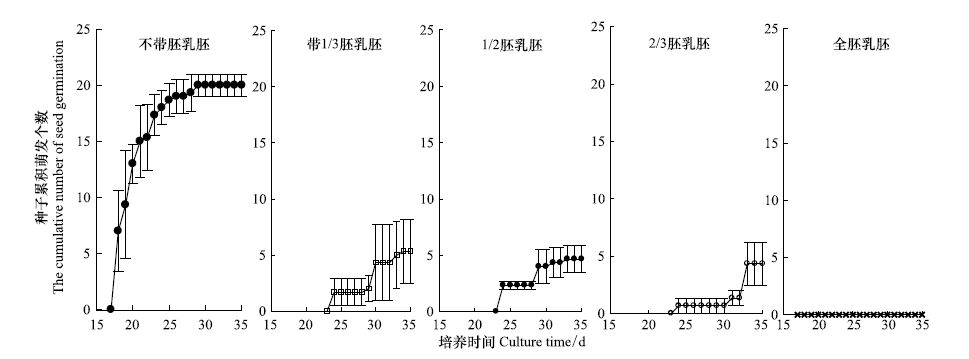
在云南红豆杉离体胚培养中,种胚所带胚乳的多少对胚萌发率的影响十分明显(图 10,图 11),带全胚乳及带1/3、1/2、2/3胚乳和不带胚乳胚的萌发进程均不理想,每个处理的初始萌发时间差别很大,较早(不带胚乳)于18d开始萌发,较晚(全胚乳)甚至没有萌发的迹象,由于本研究仅观察到35d,故不排除35d后仍有种子再萌发的情况。
|
| 图10 种胚带不同大小胚乳萌发动态 Fig.10 The germination dynamic of embryo with endosperm of different sizes |
|
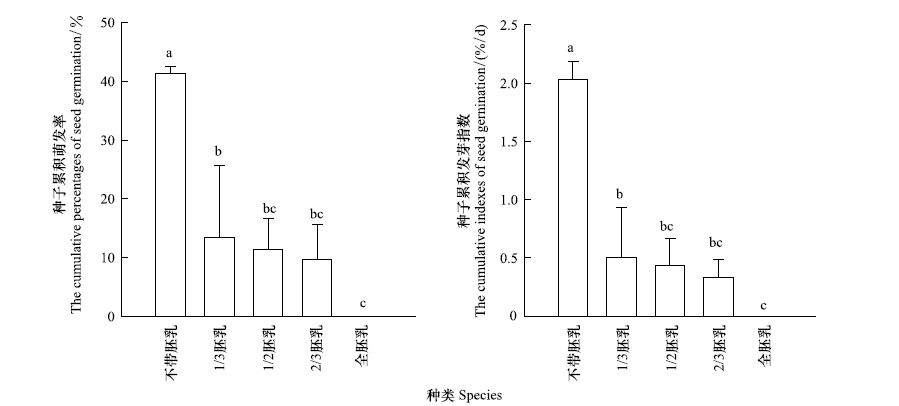
| 图11 种胚带不同大小胚乳萌发率与发芽指数 Fig.11 The germination rate and germination index of embryo with endosperm of different sizes |
在研究期限内,不带胚乳的胚的萌发率(41.3%)最高,带部分胚乳的萌发率在9.7%—13.3%之间,全胚乳胚萌发率最低为0。方差分析表明,离体胚培养过程中,胚带胚乳的多少对萌发率(Gp)和发芽指数(Gi)的影响达极显著水平(FGp=16.629 > F0.01=5.99,P<0.01;FGi=32.397 > F0.01=5.99,P<0.01)。LSD多重比较(图 11)进一步表明,不带胚乳胚的萌发率高于1/3胚乳胚、1/2胚乳胚、2/3胚乳胚和全胚乳胚,且萌发率和萌发指数的差异达极显著水平;1/3胚乳胚显著高于全胚乳胚;其余种子之间差异不显著。
3 结论与讨论 3.1 云南红豆杉离体胚萌发率的影响因素云南红豆杉的离体胚培养采用MS培养基时,种胚萌发率的差异很大,赵沛基等[13]测定的萌发率高达82%,王兵益等[14]测定的萌发率为70%,而杨玲等[15]测定的萌发率仅有8.5%。这些研究均以新鲜、成熟(以假种皮变红为标志)的种子为试验材料,培养方法基本一致。本研究表明,种子和胚的体积大小很可能是其离体胚培养萌发率差异较大的成因之一。云南红豆杉新采收种子和种胚的体积分别在51.658—109.649mm3和0.156—1.012mm3之间,变异幅度较大。种子大小对离体胚的萌发率影响显著,特大种子(体积98.051—109.649 mm3)的萌发率高达80%,而特小种子(体积51.658—63.256 mm3)的萌发率仅有44%。云南红豆杉种子的体积与种胚的体积之间存在显著的正相关(图 5),可以认为胚的大小也是影响离体胚萌发率的因素。以往的研究,忽视了种子、胚的大小对离体胚萌发率的影响,这可能是导致云南红豆杉离体胚培养种胚萌发率差异巨大的重要因素。在今后的研究中,应加强种子的大小对萌发率影响及其与种子成熟度关系的探索,并在实生苗木培育过程中对种子进行分级处理。
本研究所用云南红豆杉种子采于2013年12月5日,同月19日接种第一批离体胚,24日接种第二批离体胚。第一批接种的带部分胚乳离体胚的萌发率为44%—80%(图 9),而第二批带部分胚乳离体胚的萌发率仅为9.7%—13.3%(图 11)。结果显示,用新采收云南红豆杉种子进行离体胚培养时,接种时间的早晚对种胚萌发率也有较大的影响,有研究报道鲜种在采后一周发芽率可达90%[10]。然而,先前的研究尚未认识到离体胚或种子的新鲜程度(种子采集后到接种或播种的时间长短)对种胚萌发率的影响。可见,种胚的新鲜程度也是导致云南红豆杉离体胚萌发率波动的重要因素。关于云南红豆杉的离体胚培养、种子萌发及休眠机理的研究,既要注意培育条件的相同,又要重视试验材料的一致性,深入探讨试验材料的差异性在揭示红豆杉休眠机理和突破红豆杉快速解除休眠技术方面具有重要的价值,应给予充分重视。
3.2 云南红豆杉的休眠类型及其成因如前所述,Baskin和Baskin[16, 18]将种子休眠分为生理休眠(PD) 、形态休眠(MD)、形态生理休眠(MPD)、物理休眠(PY)和复合休眠(PY+PD)5 种类型。本研究中,带全胚乳的种胚在35d试验期的萌发率为0,按照Baskin和Baskin[16, 18]的标准(四周不萌发),该物种具有休眠特性。解剖发现,试验用种都已分化完全,可明显观察到种皮、胚乳以及胚的胚根、胚轴、子叶等组织,且云南红豆杉新采收种子的离体胚在12—18d左右能够正常生长(图 7),其它研究也未发现种子贮藏过程中胚结构的明显变化[14],因此云南红豆杉种子的休眠不属于形态休眠类型。本研究显示,完整种子的吸水率虽然比破皮种子、酸蚀40min、酸蚀20min处理种子的吸水率低,但浸泡144h后,前者的吸水率仅比后3类处理低5%左右。这与赵盛军[11]认为云南红豆杉种皮透水性较好的结论一致,所以云南红豆杉种子的休眠也不属于物理休眠。对比有胚乳和没有胚乳的离体胚的萌发结果发现,胚乳是影响离体胚萌发的重要因素,由此可推断,云南红豆杉种子的休眠属于Baskin和Baskin[18]休眠分类体系中的中度生理休眠类型。
导致生理休眠的原因很多,但是离体胚培养中种胚带胚乳的多少和种子的新鲜程度对云南红豆杉离体胚萌发的影响值得深入研究。本研究中,不带胚乳离体胚的萌发率显著高于带胚乳离体胚的萌发率,与赵沛基等[13]的研究结论相反。产生这一矛盾的原因可能是试验用种新鲜程度的影响。以往研究都假定种子采集到接种的时间不影响种子的萌发率,均未注明种子的采集时间和胚的接种时间。但本研究结果表明,离体胚培养过程中所用种子的新鲜程度严重影响胚的萌发率。目前,普遍认为种子中的抑制物是导致红豆杉休眠的主要原因[8, 20, 24, 25, 26, 27, 28]。通过研究云南红豆杉种子中抑制物含量与种子新鲜程度的关系,胚乳中抑制物含量对萌发率的影响,可以解释产生上述矛盾的成因,这是云南红豆杉休眠研究的重点。
| [1] | 苏建荣, 张志钧, 邓疆, 李国松. 云南红豆杉的地理分布与气候关系. 林业科学研究, 2005, 18(5): 510-515. |
| [2] | Cragg G M, Schepartz S A, Suffness M, Grever M R. The taxol supply crisis. New NCI policies for handling the large-scale production of novel natural product anticancer and anti-HIV agents. Journal of Natural Products, 1993, 56(10): 1657-1668. |
| [3] | 苏建荣, 张志钧, 邓疆. 不同树龄、不同地理种源云南红豆杉紫杉醇含量变化的研究. 林业科学研究, 2005, 18(4): 369-374. |
| [4] | 苏建荣, 缪迎春, 张志钧. 云南红豆杉紫杉醇含量变异及其相关的RAPD分子标记. 林业科学, 2009, 45(7): 26-28. |
| [5] | 美国农业部林务局. 美国木本植物种子手册. 李霆, 陈幼生, 译. 北京: 中国林业出版社, 1984. |
| [6] | 黄儒珠, 方兴添, 郭祥泉, 郑珂晖, 罗荔仙. 南方红豆杉种子的化学成分分析. 应用与环境生物学报, 2002, 8(4): 392-394. |
| [7] | 程广有, 唐晓杰, 高红兵, 沈熙环. 东北红豆杉种子休眠机理与解除技术探讨. 北京林业大学学报, 2004, 26(1): 5-9. |
| [8] | 张志权, 廖文波, 钟翎, 陈志明. 南方红豆杉种子萌发生物学研究. 林业科学研究, 2000, 13(3): 280-285. |
| [9] | 张艳杰, 申慧, 饶玮, 鲁顺保, 高捍东. 南方红豆杉种子生物学特性研究. 安徽农业科学, 2010, 38(1): 440-442. |
| [10] | 王卫斌, 王达明. 云南红豆杉. 昆明: 云南大学出版社, 2006. |
| [11] | 赵盛军. 云南红豆杉种子休眠原因的初步研究. 林业调查规划, 1996, (1): 44-46. |
| [12] | 臧新, 吕晓辉, 杨冬之, 黄象男. 2种红豆杉的离体胚培养. 郑州大学学报: 理学版, 2006, 38(2): 107-112. |
| [13] | 赵沛基, 沈月毛, 彭丽萍, 甘烦远. 云南红豆杉离体胚的培养. 植物生理学通讯, 2003, 39(4): 327-329. |
| [14] | 王兵益, 苏建荣, 张志钧. 云南红豆杉种子贮藏过程中胚的变化. 林业科学研究, 2009, 22(1): 26-28. |
| [15] | 杨玲, 陈虎庚, 牛祖林, 石文雅. 浸种催芽对打破云南红豆杉种子休眠的初步研究. 湖北农业科学, 2011, 50(10): 2057-2059, 2063-2063. |
| [16] | Baskin J M, Baskin C C. A classification system for seed dormancy. Seed Science Research, 2004, 14(1): 1-16. |
| [17] | Finch-Savage W E, Leubner-Metzger G. Seed dormancy and the control of germination. New Phytologist, 2006, 171(3): 501-523. |
| [18] | Baskin J M, Baskin C C. Some considerations for adoption of Nikolaeva's formula system into seed dormancy classification. Seed Science Research, 2008, 18(3): 131-137. |
| [19] | 付婷婷, 程红焱, 宋松泉. 种子休眠的研究进展. 植物学报, 2009, 44(5): 629-641. |
| [20] | 张雪梅, 龙雯虹, 荣剑. 红豆杉种子休眠机理及休眠解除研究进展. 西南林业大学学报, 2012, 32(5): 92-95. |
| [21] | 国家标准总局. GB 2772-1999, 林木种子检验规程. 北京: 中国标准出版社, 1999. |
| [22] | 宋松泉, 程红炎, 龙春林, 姜孝成. 种子生物学研究指南. 北京: 科学出版社. 2005. |
| [23] | 尚旭岚, 徐锡增, 方升佐. 青钱柳种子休眠机制. 林业科学, 2011, 47(3): 68-74. |
| [24] | Le Page Degivry M T. Non-acidic inhibitors and embryo dormancy in Taxus baccata. Physiologia Plantarum, 1977, 41(1): 85-88. |
| [25] | 高红兵, 吴榜华, 孙振良. 东北红豆杉种子层积过程中内源生长素和脱落酸含量的变化. 吉林林学院学报, 1998, 14(4): 187-189. |
| [26] | 朱念德, 刘蔚秋, 伍建军, 廖文波. 影响南方红豆杉种子萌发因素的研究. 中山大学学报: 自然科学版, 1999, 38(2): 75-79. |
| [27] | 黄儒珠, 郭祥泉, 方兴添, 李玉蕾. 变温层积处理对南方红豆杉种子生理生化特性的影响. 福建师范大学学报: 自然科学版, 2006, 22(2): 95-98. |
| [28] | 张艳杰, 高捍东, 鲁顺保. 南方红豆杉种子中发芽抑制物的研究. 南京林业大学学报: 自然科学版, 2007, 31(4): 51-56. |
 2015, Vol. 35
2015, Vol. 35




