文章信息
- 王穗子, 金则新, 李月灵, 谷银芳
- WANG Suizi, JIN Zexin, LI Yueling, GU Yinfang
- 铜胁迫条件下AMF对海州香薷光合色素含量、抗氧化能力和膜脂过氧化的影响
- Effects of arbuscular mycorrhizal fungi inoculation on the photosynthetic pigment contents, anti-oxidation capacity and membrane lipid peroxidation of Elsholtzia splendens leaves under copper stress
- 生态学报, 2015, 35(23): 7699-7708
- Acta Ecologica Sinica, 2015, 35(23): 7699-7708
- http://dx.doi.org/10.5846/stxb201407251511
-
文章历史
- 收稿日期: 2014-07-25
- 网络出版日期: 2015-05-19
2. 三峡库区生态环境教育部重点实验室, 重庆 400715;
3. 台州学院生态研究所, 台州 318000;
4. 浙江省植物进化生态学与保护重点实验室, 台州 318000;
5. 上海师范大学生命与环境科学学院, 上海 200234
2. Key Laboratory of Eco environments in Three Gorges Reservoir Region of the Ministry of Education, Chongqing 400715, China;
3. Institute of Ecology, Taizhou University, Taizhou 318000, China;
4. Zhejiang Provincial Key Laboratory of Plant Evolutionary and Conservation, Taizhou 318000, China;
5. School of Life and environment Science, Shanghai Normal University, Shanghai 200234, China
海州香薷(Elsholtzia splendens)属唇形科(Labiatae)的一年生草本植物,又名铜草,为Cu矿的指示植物。海州香薷野生资源丰富,生物量较大,是一种有潜力的Cu污染土壤的修复植物[1, 2]。Cu矿区的海州香薷叶片Cu含量为18—391 μg/g,根部为700—800 μg/g[3],海州香薷主要积累大量Cu于根部,而限制其向地上部分运输[1]。Yang等[4]认为海州香薷是Cu的耐性和富集植物,开展水培实验发现其地上部分Cu累积超过1000 mg/kg。Cu是植物生长发育必需的微量元素,广泛参与植物各种生理代谢过程[5]。但是Cu浓度过高会影响植物光合作用,破坏蛋白质的代谢,影响矿质元素的吸收[6, 7, 8],并且会引起巯基依附于蛋白,使得蛋白失活或结构改变,将一些必需阳离子替换,产生自由基和活性氧,植物膜脂过氧化[9],使膜受到损伤,增加离子渗透[10],导致植物Cu毒害。为了抵御Cu胁迫带来的损伤,植物在一定范围内会产生超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)、抗坏血酸过氧化物酶(APX)等抗氧化酶和抗坏血酸(AsA)、还原型谷胱甘肽(GSH)等抗氧化剂,用于清除过量的活性氧,帮助植物抵抗逆境[11]。
丛枝菌根真菌(AMF)与80%以上陆生植物具有共生关系[12],接种AMF可以增强植物对水分与营养的吸收能力[13],进而提高植物对重金属的耐受性[14]。也有研究发现AMF通过改变植物细胞膜Zn2+转运基因MtZ-IP2的表达,从而减轻植物对重金属的吸收,缓解重金属对植物的毒害[15]。人工接种AMF将更利于海州香薷对Cu的耐受、吸收和积累[16, 17]。海州香薷在不同浓度Cu处理下,接种AMF植株地上部分的Cu含量增加,但在Cu浓度为400 mg/kg时,接种AMF和对照之间地上部分的Cu含量无显著性差异[18]。Wang等[16]通过对接种单一和混合菌种表明,在复合污染中接种混合AMF菌种显著增加海州香薷的生物量以及地上部分中的Cu、Zn、P、Pb的含量,提升了植物Cu、Zn、Pb、Cd的吸收能力。目前,已有较多重金属胁迫下接种AMF对植物膜脂过氧化程度、活性氧的产生以及抗氧化酶活性影响的报道,如重金属Cd胁迫下接种AMF,使秋茄(Kandelia candel)幼苗生物量增加,丙二醛(MDA)含量降低,植物抗氧化酶活性增加,减轻植物膜脂过氧化[19]。但鲜有在Cu胁迫条件下,接种AMF对海州香薷抗氧化能力影响的研究。
本研究通过室内盆栽实验,分析Cu胁迫条件下接种Cu矿区中与海州香薷共生多年的AMF对海州香薷光合色素含量、抗氧化能力、膜脂过氧化程度的影响,以期阐明AMF在海州香薷抗Cu胁迫过程中的作用,探讨AMF在提高海州香薷Cu耐性的生理机制。为进一步了解在Cu胁迫下,海州香薷如何适应环境的巨大压力,成为Cu矿区和Cu污染区优势种群提供理论依据。也为Cu污染土壤的修复和Cu矿区生态重建提供技术支撑。
1 材料和方法 1.1 供试材料海州香薷种子采自湖北省红安县无污染地区(31° 30.632′ N、114° 32.620′ E,海拔118 m),野外供接种土壤采自湖北省阳新县赤马山Cu矿(29° 59.776′ N、115° 05.856′ E,海拔138 m),供接种土壤的AMF孢子密度为每100 g土壤中780个孢子。栽培土壤为经过121 ℃灭菌2 h后的基质(泥炭土∶砂石∶蛭石=6∶3∶1)。于2013年5月上旬将海州香薷种子进行杀菌处理,放置于48孔穴盘中萌发。于2013年6月上旬,取大小相似长至6叶苗龄的幼苗,移栽至上盆口内直径19 cm、下盆口内直径12 cm、高15 cm的塑料圆盆中(内装有干重为1.7 kg的土壤),每盆一株且添加0.05 g复合肥,随机摆放于智能玻璃温室中进行继续培养。土壤基本理化性质为:pH值5.73,有机质20.16 g/kg,全氮14.61 mg/kg,有效磷17.86 mg/kg,速效钾56.67 mg/kg。
1.2 实验设计与处理采用两因素两水平完全随机设计,分为添加与不添加铜(Cu)以及接种与不接种AMF,共4个处理,即对照(CK)、添加Cu(Cu)、接种AMF(AMF)、添加Cu和接种AMF(Cu+AMF),每个处理15个重复。Cu的添加采用加入CuSO4溶液至Cu2+浓度达1000 mg/kg土壤,以添加等体积的无菌水作为不添加Cu的处理。接种AMF采用5%野外采集的土壤与95%基质(体积比),混匀后待用[20, 21]。为保证不接种和接种AMF土壤中的细菌、放线菌等微生物群落区系基本一致,参考Walling等[21]方法,在不接种AMF的土壤中加入5%野外采集的土壤(体积比)经11 μm滤膜(Whatman)过滤出的土壤浸提液50 mL。4种处理完成后,将土壤放置1周,正常浇水,待重金属平衡稳定后,将幼苗移栽于花盆中。所有植株按常规管理,保持水肥一致。温室培养条件:白天相对湿度为(70±10.5)%,晚上为(57±7.2)%,白天温度为(30.0±5)℃,夜间为(18.0±2)℃,自然光照条件。于2013年10月中旬,进行各项生理指标的测定,并收获植株。
1.3 指标测定 1.3.1 菌根侵染率测定取植物新鲜根系,用FAA固定液固定24 h以上,进行净化、软化、酸化、染色、脱色[22],每株植物随机选取细根30段(1 cm /每段),制成装片,于40倍显微镜下观察菌根侵染情况。菌根侵染率的计算按照下面公式进行:
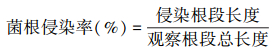
随机取相同部位的叶片,洗净并用蒸馏水冲洗,吸水纸将其擦干,待测。采用Arnon法[23]测定并计算叶绿素a (Chl a)、叶绿素b (Chl b)、总叶绿素(Chl (a+b))和类胡萝卜素(Car)的含量以及叶绿素a/b (Chl a/b)值。
1.3.3 抗氧化酶活性测定以样品鲜质量计算样品酶活性。超氧化物歧化酶(SOD)活性:采用Bewley等[24]的氮蓝四唑(NBT)光还原法测定。以560 nm时抑制NBT光化学还原50%的酶量为1个酶活性单位(U)。过氧化物酶(POD)活性:采用愈创木酚显色法测定。以每分钟内OD470变化0.01为1个酶活性单位(U)[23]。过氧化氢酶(CAT)活性:采用紫外吸收法测定。以每分钟内OD240降低0.01为1个酶活性单位(U)[25]。抗坏血酸过氧化物酶(APX)活性:采用Nakamo和Asada[26]的方法测定APX活性,以△A290每分钟降低1.0为一个酶活性单位(U)。
1.3.4 抗氧化剂含量测定抗坏血酸(AsA):红菲罗啉(BP)显色法[27]。还原型谷胱甘肽(GSH):5,5-二巯基-2,2-二硝基苯甲酸(5,5-Dithio-dintrob enzoic acid,DTNB)显色法[28]。
1.3.5 膜脂过氧化程度测定质膜相对透性(MRP)采用郝再彬等[29]的电导率法。丙二醛(MDA)含量测定参照李合生等[27]的硫代巴比妥酸(TBA)比色法。
1.3.6 生物量测定植株用蒸馏水清洗干净后,将其分为根、茎、叶、花序分别放入纸袋,105 ℃杀青20 min,80 ℃烘干至恒重。分别测定根、茎、叶、花序生物量,计算总生物量和根冠比。
1.4 统计分析4个处理之间单因子数据差异显著性采用单因素方差分析(One-way ANOVA)和LSD多重比较。添加Cu和接种AMF的交互作用对海州香薷各参数的差异显著性采用双因素方差分析(Two-way ANOVA)检验(SPSS 16.0)。用Origin8.5进行绘图。
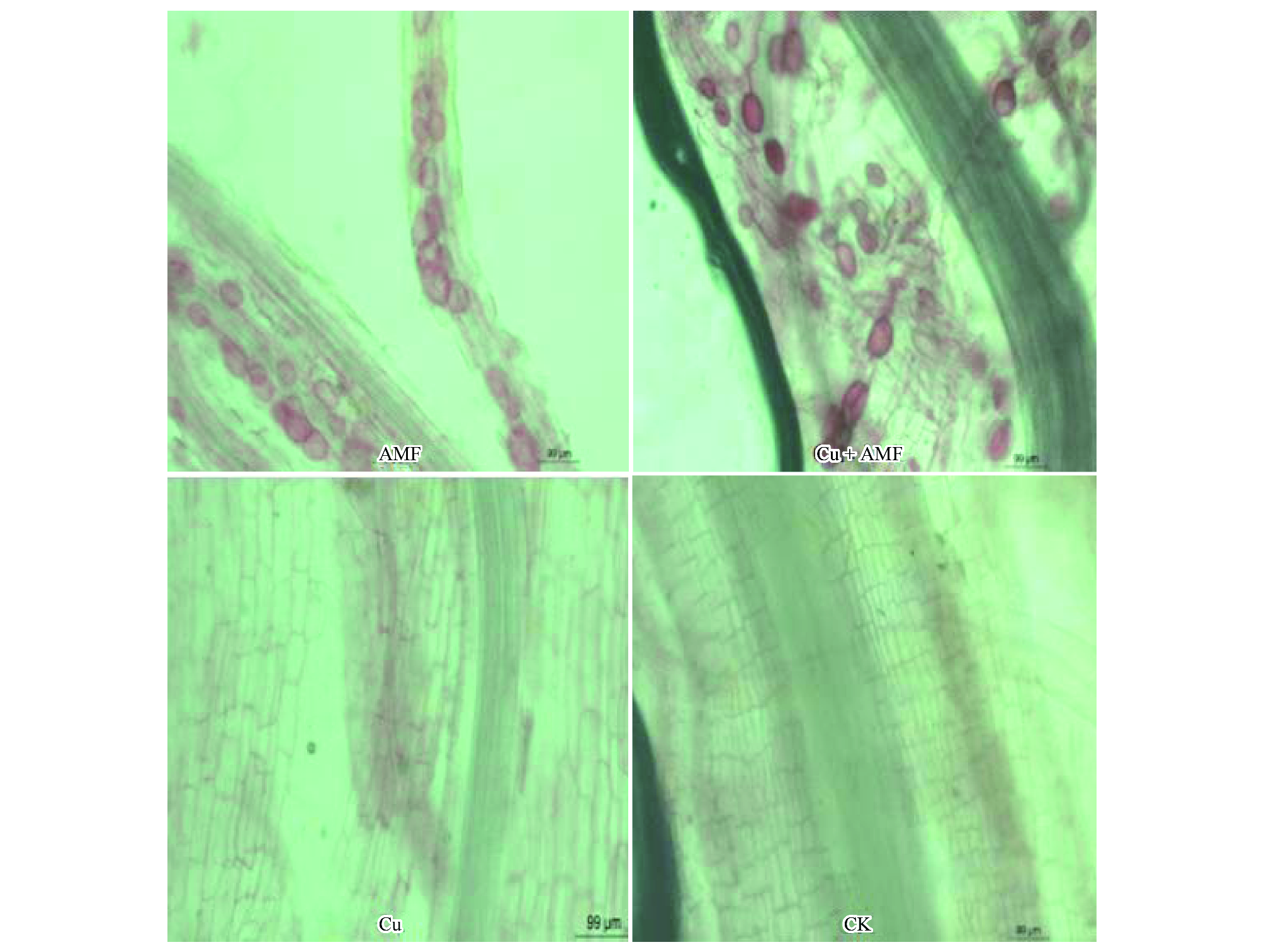
2 结果与分析 2.1 铜胁迫条件下接种AMF对海州香薷菌根侵染率的影响各处理海州香薷根系AMF侵染情况如图1所示。AMF处理海州香薷菌根侵染率为60.7%,Cu+AMF处理的根侵染率为57.3%。在40倍显微镜下,CK和Cu处理均未观测到明显的菌丝及囊泡结构,其侵染率均为0。表明无论Cu胁迫与否,接种AMF对海州香薷根系均具有良好的侵染效果。
|
| 图 1 不同处理下海州香薷根系丛枝菌根真菌侵染的情况 Fig.1 Mycorrhizal colonization of E. splendens roots under different treatments CK:对照; Cu:添加铜; AMF:接种丛枝菌根真菌; Cu+AMF:添加铜+接种丛枝菌根真菌 |
不同处理的海州香薷叶片Chl (a+b)含量大小为:AMF>CK>Cu+AMF>Cu,它们之间均差异显著(表1),接种AMF叶片Chl (a+b)含量比CK增加了17.9%,Cu处理则比CK下降了55.1%,而Cu+AMF处理较Cu处理增加了34.8%。4种处理海州香薷叶片Chl a和Chl b含量大小顺序与Chl (a+b)相同,各处理之间均差异显著。与CK相比,接种AMF的Chl a和Chl b含量分别增加了20.0%和12.6%,Cu处理分别降低了56.2%和52.6%。Cu+AMF处理比Cu处理的Chl a、Chl b含量分别增加了36.7%和30.6%,表明Cu胁迫下接种AMF可显著提高叶片叶绿素含量。
| 处理 Treatments | 叶绿素a Chl a/(mg/g) | 叶绿素b Chl b/(mg/g) | 叶绿素a+b Chl(a+b)/(mg/g) | 叶绿素a/b Chl a/b | 类胡萝卜素 Car /(mg/g) |
| CK:对照; Cu:添加铜; AMF:接种丛枝菌根真菌; Cu+AMF:添加铜+接种丛枝菌根真菌; 表中数值为平均值±标准差,同列数据中不同小写字母表示差异显著(P<0.05);* P<0.05;** P<0.01 | |||||
| CK | 1.08±0.07b | 0.46± 0.05b | 1.54± 0.12b | 2.35± 0.17ab | 0.27± 0.03a |
| Cu | 0.47± 0.09d | 0.22± 0.04d | 0.69± 0.12d | 2.17± 0.09c | 0.13± 0.01b |
| Cu+AMF | 0.65± 0.09c | 0.29± 0.04c | 0.93± 0.13c | 2.26± 0.17bc | 0.15± 0.02b |
| AMF | 1.30± 0.07a | 0.52± 0.05a | 1.82± 0.12a | 2.45± 0.13a | 0.27± 0.03a |
| F | |||||
| Cu | 310.66** | 146.09** | 262.70** | 11.55** | 128.69** |
| AMF | 29.91** | 10.18** | 23.24** | 4.09 | 1.30 |
| Cu×AMF | 0.13 | 0.05 | 0.11 | 0.13 | 0.63 |
海州香薷叶片Chl a/b以接种AMF最高,与Cu处理、Cu+AMF处理差异显著;Cu处理最低,比CK降低了7.5%,差异显著(表1)。Cu处理、Cu+AMF处理的Car含量分别比CK降低了49.8%和43.1%,差异显著。接种AMF的Car含量显著高于Cu处理、Cu+AMF处理。
经双因素方差分析(表1),Cu处理对植株叶片Chl a、Chl b、Chl (a+b)、Car含量和Chl a/b作用均极显著;接种AMF对Chl a、Chl b、Chl (a+b)影响极显著;而两者的交互作用对光合色素各指标均无显著影响。
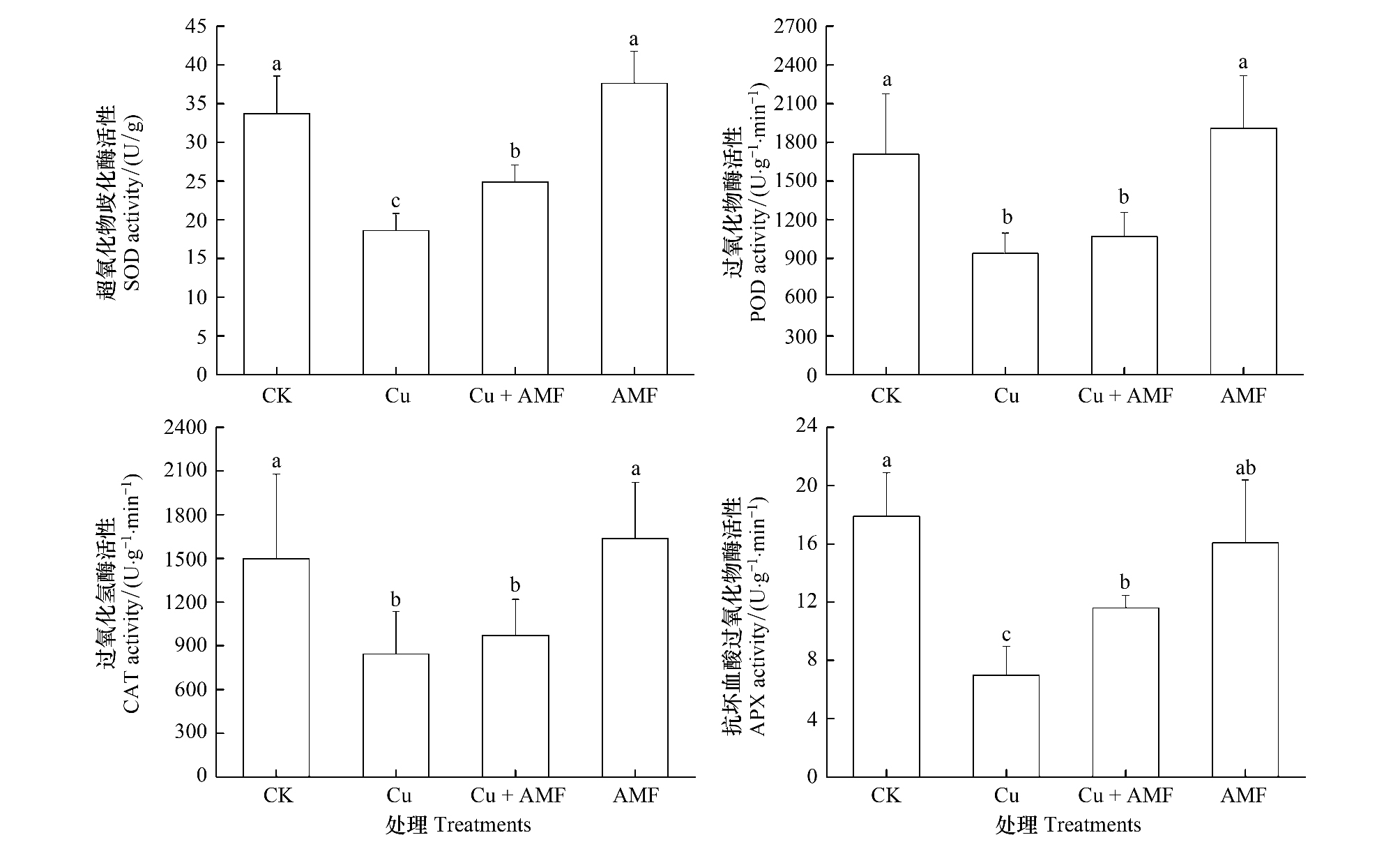
2.3 铜胁迫条件下接种AMF对海州香薷抗氧化能力的影响 2.3.1 铜胁迫条件下接种AMF对海州香薷抗氧化酶活性的影响Cu、Cu+AMF处理的SOD、POD、CAT、APX活性均低于CK,差异显著。而Cu+AMF处理的SOD、APX活性比Cu处理分别提高了33.7%和66.1%,差异显著(图2)。表明Cu胁迫使得海州香薷叶片SOD、POD、CAT和APX的活性降低,而Cu胁迫下接种AMF可明显提高SOD、APX的活性。
|
| 图 2 不同处理海州香薷叶片超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)、抗坏血酸过氧化物酶(APX)活性的比较 Fig.2 The comparison of superoxide dismutase (SOD), peroxidase (POD), catalase (CAT) and ascorbate peroxidase (APX) activities in E. splendens leaves under different treatments CK:对照; Cu:添加铜; AMF:接种丛枝菌根真菌; Cu+AMF:添加铜+接种丛枝菌根真菌 |
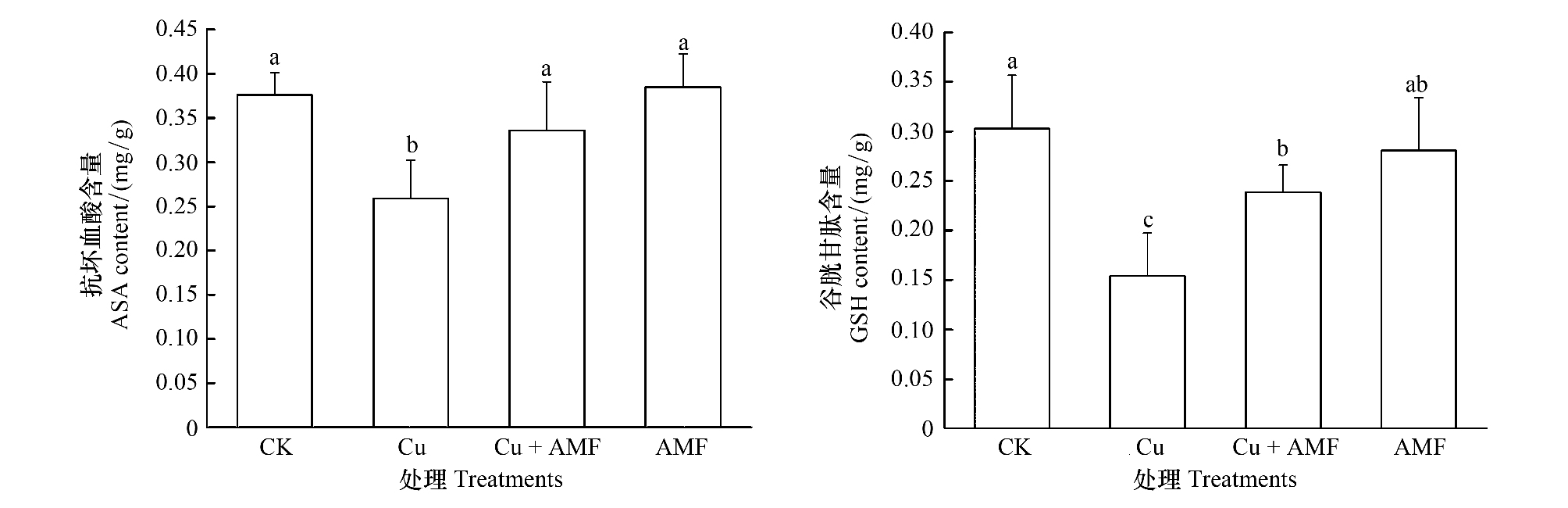
海州香薷叶片AsA、GSH含量均以Cu处理最低,仅为CK 的69.0%、49.1%,与AMF、Cu+AMF、CK均差异显著(图3);Cu+AMF处理的AsA、GSH含量分别比Cu处理增加了29.6%和55.1%,差异显著。Cu+AMF处理的GSH含量低于CK,差异显著。
|
| 图 3 不同处理海州香薷叶片抗坏血酸(AsA)和谷胱甘肽(GSH)含量的比较 Fig.3 The comparison of ascorbic acid (AsA) and glutathione (GSH) contents in E. splendens leaves under different treatments CK:对照; Cu:添加铜; AMF:接种丛枝菌根真菌; Cu+AMF:添加铜+接种丛枝菌根真菌。不同小写字母表示差异显著(P<0.05) |
双因素方差分析表明(表2),Cu胁迫处理对海州香薷叶片抗氧化酶活性和抗氧化剂含量的影响均达到了极显著水平,AMF处理仅对叶片APX活性和AsA含量影响显著,Cu胁迫与接种AMF交互作用对海州香薷叶片GSH含量的影响达到显著水平。
| F | 超氧化物 歧化酶SOD | 过氧化物酶 POD | 过氧化氢酶 CAT | 抗坏血酸 过氧化物酶 APX | 谷胱甘肽 GSH | 抗坏血酸 AsA | 丙二醛 MDA | 质膜相对透性 MRP |
| SOD:superoxide dismutase; POD:peroxidase; CAT:catalase; APX:ascorbate peroxidase; GSH:glutathione; AsA:ascorbic acid; MDA:malondialdehyde; MRP:membrane relative permeability; Cu:添加铜; AMF:接种丛枝菌根真菌; Cu×AMF:添加铜×接种丛枝菌根真菌; * P<0.05; ** P<0.01 | ||||||||
| Cu | 46.64** | 29.06** | 13.80** | 36.60** | 21.58** | 19.79** | 26.96** | 201.26** |
| AMF | 2.05 | 1.28 | 0.56 | 6.41* | 2.35 | 5.31* | 3.92 | 7.67* |
| Cu×AMF | 0.15 | 0.06 | 0.00 | 1.21 | 6.76* | 3.33 | 2.71 | 11.41** |
海州香薷植株叶片MDA含量以Cu处理最高,为CK 的161.5%,与Cu+AMF、AMF、CK均差异显著(图4);Cu+AMF处理显著高于AMF、CK。Cu+AMF处理叶片MDA含量为Cu处理的的79.8%,可看出Cu胁迫下接种AMF显著降低了MDA的含量。
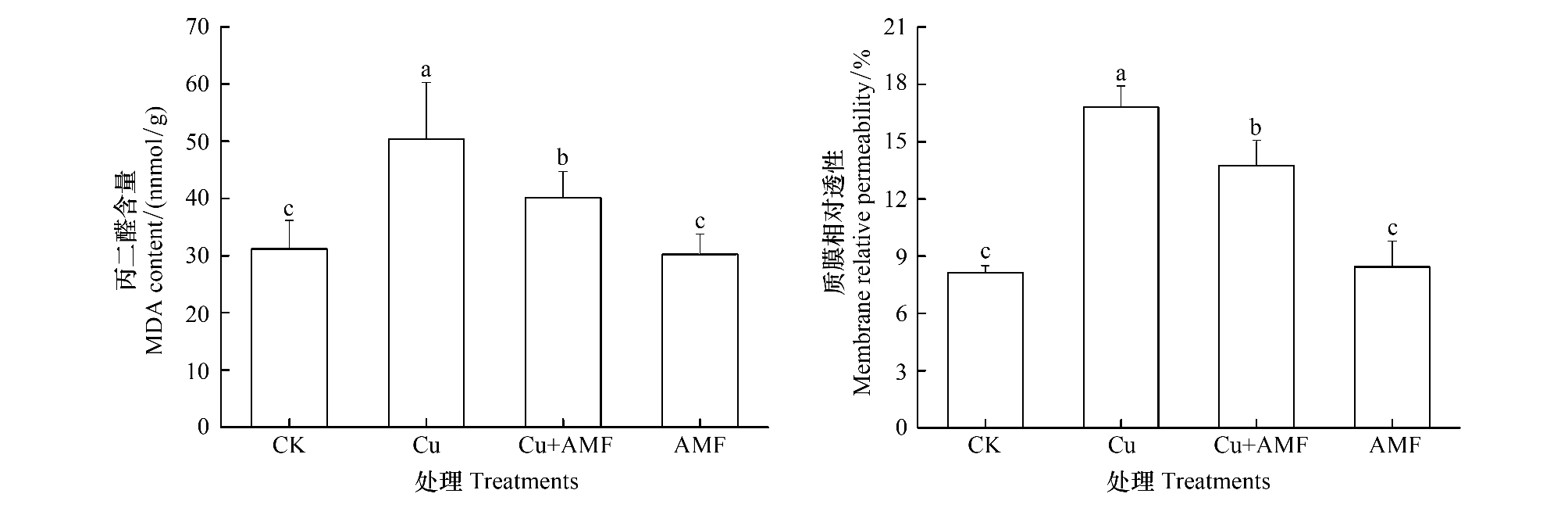
|
| 图 4 不同处理海州香薷叶片丙二醛(MDA)含量和质膜相对透性(MRP)的比较 Fig.4 The comparison of malondialdehyde (MDA) content and membrane relative permeability (MRP) in E. splendens leaves under different treatments CK:对照; Cu:添加铜; AMF:接种丛枝菌根真菌; Cu+AMF:添加铜+接种丛枝菌根真菌。不同小写字母表示差异显著(P<0.05) |
海州香薷叶片MRP也以Cu处理最高,为CK的206.3%。与Cu+AMF、AMF、CK均差异显著(图4);Cu+AMF处理显著高于AMF、CK。Cu+AMF处理的叶片MRP是Cu处理的82.0%,同样可看出,在Cu胁迫下接种AMF显著降低了叶片MRP。
双因素方差分析可看出(表2),Cu胁迫对海州香薷叶片MDA含量和MRP的影响均达到了极显著水平。接种AMF仅对海州香薷叶片MRP具显著性影响。添加Cu及接种AMF交互作用对海州香薷叶片MRP影响达到极显著水平。
2.5 铜胁迫条件下接种AMF对海州香薷生物量的影响由表3可看出,Cu处理的海州香薷根、茎、叶、花序生物量和总生物量分别比CK下降了67.1%、72.4%、31.2%、75.2%和64.4%,Cu胁迫使得海州香薷各器官和总生物量明显降低。而Cu处理下接种AMF海州香薷根、茎、叶、花序和总生物量分别比Cu处理提高了36.1%、138.9%、47.3%、68.4%和79.7%,表明接种AMF可缓解Cu胁迫对植株的影响。
| 处理 Treatments | 根生物量 Root biomass/g | 茎生物量 Stem biomass/g | 叶生物量 Leaf biomass/g | 花序生物量 Inflorescence biomass/g | 总生物量 Total biomass/g | 根冠比 Root-Shoot Ratio |
| Cu:添加铜; AMF:接种丛枝菌根真菌; Cu+AMF:添加铜+接种丛枝菌根真菌; 表中数值为平均值±标准差,同列数据中不同小写字母表示差异显著(P<0.05);* P<0.05; ** P<0.01 | ||||||
| CK | 6.27±0.71a | 16.05±2.44b | 6.79±1.06a | 7.33±1.23b | 36.44±3.71a | 0.21±0.04a |
| Cu | 2.06±0.65b | 4.43±1.00d | 4.67±0.78b | 1.82±0.44d | 12.98±2.11c | 0.19±0.05a |
| Cu+AMF | 2.81±0.49b | 10.59±1.20c | 6.87±0.58a | 3.06±0.68c | 23.33±1.81b | 0.14±0.03b |
| AMF | 5.45±0.75a | 20.32±3.18a | 5.89±1.22ab | 5.82±0.74a | 37.48±4.08a | 0.17±0.02ab |
| F | ||||||
| Cu | 134.58** | 123.15** | 1.82 | 125.70** | 185.75** | 2.81 |
| AMF | 0.02 | 29.34** | 2.41 | 0.13 | 17.03** | 8.33** |
| Cu×AMF | 7.03* | 0.97 | 13.53** | 13.90** | 11.38** | 0.09 |
双因素方差分析表明(表3),Cu处理对植株根、茎、花序生物量和总生物量的影响均极显著;接种AMF对植株茎生物量、总生物量及根冠比影响极显著;接种AMF和Cu胁迫交互作用对根生物量影响显著,对叶、花序和总生物量影响极显著。
3 讨论植物在受到胁迫时会导致光合色素含量发生变化,从而改变其光合能力[30]。本研究表明,Cu胁迫显著降低了海州香薷叶片中叶绿素含量,而接种AMF可以显著增加叶绿素含量。这是由于植物在受到重金属胁迫时,叶绿体酶活性比例失调,叶绿素快速分解,并且重金属离子改变了合成叶绿素的几种重要酶的肽链的SH部分,从而抑制了叶绿素的合成[31]。而在Cu胁迫下接种AMF后,能在海州香薷根外生出很多菌丝,大大增加根部的吸收面积,帮助吸收水分和营养元素;另外AMF能降低海州香薷根系对Cu的吸收[18],缓解Cu对植物造成的损伤,使得叶绿素含量显著提高。叶绿素含量的提高,有利于光合作用能力的增强,促进体内有机物的积累,从而提高了植株的生物量。
细胞膜作为植物调节和控制细胞内外物质运输和交换的重要结构[32],在逆境胁迫时,植物体内会产生大量的活性氧,活性氧的积累会造成膜脂过氧化,其重要产物是丙二醛(MDA)[33]。在本试验中,Cu处理的海州香薷叶片MDA含量、质膜透性均显著高于其它处理,表明Cu胁迫导致细胞结构发生变化,Cu可与细胞膜蛋白的巯基或磷脂分子层的磷脂类物质反应,造成膜蛋白磷脂结构改变,膜透性增大。此外,Cu胁迫会使海州香薷叶片产生大量的活性氧,活性氧的积累加重细胞膜脂过氧化程度,使得细胞的正常生命活动受到干扰,植物生长异常。在Cu胁迫下接种AMF后,海州香薷叶片MDA含量和质膜透性虽然比CK显著增加,但比Cu处理显著降低,减轻了Cu胁迫造成的膜脂过氧化程度,缓解Cu胁迫对海州香薷造成的危害。这与丛枝菌根真菌根内球囊霉、幼套球囊霉能显著降低Cu污染土壤中白三叶(Trifolium repens)地上部分MDA含量相似[34]。
植物体内存在着酶促(SOD、POD、CAT、APX等)和非酶促(AsA、GSH等)两类活性氧自由基清除系统,对维持膜结构的完整性和防御活性氧自由基对膜脂的攻击引起的伤害有重要作用。正常情况下,SOD、POD、CAT和APX及其它保护性物质能够维持自由基在植物体内产生和清除的动态平衡。本研究发现,Cu处理的海州香薷叶片SOD、POD、CAT、APX活性和AsA、GSH含量均显著低于CK,表明在较强的Cu胁迫下,细胞中活性氧自由基积累到一定程度,会使抗氧化酶的结构破坏或活性降低[35],抗氧化剂的含量下降。而在Cu胁迫下接种AMF后,海州香薷叶片的SOD、APX的活性显著提高,AsA、GSH的含量显著增大,植株对氧自由基的清除能力增强,减缓活性氧对植物体内的伤害和膜脂过氧化程度,提高了海州香薷的抗逆性。
Cu处理下明显抑制了海州香薷的生长,使植株的根、茎、叶、花序生物量和总生物量比CK显著下降。这是因为Cu胁迫下叶片的光合色素含量下降,植物的光合作用能力减弱,有机物质积累减少;叶片的抗氧化酶活性和抗氧化剂含量明显下降;膜透性增大,造成膜结构改变,危害植物的生长,这些均可导致Cu胁迫下植物生物量的下降。但Cu胁迫下接种AMF后,AMF为了帮助自己和宿主植物能在Cu污染土壤中存活,主要采用躲避和区域化分布策略。一方面限制Cu进入细胞质,通过分泌大量球囊霉素,帮助土壤形成团聚体,形成Cu-球囊霉素复合物,从而降低Cu的生物利用率[36]。另一方面通过特殊的金属转运蛋白,使Cu进入一些亚细胞结构如液泡等,以及根外孢子和根内囊泡中,从而减少Cu的毒害。此外,AMF对Cu引起的氧化胁迫进行响应,并修复氧化胁迫引起的损伤[37]。由于接种AMF后,能缓解Cu胁迫对其的伤害,因此,海州香薷生物量显著增加。
综上所述,接种AMF可提高Cu胁迫下海州香薷叶片的叶绿素含量、抗氧化酶活性、抗氧化物含量,降低MDA含量和质膜透性,增加植株的生物量。说明AMF可以通过提高Cu胁迫下海州香薷叶片光合色素含量和抗氧化能力,来增强植物光合作用能力和降低膜脂过氧化水平,从而缓解Cu胁迫对海州香薷造成的伤害,促进植物生长,提高植株的生物量,增强海州香薷对Cu胁迫的适应性,成为Cu矿区和Cu污染区的优势种群。本研究供接种的AMF取自Cu矿区土壤,取材容易,操作简便,可广泛应用于Cu污染土壤、Cu矿区的生态修复和重建中。
| [1] | Song J, Zhao F J, Luo Y M, McGrath S P, Zhang H. Copper uptake by Elsholtzia splendens and Silene vulgaris and assessment of copper phytoavailability in contaminated soils. Environmental Pollution, 2004, 128(3): 307-315. |
| [2] | Weng G Y, Wu L H, Wang Z Q, Christie P. Copper uptake by four Elsholtzia ecotypes supplied with varying levels of copper in solution culture. Environment International, 2005, 31(6): 880-884. |
| [3] | Lou L Q, Shen Z G, Li X D. The copper tolerance mechanisms of Elsholtzia haichowensis, a plant from copper-enriched soils. Environmental and Experimental Botany, 2004, 51(2): 111-120. |
| [4] | Yang M J, Yang X E, Römheld V. Growth and nutrient composition of Elsholtzia splendens Nakai under copper toxicity. Journal of Plant Nutrition, 2002, 25(7): 1359-1375. |
| [5] | Kim B E, Nevitt T, Thiele D J. Mechanisms for copper acquisition, distribution and regulation. Nature Chemical Biology, 2008, 4(3): 176-185. |
| [6] | Kováik J, Klejdus B, Hedbavny J, Ba kor M. Effect of copper and salicylic acid on phenolic metabolites and free amino acids in Scenedesmus quadricauda (Chlorophyceae). Plant Science, 2010, 178(3): 307-311. |
| [7] | Li J M, Jin Z X, Gu Q P. Effect of plant species on the function and structure of the bacterial community in the rhizosphere of lead-zinc mine tailings in Zhejiang, China. Canadian Journal of Microbiology, 2011, 57(7): 569-577. |
| [8] | 沈章军, 孙庆业, 田胜尼. 铜尾矿自然定居白茅对体内氮磷的适时分配及叶片氮磷代谢调节酶活性动态. 植物生态学报, 2012, 36(2): 159-168. |
| [9] | Andre C M, Larondelle Y, Evers D. Dietary antioxidants and oxidative stress from a human and plant perspective: a review. Current Nutrition and Food Science, 2010, 6(1): 2-12. |
| [10] | Chamseddine M, Wided B A, Guy H, Marie-Edith C, Fatma J. Cadmium and copper induction of oxidative stress and antioxidative response in tomato (Solanum lycopersicon) leaves. Plant Growth Regulation, 2009, 57(1): 89-99. |
| [11] | Thounaojam T C, Panda P, Mazumdar P, Kumar D, Sharma G D, Sahoo L, Panda S K. Excess copper induced oxidative stress and response of antioxidants in rice. Plant Physiology and Biochemistry, 2012, 53: 33-39. |
| [12] | Wang B, Qiu Y L. Phylogenetic distribution and evolution of mycorrhizas in land plants. Mycorrhiza, 2006, 16(5): 299-363. |
| [13] | 罗巧玉, 王晓娟, 林双双, 李媛媛, 孙莉, 金樑. AM真菌对重金属污染土壤生物修复的应用与机理. 生态学报. 2013, 33(13): 3898-3906. |
| [14] | Rodriguez R J, Henson J, van Volkenburgh E, Hoy M, Wright L, Beckwith F, Kim Y, Resman R S. Stress tolerance in plants via habitat-adapted symbiosis. Multidisciplinary Journal of Microbial Ecology, 2008, 2(4): 404-416. |
| [15] | Burleigh S H, Kristensen B K, Bechmann I E. A plasma membrane zinc transporter from Medicago truncatula is up-regulated in roots by Zn fertilization, yet down-regulated by arbuscular mycorrhizal colonization. Plant Molecular Biology, 2003, 52(5): 1077-1088. |
| [16] | Wang F Y, Lin X G, Yin R. Heavy metal uptake by arbuscular mycorrhizas of Elsholtzia splendens and the potential for phytoremediation of contaminated soil. Plant and Soil, 2005, 269(1-2): 225-232. |
| [17] | Wang F Y, Lin X G, Yin R. Role of microbial inoculation and chitosan in phytoextraction of Cu, Zn, Pb and Cd by Elsholtzia splendens-a field case. Environmental Pollution, 2007, 147(1): 248-255. |
| [18] | 王发园, 林先贵, 尹睿. 丛枝菌根真菌对海州香薷生长及其Cu吸收的影响. 环境科学, 2005, 26(5): 174-180. |
| [19] | 谢翔宇, 翁铂森, 赵素贞, 严重玲. Cd胁迫下接种丛枝菌根真菌对秋茄幼苗生长与抗氧化酶系统的影响. 厦门大学学报: 自然科学版, 2013, 52(2): 244-253. |
| [20] | Lau J A, Lennon J T. Evolutionary ecology of plant-microbe interactions: soil microbial structure alters selection on plant traits. New Phytologist, 2010, 192(1): 215-224. |
| [21] | Walling S Z, Zabinski C A. Defoliation effects on arbuscular mycorrhizae and plant growth of two native bunchgrasses and an invasive forb. Applied Soil Ecology, 2006, 32(1): 111-117. |
| [22] | Phillips J M, Hayman D S. Improved procedures for clearing roots and staining parasitic and vesicular-arbuscular mycorrhizal fungi for rapid assessment of infection. Transactions of the British Mycological Society, 1970, 55(1): 158-161. |
| [23] | 张志良, 翟伟菁. 植物生理学实验指导(第3版). 北京: 高等教育出版社, 2004. |
| [24] | Bewley T D. Physiological aspects of desiccation tolerance. Annual Review of Plant Physiology, 1979, 30: 195-238. |
| [25] | 何冰, 叶海波, 杨肖娥. 铅胁迫下不同生态型东南景天叶片抗氧化酶活性及叶绿素含量比较. 农业环境科学学报, 2003, 22(3): 274-278. |
| [26] | Nakano Y, Asada K. Hydrogen peroxide is scavenged by ascorbate-specific peroxidase in spinach chloroplasts. Plant Cell Physiology, 1987, 22(5): 867-880. |
| [27] | 李合生, 孙群, 赵世杰. 植物生理生化实验原理和技术. 北京: 高等教育出版社, 2000. |
| [28] | 於丙军, 刘友良. 盐胁迫对一年生盐生野大豆幼苗活性氧代谢的影响. 西北植物学报, 2003, 23(1): 18-22. |
| [29] | 郝再彬, 苍晶, 徐仲. 植物生理实验. 哈尔滨: 哈尔滨工业大学出版社, 2004. |
| [30] | CambrolléJ, Mancilla-Leytón J M, Muñoz-Vallés S, Figueroa-Luque E, Luque T, Figueroa M E. Effects of copper sulfate on growth and physiological responses of Limoniastrum monopetalum. Environmental Science and Pollution Research, 2013, 20(12): 8839-8847. |
| [31] | Jeon M W, Ali M B, Hahn E J, Paek K Y. Photosynthetic pigments, morphology and leaf gas exchange during ex vitro acclimatization of micropropagated CAM Doritaenopsis plantlets under relative humidity and air temperature. Environmental and Experimental Botany, 2006, 55(1-2): 183-194. |
| [32] | 江玲, 杨芸, 徐卫红, 王崇力, 陈蓉, 熊仕娟, 谢文文, 张进忠, 熊治庭, 王正银, 谢德体. 黑麦草-丛枝菌根对不同番茄品种抗氧化酶活性、镉积累及化学形态的影响. 环境科学, 2014, 35(6): 2349-2357. |
| [33] | Abuja P M, Lohner K, Prassl R. Modification of the lipid-protein interaction in human low-density lipoprotein destabilizes ApoB-100 and decreases oxidizability. Biochemistry, 1999, 38(11): 3401-3408. |
| [34] | 肖家欣, 安静, 杨安娜, 吴雪俊. 五种丛枝菌根真菌对白三叶耐铜污染的影响. 中国草地学报, 2011, 33(6): 57-63. |
| [35] | 王春乙, 白月明, 温民, 黄辉. CO2和O3浓度倍增及复合效应对大豆生长和产量的影响. 环境科学, 2004, 25(6): 6-10. |
| [36] | Cornejo P, Meier S, Borie G, Rillig M C, Borie F. Glomalin-related soil protein in a Mediterranean ecosystem affected by a copper smelter and its contribution to Cu and Zn sequestration. Science of the Total Environment, 2008, 406(1-2): 154-160. |
| [37] | Ferrol N, González-Guerrero M, Valderas A, Benabdellah K, Azcón-Aguilar C. Survival strategies of arbuscular mycorrhizal fungi in Cu-polluted environments. Phytochemistry Reviews, 2009, 8(3): 551-559. |
 2015, Vol. 35
2015, Vol. 35




