文章信息
- 刘会玉, 林振山, 齐相贞, 刘金雪, 许晓娟
- LIU Huiyu, LIN Zhenshan, QI Xiangzhen, LIU Jinxue, XU Xiaojuan
- 基于个体的空间显性模型和遥感技术模拟入侵植物扩张机制
- The dispersal mechanism of invasive plants based on a spatially explicit individual-based model and Remote sensing technology: a case study of Spartina alterniflora
- 生态学报, 2015, 35(23): 7794-7802
- Acta Ecologica Sinica, 2015, 35(23): 7794-7802
- http://dx.doi.org/10.5846/stxb201405090918
-
文章历史
- 收稿日期: 2014-05-09
- 网络出版日期: 2015-05-19
2. 江苏省环境演变与生态建设重点实验室, 南京 210023;
3. 江苏省地理信息资源开发与利用协同创新中心, 南京 210023
2. Jiangsu Key Laboratory of Environmental Change and Ecological Construction, Nanjing 210023, China;
3. Jiangsu Center for Collaborative Innovation in Geographical Information Resource Development and Application, Nanjing 210023, China
外来入侵植物在生长、繁殖和竞争等方面具有非常显著的优势,对本地生态系统构成极大威胁,被认为是仅次于栖息地毁坏的全球生物多样性减少的第二大因素[1]。随着全球化进程的加快,新的生物入侵风险进一步加剧,已成为21世纪五大全球性环境问题之一[2]。要有效地预防和控制生物入侵,必须能准确地预测其种群扩张,揭示其入侵机制,从而制定合适的长期的管理策略[3]。
理论模型可以研究入侵植物的种群扩张潜力,确定对种群扩张有重要影响的生物和非生物因子,更为重要的是,可以作为管理工具来制定一些经济有效的目标控制策略[4]。已有模型模拟了外来入侵植物的种群动态[5, 6, 7]及其控制策略[8, 9]。然而这些研究,或者没有考虑物种的生活史特征[6, 8]或者没有考虑景观异质性和土地利用的变化[5, 6, 7, 8, 9]。基于个体的空间显性模型不仅考虑了外来植物的生活史特征,还可以结合扩散过程和非生物因子,被广泛用来模拟种群动态[10]。遥感技术是从大尺度上研究影响植物入侵的植被格局变化的重要工具[11]。因此,基于个体的空间显性模型与遥感的结合,能很好地模拟外来植物入侵动态,并揭示其入侵机制,被广泛应用于生态学各个领域[10]。然而,很少有研究将基于个体的空间显性模型与遥感相结合,来考虑土地利用的时空变化对外来入侵植物的影响[12, 13]。
互花米草(Spartina alterniflora)原产于北美海岸带,在20世纪70年代末引入中国,由于耐盐、耐淹、繁殖力强等特点,迅速地在沿海11个省扩展[14]。互花米草具有有性繁殖与无性繁殖两种繁殖方式。其借助种子占据新生境后,通过无性繁殖扩张成入侵斑块,并连接成片,形成浓密的互花米草草地。互花米草与本地种芦苇和碱蓬等竞争,并最终取代它们,对本地生态系统造成了严重的破坏[14, 15]。因此,控制互花米草扩张对于保护盐沼地生态系统来说十分重要。本文以互花米草为例,通过基于个体的空间显性模型,结合遥感技术,模拟其扩张动态,并揭示其扩张机制,以期为控制互花米草入侵提供科学建议,并为研究其它外来入侵植物种群扩张提供理论依据与方法体系。
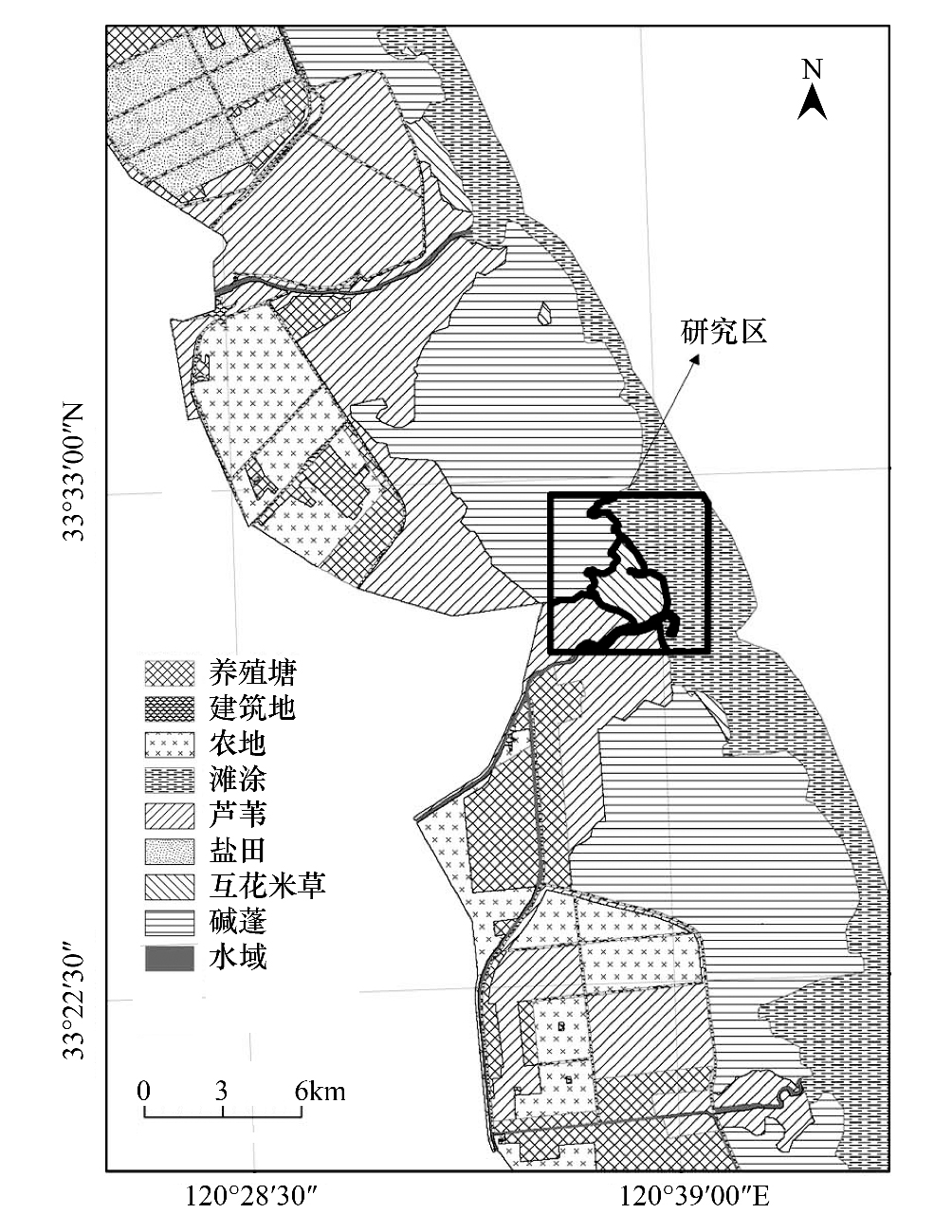
1 研究区概况和数据来源 1.1 研究区概况研究区位于江苏省盐城市斗龙港附近(33°28′—33°35′N,120°35′—120°41′E),其潮间带盐沼地植被保持相对完整。该研究区位于亚热带和温带之间,具有较强的温带海洋和季风潮湿气候,年均温大概为13.8°C,年降水量大概为1023.8 mm,其中60%的降水集中在夏季。
1.2 数据来源尽管互花米草在20世纪80年代引入江苏省,然而在本研究区直到1995年后才能从遥感图像中获取足够的信息来提取其分布。同时,由于遥感影像资料的有限性和解译的难度,本研究仅提取了1997,1999,2001,2003,2005和2006年土地利用类型的变化对互花米草的影响,并以2010年的实际分布对模型进行评价。所有遥感影像成像于互花米草生长期或者能够清晰与其它植被区分的季节。其中,1995—2005年的遥感数据来自Landsat Thematic Mapper (TM) 和Enhanced Thematic Mapper (ETM+),空间分辨率为30 m,而2006和2010年的数据来自Advanced Land Observing Satellite data (ALOS),空间分辨率为10 m。
2 研究方法 2.1 遥感影像解译首先,在ERDAS9.0中进行几何校正,通过缨帽转换和归一化植被指数方法对遥感影像进行光谱增强。其次,利用最大似然法进行监督分类,将土地利用类型分为9大类:水体、滩涂、水产地、盐田、建筑用地、农田、互花米草、碱蓬和芦苇。同时,将监督分类所得影像在ARCMAP9.0中成图。将ALOS遥感影像解译的结果进行重采样,使其空间分辨率为30 m。最终,将研究区分割为160×160个栅格(每个栅格的大小为30 m×30 m)。
2.2 基于个体的空间显性模型 2.2.1 模型的设计为了预测外来入侵植物的种群动态,本文建立了一个基于个体的空间显性模型。模型分布在1个Lx×Ly栅格中,每一步长代表1a。每1个栅格能够容纳Kmax 个体,Kmax表示1个栅格所能容纳的最大数目的互花米草数量。每个栅格都有2个状态:1和0,其中1表示该栅格为入侵植物占有,0表示未被占有。当入侵植物能从遥感影像中识别时,对应元胞的值为1。同时,假定一个元胞中个体的数目达到Kmax的一半时,即认定该元胞被入侵植物所占有,值为1,反之,值为0。每1年,成年个体的死亡率为1-q,q为成体存活率。同时,将有Pps的个体产生种子,每1株生产种子数为ns。然而,只有比例为nss的种子能保存下来,并且只有比例为nsv的种子具有活性。保留下来而有活性的种子将根据种子扩散核函数f(r)进行扩散,其中r为种子离母体的距离。当种子到达一个元胞,将有fg概率进行萌芽,成为幼苗,幼苗将有1-pss的概率死亡。当1个元胞中的个体数目达到了Kmax的一半,该元胞则认为被互花米草占有,值为1。如果个体的总数超过了Kmax,则多余的个体将会死亡。
| 参数Parameter | 定义Definition | 取值Value |
| d | 平均扩散距离Mean seed dispersal distance/unit | 3[5] |
| q | 成体存活率Annual adult survival rate /% | 100 |
| ns | 种子产量Seeds per spike/(no/culm) | 600[18] |
| nf | 分蘖数Tiller number(no/plant) | 25[18] |
| Pps | 有性繁殖率Fruiting culm /% | 50[18] |
| fg | 萌芽率Seed germination rate /% | 3.2[18] |
| Pss | 实生苗存活率Seedling survival rate /% | 70[15] |
| Psf | 分蘖存活率Asexual recruitment survival rate of /% | 80[19] |
| nsv | 种子活性Seed viability /% | 35[18] |
| nss | 种子存有率Seed retain rate /% | 1.5[18] |
| Kmax | 最大容量Maximum capacity(no/m2) | 200[18] |
| Ld | 最大扩散距离 Long dispersal distanc/Unit | 33 |
| Pld | 种子长距离扩散比例 Proportion of seed long dispersal/% | 0.1 |
许多成功入侵的外来植物一般具有强的繁殖能力,尤其是快速的无性繁殖方式[16]。因此,模型同时考虑了外来植物的无性繁殖,并假设入侵植物通过分檗进行无性繁殖。每年有Ppf比例的成年个体将会产生nf个分檗。新生分蘖将有Psf概率存活。当元胞中总个体数超过了Kmax,那么新生的分蘖将向最近八邻扩张。
本文以互花米草为例来模拟外来入侵植物的种群动态,假定Kmax 等于种群密度。由于互花米草是多年生草本植物,因此,假定q=1[5]。Taylor等[5] 和Ge等[7] 假定种子扩散遵循负指数分布:
式中,r为种子到母体的距离,而d为种子平均扩散距离。
然而,该假设仅考虑了种子的本地扩散,忽略了种子的长距离扩散,种子的长距离扩散对外来入侵植物的快速扩张有非常重要的作用[17]。因而,本文将互花米草的种子扩散分为短距离扩散和长距离扩散两种。其中,短距离扩散采用负指数模型,而长距离扩散则假定大概有Pld比例的种子在最远距离为Ld的范围内随机地扩散。根据Taylor等[5]的研究,互花米草的平均扩散距离(d)大概为90 m,而最远距离大概为1000 m。因此,假定d = 3单元(30 m/单元),Ld= 33单元(30 m/单元)。有关互花米草的种群统计学特征参数及其取值如表1。
2.2.2 土地利用与覆被变化和潮间带高程对互花米草种群扩张的影响互花米草一旦入侵到芦苇和碱蓬等本地种群落时,将竞争替代本地种[14]。为简单起见,本模型假设互花米草能替代芦苇和碱蓬群落以及光滩等自然景观,无法替代人类活动影响显著的土地利用类型,如:盐田、水产地、建筑用地和水体。随着人类活动的加剧,自2000年以来,大量的互花米草盐沼地被开垦为水产用地或者农业用地[11],因此,土地利用变化和景观异质性必然会影响互花米草的生境,应该在模型中加以考虑。本文通过遥感解译提取了1995,1997,1999,2001,2003,2005,2006和2010年的土地利用变化。
潮间带高程对互花米草的有性和无性繁殖都有着重要的影响,并进一步地影响互花米草的扩张。已有研究发现,互花米草在中潮间带生长的最快,而在低潮间带和高潮间带逐渐减慢[18, 20]。因此,假设萌芽率,幼苗存活率和无性后代存活率离中潮间带的中心越远,则越小。而中潮间带的中心假定与海岸线平行,并位于离海岸线距离的中间。
2.2.3 参数拟合和模型模拟在互花米草入侵的初期,从种子萌发,到幼苗,再到能在遥感影像上能识别出来有一定的滞后期[7]。尽管已有1995年通过遥感解译的互花米草的群落分布,但无法获得在遥感影像中未能识别的互花米草分布。因此,首先通过模拟互花米草从1995年到1997年的种群分布,并用1997年的遥感解译的分布图进行校正,获取互花米草在1997年的分布(包括能识别的和不能识别的分布)。模拟发现,从1995年模拟到1997年,要与1997年的实际分布相吻合,大概有5a的滞后,证实了互花米草在入侵初期,从建群到能从遥感识别,大概有5a的滞后期,这与他人的研究基本一致[8]。其次,本文以1997年的模拟结果为基础,考虑1997,1999,2001,2003,2005和2006年的土地利用变化和景观异质性对互花米草的影响,模拟了1997—2010年互花米草的种群动态。
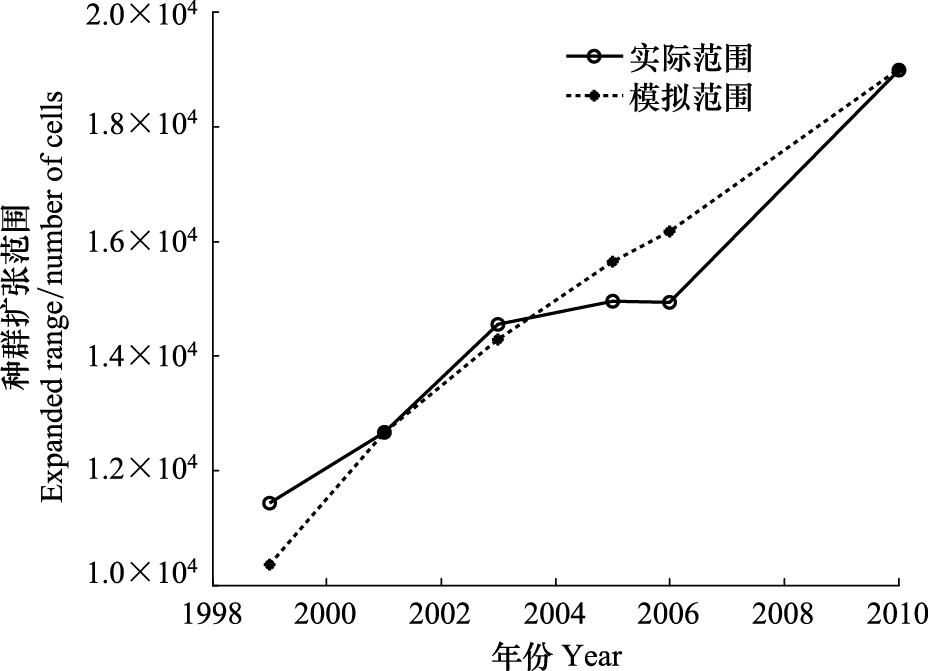
由于本地扩散与长距离扩散的比例(Pld)未知,而这也是生物模型参数化的一个普遍问题[21],因此,本文通过参数拟合来估计。通过调整本地与长距离种子扩散的比例(Pld),比较1999年到2010年互花米草扩张范围(互花米草占有的元胞个数)随时间变化的实际分布范围与模拟范围。当模拟范围与实际范围非常接近时,则选取该模拟下的Pld的值。从图1可见,当长距离扩散比例大概占了种子扩散的0.1%时,互花米草种群扩张的实际范围与模拟扩张范围比较吻合,因而,本文的模拟选取Pld=0.1%。
|
| 图 1 1999年到2010年互花米草种群扩张范围(被占据的元胞个数)的实际范围与模拟范围的比较(Pld=0.1%) Fig.1 Comparison of the actual and the simulated invasion extent (number of cells) of Spartina alterniflora from 1999 to 2010(Pld=0.1%) |
为了揭示有性和无性繁殖对互花米草种群扩张的影响,本文分别模拟了在混合繁殖(同时包含了有性和无性繁殖),有性繁殖和无性繁殖3种情况下的互花米草的种群动态。并通过敏感性分析,来研究影响互花米草种群动态的重要因素。所有的模拟都在matlab2013中进行,每个模拟都重复了100遍。
2.2.4 模型评估模型计算了2010年每个元胞互花米草发生/不发生的概率,并与其实际发生/不发生进行对比来评估模型的精度。同时,还计算了总体精度、敏感度、特异度、Kappa系数,真实技巧统计法(True skill statistic,TSS),以及接受机工作特征(Receiver operating characteristic,ROC)曲线下面积(Area under the ROC curve,AUC)。总体精度指的是正确分类的比例。敏感度指物种发生区被正确预测的比例,而特异度是物种不发生区被正确预测的。Kappa系数是一种计算分类精度的方法,被用来评估模型预测结果与实际分布的相似度。Landis和Koch[22]提出Kappa系数如下评价标准:≤0(很差),0.01—0.20(差),0.21—0.40(一般),0.41—0.60(好),0.61—0.80 (很好),和 0.81—1(极好)。 与Kappa系数相似,TSS 取值-1 到 +1,+1 表示完全一致,而取值 ≤ 0表示预测精度非常差。当TSS值> 0.8,表示模拟结果与实际分布吻合得极好[23]。 由于AUC不受诊断阈值的影响,且对物种发生率不敏感,是目前被公认为最佳的评价指标[24]。AUC取值范围从0到1,1表示实际值与预测值完全一致。当AUC的值> 0.9,表示预测结果极好。关于这些指数的含义,更详细的介绍可以参加参考文献[24]。
2.3 全局敏感性分析通过对模型的输出进行敏感性分析,有利于确定模型参数的相对重要性[25]。尽管敏感性分析被广泛用于生态建模中,然而大部分都是局域敏感性分析,而非全局敏感性分析。局域敏感性分析在评价一个参数的影响时,往往假定其他参数都是固定不变的[26]。然而生态系统往往是复杂的,不同因子之间的相互作用也是非线性的。两个或者多个变量同时变化会加大或者减小单个变量的变化对模拟结果的影响。因此,局域敏感性分析并不适合定量分析非线性系统,而全局敏感性分析则显得十分必要[27]。全局敏感性分析计算所有因子同时变化时,某一个因子对模型输出的影响,从而能确认非线性模型中各个因子间的相互作用[25]。Sobol′s 方法是一个基于方差的全局敏感性分析方法,通过提取一阶敏感性指数(与其它因子无关的主效应)和总体效应指数(包含了主效应以及与其它因子相互作用的效应),可以用来确认每个参数的单独影响,相互作用,以及对模型的集合效应[25]。为了确认影响外来入侵植物种群扩张的不同因子的相对重要性,本文通过Simlab软件[28]对影响互花米草扩散速度的因子进行了Sobel′s全局敏感性分析。
3 研究结果 3.1 互花米草种群动态已有研究认为,植物的无性繁殖要比有性繁殖对种群的增长更为重要[29]。为了验证有性繁殖和无性繁殖对互花米草种群扩张的影响,分别模拟了混合繁殖(包括有性繁殖和无性繁殖),移除有性繁殖和无性繁殖(即单繁殖模式)下互花米草的种群动态(图2)。
|
| 图 2 混合繁殖(包括了有性和无性繁殖)、有性繁殖和无性繁殖三种繁殖模式下互花米草种群扩张动态 Fig.2 Range expansion of Spartina alterniflora under mixed reproduction (both with sexual and asexual reproduction), sexual reproduction and asexual reproduction |
从图2可见,在单一繁殖模式下,种群扩张的速度要远小于混合繁殖模式(同时具有有性和无性繁殖)下的。尽管在无性繁殖模式下,互花米草种群扩张的速度要大于有性繁殖模式下。然而,移除有性繁殖使得种群扩张速度大幅下降,说明了有性繁殖对于互花米草的快速扩张来说十分重要。
3.2 模型的验证从表2可见,Kappa (0.8137>0.80),TSS (0.8184>0.80) 和 AUC (0.9286>0.9),所有值都达到了几乎完全一致的标准。而且,与实际的18993个发生元胞相比,模拟的发生元胞为19014个,两者相差不到0.11%。因此,模拟分布与实际分布基本一致,基于个体的空间显性模型结合遥感解译技术,适合用来模拟互花米草的种群扩张。
| 模拟值Modelled | 真实值 Actua | ||||||||
| 发生Presence | 不发生Absence | 总计Sum | 总体精度Overall accuracy | 敏感度Sensitivity | 特异度Specificity | Kappa系数Kappa | 真实技巧统计法True skill statistic (TSS) | 接受机工作特征曲线下面积Area under the ROC curve (AUC) | |
| 发生Presence | 18130 | 884 | 19014 | ||||||
| 不发生Absence | 863 | 5723 | 6586 | ||||||
| 总计Sum | 18993 | 6607 | 25600 | 0.9318 | 0.9546 | 0.8662 | 0.8137 | 0.8184 | 0.9286 |
为了研究土地利用变化与潮间带高程对互花米草种群扩张的影响,分别模拟了移除土地利用变化和潮间带高程时,互花米草的入侵动态,并通过比较两种情况下模型模拟精度变化的幅度来确定两者对互花米草种群扩张的影响(表3)。
| 模拟情景Simulation scenario | 总面积Total area(number of cells) | 总体精度Overall accuracy | 敏感度Sensitivity | 特异度Specificity | Kappa系数Kappa | 真实技巧统计法True skill statistic (TSS) | 接受机工作特征曲线下面积Area under the ROC curve (AUC) |
| 移除土地利用影响Removing land use | 20414 | 0.8877 | 0.9606 | 0.6781 | 0.6852 | 0.6386 | 0.8407 |
| 移除潮间带高程影响Removing tideland elevation | 22866 | 0.8487 | 1 | 0.4138 | 0.4415 | 0.5116 | 0.7295 |
从表3可见,在不考虑土地利用的影响下,Kappa系数,TSS均小于0.7,AUC小于0.8,尽管模拟结果与实际结果吻合得很好,但是与表2对比,其预测精度从极好变为很好。而不考虑潮间带高程的影响,Kappa系数、TSS与AUC大幅下降,尽管与实际结果吻合较好,但与表2相比,其预测精度下降了2个等级。对比移除土地利用与移除潮间带对互花米草扩张的影响,可以发现,移除潮间带高程的影响,要比移除土地利用变化的影响,所带来的模型模拟精度下降幅度要大得多,并且总面积增加的幅度也大,说明了潮间带高程比土地利用变化对互花米草扩张的影响更大。
3.4 参数敏感性分析为了进一步研究互花米草种群扩张影响参数的相对重要性,基于Sobel′s方法进行全局敏感性分析。通过Sobel′s方法,计算了1997—2010年互花米草扩散速度影响参数的一阶效应和总体效应,以及各个参数的排序(表4)。
| 参数 Parameters | 一阶效应First-order effect | 排序Rank | 总体效应Total effect | 排序Rank |
| 平均扩散距离Mean seed dispersal distance(d) | 0.0366 | 9 | 0.0335 | 9 |
| 成体存活率Annual adult survival rate(q) | 0.4093 | 1 | 0.4065 | 1 |
| 种子产量Seeds per spike(ns) | 0.0283 | 10 | 0.0143 | 11 |
| 分蘖数Tiller number(nf) | 0.1056 | 3 | 0.0949 | 4 |
| 有性繁殖率Fruiting culm(Pps) | 0.0417 | 8 | 0.0482 | 8 |
| 无性繁殖率Asexual reproduction rate(Ppf) | 0.0925 | 4 | 0.1085 | 3 |
| 种子萌发率Seed germination rate(fg) | 0.0616 | 6 | 0.0504 | 6 |
| 实生苗存活率Seedling survival rate(Pss) | 0.0600 | 7 | 0.0496 | 7 |
| 无性繁殖率Asexual recruitment survival rate(Psf) | 0.0857 | 5 | 0.0813 | 5 |
| 最大环境容量Maximum capacity(Kmax) | 0.0147 | 11 | 0.0127 | 12 |
| 长距离扩散距离Long-distance dispersal distance(Ld) | 0.1522 | 2 | 0.1403 | 2 |
| 长距离种子扩散比例Proportion of long-distance seed dispersal(Pld) | 0.0014 | 12 | 0.0147 | 10 |
从表4可见,无论是一阶效应或者是总效应,成体存活率对互花米草种群扩张速度的影响最大,其次是长距离种子扩散距离的影响,而最大环境容量,长距离种子扩散比例,以及种子产量对种群扩张影响最小。对于互花米草两种不同繁殖方式,无性繁殖(分蘖数,无性繁殖率与无性后代存活率)的影响大于除了种子长距离扩散外的有性繁殖(萌芽率,幼苗存活率,有性繁殖率,种子产量)。而对于种子扩散来说,长距离扩散影响要远大于本地扩散,而本地扩散距离对互花米草扩散的影响非常小。同时,种子长距离扩散的比例对互花米草扩张影响很小,说明小概率的种子长距离扩散对互花米草的种群扩散非常重要。
4 讨论本文通过基于个体的空间显性模型和RS的结合,以互花米草为例,模拟了外来入侵植物的种群扩张,揭示了土地利用变化与潮间带高程的影响,并通过全局敏感性分析揭示了种子长距离扩散,不同繁殖方式对互花米草种群扩散的相对重要性。
(1)已有研究认为潮间带高程对互花米草的有性和无性繁殖有着非常重要的影响[18, 20]。研究发现,如果不考虑潮间带高程的影响,将会大幅度地降低模型的预测精度,因而,要准确预测互花米草的种群扩张动态,必须考虑潮间带的高程。由于有限的野外观察资料和潮间带数字高程数据,无法获取潮间带高程与种子萌芽率、繁殖率、幼苗存活率等的关系。因而,本文仅简单地假设互花米草有性和无性繁殖与离中潮间带中心的距离成反比。因而,今后需要进一步地通过野外观察和室内实验来明确互花米草有性和无性繁殖与潮间带高程的关系。
(2)RS和GIS技术,可以从较大的尺度来监测土地利用的变化和入侵植物的种群扩张[6, 11]。本文通过研究发现,如果不考虑土地利用变化的影响,将会引起模型预测精度的下降,因而,土地利用变化对互花米草种群扩张有重要的影响。因此,将RS和GIS技术与基于个体的空间显性模型的结合,通过综合考虑土地利用变化和景观异质性的影响,能更好地模拟和预测外来入侵植物的种群扩张动态,并进一步地揭示影响外来入侵植物扩张的机制。
(3)通过全局敏感性分析发现,成体存活率与种子长距离扩散是影响种群扩张最重要的两个因素。同时,无性繁殖相对除了长距离种子扩散外的其他有性繁殖参数来说,更为重要。然而,通过移除有性繁殖的模拟发现,在单一的无性繁殖模式下,互花米草种群扩散的速度将会大幅下降,说明了有性繁殖和无性繁殖对加速种群扩张缺一不可。以往的研究通过野外观察和实验发现无性繁殖后代数目要远大于有性繁殖,因而认为无性繁殖比有性繁殖更为重要[29, 30]。然而它们很难将两种不同繁殖方式对种群扩张的效应分离开来,因而往往会低估有性繁殖的影响。而基于个体的空间显性模型不仅能分离出不同繁殖方式对种群扩张速度的影响,还能进一步确定不同繁殖方式的相对重要性。
(4)种子扩散是影响植物种群动态的一个非常重要的过程[31]。然而,由于野外资料的缺乏,很难得到实际的种子扩散模式。本文通过全局敏感性分析发现,种子本地短距离扩散对种群扩张的影响很小,而种子的长距离扩散的影响十分显著。同时,种子长距离扩散的比例对种群的扩张速度影响很小,说明了小概率的长距离扩散事件对种群快速扩张十分重要。因而,在实际研究中,应该更关注种子长距离扩散的距离。
Taylor 等[3]指出减少种子产量或者移除实生苗是一个有效的控制互花米草入侵的策略,然而,通过全局敏感性分析发现,种子产量和实生苗的存活率对种群扩张的影响很小;尽管成体存活率和种子长距离扩散距离是影响种群扩张最重要的两大因素。然而,如果移除成体,数量巨大,费时费力;而种子的长距离扩散事件一般是小概率事件,控制起来省时省力。并且,有性繁殖能大幅加速互花米草的种群扩张。与此同时,Grevstad[9]建议先移除入侵前沿的斑块,而Buhle等[8]建议先移除比较小的斑块。因此,本文建议抑制种子的长距离扩散,同时,移除小概率的长距离扩散事件形成的入侵前沿的小斑块来控制互花米草的种群扩张。因而,建议在种子成熟期,通过致密的布紧密地覆盖住互花米草入侵前沿的小斑块,防止种子的长距离扩散;或者在种子成熟之前,通过人工拔除入侵前沿的小斑块,从而抑制互花米草扩张。
| [1] | Ricciardi A. Assessing species invasions as a cause of extinction. Trends in Ecology and Evolution, 2004, 19(12): 619-619. |
| [2] | Millennium Ecosystem Assessment. Ecosystems and Human Well-being: Synthesis. Washington, DC: Island Press, 2005. |
| [3] | Taylor S, Kumar L. Potential distribution of an invasive species under climate change scenarios using CLIMEX and soil drainage: A case study of Lantana camara L. in Queensland, Australia. Journal of Environmental Management, 2013, 114: 414-422. |
| [4] | Lockwood J L, Hoopes M F, Marchetti M P. Invasion Ecology. Oxford: Blackwell Publishing, 2007. |
| [5] | Taylor C M, Davis H G, Civille J C, Grevstad F S, Hastings A. Consequences of an Allee effect in the invasion of a pacific estuary by Spartina alterniflora. Ecology, 2004, 85(12): 3254-3266. |
| [6] | Huang H M, Zhang L Q, Guan Y J, Wang D H. A cellular automata model for population expansion of Spartina alterniflora at Jiuduansha Shoals, Shanghai, China. Estuarine, Coastal and Shelf Science, 2008, 77(1): 47-55. |
| [7] | Ge Z M, Cao H B, Zhang L Q. A process-based grid model for the simulation of range expansion of Spartina alterniflora on the coastal saltmarshes in the Yangtze Estuary. Ecological Engineering, 2013, 58: 105-112. |
| [8] | Buhle E R, Feist B E, Hilborn R. Population dynamics and control of invasive Spartina alterniflora: inference and forecasting under uncertainty. Ecological Applications, 2012, 22(3): 880-893. |
| [9] | Grevstad F S. Simulating control strategies for a spatially structured weed invasion: Spartina alterniflora (Loisel) in Pacific Coast estuaries. Biological Invasions, 2005, 7(4): 665-677. |
| [10] | Grimm V, Railsback S F. Individual-based Modeling and Ecology. Princeton, NJ: Princeton University Press, 2005. |
| [11] | Zuo P, Zhao S H, Liu C A, Wang C H, Liang Y B. Distribution of Spartina spp. along China's coast. Ecological Engineering, 2012, 40: 160-166. |
| [12] | Parry H R, Evans A J, Morgan D. Aphid population response to agricultural landscape change: A spatially explicit, individual-based model. Ecological Modelling, 2006, 199(4): 451-463. |
| [13] | Seidl R, Spies T A, Rammer W, Steel E A, Pabst R J, Olsen K. Multi-scale drivers of spatial variation in old-growth forest carbon density disentangled with Lidar and an individual-based landscape model. Ecosystems, 2012, 15(8): 1321-1335. |
| [14] | An S Q, Gu B H, Zhou C F, Wang Z S, Deng Z F, Zhi Y B, Li H L, Chen L, Yu D H, Liu Y H. Spartina invasion in China: implications for invasive species management and future research. Weed Research, 2007, 47(3): 183-191. |
| [15] | Zhu Z C, Zhang L Q, Wang N, Schwarz C, Ysebaert T. Interactions between the range expansion of saltmarsh vegetation and hydrodynamic regimes in the Yangtze Estuary, China. Estuarine Coastal and Shelf Science, 2012, 96: 273-279. |
| [16] | Baker H G. The evolution of weeds. Annual Review of Ecology and Systematics, 1974, 5: 1-24. |
| [17] | Lesser M R, Jackson S T. Contributions of long-distance dispersal to population growth in colonising Pinus ponderosa populations. Ecology Letters, 2013, 16(3): 380-389. |
| [18] | Xiao D R, Zhang L Q, Zhu Z C. A study on seed characteristics and seed bank of Spartina alterniflora at saltmarshes in the Yangtze Estuary, China. Estuarine Coastal and Shelf Science, 2009, 83(1): 105-110. |
| [19] | 徐伟伟, 王国祥, 刘金娥, 陈正勇, 王刚. 苏北海滨湿地互花米草种子特征及实生苗生长. 生态学报, 2011, 31(16): 4560-4567. |
| [20] | Zhang R S, Shen Y M, Lu L Y, Yan S G, Wang Y H, Li J L, Zhang Z L. Formation of Spartina alterniflora salt marshes on the coast of Jiangsu Province, China. Ecological Engineering, 2004, 23(2): 95-105. |
| [21] | Fennell M, Murphy J E. Armstrong C. Gallagher T. Osborne B. Plant Spread Simulator: A model for simulating large-scale directed dispersal processes across heterogeneous environments. Ecological Modelling, 2012, 230: 1-10. |
| [22] | Landis J R, Koch G G. The measurement of observer agreement for categorical data. Biometrics, 1977, 33(1): 159-174. |
| [23] | Jones C C, Acker S A, Halpern C B. Combining local- and large-scale models to predict the distributions of invasive plant species. Ecological Applications, 2010, 20(2): 311-326. |
| [24] | Allouche O, Tsoar A, Kadmon R. Assessing the accuracy of species distribution models: prevalence, kappa and the true skill statistic (TSS). Journal of Applied Ecology, 2006, 43(6): 1223-1232. |
| [25] | Saltelli A, Tarantola S, Campolongo F, Ratto M. Sensitivity Analysis in Practice: A Guide to Assessing Scientific Models. Chichester: John Wiley, 2004. |
| [26] | Harper E B, Stella J C, Fremier A K. Global sensitivity analysis for complex ecological models: a case study of riparian cottonwood population dynamics. Ecological Applications, 2011, 21(4): 1225-1240. |
| [27] | Marino S, Hogue I B, Ray C J, Kirschner D E. A methodology for performing global uncertainty and sensitivity analysis in systems biology. Journal of Theoretical Biology, 2008, 254(1): 178-196. |
| [28] | Joint Research Centre of the European Commission. SimLab: Software package for uncertainty and sensitivity analysis, 2011. Available at: http: //simlab.jrc.ec.europa.eu. |
| [29] | Mandujano M C, Golubov J, Huenneke L F. Effect of reproductive modes and environmental heterogeneity in the population dynamics of a geographically widespread clonal desert cactus. Population Ecology, 2007, 49(2): 141-153. |
| [30] | Lambrecht-McDowell S C, Radosevich S R. Population demographics and trade-offs to reproduction of an invasive and noninvasive species of Rubus. Biological Invasions, 2005, 7(2): 281-295. |
| [31] | Hirsch B T, Visser M D, Kays R, Jansen P A. Quantifying seed dispersal kernels from truncated seed-tracking data. Methods in Ecology and Evolution, 2012, 3(3): 595-602. |
 2015, Vol. 35
2015, Vol. 35





