文章信息
- 马栋山, 郭羿宏, 张琼琼, 郭逍宇
- MA Dongshan, GUO Yihong, ZHANG Qiongqiong, GUO Xiaoyu
- 再生水补水对河道底泥细菌群落结构的影响
- Influence of reclaimed water on the bacterial community structure of sediment from an urban river
- 生态学报, 2015, 35(20): 6742-6749
- Acta Ecologica Sinica, 2015, 35(20): 6742-6749
- http://dx.doi.org/10.5846/stxb201404210791
-
文章历史
- 收稿日期: 2014-04-21
- 修订日期: 2014-12-18
2. 北京市城市环境过程与数字模拟重点实验室-省部共建国家重点实验室培育基地, 北京 100048
2. Beijing Municipal Key Laboratory of Resources Environment and GIS, Beijing 100048, China
再生水作为一种稳定的再生水源,在缓解北京市水资源供需矛盾、减轻水环境污染方面发挥重要作用。然而再生水水质特性决定了其必然会改变河道生态水文过程和污染物迁移运转,进而通过河道垂向渗漏过程影响周边地下水水质特性和污染物迁移运转。城市河道具有良好的环境污染修复能力,能有效消除水体氮、磷、各种有机物质[1,2]。河道水质特别是营养物和污染物的变化将显著影响湿地生态系统微生物群落结构与功能[3]。外源污染物稀释、迁移、转化和降解过程伴随着适应性微生物激活及非适应性微生物抑制的过程[4],尤其是水域生态系统的硝化和反硝化空间耦合关系通常发生在河道中能提供不同氧浓度梯度的底水-饱水沉积物中好氧和厌氧界面[5],因而在河道水质净化及其河道-地下水渗漏系统中污染物修复方面发挥重要作用。基于此分析再生水受纳河道中底泥细菌群落结构的空间变异,解析导致微生物群落结构空间变异的主要环境要素,揭示对关键环境要素起降解作用的优势菌属,为北京市河道再生水补水的利用提供科学合理的依据。
1 材料与方法 1.1 研究区概况麻峪湿地净化系统地处北京市西部,属于门头沟永定河段,于2011年建成。该地段位于五里坨和广宁村之间,研究全长2600m。麻峪湿地段有门城污水处理厂,位于北京市门头沟区永定河门城镇段西侧,占地10500m2。该污水处理厂日处理能力为40000m3。污水处理工艺主要包括预处理、生物处理、污泥处理和除臭工艺四部分,确保处理后的水质达到国家二级排放标准。除臭工艺是在北京市污水处理领域中首次采取,较好地解决了厂区附近区域内大气受到污染的问题,其出水排入麻峪湿地。
1.2 样品采集及理化指标分析本研究于2012年10月采集麻峪湿地河道河岸带底泥样品,依据《永定河生态功能区划》,采样点分别布设在中门寺沟和高井排洪渠补水口附近湿地、补水口上游湿地以及补水口下游湿地。具体采样点包括:取补水口上游300m处点位MK、MK1、MK2,补水断面有中门寺沟补水口MB、MP1,高井沟排洪渠补水口MP2,MH为距离补水口下游1200m处混合断面,MJ为距补水口下游2000m处净化断面。具体位置见图1。每一个采样点沿河道横断面从中间到两岸均匀采集5个平行样,采样深度距离河底20cm处,每个样点采集约500g底泥,置于干净密封的聚四氟乙烯塑料袋中,低温储藏带回实验室进行分析处理,并对样品进行编号。每个样点5个平行样共计2500g土壤搅拌混匀提取约500g作为一个样方并重新编号。编号后的样品分两部分,其中一部分进行常规理化指标分析,总氮(TN)的测定采用凯氏定氮法(GB/T11894-1989),总磷(TP)的测定采用碱熔-钼锑抗分光光度法 (HJ632-2011)、总有机碳(TOC)采用重铬酸钾氧化-分光光度法(HJ615/2011)测定,铵态氮采用2mol/L KCl浸提—靛酚蓝比色法测,ORP(Oxidation-Reduction Potential)采用ORP仪直接测量,重金属采用原子吸收光谱法来测定,具体测定结果见表1。剩余底泥样品于-4℃下保存,用于微生物群落结构分析。
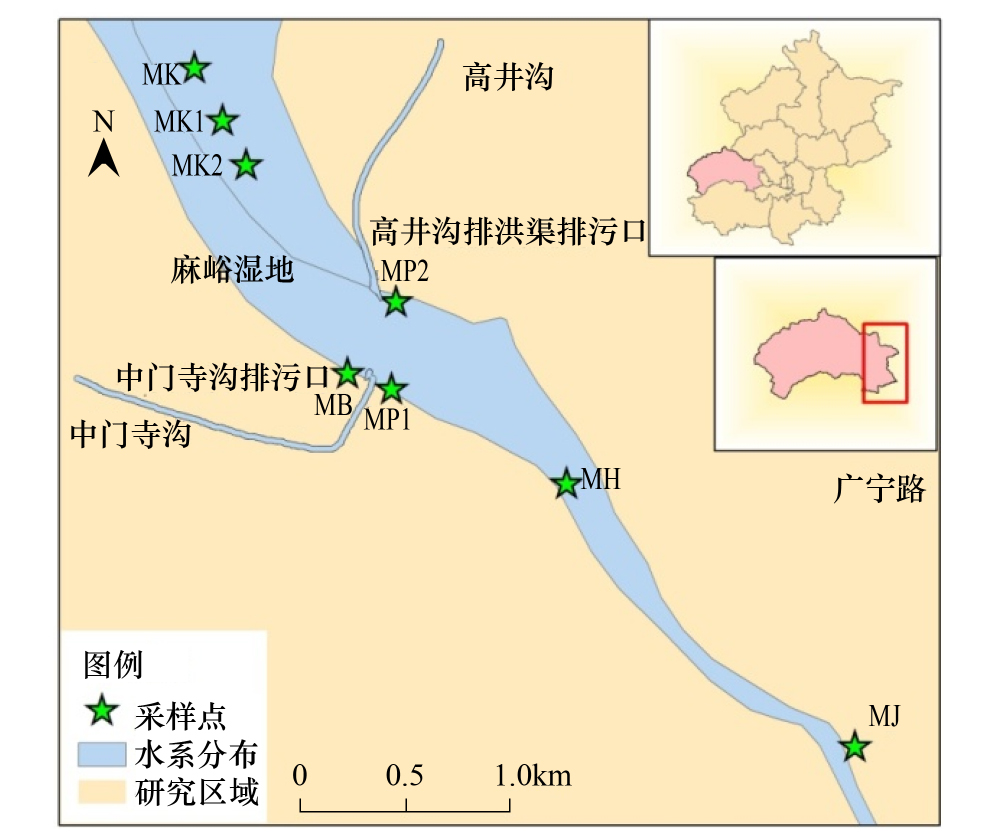
|
| 图 1 北京市麻峪湿地采样点分布图 Fig.1 The distribution map of sample sites in Beijing Ma Yu wetland MB、MP1、MP2为再生水补水口,MK、MK1和MK2为再生水补水口上游300m样点,MH为补水口下游800m处样点,MJ为再生水补水口下游2000m采样点 |
| 参数Parameter | MK1 | MK2 | MK | MP1 | MP2 | MH | MJ | MB |
| 总氮TN Total Nitrogen/(g/kg) | 29.38 | 15.45 | 9.91 | 11.57 | 13.58 | 11.73 | 12.07 | 17.48 |
| 总磷TP Total Phosphorus/(mg/kg) | 19.34 | 11.91 | 13.41 | 17.17 | 26.47 | 11.79 | 11.21 | 42.11 |
| 氧化还原电位ORP Oxidation-Reduction Potential/mV | -47.10 | 61.90 | -29.50 | -80.90 | -71.40 | 32.40 | 11.40 | -90.30 |
| 总有机碳TOC Total Organic Carbon/(mg/kg) | 0.61 | 4.57 | 2.62 | 0.99 | 5.01 | 1.63 | 0.48 | 5.55 |
| 铵态氮NH+4-N Ammoniacal Nitrogen/(mg/kg) | 3.70 | 8.25 | 17.00 | 5.75 | 19.61 | 24.66 | 0.69 | 2.94 |
| Ti/(μg/ kg) | 7.03 | 7.48 | 8.18 | 0.17 | 8.26 | 6.98 | 8.69 | 5.11 |
| Cr/(μg/ kg) | 0.18 | 0.14 | 0.20 | 0.08 | 0.19 | 0.12 | 0.19 | 0.20 |
| Mn/(μg/ kg) | 1.39 | 1.25 | 1.15 | 0.02 | 0.89 | 0.79 | 1.15 | 1.83 |
| Fe/(μg/ kg) | 50.84 | 48.31 | 60.10 | 1.43 | 58.51 | 48.11 | 60.86 | 52.92 |
| Ni/(μg/ kg) | 0.06 | 0.07 | 0.08 | 0.00 | 0.08 | 0.04 | 0.08 | 0.05 |
| Cu/(μg/ kg) | 0.04 | 0.04 | 0.04 | 0.01 | 0.10 | 0.02 | 0.04 | 0.05 |
| Zn/(μg/ kg) | 1.69 | 0.26 | 0.20 | 0.00 | 0.61 | 0.73 | 1.53 | 0.32 |
| Cd/(μg/ kg) | 0.02 | 0.01 | 0.01 | 0.00 | 0.01 | 0.01 | 0.01 | 0.01 |
| Pb/(μg/ kg) | 0.07 | 0.02 | 0.02 | 0.01 | 0.05 | 0.01 | 0.05 | 0.03 |
| V/(μg/ kg) | 0.16 | 0.15 | 0.18 | 0.00 | 0.17 | 0.15 | 0.19 | 0.16 |
采用土壤样品提取试剂盒(天根生化科技北京有限公司)提取底泥样品总DNA,操作步骤按照使用说明书进行。提取总DNA经0.8%(质量/体积)琼脂糖凝胶电泳检测鉴定,提取的DNA放置于-20℃条件下保存备用。
1.3.2 PCR扩增PCR技术依据史青应用T-RFLP 技术分析滇池污染水体的细菌群落技术[6]进行扩增。
1.3.3 末端限制性片段长度多态性(T-RFLP)分析分别采用MspⅠ、AfaⅠ、HaeⅢ对荧光PCR 产物进行酶切。在37℃下放置3—5 h。然后在65℃条件下温浴15 min使酶失活。随后将酶切产物送至天根生物技术有限公司进行基因扫描(GeneScan) ,得到T-RFLP图谱。
1.3.4 数据处理与分析T-RFLP谱图用Peak Scanner进行分析。舍去小于50 bp和大于500 bp的片段。对于细菌,由于相对数量过小的限制性末端片段(T-RFs)不会对群落的特性产生明显的影响[7,8,9]。故在本分析中舍去了相对数量<1%的T-RFs,然后分别计算图谱中每一个峰的峰面积与所有峰总面积的比值,将每个T-RF所占的百分比作为权重导入Primer软件,聚类方法选择组间平均距离法,距离选择平方欧氏距离,做出聚类分析图。借助PRIMER和Excel2007软件,以麻峪湿地的8个底泥样品的111个T-RFs类型的相对峰面积为原始矩阵,借助PRIMER软件实现样点的聚类,同时计算细菌群落物种的综合多样性指数(Shannon-weaver index)、物种丰富度指数(Margale index)和均匀度指数(evenness index),分析底泥细菌群落多样性的空间差异。借助CanoDraw for Windows和Excel2007软件对环境因子和样方进行排序分析。以8个样本中细菌菌群的相对丰度组成的物种矩阵和15种环境参数组成的环境变量矩阵为基础数据,进行DCA(Detrended correspondence analysisi)排序,在DCA分析环境梯度轴长大于4. 0的前提下,进而运用非线性的单峰排序方法CCA(Canonical correspondence analysis),得到样方、物种、环境因子相互关系的二维排序图[10]。Mica对比是将HaeⅢ、MspⅠ、AfaⅠ3种内切酶消化的T-RFLP图谱属性数据上传到Phylogenetic AssignmentTool(PAT,https://secure.Limnology.wisc.edu/trflp/newuser.jsp) 网站,并结合Mica (http://mica.ibest.uidaho. edu/pat.php) 网站通过Virtual Digest(ISPaR)模块产生的基础数据库对起主要作用T-RFs类型的系统发育分类进行推测,最终得出可能对应的种属。
2 结果与讨论 2.1 不同内切酶消化多样性比较图2是对8个样品细菌16S r DNA的荧光引物PCR扩增产物经限制性内切酶MspⅠ、HaeIII和AfaⅠ消化后的扫描图谱,该图谱总体呈现了降噪后不同T-RFs类型在不同酶切作用下细菌群落的整体分布情况。同一个样品经MspⅠ、HaeIII及AfaⅠ等3个不同的内切酶消化后,反映出的总T-RFs数和总峰面积具一定的差异,即MspⅠ和HaeIII消化结果的多样性明显优于AfaⅠ,即利用内切酶MspⅠ和HaeIII能够揭示更高的丰富度,但AfaⅠ酶切扫描图谱多样性较低。基于此,后续的多元统计分析均以经内切酶MspⅠ和HaeIII消化的T-RFLP图谱文件进行分析。
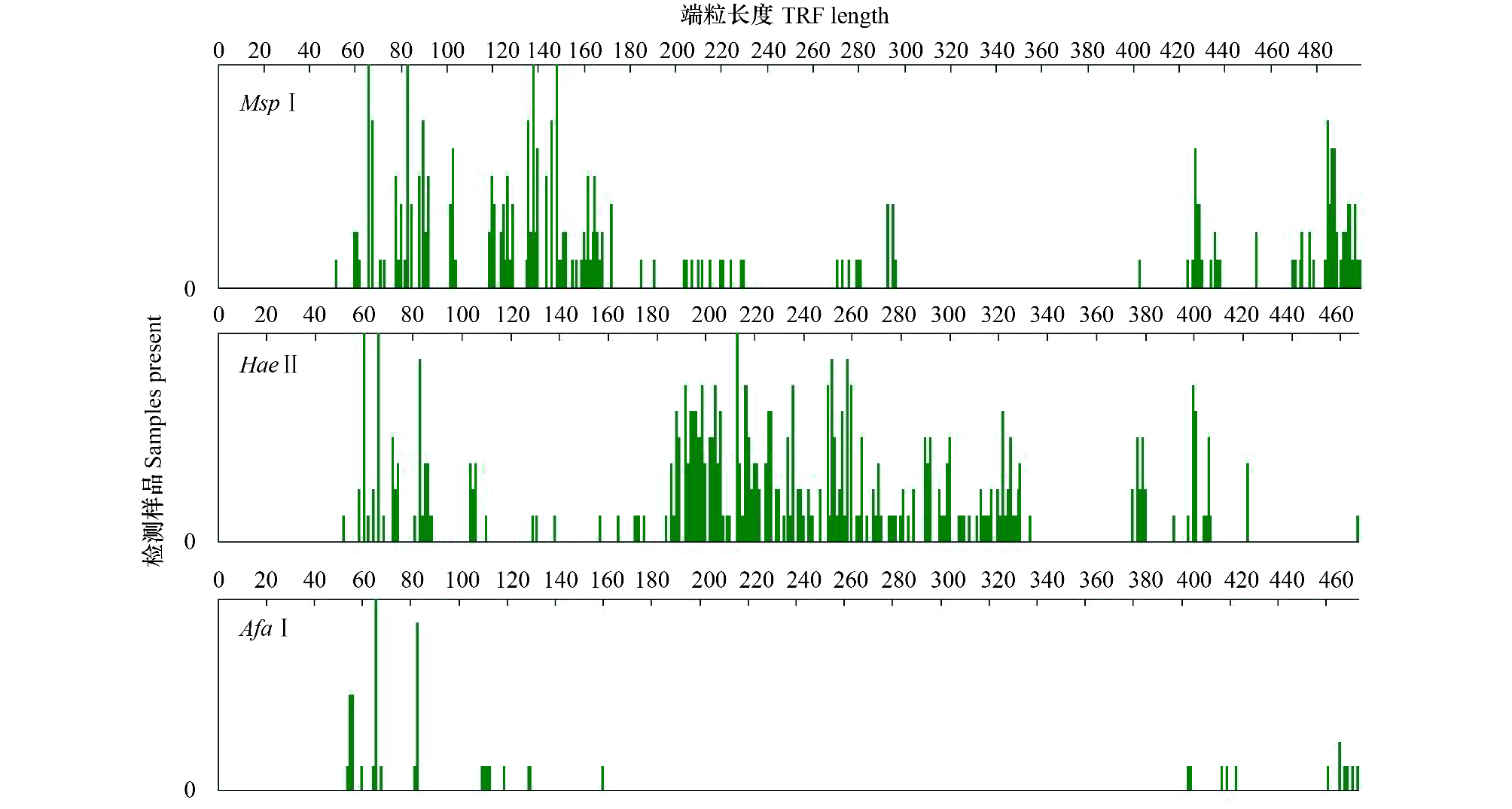
|
| 图 2 麻峪湿地底泥细菌经MspⅠ、HaeIII及AfaⅠ酶切的T-RFs Fig.2 T-RFs of Sediment bacteria with MspⅠ、HaeIII and AfaⅠdigestion in Ma Yu wetland TRF: 端粒长度Terminal Restriction Fragment |
把采集样品基于T-RFLP微生物群落结构分析的谱图进行预处理之后,采用Primer进行聚类分析,结果如图3所示。从图可以看出微生物群落结构在再生水河道补水口和上下游均发生较明显的变化。以相似性53%为标准,将其划分为四大类,第Ⅰ类:再生水河道补水口上游300m处MK、MK1、MK2样点和补水口下游2000m处的MJ样点;第Ⅱ类:再生水补水口河道底泥MP1、MP2两个样点;第Ⅲ类:距离再生水补水口河道底泥1200m的混合样点MH;第Ⅳ类:再生水补水口底泥MB样点。从聚类结果可以看出,在距补水口下游1200m的范围内,河道底泥微生物群落组成发生了较大的改变,随着再生水与上游来水径向混合渐变净化过程,在补水口2000m处,河道底泥微生物群落结构与河道再生水补水口上游趋于相似。其次,位于再生水补水口底泥微生物群落结构与其他样点间变化存在较大差异,说明补水口附近底泥的生物物理化学过程显著区别于主河道底泥,需进一步结合微生物组成成分解析。为了分析基于MspⅠ酶切T-RFLP的稳定性,将HaeⅢ酶切分析结果同样进行聚类分析,结果见图3,从分析结果可以看出两个酶切结果具有相似的结论。
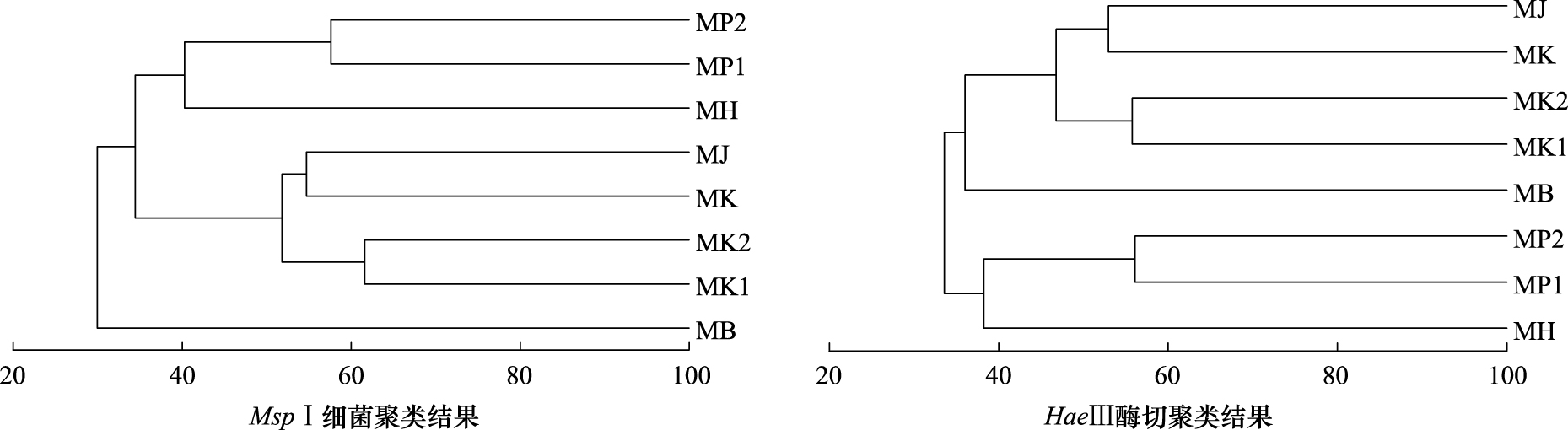
|
| 图 3 基于 T-RFLP 图谱的底泥细菌群落结构聚类分析 Fig.3 Dendrogram of hierarchical cluster analysis of Sediment bacteria based on the T-RFLP profiles |
根据聚类结果,计算了以MspⅠ为酶切的不同聚类中各片段的丰度,并定义T-RFs片段丰度值>4%的类型为优势菌群,而片段丰度值<1%的类型为偶见菌群,其余为非优势菌群[11]。从表2可以看出,第Ⅳ类物种丰富度及综合多样性指数显著高于其他类,第Ⅳ类在群落结构上表现为最高偶见菌群丰度值及最高非优势菌群丰度值,以及优势菌群比其他类稍低的丰度值。究其原因细菌偶见菌群一般是伴随着环境扰动导致新物种的产生或者已存物种的消亡而出现,细菌优势菌群则是由于适应环境变化后在群落中发挥重要净化作用而存在的物种菌群,细菌群落在不断出现新物种和逐步适应新环境这两个过程中交替演变,从而使底泥能够更准确的反应长期富集于再生水补水口附近各类准持久性有机污染物和消毒副产物。除第Ⅳ类外,其它类综合多样性指数则呈现第Ⅱ类>第Ⅲ类>第Ⅰ类的变化趋势,综合多样性指数的这种变化趋势表现为,再生水补水和上游来水汇水过程水质净化微生物生态过程相一致,即随着再生水净化过程的实现,微生物综合多样性指数呈现下降趋势。从均匀度指数的变化趋势看,第Ⅱ类具有最高均匀度指数,原因是第Ⅱ类的优势菌群、非优势菌群和偶见菌群的T-RFs数和相对丰度分布较为均匀,群落结构较为稳定,在再生水水质净化过程中发挥重要作用。而第Ⅲ类则由于其具最高优势菌群数和最优势菌群相对丰度值,偶见菌群缺失,导致其群落结构比较单一,群落多样性和均匀度指数都最低。
| 指数Index | 类别Class | ||||
| 第Ⅳ类 Fourth calss | 第Ⅱ类 Secondary class | 第Ⅲ类 Third class | 第Ⅰ类 First calss | ||
| 末端限制性片段T-RFs | 优势菌群Dominantbacteria | 4 | 7 | 7 | 5 |
| Terminal restriction fragments | 非优势菌群Non-dominant bacteria | 21 | 18 | 11 | 18 |
| 偶见菌群Rare bacteria | 38 | 24 | 0 | 34 | |
| 相对丰度relative index/% | 优势菌群Dominantbacteria | 33.7 | 48.7 | 67.8 | 45.9 |
| 非优势菌群Non-dominant bacteria | 46.9 | 36.3 | 32.2 | 37.7 | |
| 偶见菌群Rare bacteria | 19.4 | 15 | 0 | 16.4 | |
| 多样性指数diversity index | 综合多样性指数Shannon-weaver index | 3.561 | 3.192 | 2.586 | 2.567 |
| 物种丰富度Margale index | 13.463 | 7.274 | 3.692 | 5.646 | |
| 均匀度指数Evenness index | 0.859 | 0.903 | 0.835 | 0.856 | |
| 第Ⅳ类、第Ⅱ类、第Ⅲ类和第Ⅰ类按照河道位置排序,其中,第Ⅰ类中包括再生水补水口下游和上游点位 | |||||
运用典范对应分析(CCA)排序法,分析再生水补水对城市河道底泥细菌群落结构特征及其成因。在CCA排序图中,各划分因子用箭头表示,箭头连线的长短表示样方与因子相关性的大小,线越长,说明相关性越大,反之则小。连线与排序轴的角度表明功能群划分因子与该排序轴相关性的大小(Pearson相关) ,夹角越小,相关性越大。箭头所在象限表示功能群划分因子与排序轴的正负相关关系[12],各椭圆形为所划分的各类功能群,圈内的字母为样方。根据各采样点分布特点,以MspⅠ酶切的8个样点和环境因子进行趋势对应分析(CCA),排序结果表明,CCA排序图第一轴AX1和第二轴AX2的特征值累计占总特征值的65.83%,置信度P=0.03,排序图包含了大部分的信息,排序效果良好(图4)。

|
| 图 4 再生水补水河道地底泥采样点与环境因子的CCA排序图 Fig.4 CCA sequence diagram of the sample point and environmental factors on Reclaimed water in river sediment |
麻峪湿地的8个采样点四大类在CCA轴上得到了很好的分化。总的来看与第一排序轴相关性最高的环境因子是TN(0.9987),基于分类的各类型样点在x轴方向上从左到右表现为第Ⅱ类>第Ⅲ类>第Ⅰ类的变化趋势,这种变化趋势与综合多样性指数变化趋势一致,同时与再生水补水上游来水径向汇流过程相一致,环境因子及群落分布趋势联合分析表征再生水与上游来水水质净化过程中微生物净化主要体现在TN的变化过程。与第二排序轴相关性高的的环境因子是TP(0.9961)、ORP(0.72888)、TOC(0.6342),而在y轴方向上则表现为第Ⅳ类与其他群落类型之间的差异,指示第Ⅳ类底泥微生物净化过程主要以磷微生物地球化学过程为主,其次是TOC相关的生物化学过程为主,而氧化还原电位的改变是与磷、TOC微生物地球化学过程紧密联系的重要环境因子。结合图4可知第Ⅳ类独立于其他菌群位于图右上方,表明其具独特的微生物生态特征。第Ⅰ类与Pb、Fe、V、Ni、Ti、Zn、Cd等重金属具有较高相关性的结果则说明上游河流沿岸的生活污水、工业废水点源排放及农田径流非点源排放引发的重金属污染在自然营力作用下从水中沉淀下来[13],进而对底泥细菌群落结构和种群数量的影响较大。对于第Ⅱ类和第Ⅲ类则与铵态氮有密切关系,说明再生水补水口与上游来水径向渐变过程可能与氨氮降解过程有关。对于第Ⅱ类和第Ⅲ类的细菌群落由于是处在补水口以及其混合断面内,按照Drury等人的研究理论,铵态氮不会随着水流被冲向下游而逐步降解,反而是缓慢沉积在底泥中通过被吸附和固定的方式在土壤胶体表面和胶体晶格中保存下来[14],因此在第Ⅱ和Ⅲ底泥样点中的菌群表现为与铵态氮存在着密切的关系。综合以上,再生水补水口出口底泥细菌群落则主要受到总磷的影响较大,相对再生水补水与上游来水汇水过程细菌群落则主要与氨氮的净化具密切关系。以HaeⅢ酶切的CCA聚类图见图4,由图可知,以HaeⅢ酶切CCA聚类图和以MspⅠ酶切CCA聚类图具有相似的结果,在此不再赘述。
2.5 基于Mica对比的群落结构分析通过Virtual Digest(ISPAR)模块产生的基础数据库对起主要作用T-RFs类型的系统发育分类进行推测,其中有将近20%暂不能确定,显示为非培养。另外,有个别的T-RFs类型在数据中无匹配。之后通过计算其细菌T-RFs的比例,以占据整个T-RF的10%以上为优势菌种,筛选后结果见表3。 由表可知,第Ⅰ类中主要优势菌群为贪食菌属、芽孢杆菌属和链霉菌属。第Ⅱ中主要优势菌群为贪食菌属、芽孢杆菌属、葡萄球菌、肠杆菌、假单胞菌属和Geitlerinema sp.;第Ⅲ类中主要优势菌群为假单胞菌属和Geitlerinema sp.;第Ⅳ类主要优势菌群为芽孢杆菌属和气单胞菌属。而贪食菌属和芽孢杆菌属是第Ⅰ类和第Ⅱ类共有的菌属,葡萄球菌和肠杆菌是第Ⅱ类特有的菌属,气单胞菌属为第Ⅳ类独有的菌属,假单胞菌属和Geitlerinema sp.属于第Ⅱ类和第Ⅲ类。
| OTU类型(bp) | 可能属 Possible Genus | 类别Class | |||||
| MspⅠ | HaeⅢ | AfaⅠ | 第Ⅰ类 First calss | 第Ⅱ类 Secondary class | 第Ⅲ类 Third class | 第Ⅳ类 Fourth calss | |
| 66 | 218 | 427 | Variovorax paradoxus | √ | √ | — | — |
| 256 | 127 | Bacillus thuringiensis | √ | √ | — | √ | |
| 226 | 454 | Streptomyces sp. | √ | — | — | — | |
| 254 | 127 | Staphylococcus aureus | — | √ | — | — | |
| 83 | 83 | Enterobacterium | — | √ | — | — | |
| 66 | 128 | Aeromonassp. | — | — | — | √ | |
| 83 | 83 | 83 | Geitlerinema sp. | — | √ | √ | — |
| 488 | 83 | 83 | Pseudomonas plecoglossicida | — | √ | √ | — |
| “√”有细菌;“—”无细菌 | |||||||
本研究中结合基于T-RFLP片段的MiCA比对,结果表明假单胞菌属、贪食菌属、链霉菌属和芽孢杆菌属是与再生水水质净化具有密切关系的菌属。其中可反应再生水典型特征的第Ⅳ类包含芽孢杆菌属和气单胞菌属两类优势属,有报道称气单胞菌在湿地系统氮、磷循环过程中起重要作用,其生长受铵离子、氮、磷浓度影响明显[15],具有将NO-3转化为NO-2的能力[16]。芽孢杆菌属可迅速降解包括鱼的排泄物、残余饲料、浮游藻类尸体和池底淤泥在内的有机物,使之生成硝酸盐、磷酸盐、硫酸盐等无机盐类,从而降低水中COD、BOD的含量,维持良好的水域生态环境[17]。本研究中仅出现在第Ⅳ类中的气单胞菌属和在各菌群普遍存在的芽孢杆菌属说明再生水补水口附近底泥细菌受到磷浓度及有机物的影响较大,这与CCA分析的与环境因子TP、TOC关系密切的结果保持一致。再生水与上游来水混合渐变过程中的第Ⅱ类和第Ⅲ类具共有优势菌属假单胞菌属和Geitlerinema sp.属。据文献可知假单胞菌属是一种有机污染中普遍存在的菌属,可以利用包括单碳在内的许多有机物作为自身的能量和碳源,以有机氮或无机氮为氮源进行化能营养生活[18],而Geitlerinema sp.是专性属于底栖生物环境,隶属于蓝菌门(Cyanophyta)的颤藻目(Oscillatoriales),与水环境中氮的循环具有密切关系已得到普遍的认同[19],这与CCA分析中第Ⅱ类和第Ⅲ类与环境因子氮循环具有密切关系的结果保持一致。除假单胞菌属和Geitlerinema sp.属外,贪食菌属、芽孢杆菌属、葡萄球菌属、肠杆菌属同样为第Ⅱ类优势菌属,其中贪食菌属与Variovorax paradoxus密切的关系,且仅出现于与再生水干扰强度较高的第Ⅰ类和第Ⅱ类中,文献表明Variovorax paradoxus在降低毒性等方面发挥重要作用,与CCA分析中第Ⅰ类与重金属生物循环具密切关系的结果相一致[20]。
3 结论(1)污水处理厂的再生水直接影响到麻峪湿地微生物群落结构的变化以及微生物群落组成,再生水补水口下游1200米内河道底泥微生物群落对再生水产生净化作用,在补水口2000m处,河道底泥微生物群落结构与河道再生水补水口上游趋于相似。
(2)再生水补水口出口底泥细菌群落则主要受到立地生境中总磷浓度的影响较大,相对再生水补水与上游来水汇水过程中细菌群落则主要与氨氮的净化过程具密切关系。
(3)假单胞菌属和Geitlerinema作为河道底泥净化过程中的优势菌属表明再生水补水与上游来水混合的径向渐变过程中菌群主要与有机物和氮的降解具密切关系;气单胞菌出现在中门寺补水口说明其附近底泥细菌群落结构的变化受到磷浓度的影响较大;Variovorax paradoxus可能在降低环境中的重金属毒性方面发挥重要作用。
| [1] | 赵阳国, 任南琪, 王爱杰, 万春黎. 有机污染物对水体真细菌群落结构的影响. 微生物学报, 2007, 47(2):313-318. |
| [2] | Thurston J A, Foster K E, Karpiscak M M. Fate of indicator microorganisms, giardia and cryptosporidium in subsurface flow constructed wetlands. Water Research, 2001, 35(6):1547-1551. |
| [3] | Wassen M J, Barendregt A. Topographic position and water chemistry of fens in a Dutch river plain. Journal of Vegetation Science, 1992, 3(4):447-456. |
| [4] | 王莹. 污染河流中微生物群落结构的空间变化解析 [D]. 吉林:东北师范大学, 2008. |
| [5] | Seitzinger S, Harrison J A, Böhlke J K, Bouwman A F, Lowrance R, Peterson B, Tobias C, Van Drecht G. Denitrification across landscapes and waterscapes:A synthesis. Ecological Applications, 2006, 16(6):2064-2090. |
| [6] | 史青, 柏耀辉, 李宗逊, 冯传平, 温东辉. 应用T-RFLP 技术分析滇池污染水体的细菌群落. 环境科学, 2011, 32(6):1786-1792. |
| [7] | Liu W T, Marsh T L, Cheng H, Forney L J. Characterization of microbial diversity by determining terminal restriction fragment length polymorphisms of genes encoding 16S rRNA. Applied and Environmental Microbiology, 1997, 63(11):4516-4522. |
| [8] | Mayrand P E, Corcoran K P, Ziegle J S, Robertson J M, HoffL L B, Kronick M N. The use of fluorescence detection and internal lane standards to size PCR products automatically. Applied and Theoretical Electrophoresis, 1992, 3(1):1-11. |
| [9] | Ziegle J S, Su Y, Corcoran K P, Nie L, Eric Mayrand P, Hoff L B, McBride L, Kronick M N, Diehl S R. Application of automated DNA sizing technology for genotyping microsatellite loci. Genomics, 1992, 14(4):1026-1031. |
| [10] | 熊薇, 郭逍宇, 赵霏. 湿地芦苇根结合好气细菌群落时空分布及其与水质因子的关系. 生态学报, 2013, 33(5):1443-1455. |
| [11] | Zhang R, Thiyagarajan V, Qian P Y. Evaluation of terminal-restriction fragment length polymorphism analysis in contrasting marine environments. FEMS Microbiology Ecology, 2008, 65(1):169-178. |
| [12] | 邓福英, 臧润国. 海南岛热带山地雨林天然次生林的功能群划分. 生态学报, 2007, 27(8):3240-3249. |
| [13] | 陈明, 刘晓端, 魏连伟, 陈鸿汉, 张玲金, 王羽虹, 林剑. 永定河上游水体与底泥中污染物的分布规律. 岩矿测试, 2001, 20(2):131-135, 141-141. |
| [14] | Beauchamp E G, Drury C F. Ammonium fixation, release, nitrification and immobilization in high- and low-fixing soils. Soil Science Society of America Journal, 1991, 55(1):125-129. |
| [15] | Miñana-Galbis D, Farfán M C, Fusté M C, Lorén J G. Aeromonas bivalvium sp. nov., isolated from bivalve molluscs. International Journal of Systematic and Evolutionary Microbiology, 2007, 57(3):582-587. |
| [16] | Pianetti A, Bruscolini F, Rocchi M B L, Sabatini L, Citterio B. Influence of different concentrations of nitrogen and phosphorous on Aeromonas spp. growth. Igiene E Sanità Pubblica, 2006, 62(6):609-622. |
| [17] | Fu T X, Wei K J, Xu G H. The research and application of bacillus in aquaculture. Reservoir Fisheries, 2007, 27(3):102-104. |
| [18] | Moore E R B, Tindall B J, Martins Dos Santos V A P, Pieper D H, Ramos J L, Palleroni N J. Nonmedical:Pseudomonas. The Prokaryotes 2006, 6:646-703. |
| [19] | Andrianasolo1 E H, Goeger D, Gerwick W H. Mitsoamide:A cytotoxic linear lipopeptide from the Madagascar marine cyanobacterium Geitlerinema sp. Pure and Applied Chemistry, 2007, 79(4):593-602. |
| [20] | Abou-Shanab R A I, van Berkum P, Angle J S. Heavy metal resistance and genotypic analysis of metal resistance genes in gram-positive and gram-negative bacteria present in Ni-rich serpentine soil and in the rhizosphere of Alyssum murale. Chemosphere, 2007, 68(2):360-367. |
 2015, Vol. 35
2015, Vol. 35




