文章信息
- 周波, 唐晶磊, 代金君, 许欢, 杨小雪, 陈旭飞, 张池, 戴军
- ZHOU Bo, TANG Jinglei, DAI Jinjun, XU Huan, YANG Xiaoxue, CHEN Xufei, ZHANG Chi, DAI Jun
- 蚯蚓作用下污泥重金属形态变化及其与化学生物学性质变化的关系
- Remediating effluent sludge with earthworms: changes in heavy metal speciation and associated chemical and biological properties
- 生态学报, 2015, 35(19): 6269-6279
- Acta Ecologica Sinica, 2015, 35(19): 6269-6279
- http://dx.doi.org/10.5846/stxb201402110233
-
文章历史
- 收稿日期: 2014-02-11
- 网络出版日期: 2014-12-04
2. 广东省农业科学院饮用植物研究所, 广州 510640;
3. 莱芜市疾病预防控制中心, 莱芜 271100
2. Dringkable Plants Research Institute, Guangdong Academy of Agricultural Sciences, Guangzhou 510640, China;
3. Laiwu City Center for Disease Control and Prevention, Laiwu 271100, China
污泥是城市污水处理的产物,含有大量有机成分和氮磷钾等矿质营养成分,但同时也含有大量重金属以及病原微生物,而且其数量巨大并会产生恶臭气体,影响生态环境和人类健康,城市污泥处置已成为一个世界性的难题[1]。传统的污泥处置方法包括填埋、焚烧和农用等,填埋浪费大量土地并容易产生渗滤污染,而焚烧则需要消耗大量能源并易导致空气污染[2]。因此,在我国土地和能源紧缺的背景下,污泥农用是一种较有前景的处置方式。研究表明,污泥不经任何处理直接农用,会降低土壤微生物活性,影响植物生长,并且污泥中的重金属也会造成二次环境污染[3]。有研究者提出利用蚯蚓堆置处理污泥,蚯蚓可以促进污泥中的有机质分解,提高有效矿质营养的含量,增加重金属的生物有效性,结合植物修复技术具有用于修复污泥中重金属污染的潜力[4]。利用蚯蚓的活动改善污泥的理化性状为修复植物的正常生长提供基础的肥力条件,增加修复植物的生物量,同时提高重金属的生物有效性,从而促进修复植物对重金属的吸收,最终降低污泥重金属的含量[5, 6, 7]。也有研究者发现蚯蚓在控制污泥微生物数量的同时,可以增强微生物的活性[8, 9]。然而,蚯蚓作用对污泥中不同重金属形态的影响,对氧化还原条件、化学和微生物性质的影响,以及在蚯蚓作用下重金属形态和理化、微生物特征之间内在关系的系统研究较少。
为此,本研究以新鲜城市脱水污泥为研究对象,接种赤子爱胜蚓(Eisenia fetida)进行室内培养试验,系统研究蚯蚓作用下污泥重金属形态的变化,及其与污泥氧化还原条件、化学和微生物性质变化的关系,以期为蚯蚓-超富集植物联合修复技术在污泥重金属处理中的应用提供理论依据。
1 材料与方法 1.1 供试材料供试污泥为取自东莞市虎门污水处理厂的新鲜脱水污泥,废水来源主要是城市生活污水及工业废水,污泥含水量约为70%,基础理化性质见表1。供试蚯蚓为实验室自行培养的赤子爱胜蚓(Eisenia fetida),挑选单条鲜重0.35 g左右的健壮蚯蚓进行试验。
| 指标 Index | pH | 电导率 Electrical conductivity/ (ms/cm) | 有机碳 Organic carbon/ (g/kg) | 全氮 Total N/ (g/kg) | C/N | 全磷 Total P/ (g/kg) | 全钾 Total K/ (g/kg) | Fe/ (g/kg) |
| 数值Value | 6.49 | 1.32 | 219.92 | 27.39 | 8.03 | 21.31 | 6.62 | 50.35 |
| 指标 Index | Mn/ (mg/kg) | Pb/ (mg/kg) | Cr/ (mg/kg) | Cd/ (mg/kg) | Cu/ (mg/kg) | Zn/ (mg/kg) | Ni/ (mg/kg) | |
| 数值Value | 500.6 | 88.1 | 942.7 | 1.5 | 1546.7 | 1887.2 | 58.7 |
试验分蚯蚓处理组和同条件不加蚯蚓对照组,每组3个重复。取相当于400 g干重的新鲜污泥装入直径15 cm高20 cm的圆形塑料花盆中,底部和上口均放置35目孔径的塑料纱网防止蚯蚓逃逸。蚯蚓处理组每盆接种20条单重在(0.35±0.03) g的健壮蚯蚓,总重量为7 g左右,重复间无显著差异,并记录蚯蚓总重。所有处理均置于室内,用黑色遮阴网遮光,室温维持(25±1) ℃,并采用称重法每天补充蒸馏水维持污泥含水量在60%—70%。试验维持80 d,每20 d检查1次蚯蚓处理组蚯蚓的数量和生物量,将蚯蚓计数,并用蒸馏水漂洗干净,用吸水纸轻轻擦干称重,然后将所有蚯蚓重新接种回原污泥中。同时将对照组进行翻堆,保持和蚯蚓处理组的一致性。原始污泥和试验结束后的污泥,均一部分冷藏于4 ℃冰箱,用于分析测试氧化还原状况及微生物特征的相关指标;另一部分风干、磨细过筛,用于测试重金属形态和基础理化性质。
1.3 样品测定方法不同化学形态重金属含量的测定参考BCR(European Community Bureau of Reference,BCR欧洲共同体参考局)连续浸提法[10],用蒸馏水(固液比1∶40)浸提为水溶态;继续用0.11 mol/L醋酸(固液比1∶40)浸提为交换态;继续用0.5 mol/L的盐酸羟胺(固液比1∶40)浸提为铁锰态;继续用30%的H2O2消化残渣中的有机质后,用1 mol/L的醋酸铵(固液比1∶50)浸提为有机态;剩余残渣烘干后用三酸消煮法测定重金属为残渣态。
氧化还原物质的量可以反映氧化还原的数量因素,除影响重金属形态外,对污泥营养状况和修复植物的生长具有重要作用。游离氧化铁的测定采用连二亚硫酸钠-柠檬酸钠-重碳酸钠提取法,非晶质氧化铁采用酸性草酸铵溶液提取法,络合态铁采用焦磷酸钠提取法。还原性物质总量的测定采用硫酸铝浸提-重铬酸钾氧化法,活性还原性物质采用高锰酸钾滴定法,亚铁含量采用邻菲罗啉比色法,活性有机还原性物质为活性还原性物质与亚铁含量的差[11]。
pH值和电导率用pH计和电导率仪测定,水土比分别为2.5∶1和5∶1;有机碳、全氮、胡敏酸、富里酸、硝态氮(NO-3-N)、铵态氮(NH+4-N)、全磷、有效磷、全钾、速效钾等影响修复植物生长的养分指标的测定均参照土壤农化常规分析法[12]。
酶和微生物相关指标值可以反映污泥中微生物的数量和活性,而微生物不论是对重金属的形态还是对超富集植物的生长都具有重要影响。脲酶采用苯酚钠比色法测定,活性以每千克污泥每天产生的NH+4-N表示(g kg-1 d-1)。过氧化氢酶采用KMnO4容量法测定,活性以每克污泥消耗的0.004 mol/L高锰酸钾表示(mL/g)。转化酶采用滴定法测定,酶活性以每克污泥37 ℃培养24 h后消耗的0.1 mol/L硫代硫酸钠表示(mL g-1 d-1)。β-葡萄糖苷酶和荧光素二乙酸酯酶均利用各自酶促反应试剂、采用比色法进行测定,β-葡萄糖苷酶的活性以蔗糖为基质,在单位时间内经单位重量污泥作用后生成的还原糖的量表示(mg g-1 d-1)。荧光素二乙酸酯酶的活性以荧光素二乙酸为基质,在单位时间内经单位重量污泥作用后生成的荧光素的量表示(mg g-1 h-1)。微生物量碳采用氯仿熏蒸-硫酸钾浸提法测定。呼吸量采用NaOH密闭吸收法测定,用单位重量的污泥在单位时间内产生的CO2量表示。呼吸速率为单位时间内单位有机碳含量的呼吸量(g Kg-1 d-1)。微生物熵通过微生物量碳与有机碳的百分比来确定。代谢熵以单位微生物量碳每天产生的CO2量表示(mgCco2/gCbio)。细菌、真菌、放线菌的测定采用平板计数法[12]。
1.4 数据统计利用方差和多重比较分析不同处理间重金属形态和化学及生物学指标的差异。采用主成分分析(Principal Components Analysis)借助ADE-4 软件,将多个相互关联的变量进行综合分析,利用二维空间载荷图和得分图反映分析结果,并应用置换检验(Permutation test)比较不同处理间污泥综合属性特征的差异水平。数据统计采用SAS统计软件(SAS 8.0 Software,SAS Institute Inc.)和 ADE-4多元数据分析软件[13]。
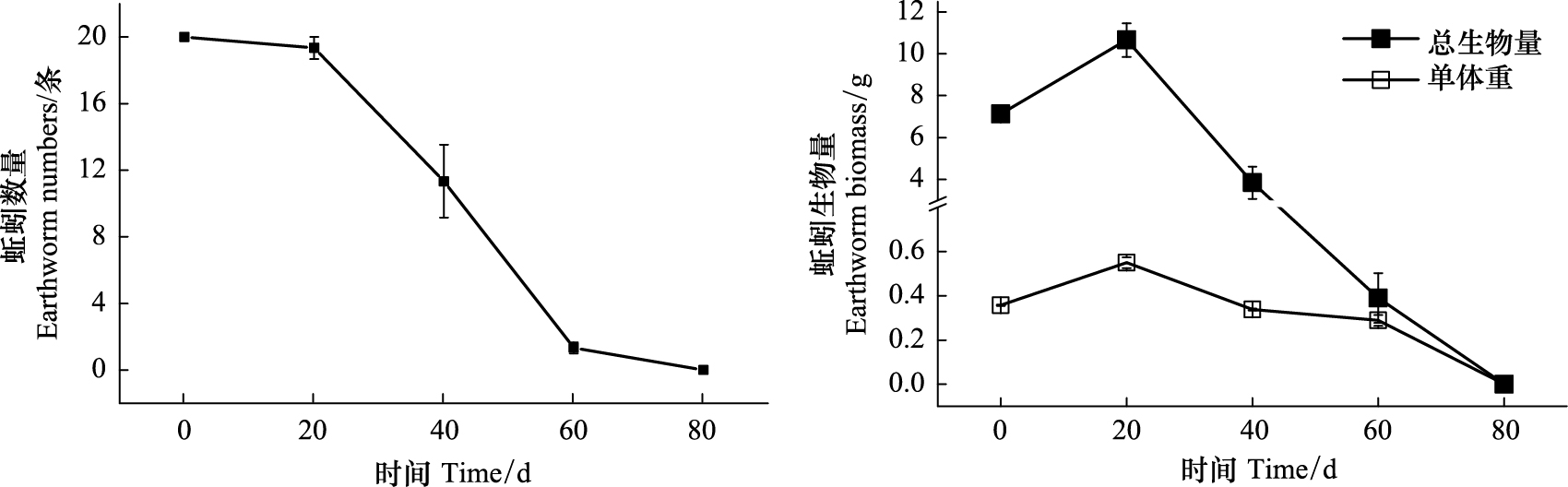
2 结果与分析 2.1 蚯蚓在污泥中的生长情况试验期间,蚯蚓处理组的蚯蚓数量在前20 d基本不变,20 d之后呈逐渐下降趋势(图1),到第80天时蚯蚓全部消失。整个培养过程中,蚯蚓的活性正常,但没有蚓茧和幼蚓产生。总生物量和单体重均在第20天时达到最大值,分别为10.66 g和0.55 g,总生物量增加了52%,之后呈逐渐下降趋势(图1)。
|
| 图 1 蚯蚓数量和生物量变化 Fig.1 Changes of earthworm number and biomass |
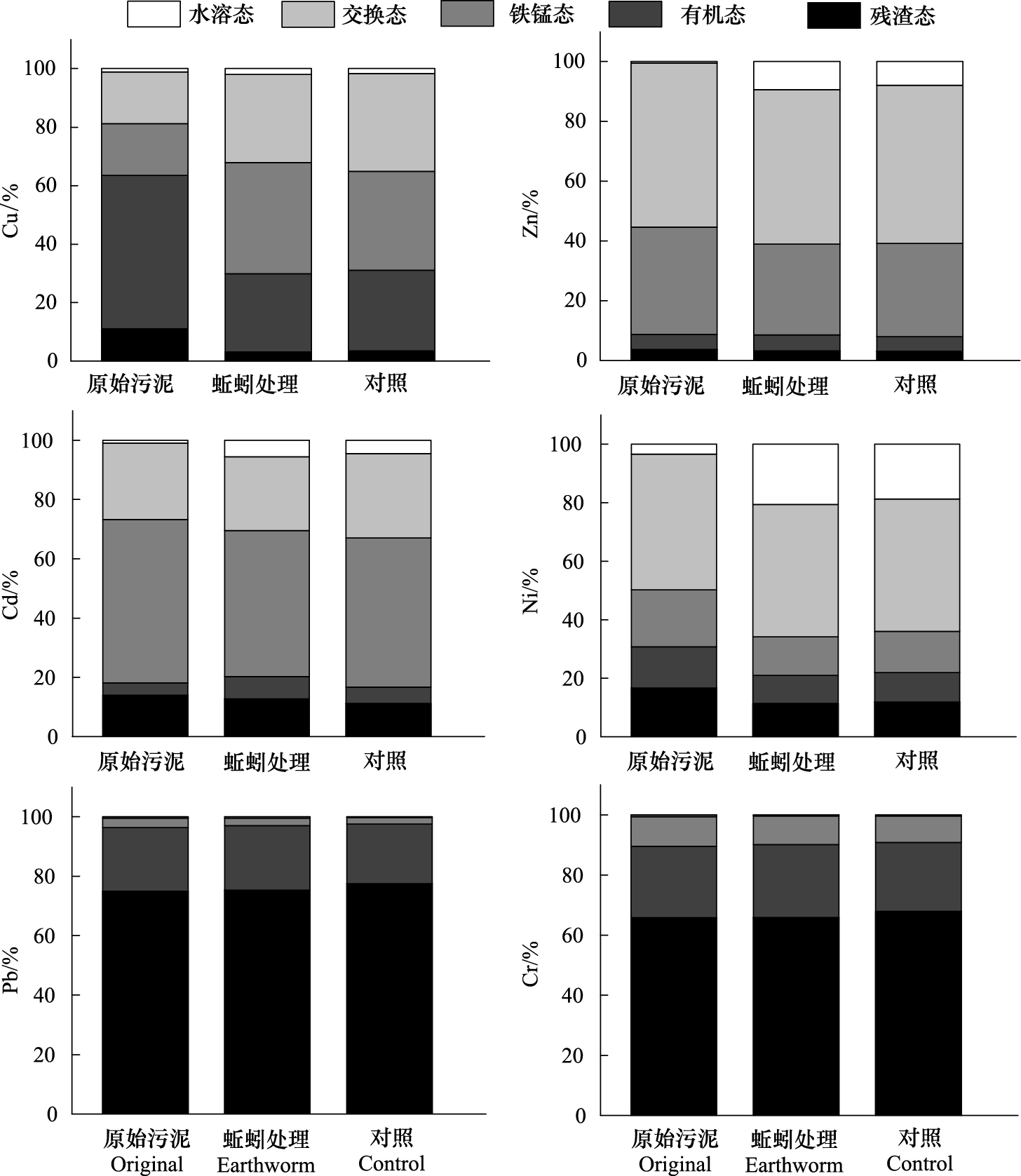
本试验中蚯蚓处理未降低污泥中重金属的总含量,但对部分重金属的化学形态具有显著影响。6种重金属中Cu、Zn、Cd、Ni的残渣态所占重金属总量的比例下降,交换态和水溶态比例上升,与之相反的是,Pb和Cr的残渣态比例增加,交换态和水溶态比例降低(图2)。
|
| 图 2 污泥重金属形态变化 Fig.2 Variations of speciation of six heavy metals of sludge |
各重金属形态变化幅度较大的主要包括:Cu在蚯蚓处理组和对照组中的残渣态所占总量的比例分别从11%下降到3%和4%,有机态比例都从53%下降为27%,铁锰态比例则从18%升高到38%和34%,交换态从18%升高到30%和33%,下降和上升的幅度都达到显著水平,但是蚯蚓处理组和对照组的差异不显著(P > 0.05);Zn、Cd、Ni的残渣态、有机态和交换态单独的变化幅度都不显著,而它们的铁锰态比例均显著下降,水溶态比例均显著上升,与Cu的结果类似,蚯蚓组的下降和上升幅度均大于对照组,但均未达显著水平。此外,在蚯蚓处理中Pb和Cr均表现出与上述重金属不同的规律。Pb、Cr在蚯蚓组和对照组中所有形态的变化幅度均未达显著水平。
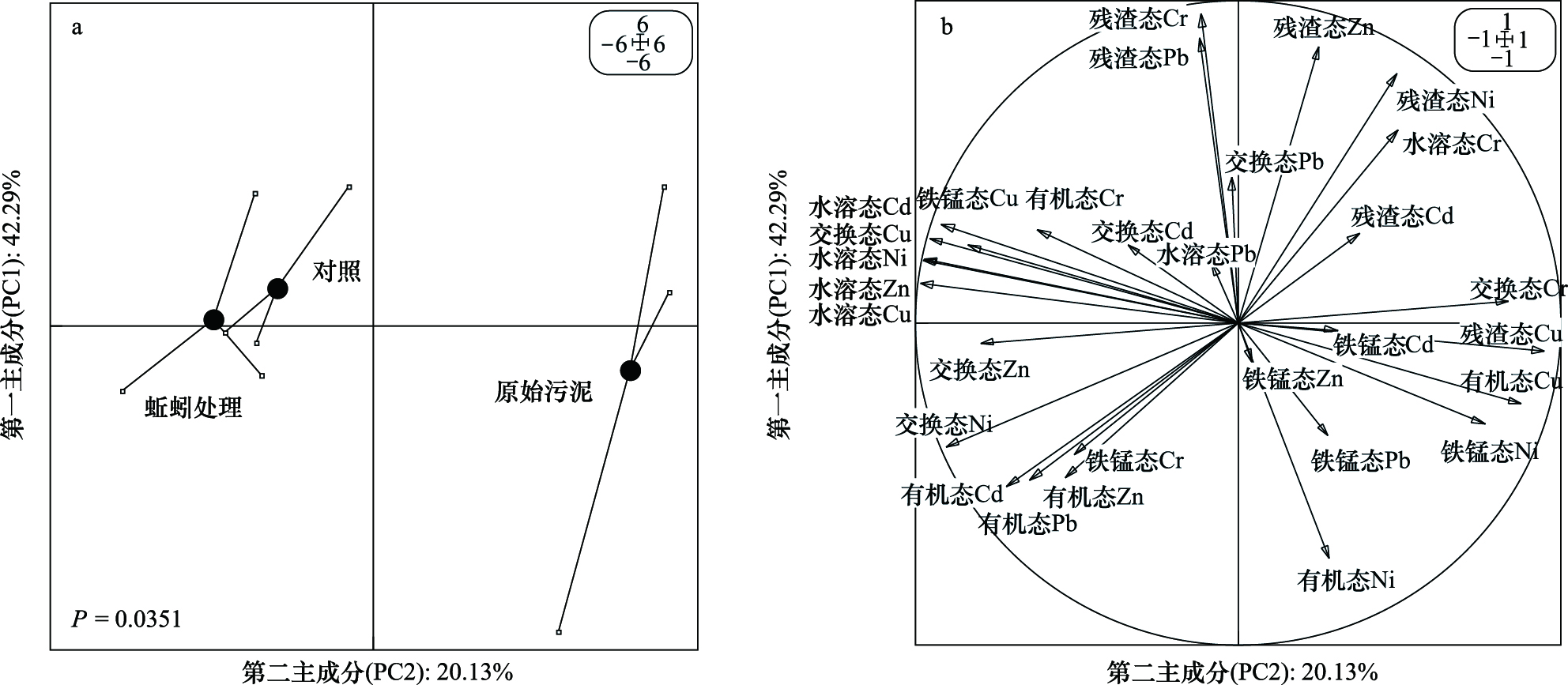
对重金属各化学形态含量的变化情况进行综合分析(图3),由图3a可见,蚯蚓作用对重金属化学形态的综合影响效果达到了显著程度(P=0.0351),蚯蚓处理组显著向第一主成分的负方向偏移。由图3b可知,第一主成分的负方向主要代表的是水溶态和交换态Cu、Zn、Cd、Ni等的信息。由此可见,蚯蚓作用显著促进了Cu、Zn、Cd、Ni等重金属向水溶态和交换态等形态转变。
|
| 图 3 各处理污泥重金属形态的主成分分析 Fig.3 Principal component analysis of sludge heavy metal speciation in treatments |
污泥氧化还原性物质的变化情况如表2所示。氧化性物质和还原性物质的量可以表征氧化还原的数量因素,特别是后者能在很大程度上影响各种离子的有效性、土壤养分及植物生长。本研究中测定的3种污泥氧化性物质的含量,蚯蚓组与对照组均差异不显著(P > 0.05),蚯蚓作用对污泥氧化性物质的含量均未产生显著影响。但蚯蚓处理组的还原性物质总量、活性还原性物质和活性有机还原性物质的含量均显著低于对照组,蚯蚓作用可以显著降低除亚铁外的其余3种还原性物质的含量。
| 氧化性物质Oxidizing substances | 还原性物质reductive substance | ||||||
| 处理 Treatment | 游离氧化铁 (Fe2O3) Free iron oxide/ (g/kg) | 非晶质氧化 铁(Fe2O3) Amorphous iron oxide / (g/kg) | 络合态铁(Fe) Complex iron/ (g/kg) | 还原性 物质总量 Total reductive substance/ (cmol/kg) | 活性还原物质 Active reductive substance/ (cmol/kg) | 亚铁含 量(Fe2+) Ferrous iron/ (cmol/kg) | 活性有机 还原物质 Active organic reductive substance/ (cmol/kg) |
| 平均值±标准差(n=3),表中同一列数据后跟相同小写字母者表示在方差分析中于0.05水平上无显著差异 | |||||||
| 原始污泥 Original sludge | 33.32±2.48b | 30.32±3.17a | 6.31±0.74b | 12.93±3.11a | 6.50±0.55a | 0.26±0.02a | 6.24±0.54a |
| 蚯蚓处理 Earthworm | 38.64±4.86a | 28.98±2.12a | 7.88±0.33a | 4.92±0.66c | 1.75±0.66c | 0.16±0.01b | 1.56±0.66c |
| 对照Control | 41.92±0.91a | 27.64±0.78a | 7.38±0.15a | 7.13±1.22b | 3.00±0.33b | 0.19±0.01b | 2.83±0.33b |
| F | 12.29 | 0.75 | 10.00 | 7.99 | 26.97 | 12.20 | 26.16 |
| P | 0.0160 | 0.6068 | 0.0233 | 0.0344 | 0.0037 | 0.0163 | 0.0040 |
表3为部分与污泥肥力相关的化学性质的变化情况,蚯蚓组的pH值显著高于对照组,但二者均显著低于原始污泥,蚯蚓作用减缓了pH值的降低速度。由于蚯蚓自身的新陈代谢消耗了部分有机养分,蚯蚓组总有机碳和富里酸的含量均显著低于对照组。蚯蚓组铵态氮的含量显著低于对照组,而硝态氮的含量则显著高于对照组,蚯蚓作用显著降低了对作物具有毒害作用的铵态氮的含量,并显著升高了作物可以吸收利用的硝态氮的含量。蚯蚓组和对照组中其它种类矿质养分的差异未达到显著水平。
| 处理 Treatment | 酸碱度 Acidity-basicity pH | 腐殖质Humic substance | 全量及有效养分Total and available nutrition | |||||||||
| 总有机碳 Total organic carbon/ (g/kg) | 胡敏酸 Humic acid/ (g/kg) | 富里酸 Fulvic acid/ (g/kg) | 全氮 Total N/ (g/kg) | NO-3-N/ (mg/kg) | NH+4-N/ (mg/kg) | 全磷 Total P/ (g/kg) | 有效磷 Available P/ (mg/kg) | 全钾 Total K/ (g/kg) | 速效钾 Available K/ (mg/kg) | 电导率 Electrical conductivity/ (ms/cm) | ||
| 原始污泥 Original sludge | 6.49±0.07a | 219.92±1.27a | 24.88±2.43a | 103.26±1.78a | 27.39±0.60a | 693.7±11.3c | 989.1±14.1a | 21.31±0.64a | 363.4±13.1a | 6.62±0.11a | 568.5±25.6a | 1.32±0.04b |
| 蚯蚓处理 Earthworm | 5.62±0.12b | 179.22±3.48c | 20.38±1.11a | 81.75±2.27c | 23.06±0.46b | 2608.4±170.3a | 118.3±5.5c | 21.60±0.82a | 350.4±25.7a | 6.66±0.22a | 537.7±26.6a | 2.61±0.31a |
| 对照Control | 5.20±0.15c | 194.00±2.83b | 19.02±2.36a | 97.17±1.07b | 23.34±1.14b | 2276.9±95.5b | 197.2±6.0b | 21.83±0.38a | 364.2±19.2a | 6.96±0.22a | 630.0±27.6a | 2.56±0.18a |
| F | 43.92 | 378.75 | 5.99 | 119.40 | 14.49 | 85.46 | 355.10 | 0.22 | 17.60 | 3.04 | 6.40 | 14.88 |
| P | 0.0015 | <0.0001 | 0.0555 | 0.0002 | 0.0120 | 0.0004 | <0.0001 | 0.9131 | 0.084 | 0.1532 | 0.0598 | 0.0114 |
表4为污泥部分生物学性质的变化情况,蚯蚓处理组的过氧化氢酶活性显著升高,这反映出该组污泥中微生物的活性有所增强,而转化酶和荧光素二乙酸酯酶的活性显著降低,这主要与污泥中有机碳含量和微生物数量降低有关。蚯蚓处理组的微生物量碳含量显著低于对照组,而代谢熵则显著高于对照组,这也说明了蚯蚓处理降低了微生物的数量,但是微生物的活性增强了。可培养微生物中真菌和放线菌数量的显著降低也在一定程度上反映出了微生物数量的下降。
| 处理 Treatment | 部分氧化和水解酶 Some oxidation and hydrolytic enzymes | 微生物数量和活性 The number and activity of microorganisms | 可培养微生物 Culturable microorganisms | ||||||||
| 过氧化氢酶 Catalase/ (ml/g) | 脲酶 Urease/ (g kg-1 d-1) | 转化酶 Invertase/ (mL g-1 d-1) | β-葡萄糖苷酶 β-glucosidase/ (mg g-1 d-1) | 荧光素二乙酸 酯酶FDA/ (mg g-1 h-1) | 微生物量碳 Microbial biomass C/ (g/kg) | 呼吸速率 Respiration rate/ (g/kg/d) | 微生物熵 Microbial quotient/% | 代谢熵 Metabolic quotient/ (mgCco2/ gCbio) | 细菌 Bacteria/ (×106cfu/g) | 真菌 Fungi/ (×103cfu/g) | |
| 原始污泥 Original sludge | 40.88±0.69c | 0.37±0.06a | 9.93±1.09a | 1.64±0.18a | 1.77±0.12a | 5.30±0.86a | 25.85±1.48a | 2.41±0.38a | 1080±370c | 95.83±20.23a | 23.33±2.11a |
| 蚯蚓处理 Earthworm | 43.51±0.14a | 0.15±0.09b | 4.05±0.66c | 1.56±0.04a | 1.19±0.20b | 2.59±0.33c | 12.95±1.39b | 1.44±0.18b | 1710±260a | 33.00±6.80b | 8.21±3.05c |
| 对照Control | 41.42±0.92b | 0.13±0.08b | 6.80±1.49b | 1.63±0.26a | 1.51±0.08a | 3.42±0.19b | 15.77±1.44b | 1.76±0.12b | 1440±190b | 48.17±6.25b | 16.71±2.14b |
| F | 18.02 | 8.24 | 8.03 | 0.29 | 7.24 | 9.64 | 32.22 | 9.19 | 9.15 | 20.35 | 14.55 |
| P | 0.0080 | 0.0410 | 0.0341 | 0.8738 | 0.0406 | 0.0249 | 0.0027 | 0.0299 | 0.0295 | 0.0064 | 0.0119 |
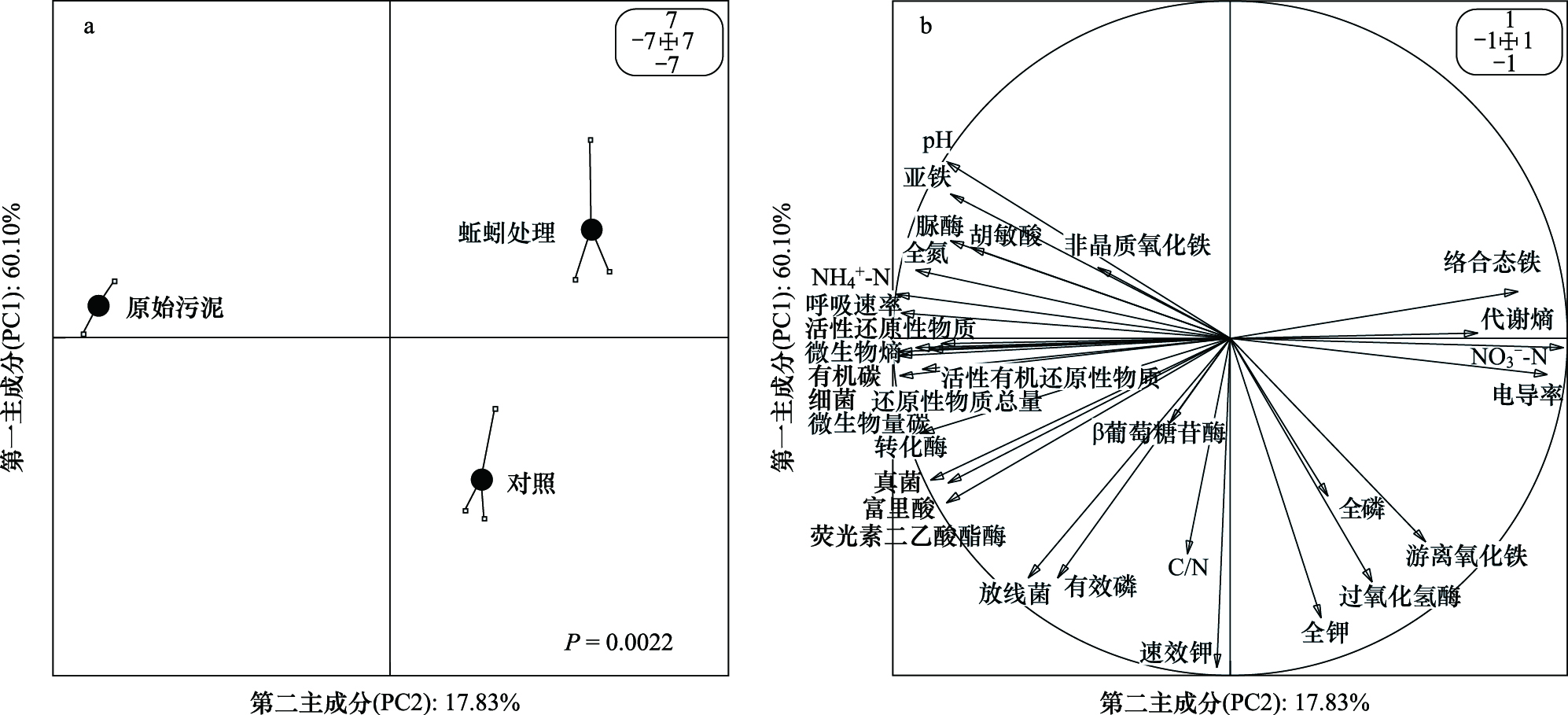
对蚯蚓作用下污泥化学和生物学性质的变化情况进行综合分析(图4)发现,蚯蚓作用对污泥和化学和生物学性质的综合影响达到显著水平(P=0.0022),与对照组相比蚯蚓处理组偏向于第一和第二主成分的正方向(图4)。由图4结合表2—表4分析可知,第一主成分正方向主要是硝态氮和代谢熵较高,而铵态氮、还原性物质的量和微生物数量较低的方向,第二主成分的正方向则主要是pH值较高的方向。综上所述,蚯蚓作用显著降低了还原性物质的含量,减缓了pH值的下降速度,减少了有机碳和铵态氮的含量,同时增加了硝态氮的含量。降低了反映微生物数量的相关指标值,但升高了与其活性相关的指标值。
|
| 图 4 各处理污泥化学及生物学属性的主成分分析 Fig.4 Principal component analysis of sludge chemical and biological properties in treatments |
将在蚯蚓作用下污泥中发生显著变化的重金属形态与化学和生物学性质进行相关分析(表5)。交换态和水溶态Cu、Zn、Cd、Ni与3种还原性物质的含量均表现出负相关关系,并多数都达到了显著或极显著的水平;多数交换态和水溶态Cu、Zn、Cd、Ni与pH值均呈显著或极显著的负相关,除交换态Zn外,与有机碳、铵态氮均呈显著或极显著的负相关,而与硝态氮均呈显著或极显著的正相关;交换态和水溶态Cu、Zn、Cd、Ni均与表征微生物活性的代谢熵、过氧化氢酶呈正相关,而与表征微生物数量的微生物量碳、真菌、转化酶、荧光素二乙酸酯酶等指标均呈负相关,并且上述相关多数达到显著或极显著水平。
| 指标 Index | 还原性物质 reductive substance | 肥力相关 Fertilizer | 微生物数量和活性 The number and activity of microorganisms | ||||||||||
| 还原性物 质总量 Total reductive matter | 活性还 原物质 Active reductive matter | 活性有机 还原物质 Active organic reductive matter | pH | 有机碳 Organic carbon | NO3--N | NH4+-N | 代谢熵 Metabolic quotient | 过氧化氢酶 Catalase | 转化酶 Invertase | 荧光素二 乙酸酯酶 FDA | 微生物量碳 Microbial biomass C | 真菌 Fungi | |
| n=9,*两个指标间相关性显著(P < 0.05),**两指标间相关性极显著(P < 0.01) | |||||||||||||
| 交换态Cu Exchangeable | -0.68* | -0.82** | -0.82** | -0.86** | -0.66 | 0.80** | -0.82** | 0.47 | 0.68* | -0.63 | -0.60 | -0.66 | -0.64 |
| 交换态Zn Exchangeable | -0.75* | -0.66 | -0.66 | -0.70* | -0.57 | 0.67* | -0.69* | 0.48 | 0.75* | -0.54 | -0.51 | -0.68* | -0.61 |
| 交换态Cd Exchangeable | -0.87** | -0.76* | -0.76* | -0.77* | -0.84** | 0.84** | -0.86** | 0.64 | 0.51 | -0.71* | 0.60 | -0.82** | -0.63 |
| 交换态Ni Exchangeable | -0.75* | -0.72* | -0.72* | -0.65 | -0.73* | 0.78* | -0.77* | 0.45 | 0.77* | -0.55 | -0.70* | -0.71* | -0.69* |
| 水溶态Cu Water-soluble | -0.91** | -0.95** | -0.95** | -0.84** | -0.92** | 0.98** | -0.97** | 0.68* | 0.66 | -0.86** | -0.84** | -0.91** | -0.88** |
| 水溶态Zn Water-soluble | -0.9** | -0.97** | -0.97** | -0.84** | -0.93** | 0.98** | -0.97** | 0.67* | 0.78* | -0.88** | -0.86** | -0.89** | -0.89** |
| 水溶态Cd Water-soluble | -0.85** | -0.96** | -0.96** | -0.80** | -0.92** | 0.97** | -0.95** | 0.67* | 0.68* | -0.89** | -0.88** | -0.86** | -0.92** |
| 水溶态Ni Water-soluble | -0.90** | -0.96** | -0.96** | -0.86** | -0.94** | 0.99** | -0.98** | 0.68* | 0.81** | -0.88** | -0.85** | -0.89** | -0.87** |
在本试验条件下,蚯蚓在污泥中可以正常存活和生长,前期总生物量显著升高(图1),但随着时间的延长,蚯蚓可利用的营养成分含量下降,营养限制使其数量和生物量都逐渐下降[14],因此,在利用蚯蚓处理污泥过程中应注意处理时间的选择,并可补充适量有机物料。
本研究结果显示,蚯蚓作用可以促进Cu、Zn、Cd、Ni等重金属向交换态和水溶态转化,但对Pb、Cr化学形态的影响较小(图2),并且蚯蚓对重金属形态影响的综合效果达到显著水平(P = 0.0351,图3)。本研究结果说明蚯蚓具有活化污泥中Cu、Zn、Cd、Ni等重金属的作用,这与Sizmur 等人的研究结果一致[15, 16]。然而,在本试验中蚯蚓对Pb、Cr等重金属的形态未产生显著影响,这说明Pb、Cr等重金属在污泥中形态较为稳定,不容易被活化,Wang等[17]在对污泥重金属形态的研究中也发现了类似的结果。
本研究结果还显示,蚯蚓处理组的还原性物质总量、活性还原性物质和有机还原性物质的量都显著下降(表2),这说明蚯蚓作用可以显著降低污泥中还原性物质的量,促进污泥从还原态向氧化态转变。还原性物质含量的下降可以减少污泥对重金属离子的专性吸附,促进其活化[18]。本研究中,还原性物质总量、活性还原性物质和有机还原性物质的量与Cu、Zn、Cd、Ni的水溶态、交换态含量多数呈显著或极显著的负相关关系(表5),也进一步说明蚯蚓作用可能会通过降低污泥中还原性物质的量,改变其氧化还原状态,进而促进重金属活化。此外,还原性物质含量下降,更有利于修复植物在污泥中的生长[19],这也是蚯蚓应用于污泥重金属治理中的一个重要作用。
Kocik等人在研究蚯蚓对污泥的影响时未观测到pH值的显著变化[20],而本研究中,蚯蚓处理组的pH值显著高于对照组(表3),蚯蚓作用促进pH值趋向于中性。蚯蚓处理组总有机碳和富里酸的含量显著降低,这主要与蚯蚓自身代谢有关,也进一步说明在处理过程中适量补充有机物料的重要性[21]。此外,蚯蚓处理组的铵态氮含量显著降低,而硝态氮含量则显著升高(表3),这可能与蚯蚓促进有机氮的矿化和铵态氮的转化有关[22],这说明蚯蚓作用可以促进污泥中的铵态氮向硝态氮转化,这对修复植物在污泥中的生长有利。水溶态和交换态Cu、Zn、Cd、Ni与pH值多数具有显著或极显著的负相关关系(表5),酸性环境更利于重金属活化,蚯蚓作用会促进pH值趋于中性,但本试验中蚯蚓处理组和对照组的污泥pH值均介于5.20—5.62之间,pH值的改变幅度较小,故其对重金属形态的影响也比较微弱。此外,蚯蚓显著促进硝态氮含量升高,而硝态氮与水溶态和交换态Cu、Zn、Cd、Ni也多数具有显著或极显著的正相关关系(表5),蚯蚓是否会通过硝态氮的改变影响重金属形态,还有待进一步研究。
在本研究中,蚯蚓处理组的过氧化氢酶和代谢熵显著升高,而微生物量碳、转化酶、荧光素二乙酸酯酶、真菌和放线菌数量都显著下降(表4),这说明蚯蚓作用增加了微生物的活性,但是减少了微生物的数量。可能是因为蚯蚓会吞食某些微生物[23],这也与wani等[24]和Aira等[25]研究的蚯蚓对微生物种群的影响结果一致。蚯蚓作用改变了微生物种群结构,使其趋于年轻化[26],同时微生物数量减少,营养来源相对充足,因而剩余微生物的活性反而增强[27]。而过氧化氢酶、代谢熵与水溶态和交换态Cu、Zn、Cd、Ni多数呈显著或极显著的正相关(表5),说明蚯蚓作用增强了微生物的活性,进而促进了重金属的活化。
4 结论试验前期蚯蚓在污泥中能正常生长和存活,前20 d总生物量增加了52%。蚯蚓可以显著促进污泥中的Cu、Zn、Cd、Ni等重金属从残渣态、有机态和铁锰态等稳定形态向交换态和水溶态等有效形态转化(P = 0.0351)。还可以显著降低污泥中还原性物质的含量,减缓pH值下降速度,降低总有机碳含量,促进铵态氮向硝态氮转化,减少污泥微生物的数量并增加其种群活性(P = 0.0022)。蚯蚓作用下,污泥中重金属的活化程度与还原性物质的含量呈显著负相关,而与微生物种群的活性呈显著正相关(P < 0.05)。综上所述,蚯蚓可以促进污泥重金属的活化,并改善污泥的肥力条件,为修复植物在污泥中的正常生长和对重金属离子的快速吸收提供有利条件。
致谢:感谢李志安研究员对本文写作的帮助。
| [1] | Xu J Q,Yu R L,Dong X Y,Hu G R,Shang X S,Wang Q,Li H W. Effects of municipal sewage sludge stabilized by fly ash on the growth of manilagrass and transfer of heavy metals. Journal of Hazardous Materials,2012,217:58-66. |
| [2] | Zheng G D,Chen T B,Gao D,Luo W. Dynamic of lead speciation in sewage sludge composting. Water Science Technology,2004,50(9):75-82. |
| [3] | Nowak B,Aschenbrenner P,Winter F. Heavy metal removal from sewage sludge ash and municipal solid waste fly ash-a comparison. Fuel Processing Technology,2013,105:195-201. |
| [4] | Khwairakpam M,Bhargava R. Vermitechnology for sewage sludge recycling. Journal of Hazardous Materials,2009,161(2/3):948-954. |
| [5] | Ruiz E,Alonso-Azcárate J,Rodríguez L. Lumbricus terrestris L. activity increases the availability of metals and their accumulation in maize and barley. Environmental Pollution,2011,159(3):722-728. |
| [6] | Sizmur T,Palumbo-Roe B,Watts M J,Hodson M E. Impact of the earthworm Lumbricus terrestris (L.) on As, Cu, Pb and Zn mobility and speciation in contaminated soils. Environmental Pollution,2011,159(3):742-748. |
| [7] | Jusselme M D,Poly F,Miambi E,Mora P,Blouin M,Pando A,Rouland-Lefèvre C. Effect of earthworms on plant Lantana camara Pb-uptake and on bacterial communities in root-adhering soil. Science of the Total Environment,2012,416:200-207. |
| [8] | Liu J,Lu Z,Yang J,Xing M,Yu F,Guo M. Effect of earthworms on the performance and microbial communities of excess sludge treatment process in vermifilter. Bioresource Technology,2012,117:214-221. |
| [9] | Yang J,Liu J,Xing M,Lu Z,Yan Q. Effect of earthworms on the biochemical characterization of biofilms in vermifiltration treatment of excess sludge. Bioresource Technology,2013,143:10-17. |
| [10] | Rauret G,López-Sánchez J F,Sahuquillo A,Rubio R,Davidson C,Ure A,Quevauviller P H. Improvement of the BCR three step sequential extraction procedure prior to the certification of new sediment and soil reference materials. Journal of Environmental Monitoring,1999,1(1):57-61. |
| [11] | 鲁如坤. 土壤农业化学分析方法. 北京: 中国农业科技出版社,2000. |
| [12] | 李振高,骆永明,滕应. 土壤与环境微生物研究法. 北京: 科学出版社,2008. |
| [13] | Thioulouse J,Chessel D,Dole S,Olivier J M. ADE-4: a multivariate analysis and graphical display software. Statistics and Computing,1997,7(1):75-83. |
| [14] | Curry J P,Doherty P,Purvis G,Schmidt O. Relationships between earthworm populations and management intensity in cattle-grazed pastures in Ireland. Applied Soil Ecology,2008,39(1):58-64. |
| [15] | Sizmur T,Hodson M E. Do earthworms impact metal mobility and availability in soil?-A review. Environmental Pollution,2009,157(7):1981-1989. |
| [16] | Sizmur T,Tilston E L,Charnock J,Palumbo-Roe B,Watts M J,Hodson M E. Impacts of epigeic, anecic and endogeic earthworms on metal and metalloid mobility and availability. Journal of Environmental Monitoring,2011,13(2):266-273. |
| [17] | Wang C,Hu X,Chen M,Wu Y. Total Concentrations and Fractions of Cd, Cr, Pb, Cu, Ni and Zn in sewage sludge From municipal and industrial wastewater treatment plants. Journal of Hazardous Materials,2005,119(1/3):245-249. |
| [18] | Hao T,Yang C,Rao X,Wang J,Niu C,Su X. Facile additive-free synthesis of iron oxide nanoparticles for efficient adsorptive removal of Congo red and Cr (VI). Applied Surface Science,2014,292:174-180. |
| [19] | 黄昌勇. 土壤学. 北京: 中国农业出版社,2000:180-182. |
| [20] | Kocik A,Truchan M,Rozen A. Application of willows (Salix viminalis) and earthworms (Eisenia fetida) in sewage sludge treatment. European Journal of Soil Biology,2007,43:S327-S331. |
| [21] | Gupta R,Mutiyar P K,Rawat N K,Saini M S,Garg V K. Development of a water hyacinth based vermireactor using an epigeic earthworm Eisenia foetida. Bioresource Technology,2007,98(13):2605-2610. |
| [22] | Costello D M,Lamberti G A. Non-native earthworms in riparian soils increase nitrogen flux into adjacent aquatic ecosystems. Oecologia,2008,158(3):499-510. |
| [23] | Fusilero M A,Mangubat J,Ragas R E,Baguinon N,Taya H,Rasco E Jr. Weed management systems and other factors affecting the earthworm population in a banana plantation. European Journal of Soil Biology,2013,56:89-94. |
| [24] | Wani K A,Mamta,Rao R J. Bioconversion of garden waste, kitchen waste and cow dung into value-added products using earthworm Eisenia fetida. Saudi Journal of Biological Sciences,2013,20(2):149-154. |
| [25] | Aira M,Monroy F,Domínguez J. Earthworms strongly modify microbial biomass and activity triggering enzymatic activities during vermicomposting independently of the application rates of pig slurry. Science of the Total Environment,2007,385(1):252-261. |
| [26] | Zhang B G,Li G T,Shen T S,Wang J K,Sun Z. Changes in microbial biomass C, N, and P and enzyme activities in soil incubated with the earthworms Metaphire guillelmi or Eisenia fetida. Soil Biology and Biochemistry,2000,32(14):2055-2062. |
| [27] | Marichal R,Mathieu J,Couteaux M M,Mora P,Roy J,Lavelle P. Earthworm and microbe response to litter and soils of tropical forest plantations with contrasting C:N:P stoichiometric ratios. Soil Biology & Biochemistry,2011,43(7):1528-1535. |
 2015, Vol. 35
2015, Vol. 35




