文章信息
- 肖协文, 王玉玉, 张欢, 于秀波
- XIAO Xiewen, WANG Yuyu, ZHANG Huan, YU Xiubo
- 饶河枯水期主要鱼类营养级位置及其影响因素
- Trophic position and its impact on fish in Raohe River during the dry season, Jiangxi Province
- 生态学报, 2015, 35(18): 6216-6223
- Acta Ecologica Sinica, 2015, 35(18): 6216-6223
- http://dx.doi.org/10.5846/stxb201401240180
-
文章历史
- 收稿日期: 2014-01-24
- 网络出版日期: 2014-11-19
2. 北京林业大学自然保护区学院, 北京 100083;
3. 中国科学院大学, 北京 100049
2. School of Nature Conservation, Beijing Forestry University, Beijing 100083, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China
河流食物网描述了河流生态系统中生物与生物之间复杂的营养关系及生物有机体在网络结构中所处的等级或位置,是河流生态系统结构与功能的重要组成部分[1]。研究河流食物网有利于了解生物之间的营养关系与能量流动过程[2]。同样,加强对河流食物网中消费者之间的营养级关系研究对于深入理解河流生态系统的结构与功能具有重要意义,能够为河流生态系统的健康发展和管理提供科学指导[3, 4]。
作为一种较新的技术,稳定同位素方法被广泛应用于海洋、湖泊、河流等生态系统的研究中。与传统食性方法相比,由于氮稳定同位素比值(δ15N)在相邻两个营养级水平的生物体内有3‰—4‰富集,能够更好地反映动物长时间地吸收、利用的食物信息[5]。在河流生态系统研究中,氮稳定同位素被用来构建河流食物网结构[6, 7, 8]、揭示污染物质的来源[9]、探讨重金属富集[10, 11]等热点问题。在国内,稳定同位素分析方法应用于河流生态系统的研究仍相对较少,仅在清江[12]、怒江[13]、长江三峡[14]、辽河中游[15]等河流或江段中有相关的研究报道。
饶河是鄱阳湖的五大入湖水系之一,流经亚洲最大的铜矿矿区,接纳了大量的废水,导致部分河段水体酸化,水体重金属污染严重,对饶河及鄱阳湖湖区的生态安全与水体环境产生巨大的影响[16, 17, 18]。目前,对饶河的食物网结构及鱼类等消费者的营养关系缺乏相关研究。本研究于2012年11月份枯水期在饶河不同区域采集了鱼类、螺类等生物样品,利用氮稳定同位素方法测定了饶河优势种鱼类等消费者的营养级位置,并分析了影响其营养级的主要因素。通过分析枯水期饶河消费者的营养级位置,有利于认识饶河的食物网结构特征。
1 材料与方法 1.1 研究区域饶河(116°30′—118°13′ E,28°34′—30°02′ N)位于鄱阳湖主湖区东面,由乐安河、昌江及一系列支流组成,流域面积为15,300 km2。饶河流域属于亚热带季风湿润气候区,多年平均气温在17.3 ℃左右,多年平均年降水量1850 mm,10—3月枯水期的降水量约占全年的31%,径流量约占全年的29%[19]。饶河流域土地利用类型多样,饶河上、中、下游从森林景观为主,逐渐过渡到农田与建设用地等为主[20]。采样点分布于乐安河与昌江上、中、下游及入鄱阳湖口,临近水文站的河流剖面。由于乐安河中游德兴段受铜矿开采影响,其矿山酸性废水对饶河下游及鄱阳湖区水生生物群落多样性产生不利影响[16],采样点位置选择避免了受重金属污染的河段。
1.2 样品采集与处理采集到的样品包括颗粒有机物(POM)平行样品10个、螺类10种及鱼类15种。将采集的混合河水滤过预烧(500 ℃,2 h)的GF/C玻璃纤维滤膜(直径为47 mm,Whatman),得到POM样品。利用改进彼得森采泥器和D型底栖网沿河岸采集螺、蚌等大型无脊椎动物样品,鱼类样品主要通过聘请渔民捕捞获得。鱼类的种类鉴定主要依据《中国动物志·硬骨鱼类》、《中国淡水鱼类检索》等。
将所采集的样品放置便携式冰箱带回实验室处理。将POM滤膜浸入过量的1 mol/L HCL,以消除无机碳酸盐的影响。螺类样品放入清水中过夜处理,以清空其肠含物,然后取其腹足部分用于稳定同位素分析。随机挑选个体较大的鱼类样品,取背部白色肌肉。所有样品在冷冻机内-50 ℃冷冻干燥至恒重后,用研钵将其研磨成均匀粉末,放入干燥器中保存待测。
所有样品的氮稳定同位素分析均在中国科学院地理科学与资源研究所理化实验室进行,所用仪器为美国Thermo公司的MAT-253稳定同位素比值质谱仪。氮同位素比值以δ值的形式表达,定义为:
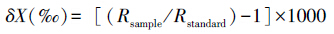
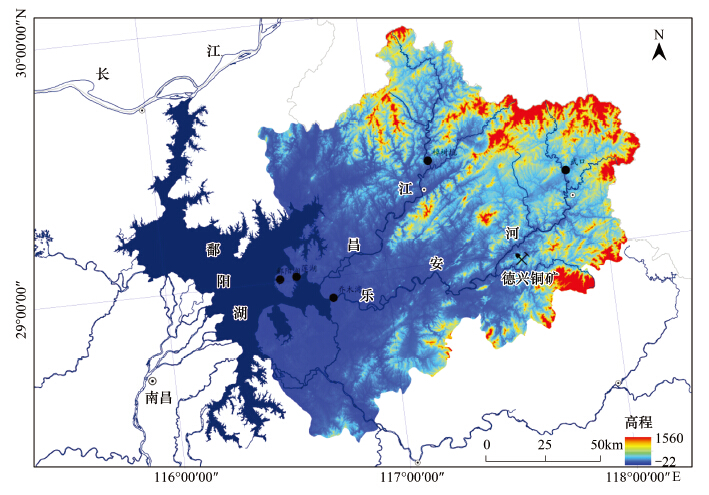
|
| 图 1 饶河流域及采样点位置(黑色圆圈表示本研究的采样点位置,深蓝色部分为鄱阳湖湖区) Fig.1 Catchment of Raohe River and sampling sites in this study(Black circles indicate sampling sites,and blue part represents Lake Poyang) |
由于在相邻两个营养级的生物间δ15N的富集为3‰—4‰,因而在食物网研究中δ15N值多被用于分析消费者的营养级,其计算公式如下[2, 7, 15]:
式中,TP表示消费者的营养等级,δ15N消费者为消费者的δ15N值,δ15N基准表示初级生产者或初级消费者的δ15N值。当δ15N基准为初级生产者时,λ为1;当δ15N基准为初级消费者时,λ为2。螺类生活周期较长,又能够反映初级生产者δ15N的季节变化的平均特征,适合做基准生物[2, 21]。为保证基准生物的一致性与可比性,因此在选择过程中尽量保证为各采样点的广布种,铜锈环棱螺(Bellamya aeruginosa)、赤豆螺(Bithynia fuchsiana)、中华沼螺(Cipangopaludina cahayensis)等作为营养位置计算的基准生物。 1.4 数据整理与分析
采用t检验和单因素方差分析(ANOVA),分别对饶河流域的同种消费者的δ15N 值进行正态性检验,以及对鱼类的δ15N 值和营养级位置的空间差异性检验。采用回归分析对鱼类的全长与鱼类的δ15N 值和营养级位置与POM的δ15N 值进行相关关系分析。上述公式的计算和数据处理、分析均通过Microsoft Excel 2007和SPSS 19.0软件中进行操作,显著性水平设为P < 0.05。实验数据用平均数±标准差(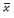 ±SD)表示。
±SD)表示。
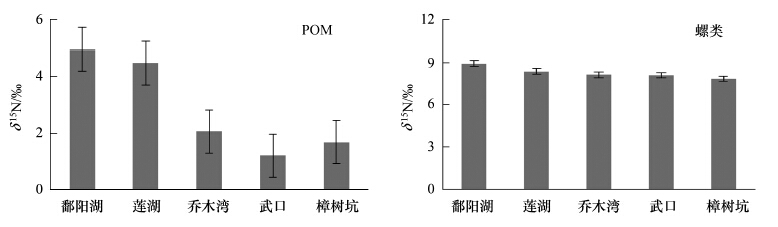
在饶河所有采样点内,POM的δ15N值取值范围为1.2‰—4.9‰,最大值出现在鄱阳湖湖区为4.9‰,最小值出现在乐安河上游支流武口处为1.2‰。其中,乐安河POM的δ15N为(2.3±1.5)‰,昌江POM的δ15N值为1.7‰。整个饶河河段内,POM的δ15N平均值在空间范围内呈现出空间差异性特点:鄱阳湖区 >乐安河段 > 昌江段(图 2a)。
|
| 图 2 饶河不同采样点POM和螺类的δ15N值 Fig.2 δ15N values of POM and snails in different sampling sites of Raohe River |
不考虑螺类的品种,它们的δ15N的平均值为(8.8±1.2)‰(n=18),最大值出现在鄱阳湖湖区的铜锈环棱螺为8.9‰,最小值出现在樟树坑位置的中华沼螺为7.8‰。在考虑螺类品种的条件下,武口与樟树坑的中华沼螺为(8.0±0.1)‰(n=6,各3个),其余采样点的铜锈环棱螺的δ15N平均值为(8.2±2.8)‰(n=12)(图 2b)。
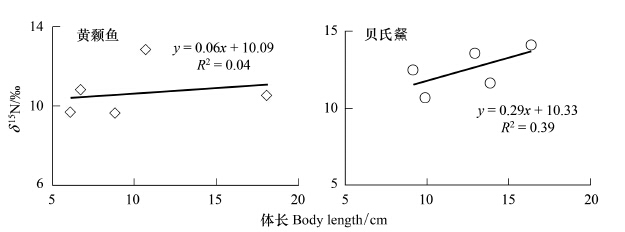
2.2 鱼类的δ15N值如表 1所示,大部分鱼类的δ15N值都集中在10‰—14‰之间,其中最大值出现鄱阳湖间下鱵(Hemiramphus intermedius)为(15.6±1.6)‰,最小值出现在乔木湾的鲫(Carassius auratus)为(4.7±0.9)‰。通过全长与鱼类的δ15N值的线性回归分析发现,广布种黄颡鱼(Pseudobagrus fulvidraco)(y=0.06x+10.09,R2 = 0.01,P<0.05)与贝氏 (Hemiculter bleekeri)(y=0.29x+10.33,R2 = 0.39,P>0.05)(图 3)并没有呈现显著的正相关关系。
| n:样品的数量number; BL: 消费者的体长Body Length; TP: 消费者的营养级位置Trophic Position | ||||||||||||||||||||
| 物种Species | 鄱阳湖 Lake Poyang | 饶河 Raohe River | ||||||||||||||||||
| 入湖口 Estuary | 乐安河 Lean River | 昌江 Changjiang River | ||||||||||||||||||
| 下游 Lower reach | 上游 Upper reach | 中游 Middle reach | ||||||||||||||||||
| 莲湖 Lianhu | 乔木湾 | 武口 | 樟树坑 | |||||||||||||||||
| n | BL/cm | δ15N/‰ | TP | n | BL/cm | δ15N/‰ | n | BL/cm | δ15N/‰ | n | BL/cm | δ15N/‰ | n | BL/cm | δ15N/‰ | |||||
| 鳊 Parabramis pekinensis | 4 | 10.5±1.4 | 13.3±3.6 | 3.3±1.0 | ||||||||||||||||
| 间下鱵 Hemiramphus intermedius | 3 | 11.5±0.9 | 15.6±1.5 | 3.9±0.4 | ||||||||||||||||
| 大眼鳜 Siniperca kneri | 6 | 18.3±2.5 | 15.1±1.5 | 3.8±0.4 | 3 | 20.9±2.9 | 12.7±1.2 | 3.5±0.3 | ||||||||||||
| 鲶 Parasilurus asotus | 5 | 310±148 | 13.4±3.3 | 3.3±0.8 | 5 | 29.5±2.6 | 10.8±1.6 | 2.8±0.4 | ||||||||||||
| 短颌鲚 Coilia brachygnathus | 7 | 14.8±0.9 | 14.6±2.0 | 3.6±0.6 | ||||||||||||||||
| 黄颡鱼 Pseudobagrus fulvidraco | 5 | 10.8±2.2 | 12.8±1.9 | 3.1±0.6 | 4 | 6.7±0.1 | 10.8±1.6 | 3.8±0.4 | 2 | 8.9±1.6 | 9.6±1.8 | 2.4±0.5 | 2 | 6.1±2.0 | 10.6±2.8 | 2.8±1.1 | 2 | 18.1±0.7 | 10.5±3.1 | 2.8±0.9 |
| 沙塘鳢 Odontobutis obscupus | 1 | 8.3 | 11.4 | 3 | ||||||||||||||||
| 马口鱼 Opsariicjthys bidens | ||||||||||||||||||||
| 贝氏 Hemiculter bleekeri | 5 | 11.4±1.3 | 14.1±2.0 | 3.5±0.5 | 10 | 7.9±1.9 | 13.6±1.2 | 3.5±0.4 | 4 | 8.9±0.7 | 11.7±2.5 | 3.0±0.7 | 2 | 4.9±1.7 | 10.7±1.0 | 2.8±0.3 | 2 | 4.2±0.8 | 9.5±1.9 | 2.4±0.5 |
| 鲫 Carassius auratus | 2 | 8.1±1.6 | 14.3±1.6 | 3.6±0.5 | 4 | 6.1±1.3 | 12.9±1.4 | 3.3±0.4 | 2 | 13.1±1.9 | 4.7±0.9 | 1.0±0.3 | 5 | 17.6±0.3 | 9.0±0.6 | 2.3±0.2 | ||||
| 鲤 Cyprinus carpio | 3 | 10.4±2.0 | 14.0±0.3 | 3.5±0.5 | 5 | 20.2±3.5 | 10.6±2.4 | 2.6±0.7 | 3 | 10.8±1.8 | 13.5±2.8 | 3.6±0.8 | ||||||||
| 泥鳅 Misgurnus anguillicaudatus | 1 | 10.8 | 14.2 | 3.5 | 2 | 7.9±1.9 | 12.8±0.0 | 3.4±0.0 | ||||||||||||
| 赤眼鳟 Squaliobarbus curriculus | 1 | 20.8 | 6.8 | 1.6 | ||||||||||||||||
| 鰟鮍 Rhodeus ocellatus | 4 | 7.6±3.5 | 11.5±2.8 | 2.7±0.8 | 9 | 1.7±0.4 | 11.1±0.9 | 2.8±0.3 | 1 | 3.7 | 9.6 | 2.4 | ||||||||
| 花 Hemibarbus maculatus | 1 | 11.4 | 13.1 | 3.2 | 3 | 10.3±0.5 | 10.3±0.6 | 2.6±0.2 | ||||||||||||
|
| 图 3 饶河黄颡鱼和贝氏 的δ15N值与体长的关系 Fig.3 The relationships between δ 15N values and body length of P. fulvidraco and H. bleekeri in Raohe River |
根据鱼类的不同食性可以看出,在鄱阳湖位置浮游食性的间下鱵δ15N值最高,肉食性的短颌鲚(Coilia brachygnathus)为(14.6±2.0)‰、大眼鳜(Siniper cakneri)为(15.1±1.5)‰,要高于杂食性的鲤(Cyprinus carpio)(14.0±0.3)‰、鲫(14.3±1.6)‰、贝氏 (14.1±2.0)‰,植食性的鳊(Parabramis pekinensis)处于中间位置。在 其他各个采样点位置,杂食性的鱼类贝氏 、鲤甚至要高于肉食性的大眼鳜。同一品种的鱼类在不同采样点位置的δ15N值也呈现明显的差异性。黄颡鱼、贝氏 作为采样点内的广布种ANOVA分析,F=7.71,df=4,P<0.001,它们的δ15N值在乐安河、昌江与鄱阳湖位置具有明显的空间差异特点。通过对鄱阳湖、樟树坑两个采样点的共有种的ANOVA分析,F=29.98,df=1,P<0.001;鄱阳湖与乐安河武口位置的共有种ANOVA分析,F=24.82,df=1,P<0.05。这种空间差异特征也表现在饶河两条支流乐安河、昌江与靠近鄱阳湖区之间。
2.3 营养级位置在饶河流域内,所有的鱼类的δ15N取值范围在4.7‰—15.6‰之间,这相当于在饶河范围内存在3个以上的营养级水平。根据公式(1)计算它们的营养级位置可知,鄱阳湖位置的间下鱵的营养级最高为3.9±0.4,营养级位置最低的为乔木湾位置的鲫,为1.0±0.3。营养级位置大于3的鱼类占了32个平行采样物种中的75%,营养级位置低于2的仅占了0.09左右,表明饶河的鱼类大部分处于同一营养级水平,鄱阳湖湖区的鱼类营养级相对较高。
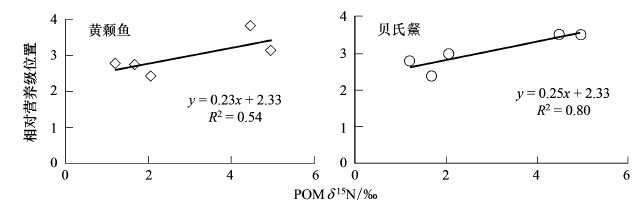
在饶河流域,广布种的黄颡鱼、贝氏 与POM的δ15N值的线性回归分析,偏肉食杂食性的黄颡鱼的相关性系数较小(R2= 0.54,P<0.05),以浮游动物为主食的杂食性贝氏 与POM的δ15N值呈显著相关(R2= 0.80,P<0.05)。
|
| 图 4 黄颡鱼和贝氏 的营养级位置与POM的δ15N值间的相关关系 Fig.4 The relationships between δ15N values of POM and trophic position of P. fulvidraco and H. bleekeri in Raohe River |
在饶河的食物网结构中,存在着3个以上的营养等级。营养级位置为3的主要为肉食性鱼类,大部分鱼类的营养级处于2—3之间。与肠含物分析结果相比,基于氮稳定同位素计算得到的营养级位置是连续的数值[21],因而能够更加客观地反映饶河鱼类等消费者的营养级和食性特征。与其他区域相比,与饶河河流域的同一品种鱼类的营养级位置存在差异性。例如,与王玉玉等[22]对鄱阳湖湖区的短颌鲚等要低一个营养级,油鲹却高一个营养级。这种现象,也同时存在于与巢湖[23]、太湖[24]的鱼类消费者品种的营养级对比(表 2)。这可能与河流食物网结构比湖泊食物网结构简单,在河流食物资源可获得性方面[25],要远远低于湖泊,高营养级水平的鱼类与低营养级水平的位置差异不够明显。
| *比较的鱼类为同属但不同种类,如短颌鲚与湖鲚(太湖、巢湖),黄颡鱼与光泽黄颡鱼; **鱼类营养级位置的数据来源为已发表的文献 | |||||||
|
物种名称 Species name | 空间位置Location | ||||||
|
巢湖* Lake Chaohu | 太湖** Lake Taihu | 饶河 Raohe River | 鄱阳湖** Lake Poyang | ||||
| 吴城 | 星子 | 都昌 | 湖口 | ||||
| 大眼鳜 Siniperca kneri | 3.5 | 3.3 | 3.2 | 2.8±0.1 | 4.0±0.6 | — | — |
| 间下鱵 Hemiramphus intermedius | 3.2 | — | 3.9 | — | — | — | — |
| 鲤 Cyprinus carpio | 3 | 2.4 | 3.3 | — | 2.8±0.3 | 3.4 | — |
| 鲫 Carassius auratus | 3 | 1.9 | 2.4 | 2.1±0.2 | 2.9±0.0 | 2.8±0.2 | — |
| 鲚Coilia ectenes * | 2.9 | 3.4 | 3.6 | — | 4.2±0.2 | — | 4.0±0.1 |
| 花 Hemibarbus maculatus | 2.9 | — | 2.9 | — | — | — | — |
| 贝氏 Hemiculter bleekeri | 2.8 | 3.1 | 3.0 | 2.5 | 2.32 | 2.8±0.3 | — |
| 高体鰟鲏 Rhodeus ocellatus | 2.4 | — | 3.0 | — | — | — | — |
| 鳊 Parabramis pekinensis | 2.36 | 1.9 | 2.9 | 2.2±0.0 | — | 3.1 | — |
| 黄颡鱼 Pseudobagrus fulvidraco | 3.2 | 3.0 | 3.0 | 3.3±0.3 | 4.2±0.1 | — | 3.7±0.0 |
此外,饶河流域鱼类的营养级位置除了与长江大型湖泊具有空间差异,在饶河流域内部,河流上、中、下游不同采样点的同一品种的鱼类的营养级位置不同。根据表 1结果显示,通过对鱼类体内的δ15N值的双因素ANOVA,鱼类的营养级位置在不同采样点具有明显的空间差异。这种空间差异特征的研究,对于研究河流食物网结构具有重要意义。
3.2 影响饶河鱼类营养级位置的因素许多研究指出,鱼类的营养级位置取决于食性和食物组成,而且受到个体发育水平或栖息生境的影响。同一物种的不同个体间也会出现明显的营养级位置高低差异,从而引起营养级的变化[4]。食性和食物组成是影响鱼类营养级位置的关键因素。在太湖、巢湖、鄱阳湖等湖泊生态系统中,以肉食性鱼类如大眼鳜、鲶等属于河流、湖泊生态系统中较高等级的消费者,杂食性与植食性的鱼类次之,以浮游生物食性的最低。
本研究结果分析表明,饶河流域内的不同品种的鱼类营养级位置的高低,同样受到它们食性的影响,肉食性大眼鳜、马口鱼、沙塘鳢等高于杂食性的鲤、鲫等的营养级位置,也高于植食性的鳊的营养级位置。由于鱼类饵料组成的季节变化较明显[26],鱼类的食性转变也会导致鱼类的营养级位置的改变。在饶河枯水期阶段,鲤的营养级位置比太湖、巢湖、鄱阳湖夏季的要高,而黄颡鱼的营养级位置要比鄱阳湖湖区的要低,杂食性的鲤、黄颡鱼等在饶河内的食物可获得性要小于大型湖泊而受到食性的季节转变引起的。
鱼类的个体大小与鱼类营养级位置高低也存在相关关系,随着个体增长,鱼类的δ15N值不断富集,营养级位置相应增加[27, 28]。Power等对鲑鱼(Salvelinus spp.)的研究中发现,鱼类体长增大,体内的δ15N值降低,营养级位置也逐渐降低[29]。而在其他区域,Jennings等人分析了英国北海底栖鱼类和无脊椎动物的营养级,结果发现,大约60%的鱼类个体体长与其δ15N值之间存在显著的相关性关系[30]。在本研究中,对于饶河上、中、下游的广布种黄颡鱼、油鲹的全长与体内的δ15N值的线性回归分析发现,这两种鱼类的全长与δ15N值的相关性并不明显。因而,可以推测出黄颡鱼等广布种鱼类的全长对它们的营养级位置的空间差异不够明显。
鱼类营养级位置的变化还能够受到栖息地生境的影响,从而导致同一物种的营养等级在不同采样点出现差异。不同来源的氮素通过影响鱼类等捕食者体内的15N值富集,进而影响它的营养级位置。在西非加纳地区,人类向泻湖排放的污水导致滤食性的粉虾(Penaeus notialis)与底栖的蓝蟹(Callinectes latimanus)体内不同部位的δ15N值升高[31]。Caroline Anderson等[8]人对加拿大魁北克省的82条河流的氮素来源分析,初级消费者、肉食性的无脊椎动物的平均δ15N值与农业生产、生活排放的污水呈现很高的相关性。在饶河流域内,饶河上游的武口、樟树坑以森林覆盖为主,到中下游地区的莲湖、鄱阳湖位置以农田、城市为主,土地利用与覆盖的差异导致POM的δ15N值的变化,饶河上游至下游的POM的δ15N值呈现增加的趋势。同时,我们发现黄颡鱼、油鲹的营养级位置也存在着明显的空间差异。通过POM的δ15N值与黄颡鱼、油鲹营养级位置分析发现呈显著相关,表明浮游食性的油鲹的营养级位置更容易受到外来营养物质输入的影响。POM的δ15N值的空间差异反映了不同生境下人为氮营养物质输入的差异[32]。通过对不同食物源的摄食,鱼类体内对15N的富集程度不同,导致鱼类的δ15N值在不同采样点的差异,最终对整个饶河鱼类的营养级产生影响。
4 结语本研究通过对饶河枯水期POM、螺类与鱼类的δ15N值测定,分析了饶河鱼类等消费者的营养级位置。结果表明,饶河鱼类占据3—4个营养等级,并且其营养级位置存在明显的空间差异,可能与上、中、下游和入湖口区域饵料生物的组成和生物量大小有关。另一方面,广布种鱼类的营养等级受个体大小的影响较小,POM的δ15N值能够影响饶河鱼类的营养级位置,表明饶河消费者的营养级受到营养物质来源的影响。本研究仅考虑了饶河枯水期河流鱼类的营养级位置和影响营养级位置的因素,今后将考虑水位变化和其他环境因素对饶河鱼类营养级关系的影响研究。
| [1] | 董哲仁. 河流生态系统结构功能模型研究. 水生态学杂志, 2008, 1(1): 1-7. |
| [2] | Post D M. Using stable isotopes to estimate trophic position: models, methods, and assumptions. Ecology, 2002, 83(3):703-718. |
| [3] | Lindeman R L. The trophic-dynamic aspect of ecology. Ecology, 1942, 23(4): 399-418. |
| [4] | 纪炜炜, 李圣法, 陈雪忠. 鱼类营养级在海洋生态系统研究中的应用. 中国水产科学, 2010, 17(4): 878-887. |
| [5] | Zanden M J V, Rasmussen J B. Primary consumer δ13C and δ15N and the trophic position of aquatic consumers. Ecology, 1999, 80(4): 1395-1404. |
| [6] | Thorp J H, Delong M D, Greenwood K S, Casper A F. Isotopic analysis of three food web theories in constricted and floodplain regions of a large river. Oecologia, 1998, 117(4): 551-563. |
| [7] | Jepsen D B, Winemiller K O. Structure of tropical river food webs revealed by stable isotope ratios. Oikos, 2002, 96(1): 46-55. |
| [8] | Anderson C, Cabana G. Estimating the trophic position of aquatic consumers in river food webs using stable nitrogen isotopes. Journal of the North American Benthological Society, 2007, 26(2): 273-285. |
| [9] | Anderson C, Cabana G. Does δ15N in river food webs reflect the intensity and origin of N loads from the watershed? Science of the Total Environment, 2006, 367(2): 968-978. |
| [10] | Ikemoto T, Tu N P C, Okuda N, Iwata A, Omori K, Tanabe S, Tuyen B C, Takeuchi I. Biomagnification of trace elements in the aquatic food web in the Mekong Delta, South Vietnam using stable carbon and nitrogen isotope analysis. Archives of environmental contamination and toxicology, 2008, 54(3): 504-515. |
| [11] | Kwon S Y, McIntyre P B, Flecker A S, Campbell L M. Mercury biomagnification in the food web of a neotropical stream. Science of the Total Environment, 2012, 417: 92-97. |
| [12] | 温芳妮. 清江流域二级河流叹气沟河大型底栖动物群落的食物网研究. 武汉: 华中科技大学, 2008. |
| [13] | 周琼. 碳、氮稳定同位素技术在湖泊与河流食物网研究中的应用. 武汉: 中国科学院水生生物研究所, 2009. |
| [14] | 李斌. 三峡库区小江鱼类食物网结构、营养级关系的C、N稳定性同位素研究. 重庆: 西南大学, 2012. |
| [15] | 霍堂斌, 姜作发, 马波, 李喆, 于洪贤. 应用同位素分析黑龙江中游主要鱼类营养层次. 淡水渔业, 2013, 43(2): 3-8. |
| [16] | 朱江, 任淑智. 德兴铜矿废水对乐安江底栖动物群落的影响. 应用与环境生物学报, 1996, 2(2): 162-168. |
| [17] | 高玉荣, 许木启. 乐安江重金属污染对浮游植物群落结构的影响. 应用与环境生物学报, 1996, 2(2): 175-183. |
| [18] | 初娜. 江西省德兴铜矿地区重金属元素的环境效应研究. 北京: 中国地质科学院, 2008. |
| [19] | 江西省水利厅. 江西河湖大典. 武汉: 长江出版社, 2010. |
| [20] | 郭延凤. 基于 CLUE 模型的江西省土地利用变化及其对水源涵养服务的影响. 合肥: 安徽师范大学, 2011. |
| [21] | 徐军, 张敏, 谢平. 氮稳定同位素基准的可变性及对营养级评价的影响. 湖泊科学, 2010, 22(1): 8-20 |
| [22] | 王玉玉, 于秀波, 张路, 徐军. 应用碳、氮稳定同位素研究鄱阳湖枯水末期水生食物网结构. 生态学报, 2009, 29(3): 1181-1188. |
| [23] | Zhang M, Xie C X, Hansson L A, Hu W M, Che J P. Trophic level changes of fishery catches in Lake Chaohu, Anhui Province, China: Trends and causes. Fisheries Research, 2012, 131-133(0):15-20. |
| [24] | Mao Z G, Gu X H, Zeng Q F, Zhou L H, Sun M B. Food web structure of a shallow eutrophic lake (Lake Taihu, China) assessed by stable isotope analysis. Hydrobiologia, 2012, 683(1): 173-183. |
| [25] | Sabo J L, Finlay J C, Kennedy T, Post D M. The role of discharge variation in scaling of drainage area and food chain length in rivers. Science, 2010, 330(6006): 965-967. |
| [26] | Grey J. Ontogeny and dietary specialization in brown trout (Salmotrutta L.) from Loch Ness, Scotland,examined using stable isotopes of carbon and nitrogen. Ecology of Freshwater Fish, 2001, 10(3): 168-176. |
| [27] | Currin C A, Wainright S C, Able K W. Determination of food web support and trophic position of the Mummichog, Fundulusheteroclitus in New Jersey smooth Cordgrass (Spartina alterniflora), common reed(Phragmites australis), and restored salt marshes. Estuaries, 2003, 26(2): 96-510. |
| [28] | Power M, Power G, Caron F, Doucett R R. Growth and dietary niche in Salvelinus alpinus and Salvelinus frontalis as revealed by stable isotopeanalysis. Environmental Biology of Fishes, 2002, 64(1/3): 75-85. |
| [29] | Jennings S, Greenstreet S P R, Hill L, Piet G J, Pinnegar J K, Warr K J. Long-termtrends in the trophic structure of the North Sea fish community: evidence from stable isotope analysis, size-spectra and communitymetrics. Marine Biology, 2002, 141(6): 1085-1097. |
| [30] | Diebel M W, Zanden M J V. Nitrogen stable isotopes in streams: effects of agricultural sources and transformations. Ecological Applications, 2009, 19(5): 1127-1134. |
| [31] | Nixon S W, Buckley B A, Granger S L, Entsua-Mensah M, Ansa-Asare O, White M J, McKinney R A, Mensah E. Anthropogenic enrichment and nutrients in some tropical lagoons of Ghana, West Africa. Ecological Applications, 2007, 17(5): 144-164. |
| [32] | Berto D, Rampazzo F, Noventa S, Cacciatore F, Gabellirni M, Aubry F B, Girolimetto A, Brusa R B. Stable carbon and nitrogen isotope ratios as tools to evaluate the nature of particulate organic matter in the Venice lagoon. Estuarine, Coastal and Shelf Science, 2013, 135: 66-76. |
 2015, Vol. 35
2015, Vol. 35





