文章信息
- 白坤栋, 莫凌, 刘铭, 张德楠, 何成新, 万贤崇, 蒋得斌
- BAI Kundong, MO Ling, LIU Ming, ZHANG Denan, HE Chengxin, WAN Xianchong, JIANG Debin
- 广西猫儿山不同海拔常绿和落叶树种的营养再吸收模式
- Nutrient resorption patterns of evergreen and deciduous tree species at different altitudes on Mao'er Mountain, Guangxi
- 生态学报, 2015, 35(17): 5776-5787
- Acta Ecologica Sinica, 2015, 35(17): 5776-5787
- http://dx.doi.org/10.5846/stxb201312092914
-
文章历史
- 收稿日期: 2013-12-09
- 网络出版日期: 2014-11-03
2. 中国林业科学研究院林业新技术研究所, 北京 100091;
3. 广西猫儿山国家级自然保护区管理局, 桂林 541316
2. Institute of New Forest Technology, Chinese Academy of Forestry, Beijing 100091, China;
3. Bureau of Guangxi Mao'er Mountain Nature Reserve, Guilin 541316, China
氮和磷是大部分陆地植物生长的限制性营养元素。植物克服氮和磷限制的一个重要策略就是从脱落前的衰老叶片中再吸收这些元素。营养再吸收可以降低对当前营养供应的依赖性,可以视为植物保存营养最重要的策略之一[1, 2, 3]。据估计,多年生植物平均近50%的氮和磷循环是通过再吸收完成的[4, 5]。由于贫瘠的土壤缺乏营养元素,一般认为土壤贫瘠生境中的植物比土壤肥沃生境中的植物具有更高的营养再吸收效率[6, 7, 8],然而,有些证据表明土壤贫瘠生境中的植物和土壤肥沃生境中的植物在营养再吸收率方面没有明显差别[1, 9]。因此,土壤养分供给性大小是否影响植物氮磷再吸收效率仍存在争议。
许多研究探讨了常绿和落叶树种之间对养分需求量和营养再吸收的差别。落叶树种由于相对频繁的落叶和发生新叶,对土壤养分的需求量大,属于营养奢侈型。常绿树种叶片寿命长,对养分需求较少,故常绿习性被认为是对贫瘠土壤生境的一种适应性[10, 11]。有的研究表明温带森林中的常绿树种的氮再吸收率显著低于落叶树种而磷再吸收效率在两者之间无显著差异[1, 12],有的研究表明热带干旱生境中的落叶树种比常绿树种有较高的氮和磷再吸收效率[8],而有的研究还表明亚热带常绿阔叶林中的落叶树种比常绿树种有较高的磷再吸收效率但氮再吸收效率在两者之间无显著差异[13, 14, 15]。这些结果表明,叶片习性对营养再吸收的影响随着生境的不同而呈现出明显的多样性。
过去的研究表明营养再吸收效率和叶片营养状态的关联程度也不一致。一些证据表明氮和磷再吸收效率随着成熟和衰老叶片氮和磷含量的增加而降低[4, 16, 17]。Huang 等[14]的研究表明氮再吸收效率和叶片氮含量没有关系,磷再吸收效率则与叶片磷含量正相关。Aerts[1]和Lal 等[8]的研究则表明,氮和磷的再吸收效率都不受成熟叶片氮和磷含量的影响。另外,还有研究表明,氮和磷再吸收效率与成熟和衰老叶片的氮:磷比没有显著的相关性[4]。
广西猫儿山(25°50′N,101°49′E)位于我国中部亚热带,孕育着典型的地带性植被常绿阔叶林,但是随着海拔的升高,在海拔1300—1800 m 的中山地带分布着水青冈占优势的落叶林带,在海拔1800 m以上常绿针叶树和常绿阔叶树重新占优势[18, 19]。猫儿山常绿树种沿海拔形成双峰分布的格局与东亚的热带地区常绿树种沿海拔的分布特征相似[20]。Kikuzawa[20, 21]利用一个叶片寿命的成本收益模型对东亚的热带地区常绿树种的双峰分布做了解释,认为低海拔植物一年中不适宜的生长季节很短,植物保持常绿有利于碳收益,随着海拔的升高,不适宜的季节变长,植物要维持冠层常绿需要消耗大量的成本,当这种消耗大于来年构建新叶的成本的时候,植物采取落叶的策略比较经济,因此中海拔落叶树种发生的频率相对较多而形成优势落叶林带,但是随着海拔的进一步升高,不适宜的季节变得更长,植物会采取延长叶片寿命的方式来分期补偿叶片建成成本,因此高海拔常绿树种会重新占据优势。白坤栋等[22]对猫儿山不同海拔常绿和落叶树种的光合作用与氮关系的分析表明高海拔常绿树种有较高的干物质投入成本(即比叶重较大)、较低的光合速率和较小的光合氮利用效率,支持了Kikuzawa的理论。然而,猫儿山土壤表土有机质和氮含量随着海拔的上升而增多而磷含量在高海拔含量最少[19],这意味着常绿植物沿着海拔形成双峰发布可能与常绿植物对土壤营养变化的适应有密切的关系,但至今树种间营养再吸收差异参与调节树种海拔分布的研究报道仍相对较少[23, 24]。本研究将分析猫儿山不同海拔常绿和落叶树种成熟和衰老叶片的氮和磷含量,探讨叶片习性和海拔在营养再吸收变化中的作用,拟解决的科学问题是:(1)树种营养再吸收效率是否随着叶片习性和海拔的不同而改变?(2)树种营养再吸收效率与成熟和衰老叶片营养状态有何关联?这些问题的探讨可以揭示营养再吸收在猫儿山常绿植物形成双峰分布中的作用,为我国亚热带山地森林生物多样性的形成以及预测这类森林营养循环提供科学依据。
1 材料和方法 1.1 样地描述研究样地位于广西猫儿山3种不同海拔的森林中,即低海拔山地亚热带气候下的常绿阔叶林、中海拔山地暖温带气候下的水青冈混交林和高海拔山地中温带气候下的铁杉混交林。根据猫儿山自然保护区九牛塘气象观测站(1200 m)的观测记录,区域年均温12.8 ℃,月均最高最低温差为19.8 ℃,年降水量2510 mm[19]。
低海拔常绿阔叶林的土壤基质为山地红壤,表层土(0—20 cm)有机质、全氮和全磷分别为7.46%、0.34%和0.123%,选择的常绿树种是罗浮栲(Castanopsis fabri)、栲树(Castanopsis fargesii)、木荷(Schima superba)、羊角杜鹃(Rhododendron cavaleriei)和虎皮楠(Daphniphyllum oldhamii),选择的落叶树种是枫香(Liquidambar formosana)、拟赤杨(Alniphyllum fortune)、茅栗(Castanea mollissima)、五裂槭(Acer oliverianum)和山胡椒(Lindera glauca)。中海拔水青冈混交林的土壤基质为山地黄棕壤,表层土有机质、全氮和全磷分别为16.80%、0.52%和0.136%,选择的落叶树种是亮叶水青冈(Fagus lucida)、青榨槭(Acer davidii)、缺萼枫香(Liquidambar acalycina)、檫树(Sassafras tzumu)和红果山胡椒(Lindera erythrocarpa),选择的常绿树种是铁锥栲(Castanopsis lamontii)、榕叶冬青(Ilex ficoidea)、桂南木莲(Manglietia chingii)、银木荷(Schima argentea)和交让木(Daphniphyllum macropodum)。高海拔铁杉混交林的土壤基质是泥炭土,表层土有机质、全氮和全磷分别为27.99%、0.93%和0.083%,选择的常绿树种是南方铁杉(Tsuga chinensis)、褐叶青冈(Cyclobalanopsis stewardiana)、细枝棱(Eurya loquaiana)、西南山茶(Camellia pitardii)和长梗冬青(Ilex pedunculosa),选择的落叶树种是白蜡树(Fraxinus chinesis)、芳香安息香(Styrax odoratissimus)、红叶木姜子(Litsea rubescens)、美脉花楸(Sorbus caloneura)和红果树(Stranvaesia davidiana)。3类森林所选代表树种总共30种,来自于13个科(表 1),其中壳斗科除茅栗之外的5个树种是这些森林中的主要优势种[19]。
1.2 实验方法冠层树种决定了森林的类型和物候,因此选择冠层的树种进行采样测定成熟和衰老叶片的营养元素含量。每个树种选择3—5株,利用高枝剪剪下每个植株冠层枝条进行采样,采样时间集中在2010—2012年两个生长季。在夏季(7—8月)采集成熟绿叶,而在秋冬季节(11月到次年2月)采集自然衰老的叶片。每个阔叶树树种的植株选取30—50片冠层树叶。对于常绿针叶树南方铁杉,由于其叶片寿命较长,每株从冠层采集3—5株枝条,选取当年成熟绿叶和自然衰老的叶片。叶片采集下来后,先自然风干,然后才拿回实验室分析。在实验室内,叶片在60 ℃的烘箱烘干至恒重,随后将叶片磨成粉末,用硫酸-高氯酸钾消化后,由比色法测定磷含量,凯氏定氮法测定氮含量[25]。营养再吸收效率按照如下公式计算[26, 27]:
营养再吸收率=100%×(成熟绿叶营养含量-衰老叶营养含量)/成熟绿叶营养含量
| 生境特征 Habitat traits | 树种拉丁名 Species latin name | 科名 Family | 叶片习性 Leaf habit |
| 低海拔Low altitude | 罗浮栲Castanopsis fabric | 壳斗科Fagaceae | 常绿 |
| <1300 m | 栲树Castanopsis fargesii | 壳斗科Fagaceae | 常绿 |
| 常绿阔叶林Evergreen broad-leaved forest | 木荷Schima superba | 茶科Thaceae | 常绿 |
| 山地红壤Montane red soil | 羊角杜鹃Rhododendron cavaleriei | 杜鹃花科Ericaceae | 常绿 |
| 山地亚热带气候Montane subtropical climate | 虎皮楠Daphniphyllum oldhamii | 交让木科Daphniphyllaceae | 常绿 |
| 枫香Liquidambar formosana | 金缕梅科Hamamelidaceae | 落叶 | |
| 拟赤杨Alniphyllum fortune | 安息香科Styraceae | 落叶 | |
| 茅栗Castanea mollissima | 壳斗科Fagaceae | 落叶 | |
| 五裂槭Acer oliverianum | 槭树科Aceraceae | 落叶 | |
| 山胡椒Lindera glauca | 樟科Lanrauceae | 落叶 | |
| 中海拔Middle altitude | 亮叶水青冈Fagus lucida | 壳斗科Fagaceae | 落叶 |
| 1300—1800 m | 青榨槭Acer davidii | 槭树科Aceraceae | 落叶 |
| 水青冈混交林Beech mixed forest | 缺萼枫香Liquidambar acalycina | 金缕梅科Hamamelidaceae | 落叶 |
| 山地黄棕壤Montane yellow-brown soil | 檫树Sassafras tzumu | 樟科Lanrauceae | 落叶 |
| 山地暖温带气候Montane warm-temperate climate | 红果山胡椒Lindera erythrocarpa | 樟科Lanrauceae | 落叶 |
| 铁锥栲Castanopsis lamontii | 壳斗科Fagaceae | 常绿 | |
| 榕叶冬青Ilex ficoidea | 冬青科Aquifoliceae | 常绿 | |
| 桂南木莲Manglietia chingii | 木兰科Magnoliaceae | 常绿 | |
| 银木荷Schima argentea | 茶科Thaceae | 常绿 | |
| 交让木Daphniphyllum macropodum | 交让木科Daphniphyllaceae | 常绿 | |
| 高海拔High altitude | 南方铁杉Tsuga chinensis | 松科Pinaceae | 常绿 |
| >1800 m | 褐叶青冈 Cyclobalanopsis stewardiana | 壳斗科Fagaceae | 常绿 |
| 铁杉混交林Hemlock mixed forest | 细枝棱Eurya loquaiana | 茶科Thaceae | 常绿 |
| 泥炭土Peat soil | 西南山茶Camellia pitardii | 茶科Thaceae | 常绿 |
| 山地中温带气候 | 长梗冬青Ilex pedunculosa | 冬青科Aquifoliceae | 常绿 |
| Montane moderate-temperate climate | 白蜡树Fraxinus chinensis | 木犀科Oleaceae | 落叶 |
| 芳香安息香Styrax odoratissimus | 安息香科Styracaceae | 落叶 | |
| 红叶木姜子Litsea rubescens | 樟科Lauraceae | 落叶 | |
| 美脉花楸Sorbus caloneura | 蔷薇科Rosaceae | 落叶 | |
| 红果树Stranvaesia davidiana | 蔷薇科Rosaceae | 落叶 |
为了提高正态分布和方差齐性,所有变量都转化成为对数形式(log10)[28]。采用双因素方差分析常绿和落叶树种之间以及不同海拔之间的差异,这两个因素是叶片习性和海拔,差异显著性水平检验的P值为0.05。采用配对T-检验分析成熟叶片和衰老叶片之间营养的差异(双尾检验)。采用配对相关性分析叶片营养特征之间的关系。所有数据的统计和分析用SPSS12.0来完成而作图用SigmaPlot10.0来完成。
2 结果与分析从表 2可知,氮再吸收效率和磷再吸收效率都受到海拔的显著影响,但是两者趋势相反。氮再吸收效率的平均值为56.5%,随海拔的增加而显著降低(P<0.01)。磷再吸收效率的平均值为52.1%,随海拔的增加而显著增加(P<0.05)。
| 树种 Species | 氮再吸 收效率 NRE/% | 磷再吸 收效率 PRE/% | 树种 Species | 氮再吸 收效率 NRE/% | 磷再吸 收效率 PRE/% | 树种 Species | 氮再吸 收效率 NRE/% | 磷再吸 收效率 PRE/% | |
| 低海拔Low altitude | 中海拔Middle altitude | 高海拔High altitude | |||||||
| 罗浮栲C. fabric | 71.3±0.7 | 56.9±1.0 | 亮叶水青冈F. lucida | 54.3±1.9 | 44.2±1.7 | 南方铁杉T.chinensis | 66.0±0.7 | 74.2±1.9 | |
| 栲树C. fargesii | 73.6±1.3 | 58.6±2.1 | 青榨槭A. davidii | 58.9±1.3 | 54.5±1.4 | 褐叶青冈C. stewardiana | 61.7±1.0 | 69.8±1.3 | |
| 木荷S. superba | 64.5±1.4 | 47.2±1.2 | 缺萼枫香L. acalycina | 46.8±1.8 | 42.6±1.5 | 细枝棱E. loquaiana | 54.3±1.4 | 62.1±2.0 | |
| 羊角杜鹃R.cavaleriei | 63.2±1.6 | 56.8±1.9 | 檫树S. tzumu | 37.6±1.2 | 35.9±1.2 | 西南山茶C. pitardii | 60.7±1.7 | 58.1±1.2 | |
| 虎皮楠D.oldhamii | 52.2±1.8 | 34.8±1.5 | 红果山胡椒L.erythrocarpa | 52.7±1.4 | 55.5±2.0 | 长梗冬青I. pedunculosa | 51.9±2.0 | 54.6±0.9 | |
| 枫香L. formosana | 65.4±2.2 | 49.5±1.8 | 铁锥栲C. lamontii | 55.7±0.7 | 61.1±1.3 | 白蜡树F.chinensis | 43.1±1.7 | 54.3±1.6 | |
| 拟赤杨A. fortune | 56.4±1.1 | 39.1±1.7 | 榕叶冬青I. ficoidea | 59.3±1.5 | 45.9±0.9 | 芳香安息香S. odoratissimus | 42.9±0.5 | 49.2±1.5 | |
| 茅栗C. mollissima | 55.8±1.6 | 37.7±2.0 | 桂南木莲M. chingii | 66.2±1.0 | 55.1±2.2 | 红叶木姜子L. rubescens | 42.6±1.1 | 44.7±1.9 | |
| 五裂槭A. oliverianum | 61.9±2.1 | 54.8±1.8 | 银木荷S. argentea | 58.1±0.8 | 56.6±1.3 | 美脉花楸S. caloneura | 50.6±1.4 | 53.2±1.8 | |
| 山胡椒L. glauca | 53.4±1.3 | 35.5±1.4 | 交让木D.macropodum | 68.6±1.8 | 63.8±1.6 | 红果树S. davidiana | 46.3±2.0 | 58.1±1.5 | |
| 常绿平均Evergreen average | 65.0±3.7 | 50.9±4.5 | 常绿平均Evergreen average | 61.6±2.5 | 56.5±3.1 | 常绿平均Evergreen average | 58.9±2.6 | 63.8±3.6 | |
| 落叶平均Deciduous average | 58.6±2.2 | 43.3±3.7 | 落叶平均Deciduous average | 50.1±3.7 | 46.5±3.7 | 落叶平均Deciduous average | 45.1±1.5 | 51.9±2.3 | |
| 总平均Total average | 61.8±2.3 | 47.1±3.0 | 总平均Total average | 55.8±2.8 | 51.5±2.8 | 总平均Total average | 52.0±2.7 | 57.8±2.8 | |
| 再吸收效率 Resorption efficiency/% | 所有树种平均 Means across species | 所有常绿平均 Means across evergreen species | 所有落叶平均 Means across deciduous species | 叶片习性 Leaf habit | 海拔Altitude | 交互作用Interaction | |||
| F | P | F | P | F | P | ||||
| 氮再吸收效率Nitrogen resorption efficiency | 56.5±1.7 | 61.8±1.7 | 51.2±2.0 | 21.5 | <0.001 | 6.1 | <0.01 | 1.4 | 0.27 |
| 磷再吸收效率Phosphorus resorption efficiency | 52.1±1.8 | 57.0±2.5 | 47.3±2.0 | 9.9 | <0.01 | 4.3 | <0.05 | 0.1 | 0.94 |
常绿树种的氮再吸收效率显著高于落叶树种(P<0.001),尤其是在高海拔山地高出30.6%(表 2)。常绿树种氮再吸收效率平均值为61.8%,其中最高和最低的分别是栲树(73.6%)和长梗冬青(51.9%)。落叶树种氮再吸收效率平均值为51.2%,其中最高和最低的分别是枫香(65.4%)和檫树(37.6%)。
落叶树种的磷再吸收效率显著低于常绿树种(P<0.01),尤其在高海拔低22.9%(表 2)。常绿树种磷再吸收效率平均值为57.0%,其中最高和最低的分别是南方铁杉(74.2%)和虎皮楠(34.8%)。落叶树种磷再吸收效率平均值为47.3%,其中最高和最低的分别是红果树(58.1%)和山胡椒(35.5%)。
氮再吸收效率与成熟叶片氮含量存在显著的负相关关系(r=- 0.43,P<0.05,图 1)。成熟叶片氮含量不受海拔的影响,但其在落叶树种中的平均值(2.53%)显著高于常绿树种(1.86%)(P<0.001,表 3)。氮再吸收效率与衰老叶片氮含量有显著的负相关关系(r=0.87,P<0.001,图 1)。衰老叶片氮含量平均值为0.97%,受到叶片习性和海拔的显著影响(表 4),常绿树种有显著较低的值 (P<0.001)而高海拔树种有显著较高的值(P<0.001)。

|
| 图1数据转换为对数形式后的氮再吸收效率与成熟和衰老叶片氮含量的关系 Fig.1 Relationship between nitrogen resorption efficiency and nitrogen content in mature and senesced leaves after data log-transformation |
| 树种 Species | 氮 N/% | 磷 P/% | 氮∶磷比 N∶P | 树种 Species | 氮 N/% | 磷 P/% | 氮∶磷比 N∶P | 树种 Species | 氮 N/% | 磷 P/% | 氮∶磷比 N∶P |
| 低海拔Low altitude | 中海拔Middle altitude | 高海拔High altitude | |||||||||
| 罗浮栲C. fabric | 2.27±0.02 | 0.172±0.003 | 12.9±0.5 | 亮叶水青冈F. lucida | 2.57±0.01 | 0.178±0.003 | 14.1±0.2 | 南方铁杉T.chinensis | 1.70±0.01 | 0.088±0.003 | 18.8±0.3 |
| 栲树C. fargesii | 1.95±0.03 | 0.178±0.003 | 11.3±0.4 | 青榨槭A. davidii | 2.44±0.02 | 0.194±0.002 | 12.2±0.3 | 褐叶青冈C. stewardiana | 2.16±0.04 | 0.124±0.005 | 17.9±0.3 |
| 木荷S. superba | 1.97±0.02 | 0.189±0.002 | 10.1±0.5 | 缺萼枫香L. acalycina | 2.46±0.01 | 0.189±0.003 | 13.3±0.2 | 细枝棱E. loquaiana | 1.63±0.02 | 0.109±0.003 | 15.6±0.2 |
| 羊角杜鹃R.cavaleriei | 1.61±0.04 | 0.155±0.001 | 10.7±0.3 | 檫树S. tzumu | 2.35±0.02 | 0.162±0.004 | 14.6±0.4 | 西南山茶C. pitardii | 2.00±0.03 | 0.118±0.001 | 16.9±0.3 |
| 虎皮楠D.oldhamii | 1.70±0.05 | 0.195±0.001 | 8.9±0.2 | 红果山胡椒L.erythrocarpa | 2.38±0.01 | 0.148±0.002 | 15.7±0.2 | 长梗冬青I. pedunculosa | 1.44±0.02 | 0.098±0.002 | 17.5±0.2 |
| 枫香L. formosana | 2.39±0.01 | 0.202±0.003 | 11.2±0.3 | 铁锥栲C. lamontii | 2.14±0.01 | 0.154±0.002 | 13.5±0.3 | 白蜡树F.chinensis | 3.16±0.05 | 0.180±0.003 | 17.8±0.3 |
| 拟赤杨A. fortune | 2.63±0.04 | 0.199±0.003 | 13.0±0.4 | 榕叶冬青I. ficoidea | 1.73±0.02 | 0.139±0.001 | 12.7±0.2 | 芳香安息香S. odoratissimus | 2.30±0.02 | 0.160±0.003 | 14.6±0.2 |
| 茅栗C. mollissima | 2.48±0.03 | 0.225±0.004 | 11.0±0.3 | 桂南木莲M. chingii | 2.11±0.03 | 0.146±0.004 | 14.8±0.4 | 红叶木姜子L. rubescens | 2.91±0.01 | 0.156±0.006 | 18.3±0.2 |
| 五裂槭A. oliverianum | 2.54±0.02 | 0.206±0.002 | 12.6±0.4 | 银木荷S. argentea | 2.07±0.02 | 0.138±0.003 | 14.5±0.3 | 美脉花楸S. caloneura | 2.21±0.02 | 0.137±0.005 | 16.6±0.3 |
| 山胡椒L. glauca | 2.70±0.03 | 0.239±0.002 | 11.7±0.2 | 交让木D.macropodum | 1.47±0.03 | 0.122±0.002 | 12.2±0.2 | 红果树S. davidiana | 2.38±0.04 | 0.141±0.002 | 17.3±0.2 |
| 常绿平均Evergreen average | 1.90±0.12 | 0.178±0.007 | 10.7±0.7 | 常绿平均Evergreen average | 1.90±0.13 | 0.140±0.005 | 13.5±0.5 | 常绿平均Evergreen average | 1.79±0.13 | 0.107±0.007 | 17.3±0.5 |
| 落叶平均Deciduous average | 2.55±0.05 | 0.214±0.008 | 11.9±0.4 | 落叶平均Deciduous average | 2.44±0.04 | 0.174±0.009 | 13.9±0.6 | 落叶平均Deciduous average | 2.59±0.19 | 0.155±0.008 | 16.9±0.6 |
| 总平均Total average | 2.22±0.12 | 0.196±0.008 | 11.3±0.4 | 总平均Total average | 2.17±0.11 | 0.157±0.007 | 13.7±0.4 | 总平均Total average | 2.19±0.17 | 0.131±0.009 | 17.1±0.4 |
| 衰老叶营养特征 Nutrient traits in senesced leaves | 所有树种平均 Means across species | 所有常绿平均 Means across evergreen species | 所有落叶平均 Means across deciduous species | 叶片习性 Leaf habit | 海拔Altitude | 交互作用Interaction | |||||
| F | P | F | P | F | P | ||||||
| 氮N/% | 2.200±0.08 | 1.860±0.07 | 2.530±0.06 | 43.5 | <0.001 | 0.1 | 0.88 | 0.5 | 0.61 | ||
| 磷P/% | 0.161±0.007 | 0.142±0.008 | 0.182±0.008 | 45.6 | <0.001 | 40.0 | <0.001 | 2.2 | 0.14 | ||
| 氮∶磷比N∶P | 14.100±0.50 | 13.900±0.8 | 14.200±0.6 | 1.1 | 0.31 | 49.1 | <0.001 | 1.2 | 0.33 | ||
| 树种 Species | 氮 N/% | 磷 P/% | 氮:磷比 N∶P | 树种 Species | 氮 N/% | 磷 P/% | 氮:磷比 N∶P | 树种 Species | 氮 N/% | 磷 P/% | 氮∶磷比 N∶P |
| 低海拔Low altitude | 中海拔Middle altitude | 高海拔High altitude | |||||||||
| 罗浮栲C. fabric | 0.63±0.02 | 0.072±0.002 | 8.3±0.2 | 亮叶水青冈F. lucida | 1.19±0.02 | 0.100±0.002 | 11.4±0.4 | 南方铁杉T.chinensis | 0.53±0.02 | 0.023±0.001 | 20.8±0.4 |
| 栲树C. fargesii | 0.51±0.01 | 0.078±0.003 | 7.3±0.3 | 青榨槭A. davidii | 1.02±0.04 | 0.089±0.004 | 11.0±0.7 | 褐叶青冈C. stewardiana | 0.84±0.03 | 0.037±0.002 | 21.1±0.6 |
| 木荷S. superba | 0.68±0.02 | 0.101±0.005 | 6.6±0.4 | 缺萼枫香L. acalycina | 1.28±0.05 | 0.107±0.003 | 12.2±0.5 | 细枝棱E. loquaiana | 0.77±0.01 | 0.042±0.002 | 17.5±0.3 |
| 羊角杜鹃R.cavaleriei | 0.57±0.02 | 0.068±0.002 | 8.9±0.3 | 檫树S. tzumu | 1.45±0.02 | 0.103±0.003 | 13.7±0.5 | 西南山茶C. pitardii | 0.80±0.02 | 0.050±0.004 | 15.8±0.7 |
| 虎皮楠D.oldhamii | 0.78±0.03 | 0.128±0.010 | 6.7±0.3 | 红果山胡椒L.erythrocarpa | 1.11±0.02 | 0.067±0.005 | 16.5±0.8 | 长梗冬青I. pedunculosa | 0.87±0.02 | 0.045±0.001 | 18.6±0.6 |
| 枫香L. formosana | 0.81±0.05 | 0.097±0.003 | 8.2±0.3 | 铁锥栲C. lamontii | 0.94±0.03 | 0.061±0.003 | 15.5±0.6 | 白蜡树F.chinensis | 1.78±0.06 | 0.083±0.003 | 21.0±0.5 |
| 拟赤杨A. fortune | 1.13±0.06 | 0.120±0.005 | 9.6±0.4 | 榕叶冬青I. ficoidea | 0.67±0.02 | 0.076±0.002 | 9.2±0.4 | 芳香安息香S. odoratissimus | 1.32±0.06 | 0.008±0.002 | 16.8±0.4 |
| 茅栗C. mollissima | 1.09±0.01 | 0.139±0.007 | 7.4±0.2 | 桂南木莲M. chingii | 0.69±0.03 | 0.065±0.003 | 10.2±0.7 | 红叶木姜子L. rubescens | 1.68±0.04 | 0.087±0.003 | 19.6±0.6 |
| 五裂槭A. oliverianum | 0.95±0.02 | 0.094±0.004 | 10.6±0.3 | 银木荷S. argentea | 0.85±0.02 | 0.059±0.001 | 14.8±0.3 | 美脉花楸S. caloneura | 1.10±0.02 | 0.065±0.001 | 16.1±0.3 |
| 山胡椒L. glauca | 1.25±0.04 | 0.153±0.005 | 8.6±0.2 | 交让木D.macropodum | 0.50±0.04 | 0.045±0.005 | 10.5±0.6 | 红果树S. davidiana | 1.27±0.04 | 0.058±0.002 | 21.6±0.7 |
| 常绿平均Evergreen average | 0.63±0.05 | 0.089±0.011 | 7.6±0.5 | 常绿平均Evergreen average | 0.73±0.08 | 0.061±0.005 | 12.0±1.3 | 常绿平均Evergreen average | 0.76±0.06 | 0.039±0.005 | 18.8±1.0 |
| 落叶平均Deciduous average | 1.05±0.08 | 0.122±0.011 | 8.9±0.6 | 落叶平均Deciduous average | 1.21±0.07 | 0.093±0.007 | 13.0±1.0 | 落叶平均Deciduous average | 1.43±0.13 | 0.075±0.006 | 19.0±1.1 |
| 总平均Total average | 0.84±0.08 | 0.106±0.009 | 8.2±0.4 | 总平均Total average | 0.97±0.09 | 0.077±0.007 | 12.5±0.8 | 总平均Total average | 1.10±0.13 | 0.057±0.007 | 18.9±0.7 |
| 衰老叶营养特征 Nutrient traits in senesced leaves | 所有树种平均 Means across species | 所有常绿平均 Means across evergreen species | 所有落叶平均 Means across deciduous species | 叶片习性 Leaf habit | 海拔Altitude | 交互作用Interaction | |||||
| F | P | F | P | F | P | ||||||
| 氮 N/% | 0.970±0.06 | 0.710±0.04 | 1.230±0.07 | 63.8 | <0.001 | 4.2 | <0.05 | 0.3 | 0.72 | ||
| 磷 P/% | 0.080±0.006 | 0.063±0.007 | 0.097±0.007 | 32.2 | <0.001 | 21.1 | <0.001 | 1.5 | 0.25 | ||
| 氮∶磷比 N∶P | 13.200±0.9 | 12.800±1.3 | 13.60±1.2 | 2.2 | 0.15 | 69.3 | <0.001 | 0.5 | 0.59 | ||
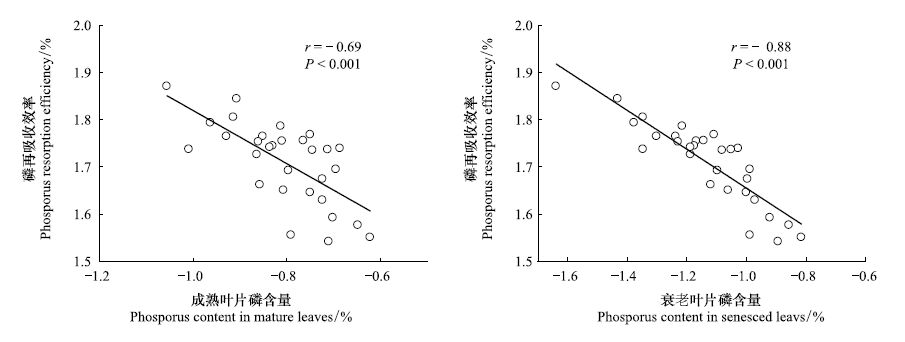
由图 2可看出,磷再吸收效率不但与成熟叶片磷含量有显著的负相关关系(r=- 0.69,P<0.001)而且与衰老叶片磷含量有显著的负相关关系 (r=- 0.88,P<0.001)。落叶树种成熟叶片磷含量(0.181%)显著高于常绿树种(0.142%)(P<0.001,表 3),而且落叶树种衰老叶片磷含量(0.097%)也显著高于常绿树种(0.063%)(P<0.001,表 4)。成熟叶片和衰老叶片磷含量都随海拔的增加而显著降低(P<0.001,表 3,表 4)。
|
| 图2 数据转换为对数形式后的磷再吸收效率与成熟和衰老叶磷含量的关系 Fig.2 Relationship between phosphorus resorption efficiency and phosporus content in mature and senesced leaves after data log-transformation |
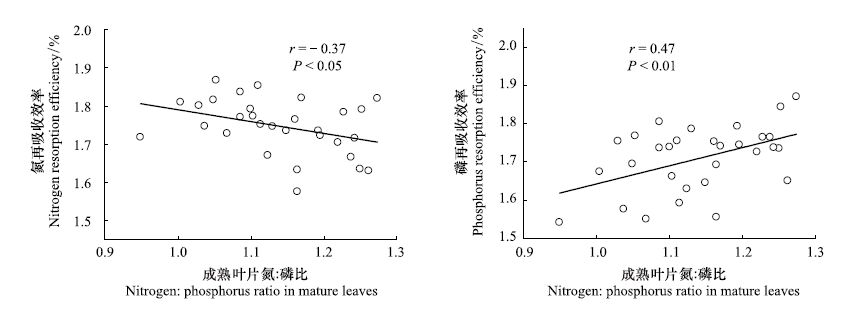
图 3表明,氮再吸收效率与成熟叶片氮 ∶磷比有显著的负相关关系(r=- 0.37,P<0.05),磷再吸收效率与成熟叶片氮 ∶磷比成显著正相关关系(r=0.47,P<0.01)。成熟叶片氮 ∶磷比平均值为14.1,不受叶片习性的影响,但是受到海拔的显著影响 (P<0.001,表 3)。高海拔和低海拔树种成熟叶片氮 ∶磷比的平均值分别为17.1和11.3(表 3)。
|
| 图3 数据转换为对数形式后的氮和磷再吸收效率与成熟叶片氮∶磷比的关系 Fig.3 Relationships of nitrogen and phosphorus resorption efficiency with nitrogen∶phosphorus ratio in mature leaves after data log-transformation |
衰老叶片氮 ∶磷比平均值为13.2,不受叶片习性的影响,但随海拔的增加而显著增加(P<0.001,表 4)。高海拔树种衰老叶片氮 ∶磷比显著高于成熟叶片氮 ∶磷比(P<0.01),低海拔树种衰老叶片氮 ∶磷比显著大于成熟叶片氮 ∶磷比(P<0.001),而中海拔衰老叶片氮 ∶磷比与成熟叶片氮 ∶磷比没有显著差异(表 3,表 4)。
|
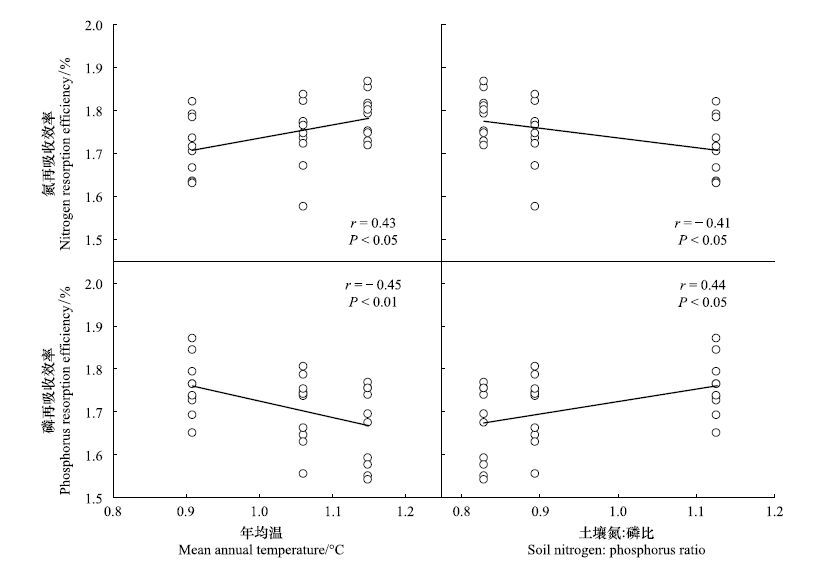
| 图4 数据转换为对数形式后的氮和磷再吸收效率与年均温和土壤氮∶磷比的关系 Fig.4 Relationships of nitrogen and phosphorus resorption efficiency with mean annual temperature and soil nitrogen ∶phosphorus ratio after data log-transformation |
图 4表明,氮再吸收效率和磷再吸收效率都与环境因子有显著的相关性。氮再吸收效率与土壤氮 ∶磷比负相关(r=- 0.41,P<0.05)而与年均温正相关(r=0.43,P<0.05)。磷再吸收效率与土壤氮 ∶磷比正相关(r=0.44,P<0.05)而与年均温负相关(r=- 0.45,P<0.01)。
3 讨论广西猫儿山树种成熟叶片平均50%以上的氮和磷在衰老期间被再吸收(表 2),支持营养再吸收是森林植物营养保存重要机制的科学假说[1, 29]。从平均值来看,猫儿山树种氮再吸收效率(56.5%)高于已报道的全球树种的平均值(46.9%)和我国华东树种的平均值(49.1%),磷再吸收效率(52.1%)则与已报道的全球树种的平均值(53.5%)和我国华东树种的平均值(51.0%)比较接近[5, 15]。
猫儿山树种氮和磷再吸收效率与叶片习性有密切的关系(表 2)。猫儿山常绿树种总体上比落叶树种有较高的氮和磷再吸收效率,这与常绿树种有较低的成熟和衰老叶片的氮和磷含量有密切的关系,这与前人研究的营养再吸收效率随着成熟和衰老叶片营养元素含量的增加而减少的结果是一致的[16, 17]。然而,营养再吸收效率是否受到叶片习性的影响还是存在争议的。Aerts[1]与Yuan和Chen[5] 的结果表明落叶树种的氮再吸收效率显著高于常绿树种。Aerts[1]和Vergutz等[3]的研究结果表明常绿和落叶树种之间的磷再吸收效率没有差异,Yuan和Chen[5]却发现常绿树种的磷再吸收效率高于落叶树种。这些研究结果的差异表明,高的营养再吸收效率可能并不是常绿习性形成的必要的优势特征。由于常绿树种叶片寿命较长,而且树种之间叶片寿命的变化幅度往往要比再吸收效率要高,有些学者因此认为叶片寿命是比营养再吸收效率更为重要的营养保存机制[30, 31]。本研究发现常绿树种比落叶树种有较低的成熟和衰老叶片营养含量(表 3,表 4),因此,常绿树种减少营养损失可以通过形成寿命长而且营养含量较低的叶片来实现。与之相反,落叶树种较低的营养再吸收效率可能是对叶片寿命短和高营养含量导致快速生长的一种成本要求[8, 31]。
猫儿山树种氮和磷再吸收效率受到海拔的显著调节(表 2)。高海拔树种比低海拔树种有显著较高的磷再吸收效率,但是前者的氮再吸收效率相对较低。这与以往的一些研究结果有很大的差异,因为有研究表明氮和磷再吸收效率在海拔之间没有显著的差异[23, 24]或者随着海拔的增加而降低[15]。这些研究差异的原因可能在于营养再吸收不是与海拔本身起作用而与海拔变化导致的气候和土壤特征的变化起作用,因为植物竞争分布在本质上是对土壤资源和气候的长期适应而形成的[11]。猫儿山年均降水量超过2500 mm[19],土壤水资源并不是本研究中常绿和落叶树种生长的限制因子。低海拔土壤氮 ∶磷比(2.8)明显低于我国热带和亚热带山地土壤氮 ∶磷比的平均值(6.4),表明土壤氮限制相对较高。高海拔土壤氮 ∶磷比(11.2)明显高于我国温带山地土壤氮 ∶磷比的平均值(4.5),表明土壤磷限制较为突出[31]。中海拔土壤氮 ∶磷比(3.8)与我国暖温带气候下的山地土壤的氮 ∶磷比(3.6)是很接近的[32],没有明显的土壤营养限制。植物成熟叶片的氮 ∶磷比可以作为植物群落生产力受到何种营养元素限制的指标,当植物成熟叶片氮 ∶磷比小于14,表明是氮限制,氮 ∶磷比大于16表明是磷限制,而氮 ∶磷比处于二者之间为氮和磷都不限制[33, 34]。本研究低海拔、中海拔和高海拔树种成熟叶片氮 ∶磷比分别为11.3、13.7和17.1,进一步表明低海拔树种缺氮、高海拔树种缺磷而中海拔营养相对均衡(表 3)。高的营养再吸收效率是一种植物在营养贫瘠环境下获得竞争优势的重要策略[12, 35],因此可以推测低海拔树种有较高的氮再吸收效率而高海拔树种有较高的磷再吸收效率。本研究发现氮再吸收效率与土壤和成熟叶片氮 ∶磷比负相关(图 3,图 4),磷再吸收效率与土壤和成熟叶片氮 ∶磷比正相关(图 3,图 4),这意味着随着海拔的升高氮再吸收效率下降而磷再吸收效率增加,这与前人研究得出的磷限制的生境有较高的磷再吸收效率而氮限制的生境有较高的氮再吸收效率的结论是相似的[15, 26, 36]。值得注意的是,低海拔树种衰老叶片氮 ∶磷比高于成熟叶片氮 ∶磷比而且高海拔树种衰老叶片氮 ∶磷比低于成熟叶片氮 ∶磷比(表 3,表 4),这反映了氮在低海拔受到优先再吸收而磷在高海拔受到优先再吸收,这种营养元素在贫瘠土壤中优先再吸收的现象在青藏高原草甸和温带雨林中也得到了证实[17, 36]。另一方面,年均温随着海拔的升高而降低,本研究发现猫儿山树种氮再吸收效率与年均温正相关而磷再吸收效率与年均温负相关(图 4)。在全球尺度上,随着温度的升高氮再吸收效率下降而磷再吸收效率增加,这意味着热带亚热带地区树种磷再吸收效率高而温带寒温带地区树种氮再吸收效率高[5]。由于全球背景下的营养再吸收模式与温度气候的关系会反映土壤基质年龄和相应的土壤营养可用性,尤其是热带亚热带地区土壤相对缺磷而温带寒温带地区土壤相对缺氮,因此这种不同温度气候下营养再吸收的变化与土壤特征变化同时发生的时候,植物在氮和磷限制的情况下更有可能会提高氮和磷的再吸收效率[5, 37]。
氮和磷再吸收效率受到叶片习性和海拔的影响与叶片自身营养水平的调节密不可分。研究发现猫儿山树种氮和磷再吸收效率随着成熟和衰老叶片氮和磷含量的增加而减少(图 2)。由于猫儿山常绿树种成熟和衰老叶片的氮和磷含量都显著低于落叶树种,这意味着常绿树种形成新叶需要较低的营养水平而且每次叶片脱落的时候会流失较低的营养来提高营养再吸收效率,与之相反,落叶树种相对频繁的落叶和发生新叶且营养成本较高,因此低海拔山地土壤氮稀缺和高海拔土壤磷稀缺都不利于落叶树种形成竞争优势,这与前人研究得出的土壤营养承载力不足会导致落叶树种在氮缺乏或者磷缺乏的环境中比常绿树种有较差的竞争力的结论是一致的[10, 11]。此外,猫儿山常绿树种较低的氮和磷含量与其较长的叶片寿命、较高的比叶重和较低的光合速率一起构成了叶片资源经济学谱带理论中慢速投资回报的策略,促进常绿树种在土壤贫瘠的生境中让营养元素长期的保留在体内,有利于常绿树种在土壤贫瘠的生境中取得竞争优势[22, 38, 39, 40, 41]。
总而言之,本研究表明猫儿山树种营养再吸收效率随着叶片习性和海拔的不同而改变,而且这种改变是通过叶片自身营养水平的调节实现的,这从营养再吸收的角度进一步解释了猫儿山常绿树种沿海拔形成双峰分布的原因,有助于提高对海拔梯度上树种更替的形成机理、树种营养循环和生态位分化模式以及生物多样性形成等方面的认识。
| [1] | Aerts R. Nutrient resorption from senescing leaves of perennials: are there general patterns? Journal of Ecology, 1996, 84(4): 597-608. |
| [2] | 苏波, 韩兴国, 黄建辉, 渠春梅. 植物的养分利用效率(NUE)及植物对养分胁迫环境的适应策略. 生态学报, 2000, 20(2): 335-343. |
| [3] | Vergutz L, Manzoni S, Porporato A, Novais R F, Jackson R B. Global resorption efficiencies and concentrations of carbon and nutrients in leaves of terresrtrial plants. Ecological Monographs, 2012, 82(2): 205-220. |
| [4] | Ratnam J, Sankaran M, Hanan N P, Grant R C, Zambatis N. Nutrient resorption patterns of plant functional groups in a tropical savanna: variation and functional significance. Oecologia, 2008, 157(1): 141-151. |
| [5] | Yuan Z Y, Chen H Y H. Global-scale patterns of nutrient resorption associated with latitude, temperature and precipitation. Global Ecology and Biogeography, 2009, 18(1): 11-18. |
| [6] | Hobbie S E. Effects of plant species on nutrient cycling. Trends in Ecology and Evolution, 1992, 7(10): 336-339. |
| [7] | Demars B G, Boerner R E J. Foliar nutrient dynamics and resorption in naturalized Lonicera maackii (Caprifoliaceae) populations in Ohio, USA. American Journal of Botany, 1997, 84(1): 112-117. |
| [8] | Lal C B, Annapurna C, Raghubanshi A S, Singh J S. Effect of leaf habit and soil type on nutrient resorption and conservation in woody species of a dry tropical environment. Canadian Journal of Botany, 2001, 79(9): 1066-1075. |
| [9] | Chen Y H, Han W X, Tang L Y, Tang Z Y, Fang J Y. Leaf nitrogen and phosphorus concentrations of woody plants differ in responses to climate, soil and plant growth form. Ecography, 2013, 36(2):178-184. |
| [10] | Aerts R. The advantages of being evergreen. Tends in Ecology and Evolution, 1995, 10(10): 402-407. |
| [11] | Givnish T J. Adaptive significance of evergreen vs. deciduous leaves: solving the triple paradox. Silva Fennich, 2001, 36(3): 703-743. |
| [12] | Aerts R. Interspecific competition in natural plant communities: mechanisms, trade-offs and plant-soil feedbacks. Journal of Experimental Botany, 1999, 50(330): 29-37. |
| [13] | 王希华, 黄建军, 阎恩荣. 天童常绿阔叶林若干树种的叶片营养转移研究. 广西植物, 2004, 24(1): 81-85. |
| [14] | Huang J J, Wang X H, Yan E R. Leaf nutrient concentration, nutrient resorption and litter decomposition in an evergreen broad-leaved forest in eastern China. Forest Ecology and Management, 2007, 239(1): 150-158. |
| [15] | Tang L Y, Han W X, Chen Y H, Fang J Y. Resorption proficiency and efficiency of leaf nutrients in woody plants in eastern China. Journal of Plant Ecology, 2013, 6(5): 408-417. |
| [16] | Kobe R K, Lepczyk C A, Iyer M. Resorption efficiency decreases with increasing green leaf nutrients in a global data set. Ecology, 2005, 86(10): 2780-2792. |
| [17] | Jiang C M, Yu G R, Li Y N, Cao G M, Yang Z P, Sheng W P, Yu W T. Nutrient resorption of coexistence species in alpine meadow of the Qinghai-Tibetan Plateau explains plant adaptation to nutrient-poor environment. Ecological Engineering, 2012, 44: 1-9. |
| [18] | 朱彪, 陈安平, 刘增力, 李光照, 方精云. 广西猫儿山植物群落物种组成、群落结构及树种多样性的垂直分布格局. 生物多样性, 2004, 12(1): 44-52. |
| [19] | 黄金玲, 蒋得斌. 广西猫儿山自然保护区综合科学考察. 长沙: 湖南科学技术出版社, 2002. |
| [20] | Kikuzawa K. Geographical distribution of leaf life span and species diversity of trees simulated by a leaf-longevity model. Vegetatio, 1996, 122(1): 61-67. |
| [21] | Kikuzawa K. A cost-benefit analysis of leaf habit and leaf longevity of trees and their geographical pattern. The American Naturalist, 1991, 138(5): 1250-1263. |
| [22] | 白坤栋, 蒋得斌, 万贤崇. 广西猫儿山不同海拔常绿树种和落叶树种光合速率与氮的关系. 生态学报, 2013, 33(16): 4930-4938. |
| [23] | Kutbay H G, Ok T. Foliar N and P resorption and nutrient levels along an elevetional gradient in Juniperous oxycedrus L. subsp. macrocarpa (Sibth. & Sm.) Ball. Annals of Forest Science, 2003, 60(5): 449-454. |
| [24] | Kilic D, Kutbay H G, Ozbucak T, Huseyinova R. Foliar resorption in Quercus petraea subsp. iberica and Arbutus andrachne along an elevational gradient. Annals of Forest Science, 2010, 67(2): 213p1-213p8. |
| [25] | 中国科学院南京土壤研究所. 土壤理化分析. 上海: 上海科学技术出版社, 1978. |
| [26] | Killingbeck K T. Nutrients in senesced leaves: keys to the search for potential resorption and resorption proficiency. Ecology, 1996, 77(6): 1716-1727. |
| [27] | Reed S C, Townsend A R, Davidson E A, Cleveland C C. Stoichiometric patterns in foliar nutrient resorption across multiple scales. The New Phytologist, 2012, 196(1): 173-180. |
| [28] | Kerkhoff A J, Enquist B J. Multiplicative by nature: why logarithmic transformation is necessary in allometry. Journal of Theoretical Biology, 2009, 257(3): 519-521. |
| [29] | Eckstein R L, Karlsson P S, Weih M. Leaf life span and nutrient resorption as determinants of plant nutrient conservation in temperate-artic regions. The New Phytologist, 1999, 143(1): 177-189. |
| [30] | Reich P B, Ellsworth D S, Uhl C. Leaf carbon and nutrient assimilation and conservation in species of differing successional status in an oligotrophic Amazonian forest. Functional Ecology, 1995, 9(1): 65-76. |
| [31] | Wright I J, Westoby M. Nutrient concentration, resorption and lifespan: leaf traits of Australian sclerophyll species. Functional Ecology, 2003, 17(1): 10-19. |
| [32] | Tian H Q, Chen G S, Zhang C, Melillo J M, Hall C A S. Pattern and variation of C : N : P ratios in China's soils: a synthesis of observational data. Biogeochemistry, 2010, 98(1/3): 139-151. |
| [33] | Koerselman W, Meuleman A F M. The vegetation N : P ratio: a new tool to detect the nature of nutrient limitation. Journal of Applied Ecology, 1996, 33(6): 1441-1450. |
| [34] | Güsewell S. N : P ratios in terrestrial plants: variation and functional significance. The New Phytologist, 2004, 164(2): 243-246. |
| [35] | Pugnaire F I, Chapin F S. Controls over nutrient resorption from leaves of evergreen Mediterranean species. Ecology, 1993, 74(1): 124-129. |
| [36] | 阎恩荣, 王希华, 郭明, 仲强, 周武. 浙江天童常绿阔叶林、常绿针叶林与落叶阔叶林的C : N : P化学计量特征. 植物生态学报, 2010, 34(1): 48-57. |
| [37] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude. Proceedings of the National Academy of Sciences of the United States of America, 2004, 101(30): 11001-11006. |
| [38] | Richardson S J, Allen R B, Doherty J E. Shifts in leaf N : P ratio during resorption reflect soil P in temperate rainforest. Functional Ecology, 2008, 22(4): 738-745. |
| [39] | Norris M D, Reich P B. Modest enhancement of nitrogen conservation via retranslocation in response to gradients in N supply and leaf N status. Plant and Soil, 2009, 316(1/2): 193-204. |
| [40] | Freschet G T, Cornelissen J H C, van Logtestijn R S P, Aerts R. Substantial nutrient resorption form leaves, stems and roots in a subarctic flora: what is the link with other resource economics traits?. The New Phytologist, 2010, 186(4): 879-889. |
| [41] | Wright I J, Reich P B, Westoby M, Ackerly D D, Baruch Z, Bongers F, Cavender-Bares J, Chapin F S, Cornelissen J H C, Diemer M, Flexas J, Garnier E, Groom P K, Gulias J, Hikosaka K, Lamont B B, Lee T, Lee W, Lusk C, Midgley J J, Navas M L, Niinemets V, Oleksyn J, Osada N, Poorter H, Poot P, Prior L, Pyankov V I, Roumet C, Thomas S C, Tjoelker M G, Veneklaas E J, Villar R. The worldwide leaf economics spectrum. Nature, 2004, 428(6985): 821-827. |
 2015, Vol. 35
2015, Vol. 35




