文章信息
- 丁俊祥, 邹杰, 唐立松, 刘卫国
- DING Junxiang, ZOU Jie, TANG Lisong, LIU Weiguo
- 沼泽、盐化沙丘过渡带和沙丘生境下芦苇的光合及生理生化特性
- Photosynthesis and physiological-biochemical characteristics of Phragmites australis in swamp, light salt meadow, and sand dune habitats
- 生态学报, 2015, 35(16): 5316-5323
- Acta Ecologica Sinica, 2015, 35(16): 5316-5323
- http://dx.doi.org/10.5846/stxb201404170756
-
文章历史
- 收稿日期: 2014-04-17
- 网络出版日期: 2014-10-08
2. 中国科学院新疆生态与地理研究所, 荒漠与绿洲生态国家重点实验室, 乌鲁木齐 830011;
3. 中国科学院大学, 北京 100049;
4. 中国科学院阜康荒漠生态系统研究站, 阜康 831505
2. State Key Laboratory of Desert and Oasis Ecology, Xinjiang Institute of Ecology and Geography, Chinese Academy of Sciences, Urumqi 830011, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. Fukang Station of Desert Ecology, Chinese Academy of Sciences, Fukang 831505, China
在内陆干旱气候区,土壤水分和盐分条件是影响植被生长、分布的主要自然环境因素[1]。为适应水分、盐分变化并保证正常的碳代谢过程,干旱区植物必须具备较强的渗透调节和抗氧化能力。芦苇(Phragmites australis)是一种适应性较强的植物,不仅能够在干旱、沼泽生境中生长,而且对盐渍化生境也具有较强的忍耐能力。此外,旱生芦苇常可作为优良的饲草和优质的造纸原料,具有一定的经济价值;沙地和盐渍化生境中生长的芦苇常具有强大的根茎和根系系统,起到固沙和促进盐碱土壤通透性的作用,具有一定的生态价值[2]。
针对水盐胁迫下芦苇的生理生化以及生态学适应特性前人已做了大量研究,如Yang[3]通过盆栽试验研究了黄河三角洲生长的盐生芦苇在水分和盐分胁迫下的光合特性和抗逆性。Gorai[4]通过营养液培养的方法研究了盐分梯度和缺氧环境下芦苇的光合特性和渗透调节。Pagter[5]通过室内培养的方式研究了不同程度水分亏缺对芦苇生长、光合及与水分亏缺有关的生理特性的影响。可见,以往的试验多集中于室内人工水分、盐分处理下芦苇的生理、生态特性。然而,自然界中的植物常常是同时或相继经受多种环境因素不同程度的作用和影响,而且植物对不同影响因子的响应方式各异,适应机理也十分复杂,很难通过室内控制实验来准确判断植物的生长状况和适应特性。另外,以往的研究多集中于探讨湿润、半湿润区水生芦苇的生理生态特性[3, 4, 5, 6, 7, 8, 9, 10],而对干旱气候区不同生境下芦苇的生理生化特性的研究较少。因此,本实验选取和田地区于田县境内3种不同生境(沼泽、盐化沙丘过渡带和沙丘)下生长的芦苇为研究对象,通过测定芦苇的光合生理指标、渗透调节物质(可溶性糖、脯氨酸)、抗逆生理指标(POD、MDA、SOD),比较水分、盐分梯度下芦苇的适应特性,探讨绿洲植物的光合、渗透调节、抗氧化系统的适应途径和策略,以期为进一步认识植物在逆境中的自我保护特点及为绿洲的恢复和保护提供理论支持。
1 材料与方法 1.1 研究区与材料实验在新疆和田地区于田县境内进行,地处东经81°14′,北纬37°02′。本研究区属暖温带内陆荒漠气候,主要特点是:四季分明、昼夜温差大,热量资源丰富,光照充足,降水稀少,蒸发量大,春夏多风沙和浮尘等灾害天气,多年平均气温为12.4 ℃,多年平均降水量47.7 mm,潜在蒸发量是2432.1 mm[11]。克里雅河流经于田绿洲,为本区自然植被生长、发育和繁衍重要水分来源。
实验所用芦苇取自和田地区于田县。在距克里雅河一定范围内,选取有芦苇广泛分布的3种不同生境,分别为沼泽、盐化沙丘过渡带和沙丘。沼泽芦苇(SR)生长在地势较低洼的水塘,常年有积水,进入生长旺季后,群落盖度在80%以上。盐化沙丘过渡带芦苇(LSMD)生长于盐碱土与沙丘交接的生境中,土壤表层有轻微盐碱累积,植被稀疏,多呈小片分布,盖度在50%左右。沙丘芦苇(DR)生长于5—8 m沙丘上,土壤为风沙土,通透性较好。芦苇多呈零星分布,分株细小,盖度在20%左右。
在2013年7月初,在3种生境内各布设5个采样点,在每个采样点选取3株长势基本一致、健壮无病虫害的芦苇植株进行标记,以芦苇植株顶端向下第2片充分伸长的叶片为试材,测定其光合作用日过程。在8月初芦苇生长旺盛时期,在每个样点分别采集同一叶位芦苇样株叶片,立即装入液氮罐保存,带回实验室用于抗逆生理指标分析。15个采样点中,1—5样株为沼泽生境,6—10为盐化沙丘过渡生境,11—15为沙丘生境。
1.2 实验方法 1.2.1 土壤水分和盐分测定在每一采样点下各设置3个1m×1m样方,每一样方内的4个角各设一个取样点,在黎明前取各样点根区土壤,并将根区的4个取样点的土样混合均匀,保鲜袋分装,烘干法测定土壤含水量,电导仪测定土壤含盐量(水土比为5∶1)。
1.2.2 光合特性测定选取晴朗天气,测定3种生境内芦苇的光合作用日过程。从当地时间8:00到19:00,每间隔1 h采用便携式光合系统分析仪LI-6400(Li-Cor,Lincoln,NE,USA)测定芦苇的净光合速率(Pn)、气孔导度(Gs)、蒸腾速率(Tr)、胞间CO2浓度( Ci)等气体交换参数,每次测定重复3次取值,并取3组叶片作组内重复。叶片水分利用效率(WUE)和气孔限制值( Ls)分别用公式计算:

可溶性糖的测定采用硫酸苯酚法[12],叶片游离脯氨酸含量的测定采用磺基水杨酸法[13]。
1.2.4 丙二醛含量和测定抗氧化酶活性的测定丙二醛(MDA)含量的测定采用双组分光光度法[14]。采用氮蓝四唑法测定超氧化物歧化酶(SOD)活性[15],以抑制NBT光化学还原的50%为1个酶还原单位(unit/mg)。采用愈创木酚显色法测定过氧化物酶(POD)活性[16],以每分钟内470 nm下的光密度(D470 nm)变化0.10为1个酶活性单位(unit mg-1 min-1)表示。过氧化氢酶(CAT)活性的测定采用紫外吸收法[16],以1 min内A240降低0.1为1个酶活性单位(unit mg-1 min-1)。
1.3 数据统计与分析采用Excel2007进行简单数据整理,结合SPSS18.0和origin8.0软件对数据进行统计分析和绘图。
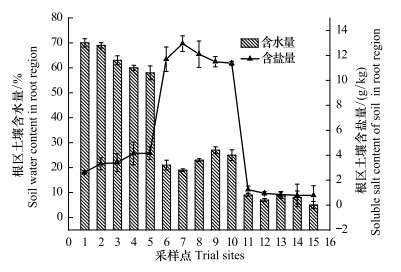
2 结果 2.1 3种生境内芦苇土壤水分和盐分含量变化3种生境15个芦苇采样点的根区土壤水分和盐分含量具有明显的梯度(图 1),沼泽生境(1—5)下芦苇根区土壤含水量显著大于盐化沙丘过渡带和沙丘生境,介于60%—70%之间,均值为64%,含盐量在2—5 g/kg之间,均值为3.53 g/kg;盐化沙丘过渡带(6—10)芦苇根区土壤含水量在20%—25%之间,均值为23%,含盐量为3种生境最高,在11—13 g/kg之间,均值为11.92 g/kg;沙丘生境(11—15)土壤含水量在5%—10%之间,均值为7.6%,含盐量在0.7—1.3 g/kg之间,均值为0.92 g/kg。
|
| 图 1 15个采样点根区土壤含水量和含盐量 Fig.1 Soil water content and soluble salt content in root region at 15 trial sites |
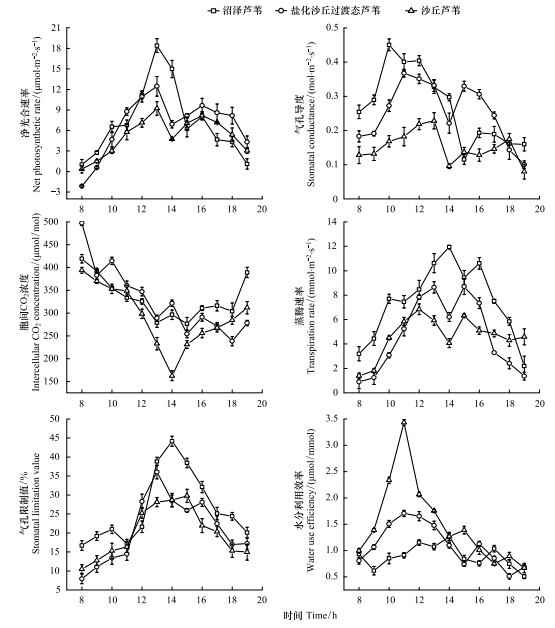
沼泽生境下芦苇Pn的日变化呈单峰曲线(图 2),在13:00左右达到峰值;生长在盐化沙丘过渡带和沙丘顶的芦苇Pn日变化为明显的双峰曲线,在14:00左右Pn迅速减小,表现出明显的“午休”现象。3种生境下,沼泽芦苇净光合速率日均值最大,其次为过渡带芦苇和沙丘芦苇,但3者间差异不显著(表 1)。不同生境下,芦苇气孔导度均有较大变化(图 2),沼泽和过渡带芦苇在8:00—11:00之间增加较快,随后逐渐减小,与午间高温存在密切关系;沙丘芦苇的气孔导度一天内变化不大,维持在较低水平,14:00左右迅速降低至一天中最小值,与光合“午休”对应。沼泽芦苇叶片胞间CO2浓度自早晨测量时开始逐渐降低(图 2),在14:00以后稍有稳定,并呈波动上升;过渡带芦苇和沙丘芦苇12:00以后的胞间CO2浓度减小显著,后缓慢上升。
|
| 图 2 3种不同生境条件下芦苇叶片光合参数的日变化 Fig.2 Diurnal variation of photosynthetic parameters in leaves of P. australis under three different habitat conditions |
3种生境下芦苇蒸腾速率的日变化与净光合速率有较好的一致性,且随干旱程度的加剧蒸腾减少显著(图 2)。盐化沙丘过渡态芦苇和沙丘芦苇叶片的气孔限制值(Ls)在13:00以前均呈上升趋势,之后,盐化沙丘过渡态芦苇的Ls开始下降,而沙丘芦苇则直到15:00以后才开始降低;在10:00之前,沼泽芦苇气孔限制值不断升高,之后一个小时内降低,并在11:00后又迅速上升,直到14:00(图 2)。在13:00之前,3种生境的芦苇水分利用效率差异显著,沙丘芦苇最高,过渡态芦苇次之,沼泽芦苇最小;13:00之后,3种生境芦苇的水分利用效率呈波动减小(图 2);在一天之内,沙丘芦苇的水分利用效率显著高于沼泽芦苇,而盐化沙丘过渡带芦苇与两者没显著差异(表 1)。
|
样地 Habitat | 净光合速率 Net photosynthetic rate/ (μmol m-2 s-1) | 水分利用效率 Water use efficiency / (μmol/mmol) | 可溶性糖 Soluble sugar content/ (mg/g) | 脯氨酸含量 Proline content/ (mg/g) | MDA含量 MDA content/ (ng/g) | SOD活性 SOD activity/ (unit/mg) | POD活性 POD activity/ (unit mg-1 min-1) | CAT活性 CAT activity/ (unit mg-1 min-1) |
| 1:沼泽生境,2:盐化沙丘过渡生境,3:沙丘生境;MDA: 丙二醛,malondialdehyde; SOD: 超氧化物歧化酶,superoxide dismutase; POD: 过氧化物酶,peroxidase; CAT: 过氧化氢酶,catalase; 数据为平均值±标准误;同列不同字母表示样地间在0.05水平差异显著 | ||||||||
| 1 | 7.17±1.54a | 0.89±0.063a | 30.56±2.21a | 0.14±0.02a | 3.39±0.15a | 2.84±0.49a | 90.24±3.58a | 0.86±0.02a |
| 2 | 6.76±1.22a | 1.10±0.12ab | 43.48±1.04b | 0.32±0.01b | 7.33±0.49b | 5.78±0.44b | 201.16±3.78b | 1.11±0.03b |
| 3 | 5.22±0.80a | 1.50±0.23b | 63.78±1.82c | 0.44±0.02c | 5.82±0.60c | 19.00±0.49c | 252.44±3.63c | 2.25±0.03c |
随干旱程度的加剧,芦苇叶片可溶性糖和脯氨酸含量呈增加趋势,其中可溶性糖含量的变化较剧烈,而脯氨酸含量的变化较平缓,表明随土壤含水量的降低,特别是荒漠沙丘地区,芦苇叶片较高的可溶性糖含量对抗旱的贡献较大(图 3)。沼泽生境下芦苇叶片可溶性糖和脯氨酸含量的平均值分别为30.56、0.14 mg/g;盐化沙丘过渡态芦苇可溶性糖和脯氨酸含量的平均值为43.48、0.32 mg/g;沙丘芦苇可溶性糖和脯氨酸含量的平均值为63.78、0.44 mg/g,3种生境下,可溶性糖和脯氨酸含量差异显著(表 1)。

|
| 图 3 3种不同生境条件下芦苇叶片可溶性糖和脯氨酸含量 Fig.3 The variance of soluble sugar and proline content in leaves of P. australis under three different habitat conditions |
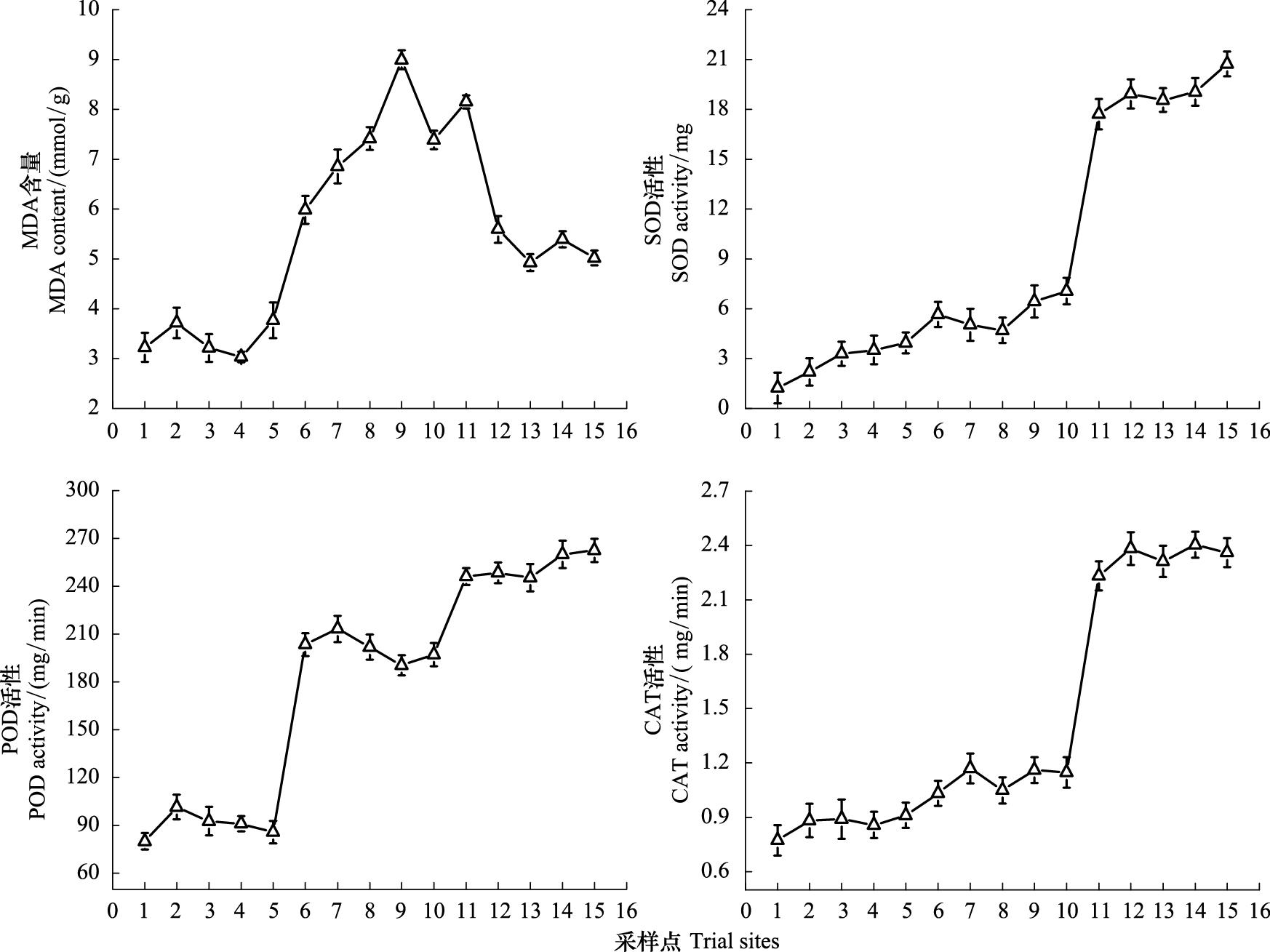
盐化沙丘过渡态芦苇叶片MDA含量在3中生境内最高,沙丘芦苇次之,沼泽芦苇最低(图 4),平均含量分别为7.33、5.82、3.39 mmol/g,且3者之间差异显著。这表明在盐渍化生境中芦苇叶片表现出较高程度的脂质过氧化,而在沙丘生境中,芦苇叶片也遭受相对较高的氧化损伤,但由于抗氧化酶活性较高,缓解了脂质过氧化过程,使叶片MDA的含量较盐化沙丘过渡带芦苇低。
|
| 图 4 3种不同生境条件下芦苇叶片丙二醛含量和超氧化物歧化酶、过氧化物酶、过氧化氢酶活性的变化 Fig.4 The variance of MDA (malondialdehyde) content and SOD (superoxide dismutase),POD (peroxidase),CAT (catalase) activities in leaves of P. australis under three different habitat conditions |
芦苇叶片SOD和CAT的活性在沼泽和盐化生境中的变化较小(图 4),而在沙丘生境中的活性是前两者的2倍之多(表 1)。POD活性在3种生境内具有明显的变化(图 4),在沙丘生境中的活性仍是最高,且显著高于沼泽和盐化沙丘过度生境(P<0.05)。这表明芦苇通过提高叶片SOD、POD和CAT的活性来应对由水分亏缺造成的不利影响,在盐渍化生境中,抗氧化酶的活性虽有提高,但远不及对干旱条件的反应敏感。可见,SOD和CAT对水分亏缺的防御反应远大于盐渍化,芦苇叶片SOD和CAT的主要作用可能是防御和清除由于水分亏缺所造成氧化伤害。
3 结论与讨论芦苇根区土壤含水量以沼泽生境最高,盐化沙丘过渡带次之,沙丘生境最低,土壤含盐量在水分条件较好的沼泽和沙丘生境较低,在水分条件适中的过渡带最高。沼泽生境下芦苇叶片Pn的日变化呈单峰曲线,盐化沙丘过渡态芦苇和沙丘芦苇Pn日变化呈双峰曲线,表现出明显的“午休”现象,“午休”现象的直接原因是气孔导度降低,由此也导致叶片蒸腾速率降低和胞间浓度CO2浓度下降。可溶性糖和脯氨酸含量随干旱和盐渍化的加剧显著增加,其中可溶性糖含量的变化剧烈,对减缓干旱和盐渍化威胁的贡献较大;脯氨酸随水分减少和盐分加剧的增加量相对较少,对水盐变化的反应并不十分敏感。SOD和CAT的活性随干旱程度的加剧而迅速升高,对水分变化的响应大于盐渍化;POD活性在盐渍化生境和含水量较低的沙丘生境内都比较高,对抵抗盐渍化和干旱起着同样重要的作用。然而,POD活性尚不足以缓解因盐渍化造成的伤害,使MDA在盐化沙丘过渡带芦苇叶片中依然具有较高含量;而较高的SOD和CAT活性,缓解了由干旱所造成的氧化损伤,使沙丘芦苇叶片MDA含量维持在相对较低水平。
在不同环境下,植物对逆境的应激方式不同,适应逆境的机理也十分复杂,很难仅仅依靠一种机制或一种酶的活性做出准确判断。事实上,自然界中的植物更多的是同时或相继经受多种环境胁迫,很少遭受单一的环境胁迫,而有关植物的抗性生理,大多限于实验室研究或对单一胁迫的反应,使人们对多种环境胁迫间的相互关系了解甚少,因而利用自然变异体系来分析植物对逆境的适应机理显得尤为重要[17]。因此,本实验选取具有水盐变异的沼泽、盐化沙丘过渡带和沙丘顶部3处生境,从光合特性、渗透调节、抗氧化酶活性等方面研究芦苇对不同生境条件的适应机制。
光合作用对环境因子的响应高度敏感,干旱缺水是植物经常遭受的逆境形式,对植物光合作用过程有着重要的影响,植物受到干旱胁迫时光合作用被限制,净光合速率下降[18]。在水分条件较好、盐分较低的沼泽生境,芦苇叶片Pn的日变化呈单峰曲线,而在盐渍化生境和水分亏缺严重的沙丘生境中,芦苇叶片的光合作用表现出明显的“午休”现象,且光合作用水平下降。气孔导度降低是叶片光合“午休”的主要原因,同时减少了叶片蒸腾耗水,防止植物因过度蒸腾而脱水死亡,是适应干旱胁迫的有效途径。对于水分亏缺条件下植物光合作用水平下降的原因,有的研究结果是气孔因素(气孔关闭引起CO2供应受阻)为主[19],或是非气孔因素(叶肉细胞光合活性下降)为主[20],也有研究认为是两者共同作用的结果[21]。Farquhar和Sharkey[22]认为,引起光合速率降低的气孔和非气孔限制因素可以根据叶片胞间CO2浓度和气孔限制值的变化方向来判断,当Pn下降时,若Ci降低而Ls增加,则表明气孔导度的降低是光合速率减小的主要原因;若Ci增加或者不变,同时Ls降低,则为非气孔限制造成净光合速率的降低,即叶肉细胞光合活性的下降。本实验中,沼泽芦苇和沙丘芦苇净光合速率下降的主要原因均出现由气孔限制转变为非气孔空限制的现象,说明沼泽和沙丘生境内芦苇叶片的光合机构受到一定程度伤害;而盐化沙丘过渡态芦苇光合作用水平降低主要是由非气孔限制因素造成,这与其所遭受的盐分胁迫有关系。有研究表明,盐分胁迫致使叶绿素含量降低,影响色素蛋白复合体的功能,降低了叶绿体对光能的吸收,而影响到光合性能[23]。Hanganu[6]以及Lissner[7]对盐分胁迫下湿地芦苇的研究中也得出类似的结论,认为当盐分浓度超过5.84 g/kg时,不仅减缓了芦苇的生长速率,同时降低了光合速率和气孔导度。然而,干旱环境抑制植物光合作用的机理比较复杂,涉及到诸多生理、生化与生态因子的影响,而且与实验植物的种类、年龄、生长状况及实验处理方式和测定指标等有关[24, 25, 26, 27]。因此,今后的研究需要在具体的实验条件下同时进行气体交换参数以及叶绿素荧光参数的测定[28],并参考光合作用过程中发生的一系列生理生化指标,特别是渗透调节物质、抗氧化酶活性的变化情况[29],才能更加深入、系统和客观的认识植物光合作用的抑制机理。
在干旱缺水以及盐渍化条件下,植物通过调节体内渗透调节物质的含量来适应环境的变化,其中可溶性糖和脯氨酸是非常重要的两种渗透调节物质[30]。本研究中,可溶性糖含量的变化对抵御干旱和盐渍化危害的贡献较大,而脯氨酸含量随水分亏缺和盐分的加剧虽有增加,但并不明显。Jampeetong[8]对槐叶萍叶片脯氨酸在不同盐分浓度下累积的研究中得出相似的结论,并认为槐叶萍尚不足以通过合成脯氨酸来抑制盐分胁迫。陈敏[31]对塔里木河中游地区3种植物抗旱机理的研究中认为植物通过可溶性糖、脯氨酸等渗透调节物质的积累来提高自身的抗旱性,植物叶片的可溶性糖和脯氨酸在抑制干旱胁迫过程中存在相互补偿的关系。王中英[32]认为可溶性糖是植物体内主要的渗透调节物质,在细胞渗透调节过程中起到重要作用,发生水分胁迫时,细胞内产生的渗透调节物质越多,对植物的渗透调节越有利,从而提高植物的抗旱能力。沙丘生境水分亏缺严重,可溶性糖含量显著增加,脯氨酸含量也有一定程度的升高,确保了植物能够在干旱缺水条件下持续吸水,这是植物主动适应干旱缺水环境的表现。
超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)等抗氧化酶类,是植物活性氧清除系统中重要的酶,能维持活性氧自由基产生与清除系统的平衡,起到保护光合机构的作用。丙二醛(MDA)是脂质过氧化作用的主要产物之一,其含量的高低在一定程度上反映质膜过氧化作用水平和膜结构的受害程度[33]。在本研究中,芦苇叶片SOD和CAT在盐渍化和沼泽生境中并不起主要防御作用,但在水分亏缺严重的沙丘生境下,两者活性明显升高。可见,SOD和CAT的主要作用是防御和清除由于水分亏缺所造成的氧化伤害,POD对缓解由盐渍化和干旱缺水所造成的不利影响起同样重要的作用,这与龚春梅等[34]对沿水分梯度分布的芦苇抗氧化保护机理研究的结果一致。然而,宫海军[35]等在小尺度上对芦苇的研究认为,与水分条件较好的芦苇相比,盐生芦苇并未出现活性氧和MDA的积累,SOD、POD、CAT等抗氧化酶的活性却显著提高。在缺水严重的沙丘生境,芦苇叶片MDA含量维持在相对较低水平,这主要是由于较高的SOD和CAT活性缓解了由干旱所造成的氧化损伤。在盐化沙丘过渡带生境中,芦苇叶片具有较高的MDA含量,表明抗氧酶活性尚不足以清除因盐分累积造成的伤害。裴斌等[33]对沙棘研究认为,当遭遇严重干旱(RWC<38.9%)时,沙棘光合作用的抗氧化酶活性发生了明显下降,MDA含量急剧升高,活性氧的产生超出了系统的清除能力导致其大量积累而引起生物膜结构和功能的破坏,并认为抗氧化酶系统损伤和光合系统的损伤一样,是导致光合作用发生非气孔限制的重要原因。
| [1] | 李卫军, 高辉远, 徐江. 不同生长型芦苇与土壤水盐相关的研究. 中国草地, 1995, (6): 20-23. |
| [2] | Kiviat E. Ecosystem services of Phragmites in North America with emphasis on habitat functions. AoB Plants, 2013, 5: plt008, doi: 10. 1093/aobpla/plt008. |
| [3] | Yang Z F, Xie T, Liu Q. Physiological responses of Phragmites australis to the combined effects of water and salinity stress. Ecohydrology, 2013, 7(2): 420-426. |
| [4] | Gorai M, Ennajeh M, Khemira H, Neffati M. Combined effect of NaCl-salinity and hypoxia on growth, photosynthesis, water relations and solute accumulation in Phragmites australis plants. Flora-Morphology, Distribution, Functional Ecology of Plants, 2010, 205(7): 462-470. |
| [5] | Pagter M, Bragato C, Brix H. Tolerance and physiological responses of Phragmites australis to water deficit. Aquatic Botany, 2005, 81(4): 285-299. |
| [6] | Hanganu J, Mihail G, Coops H. Responses of ecotypes of Phragmites australis to increased seawater influence: a field study in the Danube Delta, Romania. Aquatic Botany, 1999, 64(3): 351-358. |
| [7] | Lissner J, Schierup H H, Comín F A, Astorga V. Effect of climate on the salt tolerance of two Phragmites australis populations. II. Diurnal CO2 exchange and transpiration. Aquatic Botany, 1999, 64(3/4): 335-350. |
| [8] | Jampeetong A, Brix H. Effects of NaCl salinity on growth, morphology, photosynthesis and proline accumulation of Salvinia natans. Aquatic Botany, 2009, 91(3): 181-186. |
| [9] | 贾庆宇, 周莉, 谢艳兵, 周广胜. 盘锦湿地芦苇群落生物量动态特征研究. 气象与环境学报, 2006, 22(4): 25-29. |
| [10] | Duman F, Cicek M, Sezen G. Seasonal changes of metal accumulation and distribution in common club rush (Schoenoplectus lacustris) and common reed (Phragmites australis). Ecotoxicology, 2007, 16(6): 457-463. |
| [11] | 海米提·依米提, 冷中笑, 高前兆. 塔里木盆地南缘于田绿洲近50a来气候变化特征分析.中国沙漠, 2010, 30(3): 654-659. |
| [12] | 邹琦. 植物生理生化实验指导. 北京: 中国农业出版社, 1995: 110-111. |
| [13] | 朱广廉, 邓兴旺, 左卫能. 植物体内游离脯氨酸的测定. 植物生理学通讯, 1983, 1(1): 35-37. |
| [14] | 郝建军, 康宗利, 于洋. 植物生理学实验技术. 北京: 化学工业出版社, 2006: 159-160. |
| [15] | 郑炳松. 现代植物生理生化研究技术. 北京: 气象出版社, 2006: 91-92. |
| [16] | 孙群, 胡景江. 植物生理学研究技术. 杨凌: 西北农林科技大学出版社, 2006: 167-170. |
| [17] | Alonso-Blanco C, Koornneef M. Naturally occurring variation in Arabidopsis: an underexploited resource for plant genetics. Trends in Plant Science, 2000, 5(1): 22-29. |
| [18] | 李吉跃, Blake T J. 多重复干旱循环对苗木气体交换和水分利用效率的影响. 北京林业大学学报, 1999, 21(3): 1-8. |
| [19] | Teskey R O, Fites J A, Samuelson L J, Bongarten B C. Stomatal and nonstomatal limitations to net photosynthesis in Pinus taeda L. under different environmental conditions. Tree Physiology, 1986, 2(1/2/3): 131-142. |
| [20] | 刘孟雨, 陈培元. 水分胁迫条件下气孔与非气孔因素对小麦光合的限制. 植物生理学通讯, 1990, (4): 24-27. |
| [21] | Zhang S Y, Zhang G C, Gu S Y, Xia J B, Zhao J K. Critical responses of photosynthetic efficiency of goldspur apple tree to soil water variation in semiarid loess hilly area. Photosynthetica, 2010, 48(4): 589-595. |
| [22] | Farquhar G D, Sharkey T D. Stomatal conductance and photosynthesis. Annual Review of Plant Physiology, 1982, 33(1): 317-345. |
| [23] | 李彦, 张英鹏, 孙明, 高弼模. 盐分胁迫对植物的影响及植物耐盐机理研究进展. 中国农学通报, 2008, 24(1): 258-265. |
| [24] | 卢从明, 张其德, 匡廷云, 王忠, 高煜珠. 水分胁迫抑制水稻光合作用的机理. 作物学报, 1994, 20(5): 601-606. |
| [25] | Flexas J, Medrano H. Drought-inhibition of photosynthesis in C3 plants: stomatal and non-stomatal limitations revisited. Annals of Botany, 2002, 89(2): 183-189. |
| [26] | Wu F Z, Bao W K, Li F L, Wu N. Effects of water stress and nitrogen supply on leaf gas exchange and fluorescence parameters of Sophora davidii seedlings. Photosynthetica, 2008, 46(1): 40-48. |
| [27] | 刘锦春, 钟章成, 何跃军. 水分胁迫对重庆石灰岩地区不同龄级柏木(Cupressus funebris Endl.)幼苗气体交换的影响. 生态学报, 2007, 27(9): 3601-3608. |
| [28] | 崔晓阳, 宋金凤, 张艳华. 不同土壤水势条件下水曲柳幼苗的光合作用特征. 植物生态学报, 2004, 28(6): 794-802. |
| [29] | 张仁和, 郑友军, 马国胜, 张兴华, 路海东, 史俊通, 薛吉全. 干旱胁迫对玉米苗期叶片光合作用和保护酶的影响. 生态学报, 2011, 31(5): 1303-1311. |
| [30] | 吕晋慧, 任磊, 李艳锋, 王玄, 赵夏陆, 张春来. 不同基因型茶菊对盐胁迫的响应. 植物生态学报, 2013, 37(7): 656-664. |
| [31] | 陈敏, 陈亚宁, 李卫红, 陈亚鹏, 何斌, 湾疆辉. 塔里木河中游地区3种植物的抗旱机理研究. 西北植物学报, 2007, 27(4): 747-754. |
| [32] | 王中英. 果树抗旱生理. 北京: 中国农业出版社, 2000: 36-42. |
| [33] | 裴斌, 张光灿, 张淑勇, 吴芹, 徐志强, 徐萍. 土壤干旱胁迫对沙棘叶片光合作用和抗氧化酶活性的影响. 生态学报, 2013, 33(5): 1386-1396. |
| [34] | 龚春梅, 宁蓬勃, 王根轩, 魏小平, 贾亚宁. 沿绿洲-荒漠过渡带水分梯度分布的芦苇抗氧化保护机理. 草业学报, 2007, 16(4): 41-46. |
| [35] | 宫海军, 陈坤明, 高永生, 赵志光, 王锁民, 张承烈. 不同生境两种生态型芦苇的抗氧化系统. 西北植物学报, 2004, 24(2): 193-198. |
 2015, Vol. 35
2015, Vol. 35




