文章信息
- 冯娜, 范凡, 陶晡, 杨小凡, 魏国树
- FENG Na, FAN Fan, TAO Bu, YANG Xiaofan, WEI Guoshu
- 光谱对东亚小花蝽趋光行为的影响
- Effect of spectral sensitivity response on the phototaxis of Orius sauteri (Poppius)
- 生态学报, 2015, 35(14): 4810-4815
- Acta Ecologica Sinica, 2015, 35(14): 4810-4815
- http://dx.doi.org/10.5846/stxb201312112933
-
文章历史
- 收稿日期:2013-12-11
- 修订日期:2014-09-09
2. 河北省农作物病虫害生防工程中心, 保定 071001
2. Biological Control Center of Plant Pests of Hebei, Baoding 071001, China
小花蝽属半翅目(Hemiptera)花蝽科(Anthocoridae),在我国分布广泛,它食性广、捕食能力强,能有效控制蓟马、蚜虫、粉虱、叶螨等小型农林害虫,是一类有重大价值的天敌昆虫[1, 2]。基于小花蝽对害虫的超强控制能力,国内外对小花蝽人工饲养和自然种群保护进行了大量研究,许多国家已经成功开发出小花蝽产品[3, 4, 5, 6, 7, 8],而我国的商品化研究正处于起步阶段,因此在无公害或绿色生产中保护和利用自然种群防控害虫成为首要任务[9, 10]。在昆虫世界中,光可以直接影响昆虫许多行为活动,如搜寻食物或猎物,寻找适宜的寄主及产卵场所等。昆虫能够感觉到的光谱范围较广,并且在不同昆虫之间敏感波长有较大差异[11, 12, 13, 14, 15, 16]。因此,确定昆虫的敏感光谱在害虫防控和天敌保护利用中有着重要意义。本研究采用行为学方法,测定并明确东亚小花蝽的敏感光谱,进而为研制能够在田间吸引东亚小花蝽的光源以及光活性物质等,达到有效利用田间自然种群来对害虫进行控制的目的,同时为改进田间诱虫灯提供理论依据。
1.1 试虫及处理1.1.1 试虫
从河北农业大学标本园的玉米试验田中采集东亚小花蝽各虫态后室内饲养,食物:西花蓟马若虫,饲养条件:RXZ-300C人工气候箱(宁波江南仪器厂),温度:(27.0±0.5)℃,相对湿度:(60±5)%,光周期:16 ∶ 8 h。
1.1.2 试虫处理挑选健壮的10日龄东亚小花蝽雌雄成虫,依性别分组置于行为反应箱的栖息活动室内,每次20头,为使试虫的复眼适应状态尽量一致,每次试验处理(照光刺激)前,先使其在人工气候箱内光适应2 h(光照度水平约为800lx),再置于暗室暗适应 1h后进行光照处理。
预实验中发现东亚小花蝽对橙红光敏感度相对较高,而试虫观察是在红色光下进行的,为避免观察时红色灯光的影响,每组试虫只使用一次,观察统计后换入另一组试虫。
1.2 试验装置及方法 1.2.1 光源、光路系统及光刺激 1.2.2 行为反应装置依据东亚小花蝽成虫的行为特性并参考相关文献,自行设计趋光行为装置。其主体分为3个部分,即趋光室、避光室和栖息活动室,栖息活动室中心位置设置了一块阻止入射光进入避光反应室的挡光板,从而将趋光反应室及避光反应室在光路上分割开来(图 1)。

|
| 图1 趋光行为反应装置 Fig.1 The sketch map of light-path in phototaxis behavior experiment 1.进光孔Light inlet; 2.趋光室Phototactic room; 3.前挡板Front baffle; 4.挡光板Light shield; 5.栖息活动室roosting room; 6.后挡板Tail gate; 7.避光室Photophobism room |
各部分规格:趋光室、避光室和栖息活动室(各活动室长和直径分别为10cm 和8.5cm),挡光板直径6cm,前后挡板中央的试虫活动通道直径2cm。
1.3 试验方法试验在暗室中进行,自14:00开始。室内温度(27±0.5)℃,相对湿度(60±5)%。每次光刺激时间为20min,各处理间隔4min。为减小试验误差,每一波长采用多组试虫,试虫不重复利用。各波长处理后,红光灯下分别统计趋光室和避光室的试虫个数,计算其趋、避光反应率。
试虫每次20头为1组,重复间换用新虫组,实验中;由于虫源问题,雌虫重复6次,雄虫重复4次。
趋光行为反应百分率=趋光反应室虫数/总虫数×100%
避光行为反应百分率=避光反应室虫数/总虫数×100%
2 结果与分析 2.1 趋光行为反应从表 1和图 2可以看出,340—605 nm波谱内的14个单色光均能引发东亚小花蝽雌、雄成虫的趋光行为反应,其中雌虫趋光行为反应率较高,在所有单色光刺激下均超过了20%,最高值达47.50%(380 nm),最小值为20.00%(538 nm)。雄虫的趋光行为反应率整体上略小于雌虫,在所有单色光刺激下趋光行为反应率均超过11%,最高值达35.00%(360 nm),最小值为11.25%(562 nm)。
2.1.1 雌虫趋光行为反应从图 2中可以看出,在趋光行为反应曲线中趋光行为反应率较高的区域有3个,其中紫外区(340 nm、360 nm和380 nm)波段处较高,近似呈一趋光平台,趋光行为反应率都在45%以上,且3个单色光下的趋光行为反应率之间无显著差异;绿光区(524 nm)次之,趋光行为反应率亦能达到41.67%,此处和紫外区无显著差异;另外,在橙红光区也能引起较大趋光行为反应,582 nm、605 nm两处趋光行为反应率分别为38.33%和35.83%,显著低于紫外区域,但和绿光区之间差异不显著。其它波长亦能引起其趋光行为反应,但趋光行为反应率相对较小。
结果显示:波长因素对东亚小花蝽雌成虫趋光行为反应影响很大,且不同单色光间差异显著,通过趋光行为反应率较高的单色光推测其光感受器类型可能包括紫外、绿光和橙红光3种。
2.1.2 雄虫趋光行为反应从图 2中可以看出,在趋光行为反应曲线中趋光行为反应率较高的区域有3个,其中紫外区(340、360和380 nm)波段处最高,近似呈一趋光平台,趋光行为反应率都在30%以上,且3个单色光下的趋光行为反应率之间无显著差异;红色光区605 nm单色光处之,趋光行为反应率亦能达到27.50%,此处和紫外区380 nm处没有显著差异,但与340和 360 nm两处差异显著;在绿光区524 nm亦能达到22.50%,和红色光区之间差异不显著,但显著低于紫外区域。其它波长亦能引起其趋光行为反应,但趋光行为反应率相对较小。
结果显示:波长因素对东亚小花蝽雄成虫趋光行为影响很大,且不同单色光之间差异显著,通过趋光行为反应率较高的单色光推测其光感受器对绿光、紫外以及红光等光区敏感,这与雌虫相同,在性别之间没有差异。
2.2 避光行为反应从表 1和图 2可以看出,340—605 nm波谱内的14个单色光均能引发东亚小花蝽雌、雄成虫的避光行为反应,避光反行为应率相对较低。雌虫避光行为反应曲线为多峰型,各峰间主次明显,最高值为19.17%(400 nm),最小值仅有5.83%(360 nm)。雄虫避光行为反应曲线为一较平缓的波浪线,只有一个小峰,仅在483 nm(11.25%)单色光下超过10%。
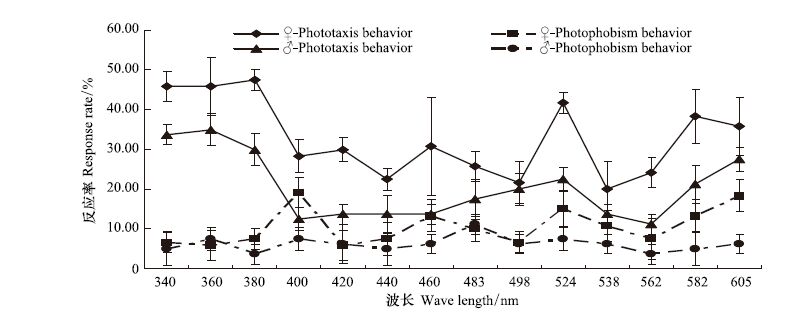
|
| 图2 东亚小花蝽趋、避光的光谱行为曲线 Fig.2 Spectral response curves Orius sauteri (Poppius) of phototaxis and photophobism behavior |
避光行为反应曲线中,避光行为反应率较高的区域亦有3个,其中蓝光近紫外区400 nm处避光行为反应率最高,为19.17%;其次为红色光区605 nm处,避光行为反应率为18.33%;绿光区524 nm处有一峰,避光行为反应率为15.00%。以上3个区域避光行为反应率之间无显著差异。其它波长亦能引起其避光行为反应,但反应率显著小于较高的两处区域。
在避光行为反应较高的3个区域除400 nm处外,另两个区域和趋光行为反应较高的区域相同,而400 nm也接近趋光行为反应率较高的紫外区。
结果显示:波长因素对东亚小花蝽雌虫避光行为反应有较大影响,且不同单色光之间差异显著。
2.2.2 雄虫避光行为反应避光行为曲线中,蓝光区483 nm避光率亦高达11.25%,其它单色光刺激下亦能引起其避光反应,但避光率相对较小,都在10.00%以下。
结果显示:波长因素对东亚小花蝽雄成虫避光行为反应影响较小,且不同单色光间避光行为反应率值相差不大。
|
单色光/nm Monochromatic light | 趋光率(均值±标准差)/% Phototactic rate (mean±S.D.) | 避光率(均值±标准差)/%
Photophobism rate (mean±S.D.) | ||
| 雌虫Female | 雄虫Male | 雌虫Female | 雄虫Male | |
| 340 | 45.83±3.76a | 33.75±2.50a | 6.67±2.58d | 5.00±4.08b |
| 360 | 45.83±7.36a | 35.00±4.08a | 5.83±3.76d | 7.50±2.89ab |
| 380 | 47.50±2.74a | 30.00±4.08ab | 7.50±2.74d | 3.75±2.50b |
| 400 | 28.33±4.08de | 12.50±2.89ef | 19.17±3.76a | 7.50±2.89ab |
| 420 | 30.00±3.16cd | 13.75±2.50ef | 5.83±3.76d | 6.25±4.79ab |
| 440 | 22.50±2.74ef | 13.75±4.79ef | 7.50±4.18d | 5.00±4.08b |
| 460 | 30.83±12.42cd | 13.75±2.50ef | 13.33±4.08bc | 6.25±2.50ab |
| 483 | 25.83±3.76def | 17.50±5.00de | 10.00±3.16cd | 11.25±2.50a |
| 498 | 21.67±5.16ef | 20.00±4.08d | 6.67±2.58d | 6.25±2.50ab |
| 524 | 41.67±2.58ab | 22.50±2.89cd | 15.00±4.47ab | 7.50±2.89ab |
| 538 | 20.00±7.07f | 13.75±2.50ef | 10.83±3.76bcd | 6.25±2.50ab |
| 562 | 24.17±3.76def | 11.25±2.50f | 7.50±5.24d | 3.75±2.50b |
| 583 | 38.33±6.83b | 21.25±4.79d | 13.33±4.08bc | 5.00±4.09b |
| 605 | 35.83±7.36bc | 27.50±2.8bc | 18.33±4.08a | 6.25±2.50ab |
| 不同字母表示同列数据的检验结果显著(P<0.05) | ||||
从表 2和图 2能够看出,雌雄之间趋、避光行为反应总趋势相似,即对紫外、蓝绿光和橙红光相对敏感,但雌虫的趋、避光行为反应率值远大于雄虫。
在趋光行为反应中,经方差分析发现,除605 nm单色光外,其它单色光下,东亚小花蝽雌成虫的趋光行为反应率要显著高于雄成虫。表明性别对东亚小花蝽成虫趋光行为反应有显著影响,雌虫趋光行为反应要显著高于雄虫。
在避光行为反应中,除个别单色光,其它单色光下,东亚小花蝽成虫的避光行为反应之间无显著差异。表明性别对东亚小花蝽成虫避光行为反应有一定影响,但影响较小。
结果表明:东亚小花蝽成虫趋光行为反应在性别之间有显著差异,雌虫的光谱敏感性远强于雄虫。避光行为反应在性别之间有一定差异,但差异较小。
| 单色光/nm light | 趋光反应率(均值±标准差)/%
Phototactic rate (mean±S.D.) |
Photophobism rate (mean±S.D.)
df | F | P |
避光反应率(均值±标准差)/%
Monochromatic | df | F | P | |||
| 雌虫 Female | 雄虫
Male | 雌虫
Female | 雄虫
Male | ||||||||
| 340 | 45.83±3.76a | 33.75±2.50b | 1 | 31.2930 | 0.0005 | 6.67±2.58a | 5.00±4.08a | 1 | 0.6400 | 0.4468 | |
| 360 | 45.83±7.36a | 35.00±4.08b | 1 | 7.0230 | 0.0292 | 5.83±3.76a | 7.50±2.89a | 1 | 0.5570 | 0.4470 | |
| 380 | 47.50±2.74a | 30.00±4.08b | 1 | 67.2000 | 0.0001 | 7.50±2.74a | 3.75±2.50a | 1 | 4.8000 | 0.0598 | |
| 400 | 28.33±4.08a | 12.50±2.89b | 1 | 44.4310 | 0.0002 | 19.17±3.76a | 7.50±2.89b | 1 | 27.2700 | 0.0008 | |
| 420 | 30.00±3.16a | 13.75±2.50b | 1 | 73.7450 | 0.0001 | 5.83±3.76a | 6.25±4.79a | 1 | 0.0240 | 0.8810 | |
| 440 | 22.50±2.74a | 13.75±4.79b | 1 | 13.8350 | 0.0059 | 7.50±4.18a | 5.00±4.08a | 1 | 0.8730 | 0.3775 | |
| 460 | 30.83±12.42a | 13.75±2.50b | 1 | 7.0970 | 0.0286 | 13.33±4.08a | 6.25±2.50b | 1 | 9.4370 | 0.0153 | |
| 483 | 25.83±3.76a | 17.50±5.00b | 1 | 9.1430 | 0.0165 | 10.00±3.16a | 11.25±2.50a | 1 | 0.4360 | 0.5274 | |
| 498 | 21.67±5.16a | 20.00±4.08b | 1 | 0.2910 | 0.6043 | 6.67±2.58a | 6.25±2.50a | 1 | 0.0640 | 0.8067 | |
| 524 | 41.67±2.58a | 22.50±2.89b | 1 | 120.9140 | 0.0001 | 15.00±4.47a | 7.50±2.89b | 1 | 8.6400 | 0.0187 | |
| 538 | 20.00±7.07a | 13.75±2.50b | 1 | 2.7910 | 0.1334 | 10.83±3.76a | 6.25±2.50a | 1 | 4.5020 | 0.0666 | |
| 562 | 24.17±3.76a | 11.25±2.50b | 1 | 35.7580 | 0.0003 | 7.50±5.24a | 3.75±2.50a | 1 | 1.7280 | 0.2251 | |
| 582 | 38.33±6.83a | 21.25±4.79b | 1 | 18.5490 | 0.0026 | 13.33±4.08a | 5.00±4.09b | 1 | 10.0000 | 0.0133 | |
| 605 | 35.83±7.36a | 27.50±2.8b | 1 | 4.5070 | 0.0665 | 18.33±4.08a | 6.25±2.50b | 1 | 27.4610 | 0.0008 | |
| 不同字母表示同行数据的检验结果显著(P≤0.05) | |||||||||||
光谱是影响昆虫活动行为的重要因素,目前针对昆虫光谱行为实验多集中于鳞翅目等害虫以及蜜蜂、蚂蚁、飞蝗和迁徙性蝴蝶等能够在飞行或运动过程中利用复眼定位的昆虫,对于能够有效控制田间害虫的天敌昆虫研究相对较少,在国内只有草蛉、瓢虫等报道[11, 12, 13, 14],这对于目前我国绿色植保中提倡的利用灯光、色板等物理方法防治害虫过程中出现误伤天敌昆虫问题的解决缺少相关理论依据。
在本研究中发现,东亚小花蝽成虫具有非常强的趋光性,尤其是雌虫,在所有光谱下其趋光率都达到了20%以上,在其敏感光谱下接近50%;虽然雄性成虫的趋光率相对较低,但在其敏感光谱下也能接近40%。而陈晓霞对与之生境、猎物均相似的龟纹瓢虫进行研究时发现,龟纹瓢虫趋光率只有20%左右,远小于东亚小花蝽[13];东亚小花蝽的猎物之一西花蓟马的趋光反应率也只有20%左右[16]。这些都表明东亚小花蝽对光更为敏感。其原因可能与体型、主要捕食对象有关,龟纹瓢虫体型要较东亚小花蝽大,主要捕食寄主表面危害的蚜虫等,而东亚小花蝽体型相对较小,捕食的猎物为喜欢隐藏危害的蓟马或低龄期的蚜虫等更小的昆虫,这就更加需要相对较强的视觉敏感性,来对猎物进行搜索、定位。
东亚小花蝽的敏感波长有3个区域,依大小为紫外区(340m、360 nm和380 nm),绿光区(524 nm),在橙红光区(583、605 nm),与龟纹瓢虫(340、524、483 nm和400—440 nm)相比可以看出,在紫外和绿光区,两者都有较高趋性,但是在紫外区,东亚小花蝽的敏感光谱更广;而龟纹瓢虫对橙红光区不敏感[13],但对蓝色光相对敏感,东亚小花蝽则反之。在体型较大的瓢虫中,七星瓢虫对365、500 nm敏感,异色瓢虫成虫能够对黄色和绿色食物进行辨别[11, 12, 13]。从以上结果整体上来看,东亚小花蝽具有较宽敏感的光谱,也就是说其能够区别更多的植物相,而龟纹瓢虫和其它瓢虫对蓝绿光敏感,两类昆虫之间的所产生的区别原因,主要是由不同种昆虫之间各种生理、生态等差异长时间选择进化所造成的。
与西花蓟马相比,两种昆虫都对524、380 nm单色光敏感,其中的524 nm对应颜色为蓝色光,通过光谱实验和田间色板诱集都证明西花蓟马对其敏感,而东亚小花蝽也对此敏感;在田间诱集中发现,西花蓟马对黄色有相对较高的趋性,东亚小花蝽的光谱行为中同样发现其对橙红光较敏感[16],以上相同点说明东亚小花蝽有可能是作为捕食者在长期寻找猎物的过程中复眼相应的进化而来。因此,在研制防治西花蓟马的光源或光活性物质如色板等相关产品的时候,应考虑选择对小花蝽等天敌的伤害,也可根据西花蓟马活动能力相对较弱而小花蝽等活动能力相对较强的习性,开发引诱小花蝽的光活性物质,吸引周围小花蝽定向迁移活动。
性别对昆虫的趋光行为有一定影响[15]。Agee报道,七星瓢虫在相同敏感光谱下,雌虫要较雄虫更敏感但差异不显著[11],在龟纹瓢虫中,雌虫对紫外和近紫外短波略敏感,雄虫对长波略敏感,但差异不显著[13]。上述报道都说明性别对趋光行为有一定影响。本文发现东亚小花蝽雌、雄成虫虽然敏感光谱在性别之间表现的相一致,但趋光反应率相差非常大。引起这种情况的原因可能是和其本身职能差异不同而导致的。从职能上,雄虫主要是寻找雌虫,并且在交尾后就完成了其使命,而雌虫交配后还要寻找含有猎物更多的、适宜的植株来进行产卵,繁育下一代,并且在冬天,雌虫还要寻找越冬场所,其复眼对光谱的敏感程度可能是这些分工差异经过长期演化而形成的。
在避光行为反应中,并没有在某个单色光下出现较高反应率,而西花蓟马在某些单色光下(440 nm)的避光反应率显著高于其它波长的单色波长[16],产生这种现象的原因有待深入研究。
| [1] | 王义平, 吴鸿, 卜文俊, 徐华潮. 小花蝽属地理分布的研究(半翅目: 花蝽科). 浙江林学院学报, 2003, 20(4): 389-393. |
| [2] | 蒋月丽, 武予清, 段云, 高新国. 释放东亚小花蝽对大棚辣椒上几种害虫的防治效果. 中国生物防治学报, 2011, 27(3): 414-417. |
| [3] | Yasunaga T. The flower bug genus Orius Wolff ( Heteroptera: Anthocoridae) from Japan and Taiwan, part II. Applied Entomology and Zoology, 1997, 32(2): 379-386. |
| [4] | Fransen J J, Boogaard M, Tolsma J. The minute pirate bug, Orius insidiosus(Say)(Hemiptera: Anthocoridae), as a predator of western flower thrips, Frankliniella occidentalis(Pergande), in chrysanthemum, rose and Saintpaulia. Bulletin OILB SROP, 1993, 16(8): 73-77. |
| [5] | Van der Meiracker R A F, Ramakers P M J. Biological control of the western flower thrips Frankliniella occidentalis, in sweet pepper, with the anthocorid predator Orius insidiosus. Mededelingen Van de Faculteit Landbouwwetenschappen Rijksuniversiteit Gent., 1991, 56(2a): 241-249. |
| [6] | Gilkeson L A, Morewood W D, Elliot D E. Current status of biological control of thrips in Canadian greenhouses with Amblyseius cucumeris and Orius tristicolor. IOBC/WPRS Bull, 1990, 13: 71-75. |
| [7] | Tellier A J, Steiner M Y. Control of the western flower thrips, Frankliniella occidentalis(Pergande), with a native predator Orius tristicolor (White) in greenhouse cucumbers and peppers in Alberta, Canada. IOBC/WPRS Bull., 1990, 13(5): 209-211. |
| [8] | Chambers R J, Long S, Helyer B L. Effectiveness of Orius laevigatus (Hem: Anthocoridae) for the control of Frankliniella occidentalis on cucumber and pepper in the United Kingdom. Biological Science Technology, 1993, 3(3): 295-307. |
| [9] | 张安盛, 于毅, 李丽莉, 张思聪. 东亚小花蝽(Orius sauteri)成虫对入侵害虫西花蓟马( Frankliniella occidentalis)成虫的捕食. 生态学报, 2007, 27(5): 1903-1909. |
| [10] | 蒋兴川, 桂富荣, 陈斌, 李志华, 穆静娟, 李正跃. 南方小花蝽在不同试验空间对西花蓟马的捕食及搜寻效应. 生物安全学报, 2012, 21(1): 20-26. |
| [11] | Agee H R, Mitchell E R, Flanders R V. Spectral sensitivity of the compound eye of Coccinella septempunctata (Coleoptera: Coccinellidae). Annals of the Entomological Society of America, 1990, 83(4): 817-819. |
| [12] | Edward B. M, Jessie L W. Unconditioned and conditioned responses to color in the predatory coccinellid, Harmonia axyridis (Coleoptera: Coccinellidae). European Journal of Entomology, 2000, 97(4): 463-467. |
| [13] | 魏国树, 张青文, 周明牂, 吴卫国. 不同光波及光强度下棉铃虫(Helicoverpa armigera)成虫的行为反应. 生物物理学报, 2000, 16(1): 8-995. |
| [14] | 张海强, 闫海霞, 刘顺, 张乃瑾, 魏国树. 光强度对大草蛉成虫感光性和趋光性行为的影响. 昆虫学报, 2009, 52(4): 461-464. |
| [15] | 程文杰, 郑霞林, 王攀, 雷朝亮, 王小平. 昆虫趋光的性别差异及其影响因素. 应用生态学报, 2011, 22(12): 3351-3357. |
| [16] | 范凡, 任红敏, 吕利华, 张莉萍, 魏国树. 光谱和光强度对西花蓟马雌虫趋光行为的影响. 生态学报, 2012, 32(6): 1790-1795. |
 2015, Vol. 35
2015, Vol. 35




