文章信息
- 王林, 代永欣, 樊兴路, 张芸香, 黄平, 万贤崇
- WANG Lin, DAI Yongxin, FAN Xinglu, ZHANG Yunxiang, HUANG Ping, WAN Xianchong
- 风对黄花蒿水力学性状和生长的影响
- Effects of wind on hydraulic properties and growth of Artemisia annua Linn
- 生态学报, 2015, 35(13): 4454-4461
- Acta Ecologica Sinica, 2015, 35(13): 4454-4461
- http://dx.doi.org/10.5846/stxb201410071963
-
文章历史
- 收稿日期:2014-10-07
- 修订日期:2015-03-26
2. 中国林业科学研究院林业新技术所, 北京 100091
2. Chinese Academy of Forestry, Institute of New Forestry Technology, Beijing 100091, China
风是重要的环境因子之一,可以影响到陆生植物的生长发育,尽管人们对风的研究已经有很长的历史,但是对风是如何影响植物生长发育,以及植物的响应机制认识不足[1, 2]。这主要是因为风对植物的影响是多方面的,不仅影响到植物的生长、生物量分配和力学特征,还会影响到植物的水力学性状和光合作用。然而,关于风对植物综合影响的系统研究尚不多见,该类研究有助于深入了解植物应对风胁迫的响应机制。
已有研究表明:风吹可以改变了植物的受力状况,增加茎干基部受力[3, 4],风吹会促进植物茎干增粗生长,以增加茎干的支持强度[5, 6];风吹也会影响到植物的生物量分配模式[3, 6],主要是增加根系和茎干基部的生物量[7, 8];风吹会影响植物的水分状况,一方面是风吹加速植物的蒸腾作用,促进水分消耗,另一方面是风可以引起植物枝叶的摆动,干扰茎干水分输导[9, 10],甚至会因水分原因导致顶端坏死,抑制树木增高生长[10, 11];风吹还会影响到叶片的气体交换[1, 12]。关于风对植物气体交换的影响,目前的研究还存在一些争议。有研究表明风吹引起空气流动加速,可以促进叶片气孔的气体交换,有利于植物的碳摄取[12],也有研究表明风会抑制植物的光合作用[13]。植物的茎一方面是支持植物保持固定姿态的器官,同时也是水分输导的通道,在机械刺激条件下,植物茎干的力学性状发生变化,刺激茎增粗生长,茎干支持组织的比例增高[14],但目前对在风胁迫下植物茎干水分输导与力学特性之间是否存在权衡研究较少,且存在不同的观点[4, 15]。对风干扰条件下植物的异速生长,水分输导和力学特性之间的关系,以及风吹对水分利用对碳摄取的影响进行综合研究有助于全面认识风对植物造成的影响,有助于制定应对措施,提高植物应对风干扰的管理。
上述可见,风对植物的影响相当复杂,不同的植物对风吹具有明显的差别响应[16]。先前我们用木本植物的苗木进行了研究,发现风抑制了这两种植物的高生长,但风对栓皮栎、侧柏这两个树种苗期形态建成的影响比较小,可能是低速风对木质化程度较高的木本植物的机械作用较小[16]。所以本研究以一年生草本植物黄花蒿(Artemisia annua Linn.)作为试验材料,进一步探索风对植物的综合影响。黄花蒿属菊科蒿属,广泛分布在世界各地,是一种中国传统中草药,也是重要的生态物种。另外,黄花蒿是一年生速生草本植物,在短期内其生物量、茎干高生长等会有较大的改变,因此可以在较短时间的处理中显现出明显的效果。本研究拟通过对导水率、栓塞和水势的分析来研究风吹对植物水力学性状的影响,分析水分平衡对气体交换的作用来研究风对植物碳摄取和生长的影响;通过对根、茎、叶生物量,根冠比、尖削度的比较来揭示风对植物生物量分配的影响;通过对植物茎干导管结构、茎导水率等水力学性状和茎干弹性模量(MOE)、抗弯刚度(EI)等力学性状的比较,研究风吹条件下植物茎干水力学结构和力学性状之间的权衡关系。本文提出假说是:(1)风吹影响了植物的水力学结构和功能,导致叶片水分匮缺,限制了叶片的光合作用,进而影响了植株的生物量。(2)风吹改变了植物的生物量分配模式,更多的碳用于维持植物的力学稳定性;同时牺牲了部分水分输导功能。
1 材料与方法本研究在山西省太谷县山西农业大学林学院试验基地进行,选择野生自然萌发的黄花蒿(萌芽时间为2014年4月中旬),选择生长状况一致的植株作为研究对象,通过人工间苗保留一定密度生长基本一致的植株,株行距约为30×30 cm,处理和对照分别为16—20株,处理和对照实验植株距离10 m左右,保持土壤相对含水量在60%—80%。于6月初开始用工业风扇进行风吹处理,处理开始时株高为(40±5.5)cm,地径为(3±0.45)mm,处理和对照之间无显著差异。吹风处理:在白天(10:00—18:00)进行,间隔15min吹风15min,每天吹风总共为4h,植物处风速为(5±0.35) m/s。每4—5株用1台工业风扇。对植物处风速检测表明不同植株处风速基本一致。这个风速对于草本植物来说是较强的风速[17],该风速能导致植物大弧度弯曲,因为研究期望发现风导致的植物机械摇晃和植物水分关系的变化对植物的影响。处理至2014年7月底结束,处理时间为60d。
1.1 生长量在处理之前和处理结束后用直尺、游标卡尺测量株高(H)、基径(离地面5mm处)(DBH)、3/4株高的茎干直径(D0.75H),并计算出尖削度(Tap=(DBH-D0.75H)/H)[16],在实验结束时仔细分离出植株的根、茎和叶片,烘干后进行称重。
1.2 水势、最大导水率和导水损失率在风吹处理1个月后(2014年7月初)进行凌晨水势、正午水势、正午气穴栓塞和最大导水率测定。水力学指标测定选择连续晴天进行,水势用PMS1505D-EXP便携式水势仪测定(PMS Albany USA),凌晨水势测定时间为5:30—6:00,正午水势测定时间为12:00—12:30。最大导水率(Kmax)和导水损失率(Percent loss in conductivity PLC)的采样时间同正午水势,测定具体步骤参照靳欣等[18]的方法。简要如下:在植株上剪取长40cm以上茎干枝条,浸没在水中截取3cm长度枝条用于PLC测定,通过茎段溶液为经过0.44 μm微孔过滤的0.025 mmol/L KCl溶液,先用5 kPa的压力推动溶液通过茎段,测定茎段初始导水率,流出液用万分之一天平定时称重,并记录在相连的电脑中,将测定茎段的直径和长度值输入LPFM软件,用LPFM软件计算初始导水率(Ki),然后用0.175 MPa压力冲洗茎段5min,冲去茎段所有气泡(预实验在0.175 MPa压力下5min可以冲掉所有栓塞),再用5 kPa的压力测定导水率,此时的导水率定义为最大导水率(Kmax),导水损失率计算公式为:
PLC (%)=(1-Ki/Kmax) ×100
1.3 气体交换指标气体交换指标(包括光合作用、气孔导度) 在吹风处理1个月后(7月初)进行,选择晴天9:00—11:00进行测定,采用Li-6400光合测定系统红蓝光源叶室(Li-Cor,Lincoln,USA)测定叶片瞬时光合速率。测量时使用大气CO2 浓度(380 mmol/mol),光合有效辐射强度设定为1500 mol m-2 s-1,所测光合速率为最大光合速率[19],本研究的预实验表明:黄花蒿的光饱和点低于1500 mol m-2 s-1。由于黄花蒿叶片不能布满整个红蓝光源叶室,气体交换测量完毕后,将叶室内的叶片剪下,利用叶面积仪精确测定叶室内的叶片面积,并将所得叶面积值输入光合仪计算其光合速率和气孔导度[16]。
1.4 茎解剖结构测定茎干结构测定在吹风处理1个月后(7月初)进行,截取1 cm左右长度茎干放入盛有FAA (70%乙醇 ∶ 福尔马林 ∶ 冰醋酸= 90 mL ∶ 5 mL ∶ 5 mL)固定液中,用于木质部导管解剖观测。将固定材料经蒸馏水冲洗后,在解剖镜下观察,用目镜测微尺测量导管直径,通过计算单位面积导管数目求得导管密度。
1.5 力学性状测定弹性模量、弹性系数测定在实验结束后进行,采用3点法用INSTRON 5544材料性能试验机(Instron,Norwood,MA)测定,具体测定方法参照Poncsák[20],计算公式为:
弯曲刚度
截面惯性矩
弹性模量
式中,P和y1分别为加载力和样品在力的方向上的位移,L是两固定点之间的距离,Rmajor茎干较粗端的半径减去髓心半径,Rminor为较细端半径减去髓心半径。
1.6 数据分析用Excel软件进行方差分析,以P< 0.05作为显著性的标准。用SigmaPlot 10.0软件进行绘图。所有的测定都有5次以上的重复,导管直径数据重复数为50—100次。
2 结果与分析 2.1 生长指标吹风显著抑制了黄花蒿的高生长(P<0.05,图 1),在处理结束时,吹风处理的株高仅为对照的68%。同时,吹风显著促进了茎干的增粗生长(P<0.05),吹风植物的地茎为(9.24±2.17)cm,而对照的地径为(7.67±0.57)cm。吹风也显著增加了茎干的尖削度(P<0.05),吹风处理的茎干尖削度约为对照植物的2倍(图 1)。

|
| 图 1 风吹条件下黄花蒿的株高、地径和尖削度变化(平均值±标准差) Fig.1 Height,basal diameter,and taping(means±SD) of Artemisia annua under different treatments 不同字母代表P<0.05下显著差异 |
吹风显著降低了黄花蒿的总生物量(P<0.05,图 2),风吹处理显著降低了茎、叶生物量 (P<0.05),吹风处理的茎和叶生物量分别为对照的69.3%和65.9%,但风吹处理对根生物量没有影响(P=0.65)。风吹显著增加了黄花蒿的根冠比(P<0.05,图 2)。

|
| 图 2 黄花蒿生物量分配(平均值±标准差) Fig.2 Biomass allocation(means±SD) of Artemisia annua under different treatments |
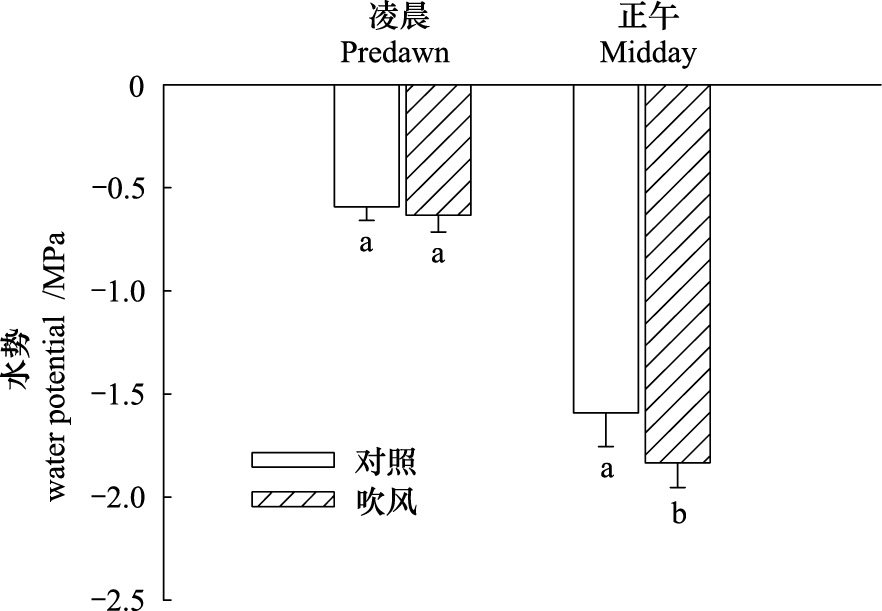
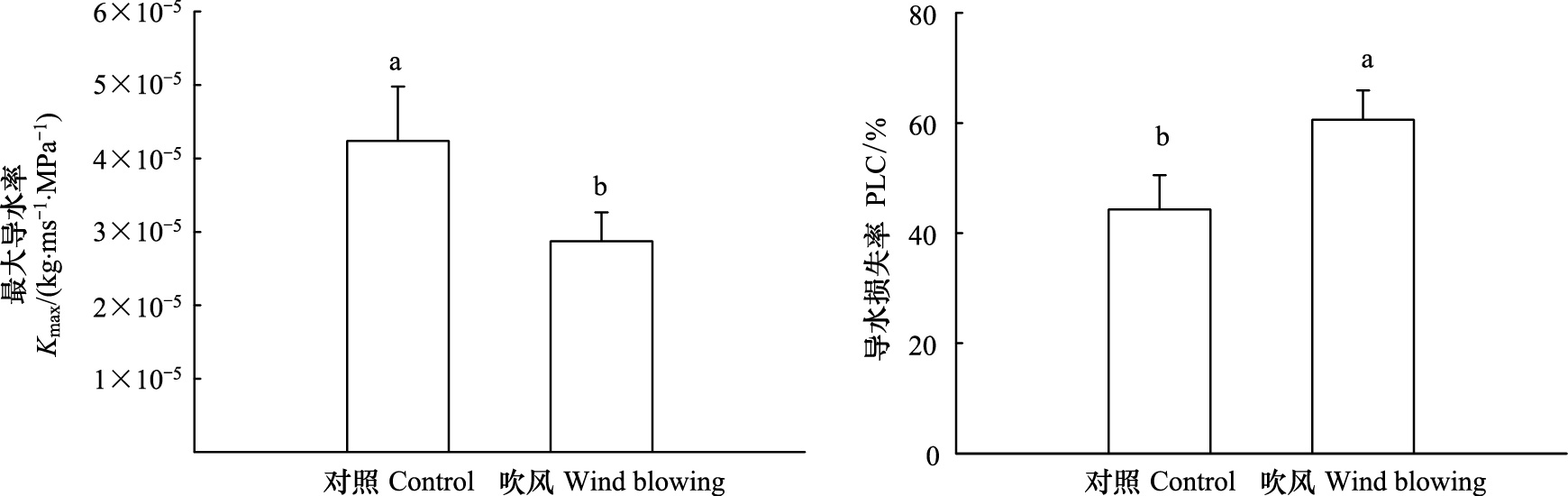
吹风处理和对照的凌晨水势没有显著差异(P=0.59),但吹风显著降低了黄花蒿的正午水势(P<0.05,图 3),风吹显著降低了茎的最大导水率(Kmax)(P<0.05)。茎干正午PLC测定结果显示:风吹显著增加了茎干的正午PLC(P<0.05,图 4),风吹植物的平均正午PLC比对照组高16%。
|
| 图 3 风吹条件下黄花蒿小枝凌晨和正午水势的变化(平均值±标准差) Fig.3 Predawn and midday twig water potential(means±SD) of Artemisia annua twigs under different treatments |
|
| 图 4 风吹处理下黄花蒿最大导水率和正午导水损失率的变化(平均值±标准差) Fig.4 The Kmax and midday PLC(means±SD) of Artemisia annua under different treatments |
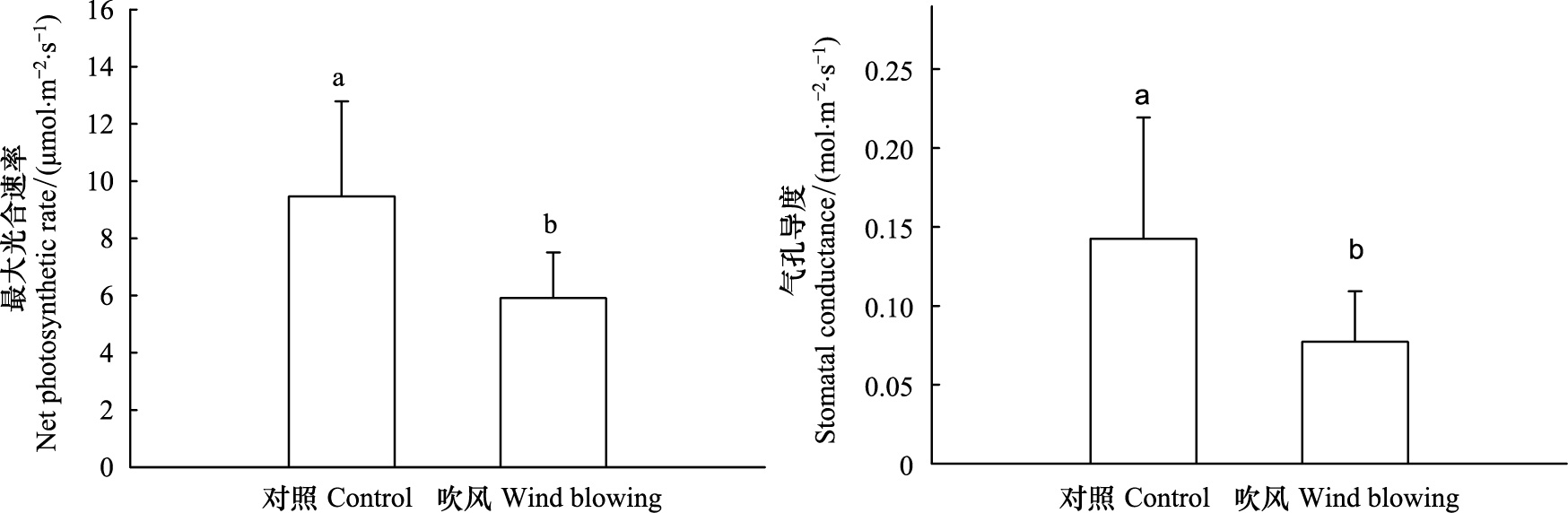
在吹风处理30d后,对照的最大光合速率为(9.47±3.32) μmol m-2 s-1,风吹处理最大光合速率为(5.91±1.6) μmol m-2 s-1。风吹显著降低了黄花蒿的叶片最大光合速率(P<0.05),吹风处理植物的最大光合速率为对照的62%。同时吹风处理植物的气孔导度显著低于对照(P<0.05,图 5),吹风处理植物的气孔导度仅仅相当于对照的55%。
|
| 图 5 风吹处理下黄花蒿最大光合速率和气孔导度的变化(平均值±标准差) Fig.5 Maximum net photosynthetic rate and stomatal conductance (means±SD) of Artemisia annua under different treatments |
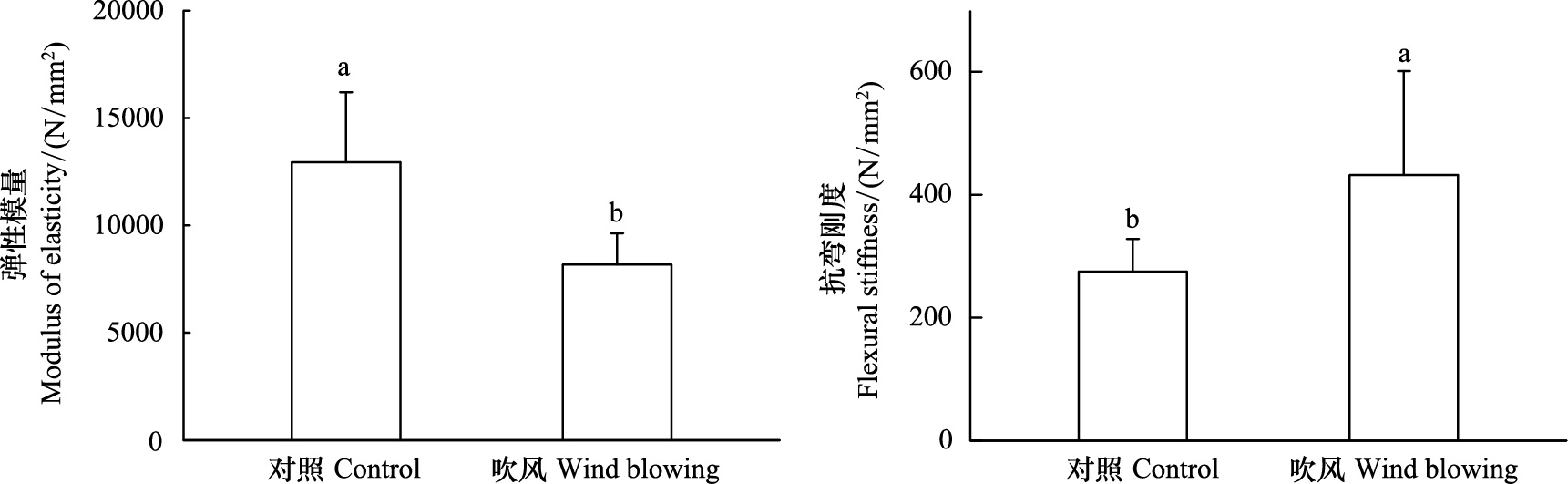
在处理结束时,对照植物的茎干弹性模量(MOE)为(12948±3253) N/mm2,风吹黄花蒿的为(8177±1463) N/mm2。吹风显著降低了茎干的弹性模量(MOE)(P<0.05),对照植物的茎干抗弯刚度(EI)为(275±53) N/mm2,风吹处理为(432±169) N/mm2风吹处理显著增加了茎干的抗弯刚度(EI)(P<0.05,图 6)。
|
| 图 6 风吹处理下黄花蒿茎干弹性模量和抗弯强度的变化(平均值±标准差) Fig.6 The MOE and EI (means±SD) of Artemisia annua stems under different treatments |
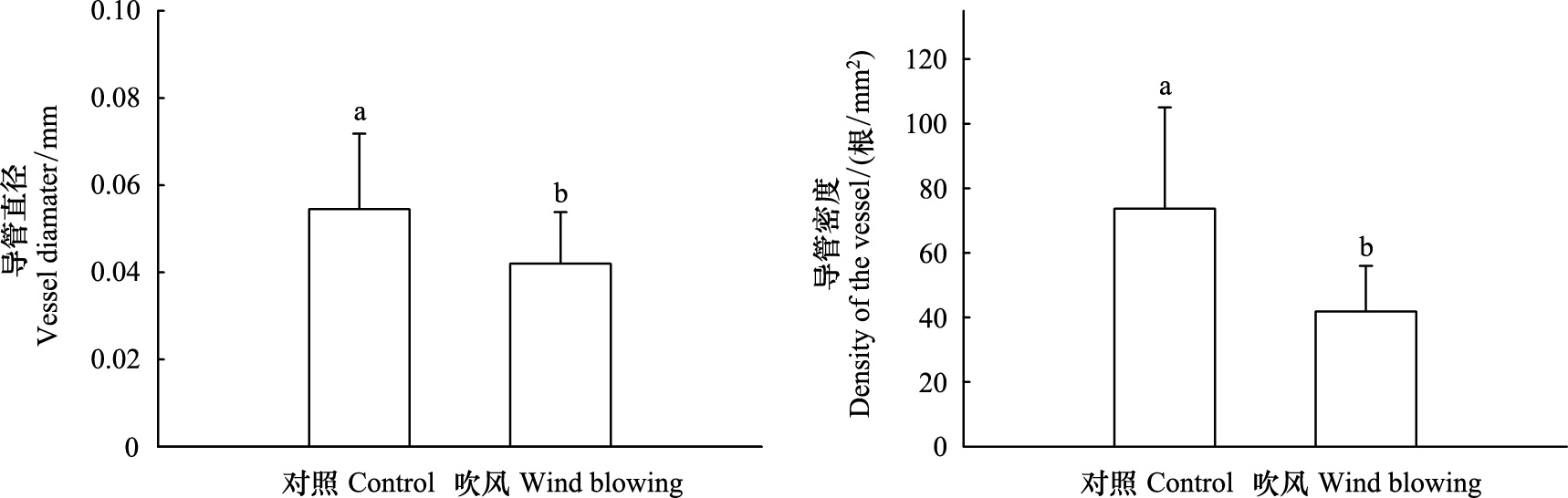
吹风显著降低了茎干的平均导管直径(P<0.05),同时也显著降低了茎干导管密度(P<0.05),风吹处理的导管直径和导管密度分别为对照的77%和55%。
|
| 图 7 茎干导管直径和导管密度(平均值±标准差) Fig.7 The stem vessel diameter and density (means±SD) of Artemisia annua under different treatments |
风吹增加了空气流动速率,会增加植物的蒸散需求[11, 12, 21],导致木质部水势降低,木质部汁液张力增加,在本研究中风吹处理植物正午水势显著低于对照,其佐证了风对植物水分代谢的影响。高的木质部汁液张力是导致茎干PLC增高的一个重要原因[22],本试验的结果显示风吹植物正午的PLC显著高于对照,表明风吹导致木质部输水能力损失更大。此外,风吹还导致茎干最大导水率(Kmax)的显著下降,说明木质部输导系统结构发生了改变,得到本文研究中茎干解剖结果证实。最大导水率下降和中午PLC的上升都说明风吹显著降低了黄花蒿长距离水分运输能力[14, 22],其结果会导致叶片供水不足,不能有效补充叶片的蒸腾失水,失去水分平衡。致使气孔导度减小,从而限制植物的光合作用,在本研究中,水分状况变差导致的气孔导度减小可能是限制光合作用的主要因素。同时风吹减小了叶片生物量,风吹植物叶生物量比对照减小32%,这意味着有更小的光合面积,也造成了碳摄取的限制,使得风吹植物总生物量降低。光合速率和光合面积的下降导致光合能力下降可能是导致风吹植物的总生物量减少的主要原因。由于风吹对植物的影响比较复杂,既有促进的因素又有抑制的因素[23],取决于风速的大小和植物种类[16]。对于草本植物黄花蒿,在本研究的风速条件下,主要引起植物过度失水,进而导致光合作用下降,生长减慢。
从生物量分配比例看,风吹条件下植物的叶片生物量比例显著降低,叶片生物量比例减小意味着相对蒸腾面积的减小,蒸腾面积的减小有利于植物水力学结构的维持,在一定程度上降低了植物水分胁迫的程度[24]。另外,夜间由于没有进行吹风处理,两个处理间在凌晨水势上没有差异,这表明白天吹风处理并没有影响到夜间植物水势的恢复。
3.2 风吹条件下黄花蒿茎干力学稳定性和水力学结构的关系风吹会使植物的生物量分配模式向着有利于维持植物力学稳定性的方向改变[4]。在本研究中风吹增加了地下部分生物量分配比例,减少了地上部分的生物量分配,包括叶的生物量分配下降显著,更小的叶面积有利于减小风的载荷[2]。同时茎干高度减小、基部增粗生长加快,茎干的尖削度增加,这些都有利于维持植物的力学稳定性[16]。风吹植物在力学结构上表现出了更多的稳定性,除了增加增粗生长之外,风吹处理的抗弯刚度(EI)显著增大,这表明茎干的抵抗外力能力增大,能够抵御更多的外力条件下保持固有姿态。虽然茎干的弹性模量(MOE)减小,EI是MOE和截面惯性矩(I)的乘积,而截面惯性矩(I)与半径的四次方成正比,因此增加半径生长会导致弹性模量在比例上减小[4],吹风虽然导致MOE减小,但在整个茎干水平上硬度增加[3, 4],这有利于直立植物在外力条件下维持固有姿态。植物茎干除了维持植物的直立姿态之外的另外一个重要功能是水分输导,对风吹植物茎干截面结构的研究表明:风吹减小了茎干导管直径和导管密度,导管直径和导管密度的同时减小意味着植物茎秆支持组织的比例更高,风吹植物茎干最大导水率的下降也证明了风胁迫下植物茎的可塑性改变影响了茎的水分输导能力,这更有利于植物维持力学性状,但牺牲了部分水分输导能力[14]。这是植物对风吹环境适应性的一种表现。
4 结论本文通过对一年生草本植物黄花蒿进行人工吹风处理,发现吹风降低了植物的正午水势,引起木质部气穴栓塞加剧,降低了植物的光合作用和气孔导度,抑制了植物的生物量积累。风吹影响了植物的生物量分配,有更多的光合产物分配到地下部分和茎干基部,减少了地上部分的生物量分配。同时,风吹处理促进了茎干的增粗生长,增加了植物机械支持能力,但是降低了茎干导管的水分输导能力,这是植物在风胁迫条件下力学稳定性和水分输导能力之间的一种权衡。这种改变有利于在有风条件下维持植物的力学稳定性,但同时降低了水分输导能力。
致谢: 感谢山西农业大学林学院高勇富、王晓玮、刘秋莲同学对试验的帮助。
| [1] | Onoda Y, Anten N P R. Challenges to understand plant responses to wind. Plant Signaling & Behavior, 2011, 6(7): 1057-1059. |
| [2] | Telewski F W. Is windswept tree growth negative thigmotropism?. Plant Science, 2012, 184: 20-28. |
| [3] | Pruyn M L, Ewers B J, Telewski F W. Thigmomorphogenesis: changes in the morphology and mechanical properties of two Populus hybrids in response to mechanical perturbation. Tree Physiology, 2000, 20(8): 535-540. |
| [4] | Kern K A, Ewers F W, Telewski F W, Koehler L. Mechanical perturbation affects conductivity, mechanical properties and aboveground biomass of hybrid poplars. Tree Physiology, 2005, 25(10): 1243-1251. |
| [5] | Niklas K J. Effects of vibration on mechanical properties and biomass allocation pattern of Capsella bursa-pastoris (Cruciferae). Annals of Botany, 1998, 82(2): 147-156. |
| [6] | Cordero R A. Ecophysiology of Cecropia schreberiana saplings in two wind regimes in an elfin cloud forest: growth, gas exchange, architecture and stem biomechanics. Tree Physiology, 1999, 19(3): 153-163. |
| [7] | Telewski FW. Wind-induced physiological and developmental responses in trees//Coutts M P, Grace J, eds. Wind and Trees. Cambridge: Cambridge University Press, 1995: 237-263. |
| [8] | Telewski F W, Pruyn M L. Thigmomorphogenesis: a dose response to flexing in Ulmus americana seedlings. Tree Physiology, 1998, 18(1): 65-68. |
| [9] | Tyree M T, Sperry J S. Vulnerability of xylem to cavitation and embolism. Annual Review of Plant Physiology and Plant Molecular Biology, 1989, 40(1): 19-38. |
| [10] | Ryan M G, Yoder B J. Hydraulic limits to tree height and tree growth. Bioscience, 1997, 47(4): 235-242. |
| [11] | Bladon K D, Silins U, Landhäusser S M, Messier C, Lieffers V J. Carbon isotope discrimination and water stress in trembling aspen following variable retention harvesting. Tree Physiology, 2007, 27(7): 1065-1071. |
| [12] | 赵哈林, 何玉惠, 岳广阳, 周瑞莲. 风吹、沙埋对沙地植物幼苗生长和光合蒸腾特性的影响. 生态学杂志, 2010, 29(3): 413-419. |
| [13] | 于云江, 史培军, 鲁春霞, 刘家琼. 不同风沙条件对几种植物生态生理特征的影响. 植物生态学报, 2003, 27(1): 53-58. |
| [14] | Christensen-Dalsgaard K K, Fournier M, Ennos A R, Barfod A S. Changes in vessel anatomy in response to mechanical loading in six species of tropical trees. New Phytologist, 2007, 176(3): 610-622. |
| [15] | Awad H, Herbette S, Brunel N, Tixier A, Pilate G, Cochard H, Badel E. No trade-off between hydraulic and mechanical properties in several transgenic poplars modified for lignins metabolism. Environmental and Experimental Botany, 2012, 77: 185-195. |
| [16] | 徐湘婷, 王林, 黄平, 万宇轩, 李建中, 万贤崇. 风和光照对侧柏、栓皮栎生长和形态建成的影响. 林业科学, 2014, 50(7): 164-168. |
| [17] | Bossdorf O, Pigliucci M. Plasticity to wind is modular and genetically variable in Arabidopsis thaliana. Evolutionary Ecology, 2009, 23(5): 669-685. |
| [18] | 靳欣, 徐洁, 白坤栋, 冯锦霞, 张劲松, 万贤崇. 从水力结构比较3种共存木本植物的抗旱策略. 北京林业大学学报, 2012, 33(6): 135-141. |
| [19] | 王林, 冯锦霞, 万贤崇. 土层厚度对刺槐旱季水分状况和生长的影响. 植物生态学报, 2013, 37(3): 248-255. |
| [20] | Poncsák S, Kocaefe D, Bouazara M, Pichette A. Effect of high temperature treatment on the mechanical properties of birch (Betula papyrifera). Wood Science and Technology, 2006, 40(8): 647-663. |
| [21] | Ennos A R. Wind as an ecological factor. Trends in Ecology and Evolution, 1997, 12(3): 108-111. |
| [22] | Tyree M T, Zimmermann M H. Xylem Structure and the Ascent of Sap. 2nd ed. Berlin, Heidelberg: Springer Verlag, 2002. |
| [23] | Kozlowski T T, Kramer P J, Pallardy J G. The Physiological Ecology of Woody Plants. San Diego: Academic Press, 1991. |
| [24] | Jacquet J S, Bosc A, O'Grady A, Jactel H. Combined effects of defoliation and water stress on pine growth and non-structural carbohydrates. Tree Physiology, 2014, 34(4): 367-376. |
 2015, Vol. 35
2015, Vol. 35







