文章信息
- 史建伟, 秦晴, 陈建文
- SHI Jianwei, QIN Qing, CHEN Jianwen
- 柠条人工林细根不同分枝根序寿命估计
- Estimating fine root longevity among different branching order root for Caragana Korshinskii plantation using Minirhizotron
- 生态学报, 2015, 35(12): 4045-4052
- Acta Ecologica Sinica, 2015, 35(12): 4045-4052
- http://dx.doi.org/10.5846/stxb201405231064
-
文章历史
- 收稿日期:2014-05-23
- 网络出版日期:2015-03-27
在陆地生态系统碳平衡和养分循环的研究中,最大的难题是植物地下部分的研究[1]。植物细根在陆地生态系统中扮演重要角色[2, 3],其分解率常比地面凋落物的分解率更高,并且在一些生态系统中细根对总初级净生产力的贡献高达约75%[4],因此细根周转估计是量化地下碳收支的重要环节之一[5],而细根寿命可准确反映细根周转。目前微根管法作为一种非破坏性的直接观测方法,可以在不干扰植物细根生长过程的前提下,能够连续多次监测单个细根从出生到死亡的过程,被广泛应用于细根寿命研究[6, 7]。
细根寿命决定每年分配到土壤中碳和养分的数量,对于精确估测森林固碳潜力有重要影响。然而以往对于细根的认识是把直径小于2 mm的根归结为结构和功能一致的统一体。而近来的研究证据表明,细根在发育结构上表现的形态特征及生理功能存在着高度的异质性[8, 9, 10, 11, 12],其中由于分枝根序生理活性上的差异导致分枝根序寿命的不同[9],因此以不同分枝根序来估计细根寿命对于估测地下碳分配可能更为准确。然而受地上与地下碳分配、土壤资源空间异质性及其季节性变化的影响,不同分枝根序生理活性明显表现差异[11, 12],可能进而影响不同分枝根序寿命,那么受季节性因素,不同季节出生的根序寿命是否存在差异?不同分枝根序又会作如何响应?而土壤资源空间异质性又较高,不同土壤空间位置上的分枝根序又有什么变化?这些问题均需考虑并作出解答。但目前的研究只将根序分枝作为影响细根寿命的一个因素[13, 14, 15],有关分枝根序寿命及其影响因素的研究还未见相关报道,而深入研究不同分枝根序寿命及其影响因素对于深入认识细根周转过程和陆地生态系统地下碳分配无疑具有重要的理论价值。
柠条(Caragana Korshinskii Kom.)属豆科锦鸡儿属,灌木,为直根系树种,主根上生有多层侧根,其主根明显,侧根发达,一般根系密集层主要分布在10—100 cm 土层内,根深和根幅多在1—4 m 范围内,根系光滑为乳黄色,是我国干旱半干旱地区的重要生态经济树种。因此本研究以晋西北黄土丘陵区-五寨县张家坪林场5年生柠条人工林为研究对象,在2007—2009年间,采用微根管技术对柠条细根的生长过程进行追踪观测,探究土层深度、出生季节及距树干位置等因素对不同分枝根序细根寿命的影响,以期进一步准确估计柠条细根寿命,为深入了解晋西北黄土丘陵区柠条人工林及其生态系统的生产力维持机制、固碳潜力和物质循环特点具有重要的理论意义和生态价值。
1 研究地概况及研究方法 1.1 研究地自然概况研究地点位于山西省五寨县张家坪林场,东经111°46.296′,北纬38°58.825′,海拔1448 m,该区属温带大陆性气候,四季分明,冬季长而寒冷,夏季短而无酷暑,常年风沙大,雨雪少,降雨多在夏秋季集中,年平均降雨量478.5 mm,潜在蒸发量1784.4 mm,年平均气温4.5—5 ℃,平均无霜期125 d,终霜期在5月13日,初霜期在9月19日前后。该区土壤为黄土状淡栗褐土,土壤肥力较低。
1.2 研究方法 1.2.1 样地设置、仪器安装试验用林分为5年生柠条人工纯林,位于梁峁缓坡部位,坡度0—5 °,该人工林于2002年秋季播种造林,行间距2 m,选择立地条件一致的林地,设置30 m×30 m样地,样地四周用2 m高铁丝网维护,形成固定样地。
2006年10月,在固定样地区域内,在距植株茎干水平距离0、50 cm处分别随机确定5个位点,共安装微根管10个,0 cm与50 cm处各5个微根管。参照Johnson等[16]介绍的方法安装微根管(美国Bartz技术公司)。先用与微根管(长为150 cm,外径5.5 cm,内径5.0 cm)的直径相等的钢管钻一个洞,与地面成45 °角插入微根管,垂直深度100 cm,地面以上部分约20 cm,安装前底部密封,微根管露出地面部分先封一层黑色胶带以防止光线进入,然后加封一层黄色胶带,微根管固定之后,用外层涂有白色涂料的盖(高20 cm)将管口封好。
1.2.2 取样和影像分析于2007年4月10日开始,至2009年10月19日,每月中旬一次,每年冬季下雪后停止观测,次年4月份再开始,采用BTC图像采集系统(美国Bartz技术公司)连续对同一位置的柠条细根生长过程进行野外影像采集,观测窗实际面积为1.8 cm×1.4 cm(长×宽),每支微根管收集约91—92张图片,3a共进行了26次观测,共对4083个细根进行追踪观测,所获图像采用RooTrack 2.0软件[17]分析处理。
在影像分析中,对于根系死活的判别以根系外观着色和形态特征为主,将白色根和褐色根定义为活根,黑色的根、皮层脱落或表皮褶皱的根定义为死根;另外,白色和褐色根系在没表现出死亡形态时的突然消失,也定义为死根。此外在影像中对于根序的判别,根据Fitter[18]对根系分枝的研究进行根序分级,将影像中明显的不具有独立侧根的细根定义为一级根,将明显可见的具有一组独立侧根的细根定义为二级根,将着生二级根的细根称为三级根,依此类推。由于实际观测图片范围较小,二级以上细根数量较少,故将一级根以外的高级别细根统称为高级根。
1.2.3 数据处理及统计分析根系寿命为以细根第一次在影像中出现时刻到第一次被定义为死亡或消失的时间。根据影像分析数据分别建立一级根和高级根寿命数据库,然后按照影响细根寿命的因素土壤层次、出生季节和空间位置分别归类。参照微根管的垂直观测深度,分为0—20 cm、20—40 cm、40—60 cm、60—80 cm、80—100 cm 5个土壤层次根群;按照试验区域物候变化,将细根划分为春季(3—5月)、夏季(6—8月)、秋季(9—10月) 3个季节根群;依据管的安装位置,分别分为距树干基部处0 cm、50 cm处两个根群。
在Excel中统计一级根和高级根不同分类根群的存活天数,运用SPSS统计软件中的Kaplan-Meier方法进行生存分析,估计细根存活率、平均寿命及中位值寿命(即存活率达到50%时所用的时间,Median root longevity),并做存活曲线;由于不同林分细根寿命是非正态分布,因此用对数秩检验(log-rank test)比较不同土壤层次、不同季节及不同空间位置对一级根和高级根存活曲线的影响及其差异。
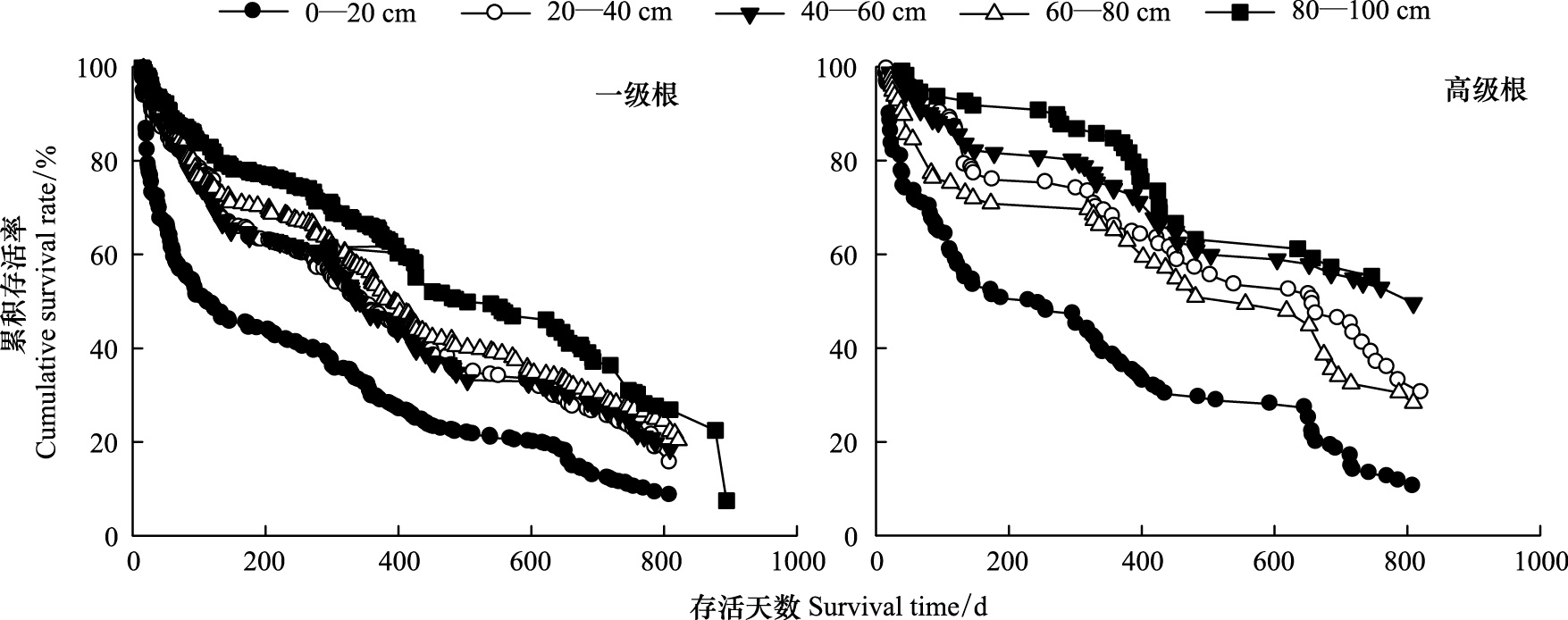
2 结果与分析 2.1 土层对不同根序细根寿命的影响受土壤环境空间异质性影响,柠条细根一级根和高级根寿命均表现随观测期延长而降低,但随土层深度变化表现不同趋势(图 1,表 1),一级根中值寿命表现随土层深度增加而增加趋势,表层(0—20 cm)为(113±16)d,深层(80—100 cm)为(504±45)d;而高级根中值寿命变化不明显,除表层0—20 cm中值寿命较短外(245±62)d,其余各土层中值寿命均较高,且各土层间变化趋势不明显,40—60 cm、80—100 cm高级根的中值寿命在观测期结束时其累积存活率仍在50%以上。此外,在各土层深度处,一级根的中值寿命均低于高级根中值寿命。统计分析表明,随土层深度增加,一级根和高级根的生存曲线除在60—80 cm土层深度处差异不显著外,在0—20 cm土层表现显著差异(P<0.05),而在20—40 cm、40—60 cm、80—100 cm 3个土层深度处表现极显著差异(P<0.01);对于一级根来说,除40—60 cm土层分别与20—40 cm、60—80 cm这两个土层间的存活曲线不存在差异外,其它各土层间的存活曲线均存在显著或极显著差异(P<0.05或P<0.01),而高级根的存活曲线除20—40 cm与60—80 cm、40—60 cm与80—100 cm间差异不显著外,20—40 cm土层与40—60 cm土层间表现显著差异(P<0.05),其余各土层间表现极显著差异(P<0.01)。
|
| 图 1 土层深度对柠条人工林一级根和高级根寿命的影响 Fig.1 The effect of soil depth on first order and higher order root longevity in Caragana Korshinskii Kom. |
| 细根分类 Root classifical |
一级根First order | 高级根Higher order | ||
| 平均寿命/d Mean root lifespan |
中值寿命/d Median root lifespan |
平均寿命/d Mean root lifespan |
中值寿命/d Median root lifespan |
|
| —表示到观测期结束时细根的累积存活率仍在50%以上 | ||||
| 土层深度Soil depth/ cm | ||||
| 0—20 | 271±11 | 113±16 | 330±23 | 245±62 |
| 20—40 | 407±12 | 357±16 | 551±25 | 658±75 |
| 40—60 | 408±13 | 342±16 | 634±28 | — |
| 60—80 | 455±15 | 394±14 | 504±34 | 556±94 |
| 80—100 | 518±14 | 504±45 | 635±27 | — |
| 季节Season | ||||
| 春季 | 373±13 | 329±31 | 469±28 | 454±35 |
| 夏季 | 405±7 | 360±11 | 515±15 | 657±57 |
| 秋季 | 421±14 | 378±18 | 586±30 | 719±30 |
| 空间位置Spatial location | ||||
| 0 cm | 432±9 | 396±14 | 558±18 | 657±48 |
| 50 cm | 376±9 | 327±10 | 486±19 | 427±62 |
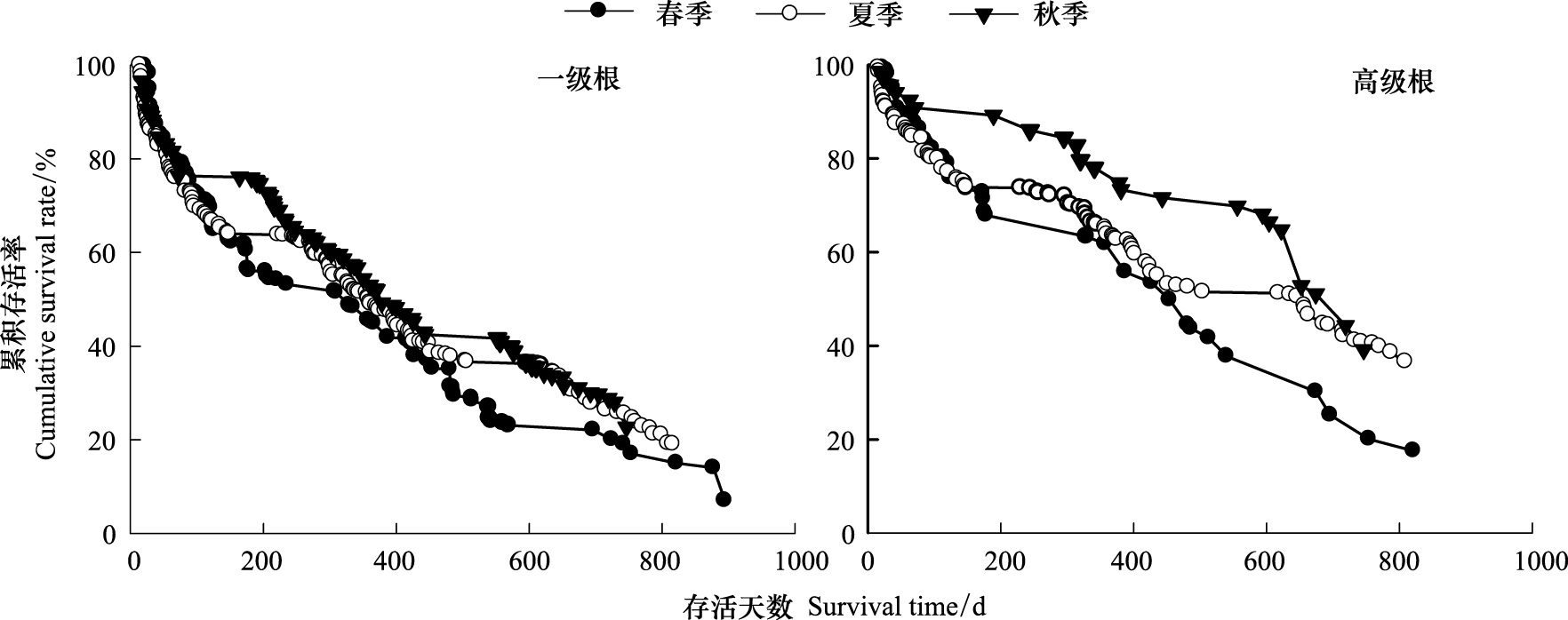
受季节性因素影响,柠条不同季节出生一级根和高级根寿命均表现季节性差异(图 2和表 1),细根寿命的季节性均表现:秋季>夏季>春季,春季出生的细根寿命最短,一级根和高级根中值寿命分别为(329±31)d和(454±35)d;秋季出生的细根寿命最长,一级根和高级根中值寿命分别为(378±18)d和(719±30)d;并且在各个季节均表现,高级根中值寿命大于一级根中值寿命。对存活曲线的统计分析表明:一级根和高级根的存活曲线也存在季节性差异,一级根与高级根的存活曲线在各个季节均表现极显著差异(P<0.01);一级根的存活曲线除夏季出生与秋季出生细根差异性不显著外,其他各季节间均存在显著性差异(P<0.05),而高级根的存活曲线是仅春季出生与秋季出生细根存在极显著差异(P<0.01),其它季节间出生细根则不存在差异。
|
| 图 2 出生季节对柠条人工林一级根和高级根寿命的影响 Fig.2 The effect of birth season on first order and higher order root longevity in Caragana Korshinskii Kom. |
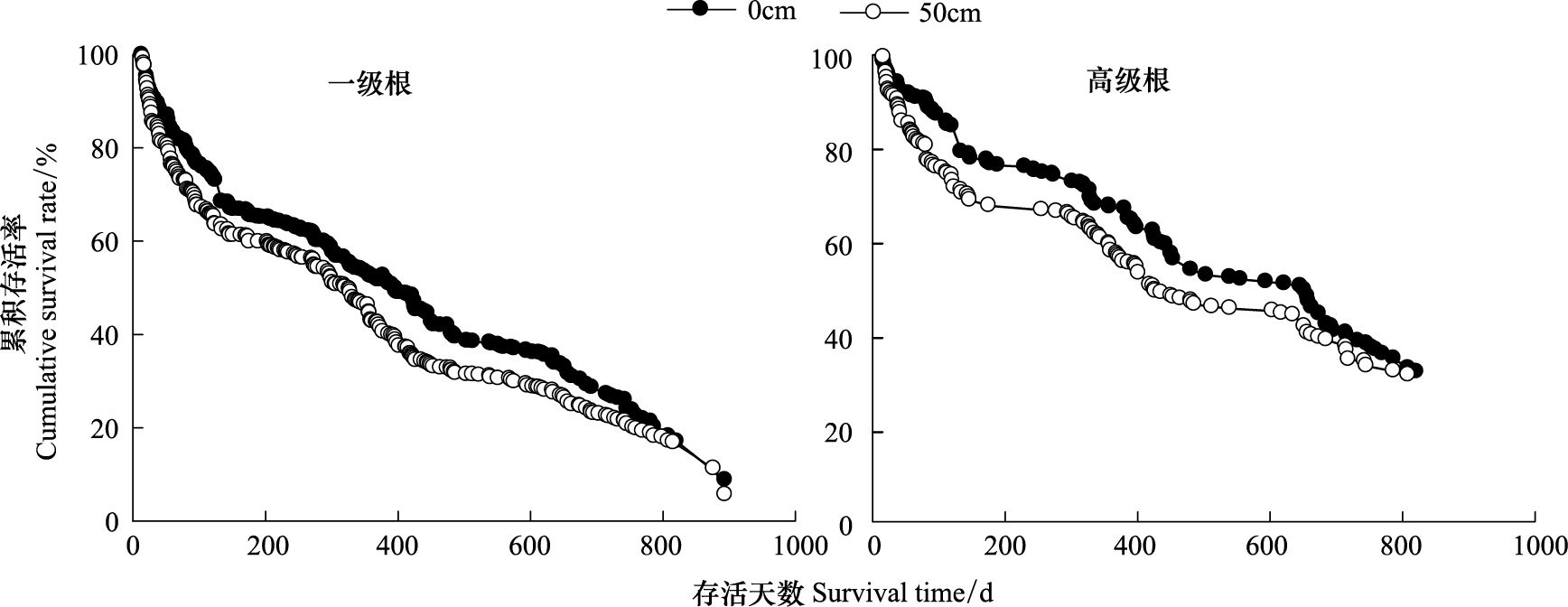
受土壤空间异质性影响,距树干基部不同位置的一级根和高级根细根寿命也表现差异(图 3和表 1)。一级根和高级根0 cm处细根中值寿命(一级根:(396±14)d,高级根:(657±48)d)分别要大于50 cm处一级根和高级根细根的中值寿命(一级根:(327±10) d,高级根:(427±62)d)。同一位置处高级根的寿命要高于一级根寿命。对距树干基部不同位置处的一级根和高级根存活曲线的统计分析表明,在距根茎0 cm处和50 cm处,一级根和高级根的存活曲线间均存在极显著差异(P<0.01),但对于高级根而言,距根茎0 cm和50 cm处的细根存活曲线间差异不明显,而一级根在这两处的细根存活曲线却表现极显著差异(P<0.01)。
|
| 图 3 空间位置对柠条人工林一级根和高级根寿命的影响 Fig.3 The effect of spatial location on first order and higher order root longevity in Caragana Korshinskii Kom. |
树木在根系发育过程中形成复杂的分枝系统,树木不同根序上的细根在形态和生理功能上存在较大差异[11]。随着根序的由小到大,直径由细变粗,根细胞中N的浓度随之下降,C的浓度则有不同程度的升高[13],生理活性也表现由强到弱,因此低级根主要执行吸收功能[19],寿命也较短,而高级根主要是运输和结构性功能[8],寿命也相对较长。本研究运用微根管法对柠条一级根序和高级根序细根寿命的监测结果也表明(表 1),一级根的生存率要小于高级根,这与已有的研究结果相一致[8, 14, 15],但受土层、出生季节和距树干位置等因素的影响,柠条细根一级根和高级根的生存率存在不同程度的差异。
3.1 土层与分枝根序寿命土层是影响细根生存的重要环境因子之一。许多研究表明,随土层深度增加,细根寿命延长[20]。然而本研究对不同根序的研究发现,一级根和高级根的寿命受土层深度影响表现差异,一级根寿命表现随土层深度增加而增加趋势,而高级根寿命变化趋势不明显,除表层较低外,其余各土层寿命均较高。一级根和高级根的生存曲线仅在60—80 cm土层深度处差异不显著。一级根与高级根寿命随土层深度变化而表现差异可能原因:与高级根相比,一级根内N浓度相对较高,呼吸代谢旺盛,吸收及消耗土壤中更多的养分和水分,寿命比高级根要短[9],对土壤环境变化反应也最敏感[11, 21]。而对于一级根和高级根寿命随土层深度变化表现差异,表层一级根和高级根寿命均较短,大多数研究认为由于表层土壤温度适宜,养分和水分较高,细根的生理活性高,因此表层细根寿命较短[22]。然而对本研究样地的测定分析发现(未发表数据),在0—100 cm土层深度内,土壤温度随土层深度增加而逐渐降低,土壤水分含量则是随土层深度增加而增加,土壤有效氮随土层深度变化趋势不明显。由于本研究区处于干旱半干旱区,土壤质地为砂土,保水保肥性差,表层土壤往往表现为水分胁迫层,因此表层一级根和高级根寿命较短可能是水分胁迫下的一种自然反应[21]。当然也不排除土壤表层植食性昆虫和病原微生物数量多引起低级根损耗增加,而导致表层细根寿命缩短[23]。随着土层深度增加,尽管土壤水分增加,但温度降低,深层根生理活性较低,特别在干旱区,为了维持生长而获取深层土壤水分[24, 25],细根的周转率较低,这也可能是干旱区植物根系对环境的一种适应性表现。然而对于一级根和高级根在不同土层深度间表现的寿命差异可能与不同根序对土壤环境变化的生理反应有关系,一级根的生理反应比高级根敏感,那么一级根寿命的变化比高级根寿命的变化要显著得多,最后可能导致一级根寿命随土层深度增加而增加,而高级根寿命只表层较短,其它土层变化不明显。
3.2 出生季节与分枝根序寿命植物光合产物在地上和地下分配的季节性变化也影响植物根系寿命。 Burton等[26]对美国密歇根州北部阔叶林的研究表明,春季出生的细根寿命要低于夏季和秋季,于水强等[27]在中国东北对水曲柳和落叶松的研究也得出了相同的结论。本研究结果也表明,柠条细根一级根和高级根寿命也均表现春季出生的短,夏、秋季出生较长,然而一级根的寿命仅夏季出生与秋季出生表现差异性不显著,而高级根寿命是仅春季出生与秋季出生细根存在极显著差异(P<0.01)。许多研究表明,温带落叶树种细根生长先于叶[28, 29]。 根据柠条的生长特点,春季展叶之前,一级根生长所需的 C 均来自于根系上一年储存的碳水化合物,展叶后来自于新叶固定的碳水化合物[30],然而由于春季土壤资源有效性的相对受限和分配到一级根的 C 有限,春季出生的一级根寿命相对较短,然而夏季C 分配格局发生改变,相当一部分 C 还是分配到地上的枝条和茎中[30],但C对地下的供应得到了有效保证,一级根吸收养分和水分与消耗的 C 之间保持一个相对的动态平衡[29]。到了秋季,地上部分停止生长,树冠逐渐衰老,对养分和水分的需求逐渐降低,C 的分配格局又发生改变,地上部分累积的 C 主要用于地下部分生长,从根系中不同根序执行的功能来考虑,这部分C可能会优先保证一级根的生长,因此在夏季和秋季C供应优先得到保证的情况下,这两个季节出生的细根寿命相对较长,差异不明显。而对于高级根来说,春季一级根生长所需C可能主要来自于高级根中上一年度贮存的C,春季贮存C的消耗,使得高级根维持成本增加,那么寿命就会缩短,而随着季节变化,C的分配格局也发生变化,由于不同根序执行功能的差异,夏季光合产物地下C的分配于一级根的可能要多于高级根,到了秋季随着气温下降、降水和地上 C 分配的减少,在保证一级根生长得到维持的前提下,大部分C在高级根中积累[30],以用于下一年根生长所需,可见高级根对于C的利用在春季与秋季正好表现两个相反的过程,因此使得在春季和秋季出生的高级根寿命表现显著差异。
3.3 空间位置与分枝根序寿命受土壤空间异质性影响,距树干基部不同位置的一级根和高级根细根寿命也表现差异。一级根和高级根0 cm处细根中值寿命分别要大于50 cm处一级根和高级根细根的中值寿命。就高级根而言,距树干基部0 cm和50 cm处的细根存活曲线间差异不明显,而一级根在这两处的细根存活曲线却表现极显著差异(P<0.01)。根据植物生理学相关理论,光合产物的供应一般遵循“就近运输,同侧分配”原则,距树干基部0 cm处比50 cm处优先得到地上部分供给的C,因此距树干基部0 cm处的一级根和高级根寿命明显要比距树干基部50 cm处的一级根和高级根寿命长。此外,徐文静等[31]通过水曲柳苗木的遮荫实验表明:在遮荫条件下,细根衰老随根序级别增加而减少,卫星等[21]的水分胁迫实验进一步证明一级根受C供应的影响最大,也最容易死亡。说明一级根要比高级根对光合产物的运输距离远近反应要明显,因此一级根寿命在不同距树干基部位置间表现差异显著,而高级根则表现差异不明显。除了C供应的影响外,不同空间位置处的土壤环境异质性也可能影响不同根序细根寿命差异,树木林冠、林隙会造成林下温度、水分具有一定的空间异质性[32],距树干基部0 cm位置由于有林冠的遮荫作用,温度较50 cm位置处要低,而50 cm处温度较高,蒸发量也相对较高,因此0 cm位置土壤水分较50 cm位置要充足。已有的研究表明,细根吸收养分和水分越多,分配到细根的C就越多,寿命也较长[33]。因此距树干基部0 cm位置的细根较50 cm位置容易得到更充足的C供应,0 cm处一级根和高级根比50 cm处一级根和高级根寿命根长,而对于一级根和高级根寿命在不同距离处的差异表现,也可能与一级根和高级根对土壤环境的生理响应程度有关。
总之,从本研究结果来看,在环境资源有效性和C供应相对丰富的情况下,一级根和高级根寿命会表现差异,而在这些资源相对不足时,则一级根和高级根寿命却又表现差异不明显。不同根序寿命对不同影响因素的响应差异可能是根序构建和维护在成本-效益方面对环境的一种适应性表现。然而本研究只是对不同根序细根寿命与影响因素分析的初步尝试,对于所得结果可能还存在着很大的不确定性。如:(1)本研究运用微根管法中所观测到的根序有限,大多为一级根,少部分为二级根和三级根,可能对一级根寿命受不同因素影响的反应较准确,而高级根寿命对各因素的响应可能还存在一定的误差;(2)本研究只对一种植物进行了监测分析,因此对于结论的可靠性和准确性还需对多种植物开展研究来加以佐证;(3)从一级根和高级根寿命对不同因素的响应差异来看,很大程度上可能与不同根序执行不同功能有关,但这个观点目前仅从细根解剖结构特征得到了证实[8],而不同根序细根生理功能对环境因素变化的响应是否也遵循同样的规律?是否还受其他因素的影响?这些问题还需作进一步研究,以进一步了解不同根序间细根寿命存在差异的机理,为深入认识细根的周转过程,准确估计陆地生态系统碳对地下的分配和养分过程无疑具有重要的理论现实意义。
4 结论(1)受土壤环境空间异质性影响,在各土层深度处,一级根中值寿命均低于高级根中值寿命,且一级根中值寿命表现随土层深度增加而增加趋势,而高级根中值寿命变化不明显,除表层0—20 cm中值寿命较短外(245±62) d,各土层间变化趋势不明显,40—60 cm、80—100 cm高级根的中值寿命在观测期结束时其累积存活率仍在50%以上。
(2)受季节性因素影响,不同季节出生的一级根和高级根寿命均表现:秋季>夏季>春季,并且在各个季节均表现,高级根寿命显著大于一级根寿命(P<0.01);一级根仅是夏季出生与秋季出生细根差异性不显著(P>0.05),而高级根仅春季出生与秋季出生细根存在极显著差异(P<0.01)。
(3)受土壤空间异质性影响,一级根和高级根0 cm处细根中值寿命分别要大于50 cm处一级根和高级根细根的中值寿命。同一位置处高级根寿命要大于一级根寿命。在距树干基部0 cm处和50 cm处,一级根和高级根的存活曲线间均存在极显著差异(P<0.01),但高级根表现在距树干基部0 cm和50 cm处间差异不明显,而一级根却表现极显著差异(P<0.01)。
| [1] | 贺金生, 王政权, 方精云. 全球变化下的地下生态学: 问题与展望. 科学通报, 2004, 49(13): 1226-1233. |
| [2] | Davis J P, Haines B, Coleman D, Hendrick R. Fine root dynamics along an elevational gradient in the southern Appalachian Mountains, USA. Forest Ecology and Management, 2004, 187(1): 19-33. |
| [3] | Norby R J, Jackson R B. Root dynamics and global change: seeking an ecosystem perspective. New Phytoligist, 2000, 147(1): 3-12. |
| [4] | Vogt K A, Vogt D J, Palmiotto P A, Boon P, O'Hara J, Asbjornsen H. Review of root dynamics in forest ecosystems grouped by climate, climatic forest type and species. Plant and Soil, 1996, 187(2): 159-219. |
| [5] | Zhou Z C, Shangguan Z P. Vertical distribution of fine roots in relation to soil factors in Pinus tabulaeformis Carr. forest of the Loess Plateau of China. Plant and Soil, 2007, 291(1/2): 119-129. |
| [6] | Hendrick R L, Pregitzer K S. Applications of minirhizotrons to understand root function in forests and other natural ecosystems. Plant and Soil, 1996, 185(2): 293-304. |
| [7] | 史建伟, 于水强, 于立忠, 韩有志, 王政权, 郭大立. 微根管在细根研究中的应用. 应用生态学报, 2006, 17(4): 715-719. |
| [8] | Guo D L, Xia M X, Wei X, Chang W J, Liu Y, Wang Z Q. Anatomical traits associated with absorption and mycorrhizal colonization are linked to root branch order in twenty-three Chinese temperate tree species. New Phytoligist, 2008, 180(3): 673-683. |
| [9] | Pregitzer K S, DeForest J L, Burton A J, Allen M F, Ruess R W, Hendrick R L. Fine root architecture of nine North American trees. Ecological Monograph, 2002, 72(2): 293-309. |
| [10] | Rewald B, Ephrath J E, Rachmilevitch S. A root is a root? Water uptake rates of citrus root orders. Plant, Cell and Environment, 2011, 34(1): 33-42. |
| [11] | Hishi T. Heterogeneity of individual roots within the fine root architecture: Causal links between physiological and ecosystem functions. Journal of Forest Research, 2007, 12(2): 126-133. |
| [12] | Guo D L, Mitchell R J, Hendricks J J. Fine root branch orders respond differentially to carbon source-sink manipulations in a longleaf pine forest. Oecologia, 2004, 140(3): 450-457. |
| [13] | Wells C E, Michael Glenn D, Eissenstat D M. Changes in the risk of fine-root mortality with age: a case study in peach, Prunus persica (Rosaceae). American Journal of Botany, 2002, 89(2): 79-87. |
| [14] | 黄锦学, 凌华, 杨智杰, 卢正立, 熊德成, 陈光水, 杨玉盛. 细柄阿丁枫和米槠细根寿命影响因素. 生态学报, 2012, 32(6): 1932-1942. |
| [15] | 凌华, 袁一丁, 杨智杰, 黄锦学, 陈光水, 杨玉盛. 杉木人工林细根寿命的影响因素. 生态学报, 2011, 31(4): 1130-1138. |
| [16] | Johnson M G, Tingey D T, Phillips D L, Storm M J. Advancing fine root research with minirhizotrons. Environmental and Experimental Botany, 2001, 45(3): 263-289. |
| [17] | Craine J, Tremmel D. Improvements to the minirhizotron system. Bulletin of the Ecological Society of America, 1995, 76(4): 234-235. |
| [18] | Fitter A H, Functional significance of root morphology and root system architecture // Fitter A H, Atkinson D, Read D J, Usher M B, eds. Ecological interactions in Soil: Plant, Microbes and Animals. Oxford: Blackwell, 1985: 87-106. |
| [19] | Pregitzer K S. Tree root architecture-form and function. New Phytoligist, 2008, 180(3): 562-564. |
| [20] | Chen H Y H, Brassard B W. Intrinsic and extrinsic controls of fine root life span. Critical Reviews in Plant Sciences, 2013, 32(3): 151-161. |
| [21] | 卫星, 王政权, 张国珍, 陈海波, 王婧. 水曲柳苗木不同根序对干旱胁迫的生理生化反应. 林业科学, 2009, 45(6): 16-21. |
| [22] | Eissenstat D M, Yanai R D. The ecology of root lifespan. Advances in Ecological Research, 1997, 27: 1-60. |
| [23] | Gill R A, Jackson R B. Global patterns of root turnover for terrestrial ecosystems. New Phytoligist, 2000, 147(1): 13-31. |
| [24] | Neumann R B, Cardon Z G. The magnitude of hydraulic redistribution by plant roots: a review and synthesis of empirical and modeling studies. New Phytoligist, 2012, 194(2): 337-352. |
| [25] | Stover D B, Day F P, Drake B G, Hinkle C R. The long-term effects of CO2 enrichment on fine root productivity, mortality, and survivorship in a scrub-oak ecosystem at Kennedy Space Center, Florida, USA. Environmental and Experimental Botany, 2010, 69(2): 214-222. |
| [26] | Burton A J, Pregitzer K S, Hendrick R L. Relationships between fine root dynamics and nitrogen availability in Michigan northern hardwood forests. Oecologia, 2000, 125(3): 389-399. |
| [27] | 于水强, 王政权, 史建伟, 全先奎, 梅莉, 孙玥, 贾淑霞, 于立忠. 水曲柳和落叶松细根寿命的估计. 植物生态学报, 2007, 31(1): 102-109. |
| [28] | Pregitzer K S, King J S, Burton A J, Brown S E. Responses of tree fine roots to temperature. New Phytologist, 2000, 147(1): 105- 115. |
| [29] | Hendrick R L, Pregitzer K S. Temporal and depth-related patterns of fine root dynamics in northern hardwood forests. Journal of Ecology, 1996, 84(2): 167-176. |
| [30] | Pregitzer K S. Woody plants, carbon allocation and fine roots. New Phytologist, 2003, 158(3): 421-424. |
| [31] | 徐文静, 王政权, 范志强, 孙海龙, 贾淑霞, 吴楚. 遮荫对水曲柳幼苗细根衰老的影响. 植物生态学报, 2006, 30(1): 104-111. |
| [32] | 史建伟, 王孟本, 陈建文, 曹建庭. 柠条细根的空间分布特征及其季节动态. 生态学报, 2011, 31(3): 726-733. |
| [33] | 梅莉, 王政权, 程云环, 郭大立. 林木细根寿命及其影响因子研究进展. 植物生态学报, 2004, 28(5):704-710. |
 2015, Vol. 35
2015, Vol. 35




