文章信息
- 马丽芳, 刘俊稚, 刘新颖, 汪志平, 陈子元
- MA Lifang, LIU Junzhi, LIU Xinying, WANG Zhiping, CHEN Ziyuan
- 富油微藻布朗葡萄藻分子生态学研究进展
- Advances in molecular ecology of the oil-rich microalga Botryococcus braunii
- 生态学报, 2015, 35(10): 3165-3171
- Acta Ecologica Sinica, 2015, 35(10): 3165-3171
- http://dx.doi.org/10.5846/stxb201308232132
-
文章历史
- 收稿日期:2013-08-23
- 网络出版日期:2014-05-30
布朗葡萄藻(Botryococcus braunii)因其脂质含量高、不占用耕地及可利用CO2光合产烃等优势,成为具有重大开发潜力的能源微藻之一[1]。布朗葡萄藻具有梨形单细胞、串状集落等典型形态特征,富含烃类和脂肪酸等代谢产物[2, 3]。其主要烃类组成与化学结构等常因藻株不同而存在明显差异,一般可据此分为A、B和L 3个化学种[4, 5, 6]。然而,由于布朗葡萄藻的形态特征和生化组分等易受环境因素影响[7, 8, 9, 10, 11],利用以形态学为主要依据的经典分类学界定布朗葡萄藻时往往会存在较大难度与争议。
随着分子生物学与生态学的相互渗透和发展,分子生态学应运而生[12, 13]。分子生态学应用分子生物学的原理和方法,使生态学研究从表观特征观察深入到生物体内各种生物活性分子以及这些分子与环境相互作用的机制,进而以宏观与微观紧密结合的角度反映生态系统中生物个体和种群间关系的本质[14, 15]。近年来,相关分子生态学研究在揭示布朗葡萄藻的分类地位、遗传多样性及系统演化等方面不断发展,并取得了一定成果。本文在简述布朗葡萄藻形态学与化学种特征的基础上,着重介绍其分子生态学研究的最新进展,并对今后面临的挑战与研究动向进行探讨与展望。
1 布朗葡萄藻的生理生态特性 1.1 形态学特征布朗葡萄藻是一种单细胞光合微藻,广泛分布于世界热带、亚热带和温带的淡水和微咸水等水域中[16],其典型形态学特征为:单细胞呈梨形,长7—13 μm,宽5—9 μm,具有一个裸露蛋白核、细胞核、叶绿体、淀粉核等;基质外壁富含脂质,使各单细胞呈辐射状聚成串状集落[1, 8, 17, 18]。在我国淡水藻志及一些其他研究中,认为布朗葡萄藻具有绿藻门(Chlorophyta)的本征性,隶属于绿藻门、绿藻纲(Chlorophyceae)、绿球藻目(Chlorococcales)、葡萄藻科(Botryococcaceae)、葡萄藻属(Botryococcus)[17, 19, 20];而根据其质体和淀粉粒的结构,胡鸿钧和魏印心[21]、Smith[22]等建议将其归入黄藻门(Xanthophyta)、黄藻纲(Xanthophyeeae)。布朗葡萄藻的形态结构不仅在不同藻株之间存在差异,即使同一藻株的不同培养条件和生长阶段也有所不同。由于布朗葡萄藻的形态结构易受温度、pH、光照等环境条件的影响[7, 8, 9, 10, 11],使得以形态学为基础的经典分类学鉴定工作的难度大为增加,且鉴定结果也易引起争议。因此,经典分类学在布朗葡萄藻藻种的分类、鉴定上存在较大局限性,还须结合分子生态学等弥补其局限和不足。
1.2 化学种类及其特征根据其烃类化学结构性质的不同,可以将布朗葡萄藻分为A、B和L 3个化学种[4, 5, 6, 23, 24, 25]。(1)化学种A:主要合成无分枝、直链、奇数碳链C23—C33的n-二烯烃、三烯烃,其中二烯烃含量较多。(2)化学种B:主要合成不饱和的三萜类烯烃(CnH2n-10,n=30—37),包括C30—C37的葡萄烯和C31—C34的甲基鲨烯等[26],其中葡萄烯含量较多,通常能占到细胞干重的27%—86%。(3)化学种L:仅合成一种分枝上存在苯环或杂环的四萜类烯烃(C40H78),含量为细胞干重的2%—8%。在上述3个化学种中,葡萄藻所含脂质均是石油和煤的主要组成成分[27, 28, 29]。其中,化学种A和化学种B的含烃量相对较高,在作为烃类燃料的生产上要优于化学种L。在实验室培养条件下,和化学种L相比,化学种A、B的细胞通常较大;而且,在稳定生长期,化学种A常呈绿色或浅黄色,而化学种B、L则呈桔红或桔褐色[8, 30]。因此,葡萄藻的这些特定形态特征可用于其化学种的初步判断。
此外,Templier等[31]发现另一种化学种Gb的二烯烃与化学种A相似,但烯键同时存在顺式和反式;Kawachi等[32]报道发现了含有C18—C20环氧树脂正烷烃的新化学种S。可见,随着研究的深入,布朗葡萄藻的化学分类正得以不断地补充和完善。
2 布朗葡萄藻的分子生态学研究 2.1 分子系统发育学研究基于形态特征的经典分类学是现代生物分类学的基础。随着分子系统学研究策略及分析手段的日益完善,植物分类学领域在注重传统经典分类学的同时,加强了以蛋白质、核酸等为证据的分子系统学研究[33],以期对经典分类学起到验证和补充的作用。布朗葡萄藻的形态、生理生化等表型特征在外界因素的影响下容易发生变化,但这种表型特征在本质上是由藻株的基因型所决定的。因此,直接反映基因型的分子数据是研究系统发育关系的理想标记,是进行基因分型和遗传多样性研究的良好位点。
分子系统发育学研究有两大分子标记,即蛋白质与核酸[34, 35]。蛋白质是分子系统学研究中最早应用的分子,随着聚合酶链反应(polymerase chain reaction,PCR)扩增及自动测序技术的发展,核酸测序分析逐渐成为阐明系统演化关系最为有效的方法。在核酸测序分析中,常用于分子系统发育学研究的基因片段包括:核基因片段18S rRNA序列、ITS序列等,叶绿体基因片段1,5-二磷酸核酮糖羧化酶/加氧酶基因(1,5-bisphosphate carboxynase/ oxygenase large subunit gene,rbcL)等,以及线粒体基因片段等[36, 37, 38]。目前,布朗葡萄藻的分子系统发育学研究主要利用核基因18S rRNA与ITS区,及叶绿体基因rbcL序列构建系统发育树进行相应的系统分析,从基因水平阐明其分类地位、遗传多样性及系统演化等。
经与其他微藻核糖体小亚基 RNA 序列[39]比对分析,Sawayama等[40]建立了第一个针对布朗葡萄藻的系统发育树,发现布朗葡萄藻B. braunii Kützing(Berkeley;化学种B)属于绿藻门、绿藻纲,同小桩藻(Characium vaculatum)和巴夫杜氏藻(Dunaliella parva)亲缘较近。Senousy等[41]构建了布朗葡萄藻不同化学种藻株与53个绿藻门藻株的18S rRNA序列系统发育树,发现布朗葡萄藻属于绿藻门、共球藻纲(Trebouxiophyceae),并与共球藻纲的Choricystis亲缘关系最近。上述结果有力支持了布朗葡萄藻属于绿藻门的观点,但对其所属纲别仍存在分歧。
Weiss等[42]针对B. braunii Berkeley藻株重建了18S rRNA序列系统发育树,并通过布朗葡萄藻β-肌动蛋白的互补脱氧核糖核酸(complementary deoxyribonucleic acid,cDNA)序列系统发育树来验证其结果,认定B. braunii Berkeley属于共球藻纲。国内王朋云等[43]利用绿球藻目(Chioroeoeeales)、柄球藻目(Misehoeoceales)、衣藻目(ehiamydomonadales)和小球藻目(Chiorellales)的rbcL序列构建了系统发育树,同样发现布朗葡萄藻株与共球藻纲、小球藻目的藻株同属一大簇群。因此,分子系统发育树证实布朗葡萄藻属绿藻门、共球藻纲,为澄清其经典分类学上的争议提供了强有力的分子证据。
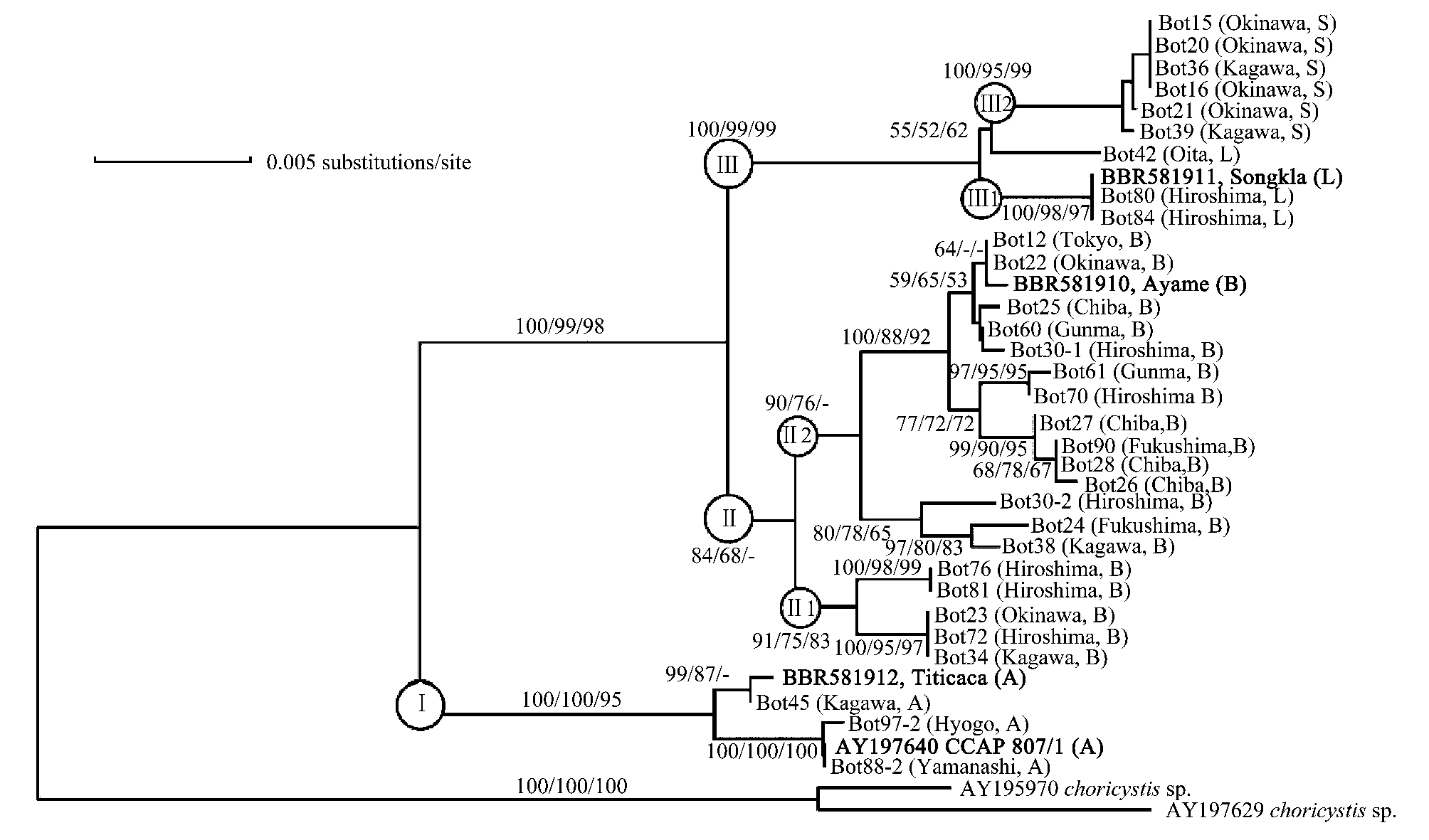
2.2 分子系统发育关系与化学种的关联性Kawachi等[32]根据气相色谱-质谱分析结果,以邻接法(Neighbor joining,NJ)、最大简约法(Maximum parsimony,MP)和最大似然法(Maximum likelihood,ML)将其分离的31个布朗葡萄藻藻株分为4个化学种(包括已知化学种A、B、L和新化学种S),并与GenBank上其他布朗葡萄藻株共同构建了基于18S rRNA序列的系统发育树(图 1)[32],形成3个主聚群Ⅰ、Ⅱ、Ⅲ,依次分别与化学种A、B、L相对应;其中,主聚群Ⅱ、Ⅲ又分别形成亚聚群Ⅱ1、Ⅱ2和Ⅲ1、Ⅲ2,而亚聚群Ⅲ1、Ⅲ2分别对应于化学种L、S。
为进一步探讨布朗葡萄藻分子系统发育与其所属化学种之间的关系,笔者从GenBank中获取了更多已知化学种类型的布朗葡萄藻的18S rRNA序列[32, 41, 42],并利用MEGA 5.05 软件以邻接法NJ、最大简约法MP和最大似然法ML构建了分子系统发育树(图 2)。可知,化学种A、B、L均属共球藻纲这个大分枝,其下分成两个谱系,分别由化学种A和化学种B、L组成。这可能与其产烃类型存在关联性,即化学种B、L产生的烃类均以类异戊二烯烃为组成单位,而化学种A主要合成二烯烃[41]。这一结果验证和补充了布朗葡萄藻的化学种分类,同时揭示其分子系统发育关系与化学种之间存在较高的关联性。
布朗葡萄藻化学种B、L在18S rRNA序列的系统发育树中属于同一谱系,即二者存在较近的进化关系,然而其基因组大小却存在明显差异。Weiss等[42, 43]测得分属化学种A、B、L的3株藻的基因组大小依次为166.0Mb、166.2Mb和211.3Mb。可见,属于同一谱系中的化学种B、L的基因组大小差距显著,而进化关系较远的化学种A、B的基因组大小反而很接近,这提示有关布朗葡萄藻化学种间的进化关系还需作更深入地探究。最近,Molnár等[44]利用已测序化学种B(B. braunii Showa)的一个转录组,构建了其主要烃类的生物合成网络,为揭示不同化学种与其主要烃类生物合成网络的联系提供了重要启示。相信随着其他化学种布朗葡萄藻基因组的测定和注释,将为揭示布朗葡萄藻不同化学种进化关系及其相应基因组特性的内在关联等提供更全面的信息。
2.4 亲缘关系、遗传多样性与地理来源间的关联性布朗葡萄藻的系统发生树通常由两大簇群组成,而每个族群又可进一步细分为不同的亚簇,表明该藻的18S rRNA、ITS序列位点具有较高的遗传多态性,不同藻株之间存在遗传上的多样性[45]。由于布朗葡萄藻广泛分布于世界各地,其较高的遗传多样性可能由一定程度的地理隔离所致。王朋云等[45, 46]以与布朗葡萄藻同科但不同属的南向球葡萄藻(Botryosphaerella sudetica UTEX 2629)的18S rRNA、ITS等序列为外群构建了布朗葡萄藻系统发育树,比较了不同地理来源的布朗葡萄藻亲缘关系的远近程度。18S rRNA的系统发育树结果表明,采自我国云南抚仙湖的藻株(B. braunii AGB-Bb02)与采自湖北武汉的藻株(B. braunii AGB-Bb03)属于同一簇群,分别与源自泰国的藻株(B. braunii Songkla Nakarin)和源于非洲科特迪瓦的藻株(B. braunii Ayame)的遗传亲缘关系较近;而采自英国剑桥的藻株(B. braunii AGB-Bb01)则属于另一簇群,与源于玻利维亚的藻株(B. braunii Titicaca)和美国明尼苏达的藻株(B. braunii Tow 9/21 P-16w)亲缘关系较近,其遗传距离分别为0.0098和0.0116。在ITS系统发育树中,AGB-Bb01与源于澳大利亚新南威尔士的藻株(B. braunii Jillamatong)亲缘关系最近,与源自英国坎布里亚的藻株(B. braunii CCAP807/2)和科特迪瓦藻株(B. braunii Yamoussoukro)亲缘关系最远。此外,Kawachi等[32]构建的基于18S rRNA序列的布朗葡萄藻系统发育树发现,一些采自同一地域的藻株也会处于不同的系统位置上。这种差异可能是由某些摄食微藻的鸟类通过觅食、迁徙等携带布朗葡萄藻传播的结果[47, 48]。布朗葡萄藻的遗传多样性与地理来源之间的联系性尚需更多实地检测和更充足的种质资源测序分析等进一步考察。
3 问题与展望近年来,分子生态学作为一门新兴学科,为生态学研究提供了崭新的角度和思路,它通过宏观与微观的结合,在阐释生命系统与环境系统相互作用的机理及其分子机制中发挥着越来越重要的作用。较其他某些藻类而言,布朗葡萄藻的分子生态学研究起步较晚,面临一些问题和挑战:(1)现有布朗葡萄藻分子系统发育学研究使用的分子标记主要集中于单一的DNA序列片段上,今后相关研究所选择的DNA分子标记应趋向于多片段、长序列,以期获得更加充足的分子数据信息,从而更全面地反映其系统发育关系[36]。(2)在布朗葡萄藻18S rRNA的系统发育树中,同一谱系的化学种B、L比化学种A存在更近的进化关系,这与它们的产烃种类存在一定关联性;但不同化学种的进化关系与其相应基因组大小的关系相反[42, 43]。布朗葡萄藻3个化学种之间存在怎样的进化关系,其基因组与主要烃类生物合成网络之间存在怎样的调控与反馈机制,这些问题的阐释需要对不同化学种的基因组进行更深入地测定分析。(3)布朗葡萄藻的遗传多样性是否由地理隔离引起[45, 46],其遗传多样性与地理来源之间存在怎样的相关性,这需要在更多实地考察和更充足的源于不同地域藻株分子数据信息的基础上深入论证。
与经典分类学研究一样,分子系统发育学也有自身的一些局限性[35]。布朗葡萄藻分子系统发育学研究只有将核酸与蛋白质数据综合起来建立更为完善的系统发育树,再与经典分类、化学分类相互结合印证,逐步建立整体体系,才能更深入准确地阐明其系统发育关系。同时,基因组和蛋白质组序列测定及相应生物信息学的迅猛发展,不仅促进有关布朗葡萄藻烃类合成的基因工程、系统基因组学和蛋白组学的兴起,而且将从微观水平上更真实直接地阐明生态现象的分子机理,从而推进布朗葡萄藻分子生态学研究及能源微藻产业化进程。
| [1] | Metzger P, Largeau C. Botryococcus braunii: a rich source for hydrocarbons and related ether lipids. Applied Microbiology and Biotechnology, 2005, 66(5): 486-496. |
| [2] | Brown A C, Knights B A, Conway E. Hydrocarbon content and its relationship to physiological state in the green alga Botryococcus braunii. Phytochemistry, 1969, 8(3): 543-547. |
| [3] | Knights B A, Brown A C, Conway E, Middleditch B S. Hydrocarbons from the green form of the freshwater alga Botryococcus braunii. Phytochemistry, 1970, 9(6): 1317-1324. |
| [4] | Metzger P, Berkaloff C, Casadevall E, Coute A. Alkadiene-and botryococcene-producing races of wild strains of Botryococcus braunii. Phytochemistry, 1985, 24(10): 2305-2312. |
| [5] | Huang Z, Dale Poulter C. Tetramethylsqualene, a triterpene from Botryococcus braunii var showa. Phytochemistry, 1989, 28(5): 1467-1470. |
| [6] | Metzger P, Allard B, Casadevall E, Berkaloff C, Couté A. Structure and chemistry of a new chemical race of Botryococcus braunii that produces lycopadiene, a tetraterpenoid hydrocarbon. Journal of Phycology, 1990, 26(2): 258-266. |
| [7] | Plain N, Largeau C, Derenne S, Couté A. Variabilité morphologique de Botryococcus braunii (Chlorococcales, Chlorophyta): corrélations avec les conditions de croissance et la teneur en lipides. Phycologia, 1993, 32(4): 259-265. |
| [8] | 马梅. 布朗葡萄藻烃成分分析, 培养条件优化及不同时期的形态结构比较 [D]. 青岛: 中国海洋大学, 2008. |
| [9] | 胡章喜, 安民, 段舜山, 徐宁, 孙凯峰, 刘晓娟, 李爱芬, 张成武. 不同氮源对布朗葡萄藻生长、总脂和总烃含量的影响. 生态学报, 2009, 29(6): 3288-3294. |
| [10] | Tanoi T, Kawachi M, Watanabe M M. Effects of carbon source on growth and morphology of Botryococcus braunii. Journal of Applied Phycology, 2011, 23(1): 25-33. |
| [11] | Ruangsomboon S. Effect of light, nutrient, cultivation time and salinity on lipid production of newly isolated strain of the green microalga, Botryococcus braunii KMITL 2. Bioresource Technology, 2012, 109: 261-265. |
| [12] | 胡志昂, 王洪新. 分子生态学研究进展. 生态学报, 1998, 18(6): 565-574. |
| [13] | 张爱兵, 谭声江, 陈建, 李典谟. 空间分子生态学——分子生态学与空间生态学相结合的新领域. 生态学报, 2002, 22(5): 752-769. |
| [14] | 黄勇平, 朱湘雄. 分子生态学——生命科学领域的新学科. 中国科学院院刊, 2003, 18(2): 84-88. |
| [15] | Krüger M, Krüger C, Walker C, Stockinger H, Schüßler A. Phylogenetic reference data for systematics and phylotaxonomy of arbuscular mycorrhizal fungi from phylum to species level. New Phytologist, 2012, 193(4): 970-984. |
| [16] | Wake L V, Hillen L W. Study of a "bloom" of the oil-rich alga Botryococcus braunii in the Darwin River Reservoir. Biotechnology and Bioengineering, 1980, 22(8): 1637-1656. |
| [17] | Noguchi T, Kakami F. Transformation of trans-Golgi network during the cell cycle in a green alga, Botryococcus braunii. Journal of Plant Research, 1999, 112(2): 175-186. |
| [18] | Komárek J, Komárková-Legnerová J. Review of the Euopean Microcystis-morphospecies (Cyanoprokaryotes) from nature. Czech Phycology, 2002, 2: 1-24. |
| [19] | 毕列爵, 胡征宇. 中国淡水藻志(第八卷). 北京: 科学出版社, 2004: 111-115. |
| [20] | Hirose H, Ogasawara N. Fine structural evidence for the systematic position of Botryococcus braunii Kützing as a member of Chlorophyceae. Bulletin of the Japanese Society of Phycology, 1977, 25: 61-69. |
| [21] | 胡鸿钧, 魏印心. 中国淡水藻类-系统、分类及生态. 北京: 科学出版社, 2006: 286-286. |
| [22] | Smith G M. The Fresh-Water Algae of the United States. New York: McGraw-Hill, 1950: 716-716. |
| [23] | Villarreal-Rosales E, Metzger P, Casadevall E. Ether lipid production in relation to growth in Botryococcus braunii. Phytochemistry, 1992, 31(9): 3021-3027. |
| [24] | Metzger P, Casadevall E. Structure de trois nouveaux "botryococcenes" synthetises par une souche de Botrycoccus braunii cultivee en laboratoire. Tetrahedron Letters, 1983, 24(37): 4013-4016. |
| [25] | Metzger P, Casadevall E. Lycopadiene, a tetraterpenoid hydrocarbon from new strains of the green alga Botryococcus braunii. Tetrahedron Letters, 1987, 28(34): 3931-3934. |
| [26] | Achitouv E, Metzger P, Rager M N, Largeau C. C31-C34 methylated squalenes from a Bolivian strain of Botryococcus braunii. Phytochemistry, 2004, 65(23): 3159-3165. |
| [27] | Glikson M, Lindsay K, Saxby J. Botryococcus-A planktonic green alga, the source of petroleum through the ages: transmission electron microscopical studies of oil shales and petroleum source rocks. Organic Geochemistry, 1989, 14(6): 595-608. |
| [28] | Summons R E, Metzger P, Largeau C, Murray A P, Hope J M. Polymethylsqualanes from Botryococcus braunii in lacustrine sediments and crude oils. Organic Geochemistry, 2002, 33(2): 99-109. |
| [29] | Adam P, Schaeffer P, Albrecht P. C40 monoaromatic lycopane derivatives as indicators of the contribution of the alga Botryococcus braunii race L to the organic matter of Messel oil shale (Eocene, Germany). Organic Geochemistry, 2006, 37(5): 584-596. |
| [30] | 徐玲. 布朗葡萄藻的培养优化与分离技术 [D]. 南京: 江南大学, 2011. |
| [31] | Templier J, Largeau C, Casadevall E. Non-specific enlongation-decarboxylation in biosynthesis of cis- and trans-alkadienes by Botryococcus braunii. Phytochemistry, 1991, 30(1): 175-183. |
| [32] | Kawachi M, Tanoi T, Demura M, Kaya K, Watanabe M M. Relationship between hydrocarbons and molecular phylogeny of Botryococcus braunii. Algal Research, 2012, 1(2): 114-119. |
| [33] | 万海清, 梁明山, 许介眉. 分子生物学手段在植物系统与进化研究中的应用. 植物学通报, 1998, 15(4): 8-17. |
| [34] | 程燕林, 梁军, 吕全, 张星耀. 葡萄座腔菌科研究进展——鉴定, 系统发育学和分子生态学. 生态学报, 2011, 31(11): 3197-3207. |
| [35] | Edwards S V. Is a new and general theory of molecular systematics emerging? Evolution, 2009, 63(1): 1-19. |
| [36] | Olson P D, Tkach V V. Advances and trends in the molecular systematics of the parasitic Platyhelminthes. Advances in Parasitology, 2005, 60: 165-243. |
| [37] | Wolfe A D, Randle C P. Recombination, heteroplasmy, haplotype polymorphism, and paralogy in plastid genes: implications for plant molecular systematics. Systematic Botany, 2004, 29(4): 1011-1020. |
| [38] | Subramaniam S, Pandey A K, Geeta R, Mort M E. Molecular systematics of Indian Crotalaria (Fabaceae) based on analyses of nuclear ribosomal ITS DNA sequences. Plant Systematics and Evolution, 2013, 299(6): 1089-1106. |
| [39] | Gunderson J H, Elwood H, Ingold A, Kindle K, Sogin M L. Phylogenetic relationships between chlorophytes, chrysophytes and oomycetes. Proceedings of the National Academy of Sciences of the United States of America, 1987, 84(16): 5823-5827. |
| [40] | Sawayama S, Inoue S, Yokoyama S Y. Phylogenetic position of Botryococcus braunii (Chlorophyceae) based on small subunit of ribosomal RNA sequence data. Journal of Phycology, 1995, 31(3): 419-420. |
| [41] | Senousy H H, Beakes G W, Hack E. Phylogenetic placement of Botryococcus braunii (Trebouxiophyceae) and Botryococcus sudeticus isolate UTEX2629 (Chlorophyceae). Journal of Phycology, 2004, 40(2): 412-423. |
| [42] | Weiss T L, Spencer Johnston J, Fujisawa K, Sumimoto K, Okada S, Chappell J, Devarenne T P. Phylogenetic placement, genome size, and GC content of the liquid-hydrocarbon-producing green microalga Botryococcus braunii strain Berkeley (Showa) (Chlorophyta). Journal of Phycology, 2010, 46(3): 534-540. |
| [43] | Weiss T L, Spencer Johnston J, Fujisawa K, Okada S, Devarenne T P. Genome size and phylogenetic analysis of the A and L races of Botryococcus braunii. Journal of Applied Phycology, 2011, 23(5): 833-839. |
| [44] | Molnár I, Lopez D, Wisecaver J H, Devarenne T P, Weiss T L, Pellegrini M, Hackett J D. Bio-crude transcriptomics: Gene discovery and metabolic network reconstruction for the biosynthesis of the terpenome of the hydrocarbon oil-producing green alga, Botryococcus braunii race B (Showa). BioMed Central Genomics, 2012, 13: 576-576. |
| [45] | 王朋云, 茅云翔, 孔凡娜, 马梅, 马飞. 丛粒藻形态多样性与遗传多样性研究. 中国海洋大学学报: 自然科学版, 2011, 41(5): 63-70. |
| [46] | 王朋云. 丛粒藻形态多样性、遗传多样性分析与培养条件优化 [D]. 青岛: 中国海洋大学, 2010. |
| [47] | 冯建祥, 黄敏参, 黄茜, 郭婕敏, 林光辉. 稳定同位素在滨海湿地生态系统研究中的应用现状与前景. 生态学杂志, 2013, 32(4): 1065-1074. |
| [48] | Kwak T J, Zedler J B. Food web analysis of southern California coastal wetlands using multiple stable isotopes. Oecologia, 1997, 110(2): 262-277. |
 2015, Vol. 35
2015, Vol. 35