文章信息
- 董鲜, 郑青松, 王敏, 周金燕, 沈其荣, 郭世伟
- DONG Xian, ZHENG Qingsong, WANG Min, ZHOU Jinyan, SHEN Qirong, GUO Shiwei
- 香蕉幼苗三类有机小分子溶质对尖孢镰刀菌侵染的生理响应
- Physiological response of three types of organic small molecule solutes in banana seedlings to Fusarium oxysporum infection
- 生态学报, 2015, 35(10): 3309-3319
- Acta Ecologica Sinica, 2015, 35(10): 3309-3319
- http://dx.doi.org/10.5846/stxb201306261785
-
文章历史
- 收稿日期:2013-06-26
- 网络出版日期:2014-05-30
香蕉枯萎病又称香蕉巴拿马病、香蕉黄叶病,是一种毁灭性的土传病害[1, 2],其病原菌为尖孢镰刀菌古巴专化型[Fusarium oxysporum f. sp. Cubense (FOC)]。根据其对不同香蕉栽培种的致病性差异,该病原菌分为4个生理小种[3],其中生理小种4号致病力最强,几乎可以侵染所有的香蕉种类。该病原菌能够在土壤中以厚垣孢子的形式存活较长时间,高温多湿天气有利于病害侵染和扩展。香蕉枯萎病发病机制,一直存在两个学说,分别是导管阻塞学说和毒素学说。导管阻塞学说认为病原菌侵染植物之后,在维管束组织中会形成胼胝质、侵填体、胶质等物质阻塞导管,最终使得地上部缺水死亡。毒素学说认为病原菌的次生代谢产物会对植株产生毒害作为,例如破坏植株细胞膜,干扰植株组织发挥功能等[4]。香蕉枯萎病的发病症状主要表现为病株凋萎和维管束变色腐烂[5, 6],从苗期到成株期均能染病,但在植株将要抽蕾时症状变得明显。发病初期,下层叶片及靠外的叶鞘变黄色,之后自下往上逐渐扩散,直至整株叶片均凋萎下垂。切开病株球茎和假茎,可见维管束呈现红棕色或褐色斑点状,靠近茎基部变色越深,病株的根系最终变黑死亡。
香蕉枯萎病为系统性维管束病害,病原菌通过根系侵入并沿着维管束向地上部扩展,最终导致植株枯萎死亡[4, 7]。由于该病菌在土壤中存活时间长,可通过土壤、水和农具等媒介传播,致病力强,感染率高,防治难度极大,目前尚未有特效药剂。研究[8, 9]表明,不同植物的根系分泌的氨基酸、有机酸和酚酸的种类和数量有明显差异,并且这些物质的含量与种类和植物的抗病性密切有关,且植物产生或累积的氨基酸、有机酸、酚酸等也可构成连作障碍的重要因素,其对抗病性的促进或降低均有不同文献报道,主要取决于氨基酸、有机酸和酚酸的种类的差异[8, 9],缺乏深入而全面的研究。国内外关于这些物质的变化与病原微生物之间关系的研究也鲜有触及。将物质变化-病原菌-植株作为一个整体进行考虑探究连作障碍机制显然具有迫切性和重要意义。本研究致力于分析尖孢镰刀菌侵染香蕉植株后,植物体内几种对病原菌生长有重要作用的物质(氨基酸、酚酸、有机酸)种类和含量的变化,以期从病原菌和植株互作角度揭示香蕉枯萎病抗性的生理机制,为进一步阐明香蕉连作障碍机制提供理论依据。
1 材料与方法 1.1 供试材料香蕉(Musa paradisiaca)品种:巴西香牙蕉,由南京农业大学海南试验基地提供。香蕉枯萎病病原菌:尖孢镰刀菌古巴专化型 (Fusarium oxysporum f. sp. cubense) 4号生理小种,来自南京农业大学植物营养与施肥系菌种保存室。
1.2 试验设计与处理组培香蕉苗栽培在无菌石英砂中,待组培苗长至2叶1心时移栽至2.5 L塑料桶里,每个塑料桶里培养4株,移苗后每4 d换一次营养液,采用Hoagland营养液配方[10],培养温度为28℃,相对湿度为(70±10)%,每天光照时间为14 h。待香蕉幼苗长至5—6叶期时,随机选取30株幼苗在浓度为1×106的尖孢镰刀菌悬浮液中浸根2 h,另选取30株幼苗在无菌水中浸根相同时间。试验共计2个处理,即对照(NI)和接种病原菌处理(I)。接种病原菌之后,于4、8、12和16 d采样,分别代表病原菌侵染的4个阶段,每次采样各处理5个重复。每次样品采集之后液氮冻干,保存于-20℃冰箱中,样品采集完成后用于氨基酸、有机酸和酚酸种类和含量的分析测定。
1.3 测定指标与方法 1.3.1 病原菌侵染植株病情分级病原菌侵染16 d后,根据植株叶片失绿程度对植株进行病情分级,即1级为轻病株:2—3个下部叶片失绿;2级为重病株:4—5个下部叶片失绿。
1.3.2 株高、鲜重、干重与相对含水量的测定从桶中取出植株,先用自来水冲洗,再用蒸馏水将鲜样洗净,用吸水纸吸干表面水分,自植株茎基部分为地上部和根部两部分,地上部再分为叶片和假茎两部分,称得鲜重(FW),自假茎基部到地上部顶端量得株高,然后在 105℃杀青 15 min 后于75℃烘干至恒重,称得干重(DW)。植株含水量计算依据公式:
含水量(%)=(鲜重-干重)/鲜重×100
1.3.3 氨基酸种类和含量的测定0.5 g冻干磨碎的香蕉植株叶片和根系粉末用3%三氯乙酸溶液稀释,样品混合液在室温中放置1 h,随即在转速10000 r/min离心15 min。收集上清液,0.45 μm微孔滤膜过滤,-20℃冰箱存储直至分析时候取出[11]。游离氨基酸含量用高效氨基酸分析仪(Hitachi,Japan)测定,分离主要用离子交换色谱柱(﹟2622SC PF),流动相为PF1、PF2、PF3、PF4、PF-RG、R-3、C-1,茚三酮溶液和缓冲液(Wako,Japan),测定时用的标准样品为type ANII和type B(Wako-shi,Japan)。
1.3.4 有机羧酸种类和含量的测定2.0 g冻干的植株样品在研钵中用5 mL超纯水研磨成匀浆液,之后在转速16000 r/min下离心20 min。收集上清液用高效液相色谱(HPLC)分析有机酸(苹果酸、柠檬酸、草酸、琥珀酸和延胡索酸)的含量[12]。测样条件为:XDB-C18色谱柱(4.6×250 mm,Agilent,USA),流动相分别为5 mmol/L H2SO4(A)和色谱纯甲醇(B)。
流动相梯度设置 0 min:95% A 和 5% B,流速为0.4 mL/min,运行10 min;15 min:90% A 和10% B,流速为 0.4 mL/min;16 min:90% A 和10% B,流速为0.4 mL/min;20 min:90% A和10% B,流速为0.5 mL/min;之后90% A 和10% B,流速为0.5 mL/min直至程序停止。
紫外检测波长为210 nm,分别配置好单个标准样品和5种物质的混合标准样品,进样后确定每种物质的保留时间,根据标准样品各个物质的保留时间,确定待测样品中的物质成分和含量[13]。
1.3.5 香蕉植株叶片与根系有机酚酸种类和含量的测定2.0 g冻干的植株样品在研钵中用5 mL色谱纯甲醇研磨成匀浆液,之后在转速16000 r/min离心15 min,上清液蒸干之后用2 mL超纯水溶解,之后用高效液相色谱(HPLC)分析酚酸(对香豆酸、β-羟基苯甲酸、绿原酸、邻苯二甲酸、咖啡酸、丁香酸、阿魏酸、水杨酸、根皮苷、肉桂酸)。
测样条件为XDB-C18色谱柱(4.6 mm×250 mm,Agilent,USA),流动相为2% 醋酸(A)和乙腈(B)梯度洗脱。
流动相梯度设置 0 min:95% A和5% B,流速为0.5 mL/min,运行10 min;25 min:95% A 和5% B,流速为1 mL/min;40 min:87% A和13% B,流速为1 mL/min;50 min:65% A和35% B,流速为1 mL/min直到程序停止。
紫外检测波长为280 nm,分别配置好单个标准样品和5种物质的混合标准样品,进样后确定每种物质的保留时间,根据标准样品各个物质的保留时间,确定待测样品中的物质成分和含量[14]。
1.4 数据处理与统计分析试验数据用Microsoft Excel和SAS 9.0软件进行数据的处理、统计分析和显著性水平检验,数据均为“平均数±标准差”格式。
2 结果与分析 2.1 病原菌侵染后植株生物量与含水量的变化病原菌侵染4 d,从植株外观上看不到伤害特征,侵染8 d,一些植株上有轻微症状,侵染12 d,症状较为明显,处理16 d,不同处理植株外观形态表现出显著的差异,取样测定分析结果(表 1)。病原菌侵染植株16 d,发病植株不同器官含水量和生物量相对于未侵染植株均不同程度的降低,且发病越严重的植株,降低幅度越大。相对于未侵染植株,重病株株高降低22%,叶片、假茎和根干重分别降低43%、21%和37%。
| 株高、生物量和含水量 Plant height,biomass and water content | 未侵染植株 Non-infected plants | 侵染植株 Infected plants | |
| 轻病株Light-disease plants | 重病株Heavy-disease plants | ||
| DW:干重 Dry weight;在同一行中不同的小写字母表示差异达到显著水平(P < 0.05) | |||
| 株高 Plant height/cm | 11.16±0.78 a | 9.64±0.23 b | 8.76±0.40 c |
| 叶片干重 Leaf DW/(g干重/株) | 0.80±0.15 a | 0.51±0.06 b | 0.46±0.04 b |
| 叶片含水量Leaf water content/% | 92.46±0.25 a | 92.03±0.19 b | 91.72±0.42 b |
| 假茎干重 Leaf DW /(g干重/株) | 0.29±0.06 a | 0.24±0.03 ab | 0.23±0.04 b |
| 假茎含水量Leaf water content/% | 96.74±0.06 a | 96.12±0.19 b | 95.81±0.14 b |
| 根干重 Leaf DW /(g干重/株) | 0.22±0.03 a | 0.17±0.04 b | 0.14±0.02 b |
| 根含水量Leaf water content/% | 95.66±0.21 a | 94.77±0.24 b | 94.75±0.31 b |
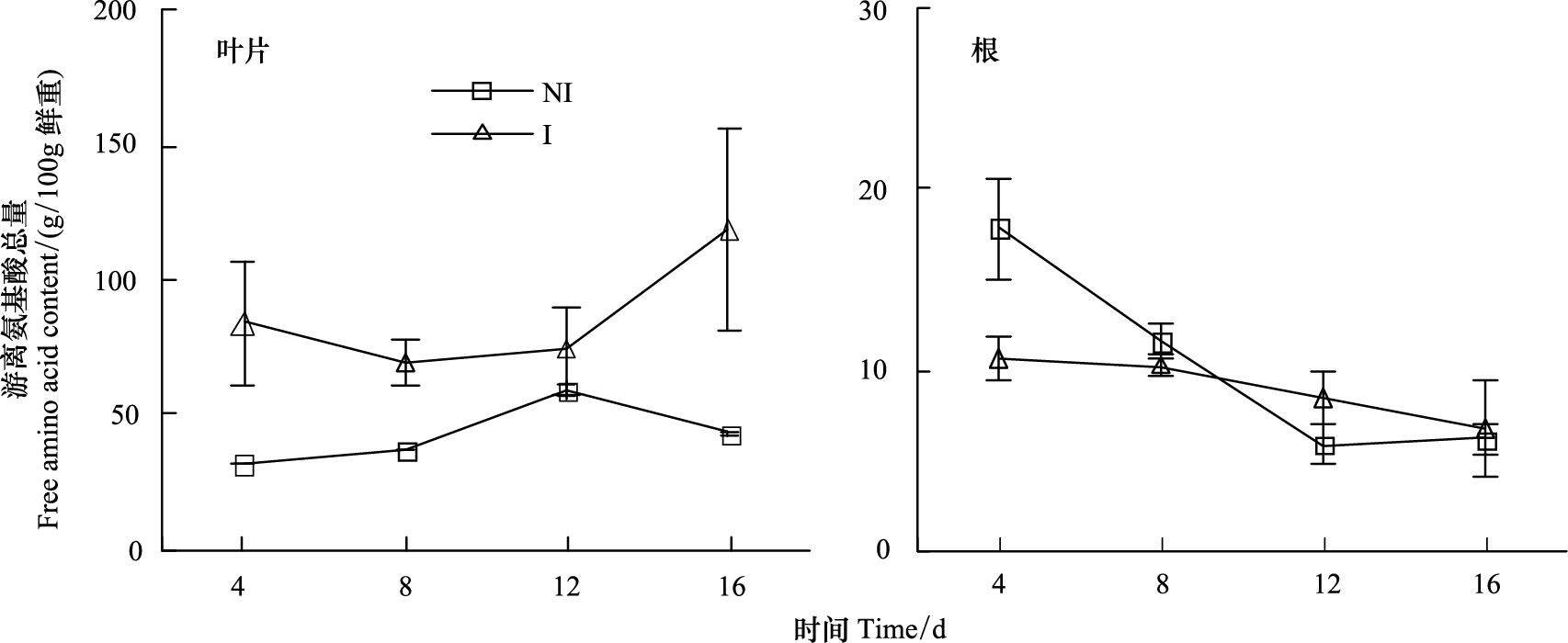
由图 1可得出,叶片中氨基酸总含量明显高于根的,并且侵染植株叶片中氨基酸总含量显著累积。在根系中,病原菌侵染4 d后,根部氨基酸总量显著低于未侵染植株根系的,之后这种差异逐渐不显著,并且无论是未侵染植株还是病原菌侵染植株,氨基酸总量随植株的生长都有一个降低的趋势。
|
| 图1 尖孢镰刀菌侵染对香蕉叶片和根中游离氨基酸总量的影响 Fig.1 Effects of infection by F. oxysporum on free amino acid content in both banana leaves and roots I:接种病原菌处理;NI:对照,即未接种病原菌处理 |
尖孢镰刀菌侵染后,植株叶片氨基酸总量显著增加(图 1)。病原菌侵染4 d,在叶片中,对比侵染与未侵染叶片,可以看到,苏氨酸(Thr)仅在侵染植株叶片中检测到,半胱氨酸(Cys)、酪氨酸(Tyr)、蛋氨酸(Met)在两个处理叶片中均未检测到,其余种类的氨基酸在两个处理中均能检测到,其中除了缬氨酸(Val)外,在侵染植株叶片中各种氨基酸含量均不同程度的高于未侵染植株叶片。病原菌侵染8 d,在叶片中,Thr在不同处理中均未检测到,Cys和Met含量均很低,分别仅仅在未侵染植株叶片和侵染植株叶片可测到;其它氨基酸在不同处理均能检测到,且侵染植株叶片中各种氨基酸含量均不同程度的高于未侵染植株叶片的。病原菌侵染12 d,Val和Thr仅在侵染植株叶片中检测到,但Cys未检测到;其它氨基酸在不同处理均能检测到,其中除了丝氨酸(Ser)外,且侵染植株叶片中各种氨基酸含量均不同程度的高于未侵染植株叶片的。病原菌侵染16 d,在侵染植株叶片中Cys和Thr未检测到,在其他检测到的氨基酸中,除了丙氨酸外,侵染植株叶片中各种氨基酸含量均不同程度的高于未侵染植株叶片的(表 2)。
在根系中,侵染与未侵染植株氨基酸种类差异不大(表 3),但氨基酸总量均逐渐显著降低(图 1)。病原菌侵染4 d后,在根系中,侵染植株氨基酸总量下降显著(图 1),其中以Ser、Ala、甘氨酸(Gly)、异亮氨酸(Ile)等下降较为显著(表 3)。病原菌侵染8、12、16 d后,侵染与未侵染植株氨基酸总量差不多(图 1),体现在具体的氨基酸含量上(表 3)。
| 氨基酸种类Amino acids | 4 d | 8 d | 12 d | 16 d | ||||
| 未侵染 NI | 侵染 I | 未侵染 NI | 侵染 I | 未侵染 NI | 侵染 I | 未侵染 NI | 侵染 I | |
| NI:未侵染植株 Non-infected plants; I:侵染植株Infected plants;nd代表未检测到数据 | ||||||||
| 天冬氨酸 (Asp)/(g/100g鲜重) | 5.94±0.29 | 15.06±6.64 | 6.44±0.02 | 9.14±0.80 | 6.87±0.41 | 8.31±0.61 | 8.13±0.71 | 12.81±2.85 |
| 丝氨酸 (Ser)/(g/100g鲜重) | 8.70±0.57 | 19.95±8.55 | 9.92±0.41 | 20.60±2.19 | 21.0±0.70 | 18.09±4.21 | 7.43±0.47 | 52.99±13.81 |
| 谷氨酸 (Glu)/(g/100g鲜重) | 9.66±0.42 | 17.03±7.17 | 11.8±0.06 | 18.48±3.99 | 13.0±0.70 | 15.50±0.11 | 11.11±0.50 | 14.55±1.11 |
| 甘氨酸 (Gly)/(g/100g鲜重) | 0.22±0.02 | 0.49±0.16 | 0.22±0.00 | 0.36±0.07 | 0.27±0.0 | 0.47±0.06 | 0.17±0.02 | 1.09±0.37 |
| 丙氨酸 (Ala)/(g/100g鲜重) | 2.15±0.15 | 7.50±3.21 | 2.55±0.11 | 2.78±0.37 | 3.15±0.13 | 3.50±0.12 | 2.79±0.09 | 2.68±0.22 |
| 缬氨酸 (Val)/(g/100g鲜重) | 1.47±0.10 | 1.25±0.76 | 0.93±0.01 | 2.19±0.19 | nd | 3.58±1.13 | 1.38±0.10 | 8.53±3.25 |
| 异亮氨酸(Ile)/(g/100g鲜重) | 0.50±0.02 | 1.06±0.81 | 0.35±0.01 | 1.40±0.16 | 0.90±0.03 | 2.55±0.90 | 1.00±0.07 | 4.38±1.27 |
| 亮氨酸 (Leu)/(g/100g鲜重) | 0.77±0.04 | 0.89±0.49 | 0.50±0.02 | 2.47±0.3 | 1.52±0.04 | 3.96±1.24 | 1.67±0.05 | 3.78±0.88 |
| 苯丙氨酸(Phe)/(g/100g鲜重) | 0.58±0.02 | 0.85±0.08 | 0.47±0.01 | 0.98±0.05 | 0.86±0.01 | 1.68±0.32 | 0.84±0.04 | 1.73±0.64 |
| 组氨酸 (His)/(g/100g鲜重) | 0.71±0.03 | 1.22±0.43 | 0.84±0.00 | 1.70±0.29 | 1.81±0.07 | 2.41±0.67 | 1.89±0.12 | 6.66±1.54 |
| 赖氨酸 (Lys)/(g/100g鲜重) | 1.59±0.07 | 2.67±0.55 | 0.84±0.00 | 2.80±0.24 | 2.10±0.04 | 3.29±1.3 | 1.72±0.06 | 3.22±1.58 |
| 精氨酸 (Arg)/(g/100g鲜重) | 2.82±0.32 | 4.21±2.33 | 0.85±0.01 | 1.21±0.17 | 2.95±0.04 | 6.00±2.23 | 1.87±0.05 | 3.38±0.63 |
| 半胱氨酸 (Cys)/(g/100g鲜重) | nd | nd | 0.15±0.00 | nd | 1.12±0.32 | nd | 0.03±0.00 | nd |
| 苏氨酸 (Thr)/(g/100g鲜重) | nd | 3.89±1.62 | nd | nd | nd | 3.43±0.74 | 1.98±0.10 | nd |
| 酪氨酸 (Tyr)/(g/100g鲜重) | nd | nd | 0.22±0.01 | 0.87±0.07 | 0.51±0.01 | 1.63±0.63 | 0.56±0.04 | 2.21±0.86 |
| 蛋氨酸 (Met)/(g/100g鲜重) | nd | nd | nd | 0.24±0.08 | 0.22±0.01 | 0.33±0.10 | 0.29±0.04 | 0.36±0.22 |
| 氨基酸种类Amino acids | 4 d | 8 d | 12 d | 16 d | ||||
| 未侵染 NI | 侵染 I | 未侵染 NI | 侵染 I | 未侵染 NI | 侵染 I | 未侵染 NI | 侵染 I | |
| nd代表未检测到数据 | ||||||||
| 天冬氨酸 (Asp)/(g/100 g鲜重) | nd | nd | nd | 1.08±0.32 | 0.53±0.10 | 0.67±0.08 | 0.55±0.04 | nd |
| 丝氨酸 (Ser)/(g/100 g鲜重) | 8.06±0.53 | 3.35±1.04 | 5.43±0.35 | 4.40±0.05 | 2.69±0.45 | 3.19±1.57 | 2.73±0.14 | 2.63±1.20 |
| 谷氨酸 (Glu)/(g/100 g鲜重) | 1.50±0.09 | 1.39±0.02 | 1.64±0.13 | 1.66±0.06 | 0.68±0.01 | 0.79±0.09 | 0.77±0.14 | 0.39±0.22 |
| 甘氨酸 (Gly)/(g/100 g鲜重) | 0.13±0.02 | 0.07±0.01 | 0.07±0.00 | 0.08±0.01 | 0.08±0.03 | 0.10±0.02 | 0.07±0.01 | 0.06±0.02 |
| 丙氨酸 (Ala)/(g/100 g鲜重) | 2.79±1.23 | 1.80±0.11 | 1.47±0.36 | 1.01±0.29 | 1.09±0.49 | 1.36±0.14 | 0.84±0.06 | 0.73±0.25 |
| 缬氨酸 (Val)/(g/100 g鲜重) | 0.34±0.06 | 0.23±0.03 | 0.27±0.03 | 0.33±0.03 | 0.28±0.04 | 0.40±0.00 | 0.29±0.05 | 0.34±0.23 |
| 异亮氨酸(Ile)/(g/100 g鲜重) | 0.12±0.02 | 0.05±0.01 | 0.08±0.00 | 0.11±0.00 | 0.11±0.01 | 0.17±0.03 | 0.13±0.01 | 0.13±0.09 |
| 亮氨酸 (Leu)/(g/100 g鲜重) | 0.16±0.03 | 0.08±0.01 | 0.12±0.11 | 0.11±0.00 | 0.11±0.01 | 0.17±0.02 | 0.13±0.01 | 0.25±0.14 |
| 苯丙氨酸(Phe)/(g/100 g鲜重) | 0.08±0.01 | 0.10±0.02 | 0.09±0.00 | 0.10±0.00 | 0.09±0.01 | 0.14±0.00 | 0.08±0.00 | 0.08±0.00 |
| 组氨酸 (His)/(g/100 g鲜重) | 0.21±0.03 | 0.18±0.05 | 0.16±0.02 | 0.23±0.03 | 0.11±0.01 | 0.31±0.05 | 0.12±0.01 | 0.50±0.10 |
| 赖氨酸 (Lys)/(g/100 g鲜重) | 0.24±0.03 | 0.21±0.02 | 0.23±0.03 | 0.27±0.03 | 0.18±0.01 | 0.27±0.01 | 0.14±0.02 | 0.20±0.04 |
| 精氨酸 (Arg)/(g/100 g鲜重) | 0.17±0.02 | 0.15±0.03 | 0.16±0.01 | 0.21±0.04 | nd | nd | nd | 0.22±0.13 |
| 半胱氨酸 (Cys)/(g/100 g鲜重) | 0.16±0.05 | 0.07±0.01 | 0.03±0.01 | 0.05±0.00 | 0.010±0.00 | nd | 0.03±0.01 | nd |
| 苏氨酸 (Thr)/(g/100 g鲜重) | nd | nd | nd | nd | nd | nd | nd | nd |
| 酪氨酸 (Tyr)/(g/100 g鲜重) | nd | nd | nd | nd | nd | nd | 0.06±0.01 | nd |
| 蛋氨酸 (Met)/(g/100 g鲜重) | nd | nd | nd | nd | nd | nd | nd | nd |
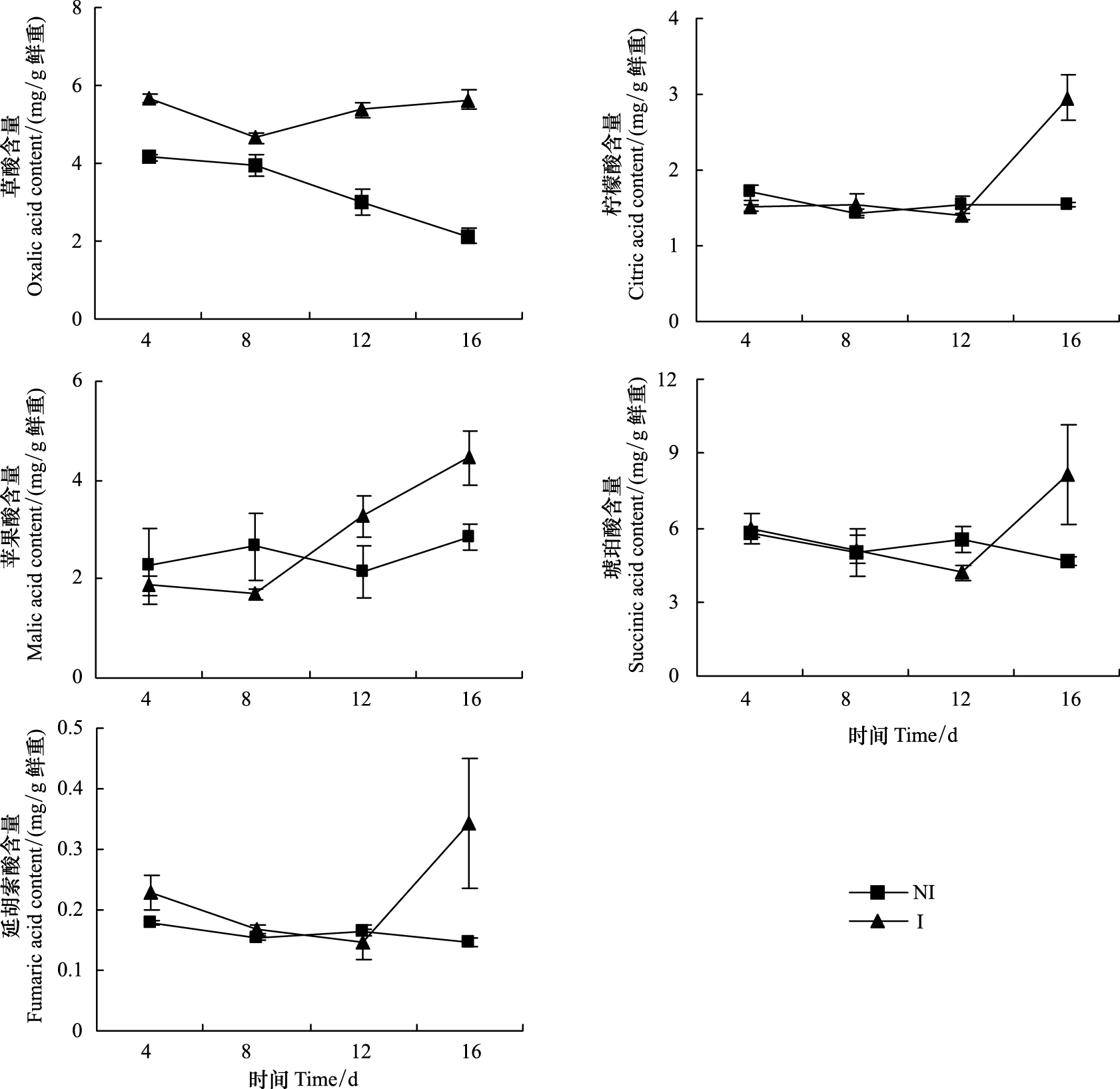
病原菌侵染植株叶片不同天数后,检测出的5种主要有机羧酸含量变化差异很大(图 2)。草酸含量在整个病原菌侵染时期,其含量均显著高于对照。柠檬酸含量在病原菌侵染4、8、12 d,其含量均无明显变化,侵染16 d,其含量显著增加。苹果酸含量在病原菌侵染12 d后,其含量显著高于对照,之后含量持续升高。琥珀酸和延胡索酸含量变化趋势较为相似,直到后期阶段含量才显著升高。病原菌侵染植株16 d后,叶片中草酸、柠檬酸、苹果酸、琥珀酸和延胡索酸分别是未侵染植株含量的2.6、1.6、1.9、1.8和2.3倍(图 2)。
|
| 图2 尖孢镰刀菌侵染香蕉对植株叶片中草酸、柠檬酸、苹果酸、琥珀酸和延胡索酸含量的影响 Fig.2 Effects of infection by F. oxysporum on contents of oxalic acid,citric acid,malic acid,succinic acid and fumaric acid in banana leaves |
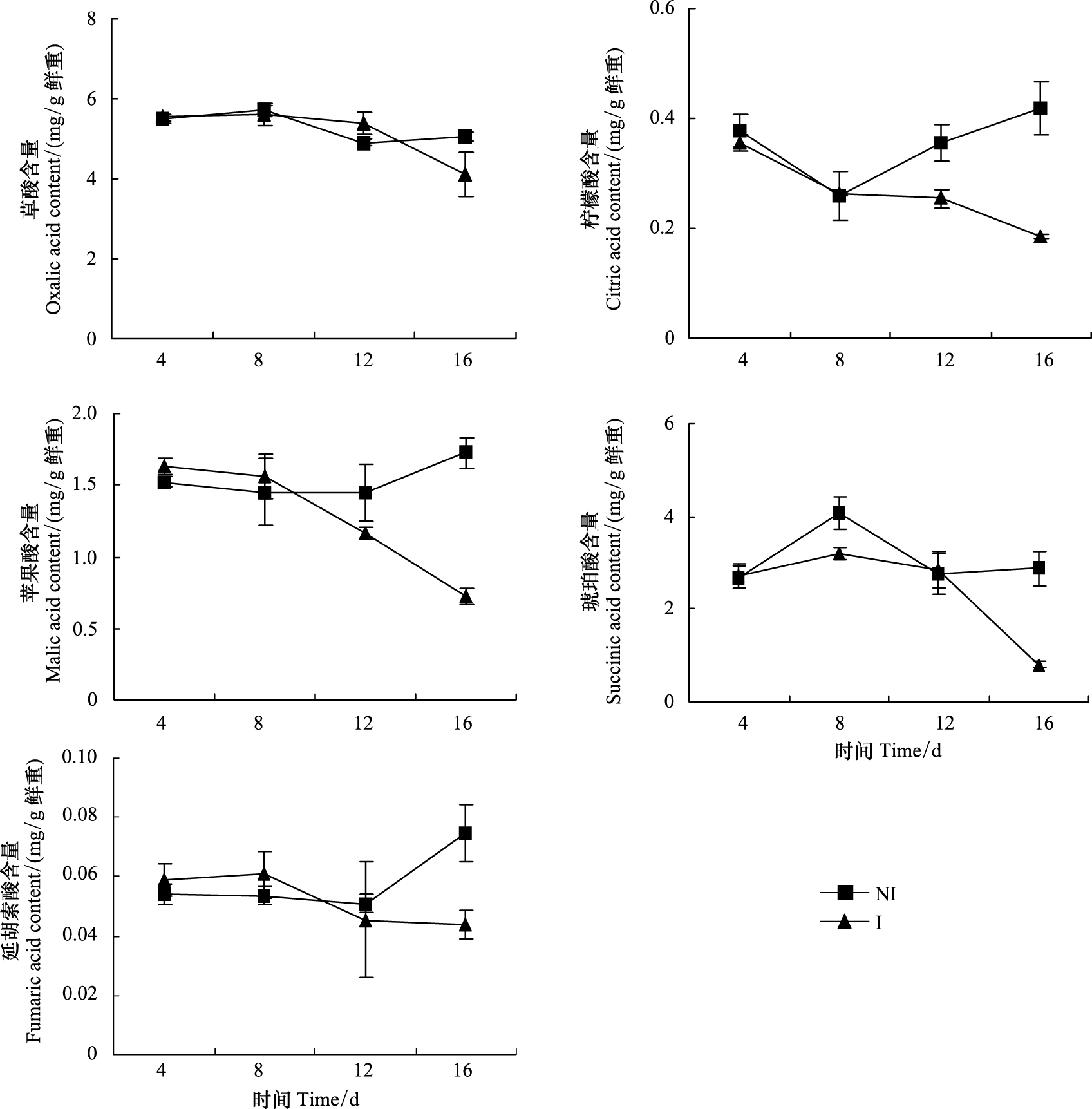
随着病原菌侵染时间的延长,根中的5种主要有机羧酸含量均显著下降,其中,侵染4 d,柠檬酸含量就显著下降,而另外4种有机羧酸下降的慢(图 3)。病原菌侵染植株16 d,根中草酸、柠檬酸、苹果酸、琥珀酸和延胡索酸分别是未侵染植株根中含量的81%、42%、44%、28%和59%。
|
| 图3 尖孢镰刀菌侵染香蕉对植株根中草酸、柠檬酸、苹果酸、琥珀酸和延胡索酸含量的影响 Fig.3 Effects of infection by F. oxysporum on contents of oxalic acid,citric acid,malic acid,succinic acid and fumaric acid in banana roots |
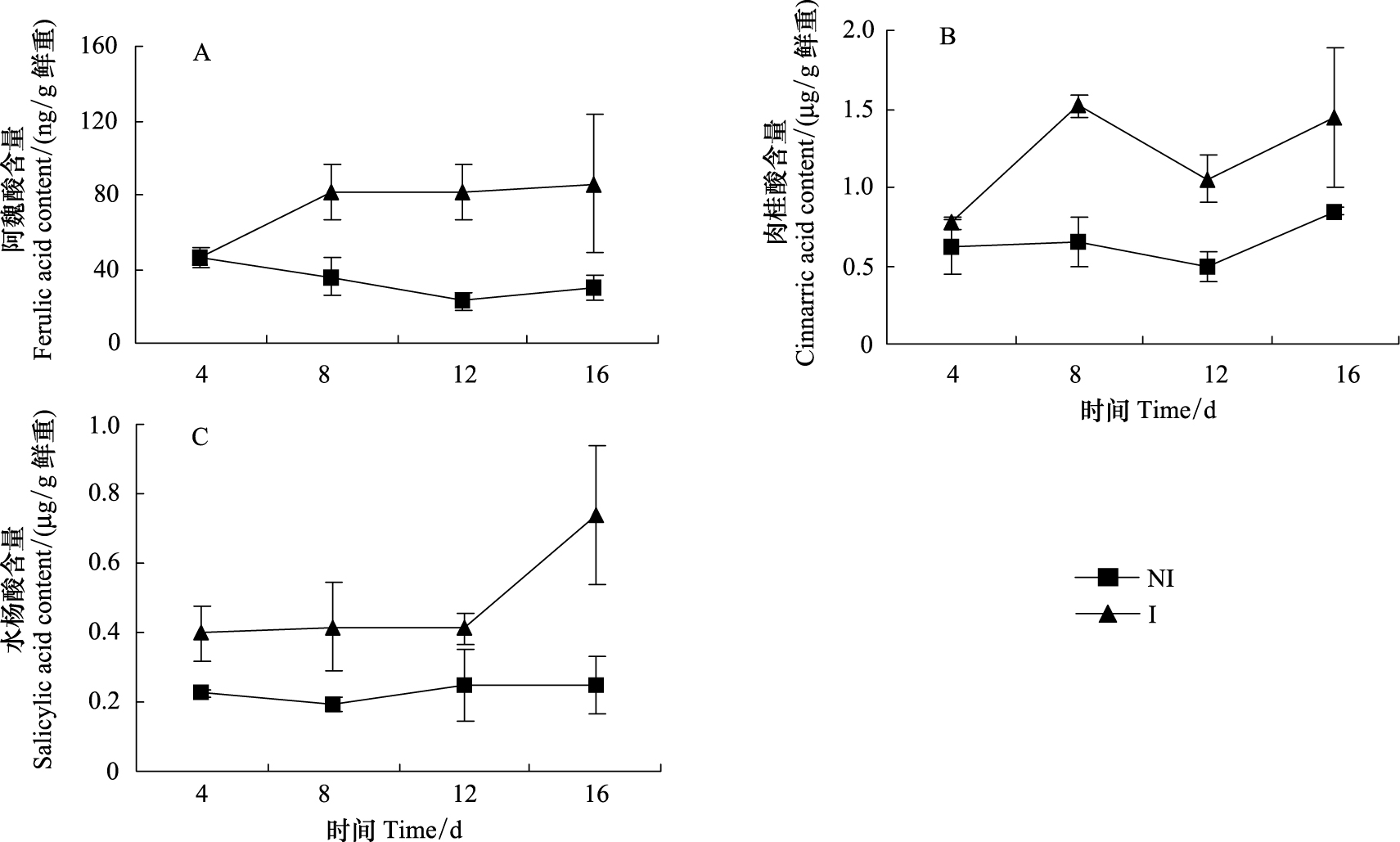
在植株叶片中,能检测到3种酚酸,分别是阿魏酸,肉桂酸和水杨酸。除了4 d的阿魏酸含量(图 4),在整个病原菌侵染时期,3种有机酚酸含量均显著高于未侵染植株的(图 4)。病原菌侵染16 d之后,阿魏酸,肉桂酸和水杨酸其含量分别是未侵染植株的2.9、1.7和2.9倍。
|
| 图4 尖孢镰刀菌侵染香蕉对植株叶片中阿魏酸、肉桂酸和水杨酸含量的影响 Fig.4 Effects of infection by F. oxysporum on contents of ferulic acid,cinnaric acid and salicylic acid in banana leaves |
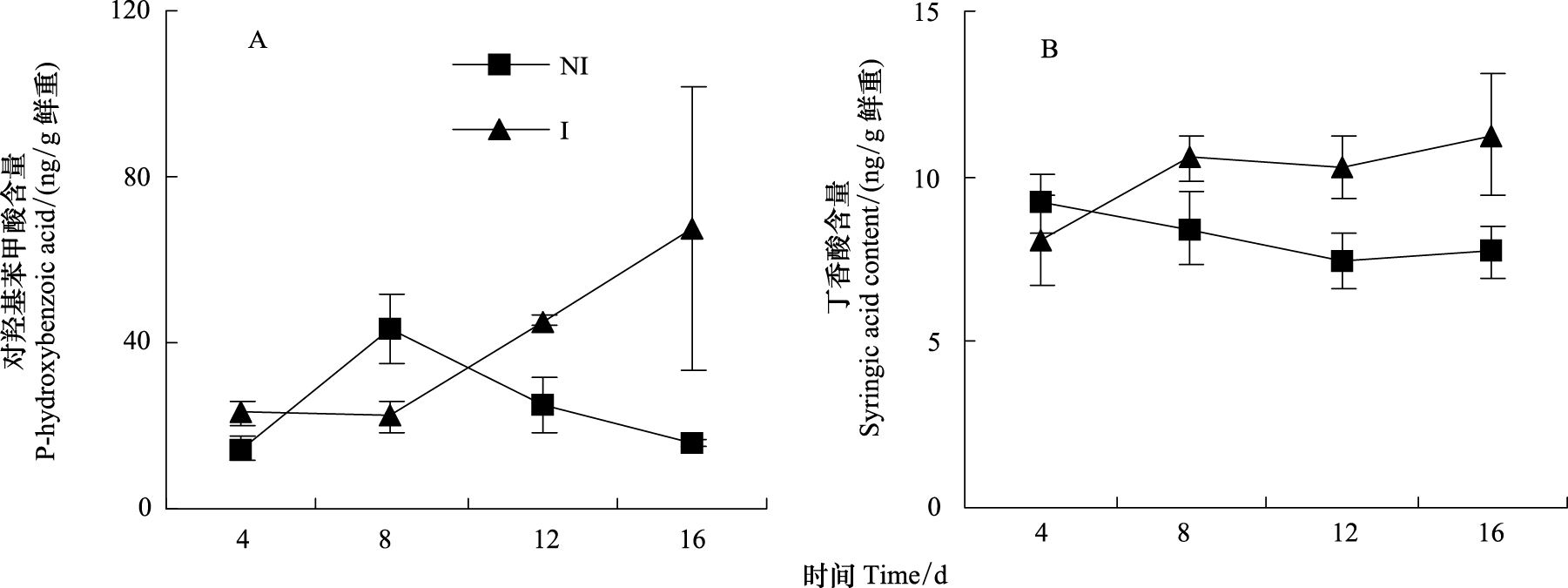
由图 5可知,在根系中,仅能检测到两种酚酸,即对羟基苯甲酸和丁香酸。其中,对羟基苯甲酸含量在病原菌侵染12d后含量显著升高,丁香酸含量在病原菌侵染8 d后相对于对照处理显著升高。病原菌侵染16 d后,对羟基苯甲酸和丁香酸含量分别是侵染植株的4.3和1.5倍。
|
| 图5 尖孢镰刀菌侵染香蕉对植株根中对羟基苯甲酸和丁香酸含量的影响 Fig.5 Effects of infection by F. oxysporum on contents of P-hydroxybenzoic acid and syringic acid in banana roots |
香蕉镰刀菌枯萎病,已经成为威胁香蕉产业的最大因素之一,几乎危害所有的香蕉栽培品种,且有进一步蔓延的趋势,目前为止没有有效的药剂抑制该病害的发生[15]。培育出优质、高产的抗病品种是彻底有效地防治香蕉枯萎病最根本的的措施,但迄今为止培育出的抗性品种数量有限,并且成本较高,并多为品质不佳,难以获得蕉农的认可而无法推广。因此,寻求其他防治香蕉枯萎病的措施迫在眉睫,而在此之前,明确香蕉枯萎病发病机制是寻找防治措施的基础。
尖孢镰刀菌是一种土壤习居菌,在土壤中能存活多年,当受到植株根系分泌物的刺激之后,厚垣孢子开始萌发,从根系侵染植株并以小型分生孢子的形态随蒸腾流由植株根部沿维管束向地上部运输。在运输过程中,病原菌会产生对植株有毒的次生代谢产物,其中尖孢镰刀菌酸(FA)是研究较多的一种尖孢镰刀菌的次生代谢产物[16]。在病原菌向上运输过程中,植物会作出相应的抗性反应,例如在维管束中产生胼胝质、侵填体、胶质等物质,从而堵塞导管,达到阻止病原菌向上运输的目的[17]。由于病原菌侵染对植株细胞膜以及相应生理过程的影响,植株水分平衡会被打破[4]。植株的养分状况很大程度上决定了植株形态组织水平、对病害的抗性程度以及病原菌在其体内的存活能力;其中,营养元素影响植物、病原菌和微生物的生长,在病害控制中扮演着重要角色。氨基酸是组成蛋白质的基本单位,也是蛋白质的分解产物,植物根系吸收、同化的氮素主要以氨基酸和酰胺的形式进行运输。大多数氨基酸在低浓度范围内可作为一种碳源,被微生物所吸收利用,因此对病原微生物的生长是有益的,但其被吸收利用的过程目前还不是十分清楚。根据氨基酸对病原菌生长的不同作用,将其分为促菌氨基酸和抑菌氨基酸[18]。促菌氨基酸包括:天冬氨酸、谷氨酸、甘氨酸、丙氨酸、缬氨酸、异亮氨酸、亮氨酸、苯丙氨酸、组氨酸、半胱氨酸、苏氨酸、酪氨酸、蛋氨酸;抑菌氨基酸包括:丝氨酸、赖氨酸、精氨酸。但是也有其他人的研究结果与此不一致,不同研究间的结果差异可能是由于研究所用病原菌种类不同而导致的[19]。本研究中,对比侵染与未侵染植株,叶片中促菌氨基酸含量增加显著的有天冬氨酸、甘氨酸、亮氨酸、组氨酸,缬氨酸等,叶片中抑菌氨基酸含量增加显著的有丝氨酸、赖氨酸、精氨酸等(表 2)。相对叶片,根中氨基酸含量偏低,每种氨基酸含量在侵染前后差异程度没有叶片高,但从侵染后的氨基酸总量可以看出,侵染后叶片氨基酸总量升高,而根中氨基酸总量降低(表 2,表 3)。病原菌为了定殖于寄主植物,它需要适应寄主环境,并且调节自己的形态,生理代谢以及分泌的次生代谢产物和蛋白等[20]。所以,病原菌为了侵染植株并在其体内生长,它会使得植株合成更多的有利于其定殖的氨基酸种类,并运输到根系供其吸收利用。但同时,植物体也会作出相应的抗性反应,合成较多的抑菌氨基酸。在黄瓜[18]和茄子[21]上的研究结果表明,感病植株根系分泌物中氨基酸种类多,数量大,能够促进病原菌的生长,增加了植株根际病害发病率。在香蕉上研究也支持了这一点。本研究中,香蕉植株中促菌氨基酸的种类要高于抑菌氨基酸种类,并且在叶片中的增加幅度要高于抑菌氨基酸的,所以虽然植物有抗性反应,但最终病原菌的侵染使得植株发病加重(表 1)。
有文献[22]报道,有机羧酸能够使有益细菌发生趋化性,有利于植物生长和提高植株的抗病性。有机酸在植物体内具有相当重要的作用,它既是各种氨基酸合成的底物,又是植物体内各种物质代谢的连接点。草酸、苹果酸、柠檬酸都是三羧酸循环中的中间物质,它们参与作物体内的合成代谢。因此,它们在植物体内含量的高低,直接与植物生长、发育及其抗性有关。在本研究中,病原菌侵染不同阶段,这些有机羧酸含量变化差异很大。叶片中草酸、柠檬酸、苹果酸、琥珀酸、延胡索酸含量在病原菌侵染后,其含量显著升高;在根系中,其含量随病原菌侵染显著降低(图 2,图 3)。这一方面可能由于病原菌侵染使得根系细胞膜破裂,一部分有机酸渗漏,所以使得其含量在根系中降低;另一方面由于植株想合成更多的氨基酸供给根系以及有机酸本身有渗透调节作用,所以其含量在叶片中显著增加。
植物的一个重要防御机制是积累可溶的或细胞壁束缚态的酚类化合物[23]。酚类物质是一种重要的化感物质。尖孢镰刀菌能够感应到酚类物质的存在并做出相应的反应。有研究[24, 25]表明,在培养基中添加肉桂酸、香豆酸、香草酸等物质能够增加毒素的产量和水解酶的活性,例如果胶酶和纤维素酶。同时,这些物质又对病原菌的生长和孢子萌发有抑制作用。很显然,从抑制病原菌生长的作用来看,植物合成的酚类物质有一定的保护功能,但从提高毒素和水解酶产生的作用来看同样又有促进病害发生的效果。本研究中,在植株叶片能检测到3种酚酸,分别是阿魏酸、肉桂酸和水杨酸(图 4)。其中,阿魏酸和肉桂酸在病原菌侵染8 d后,其含量持续升高,水杨酸含量在病原菌侵染4 d,相对于对照处理,其含量即持续升高。在根中,仅能检测到两种酚酸,分别是对羟基苯甲酸和丁香酸。其中,对羟基苯甲酸含量在病原菌侵染12 d后含量显著升高,丁香酸含量在病原菌侵染8 d后相对于对照处理显著升高(图 4,图 5)。水杨酸、对羟基苯甲酸低浓度对病原菌生长没有明显的作用,但是高浓度下,抑制孢子萌发,所以它们对尖孢镰刀菌的影响可能与其在分泌物中的浓度有关[24, 25]。肉桂酸能够加剧根系的氧化胁迫使其根系更易受镰刀菌侵染而有助于枯萎病的发生。阿魏酸随着其浓度的升高,能够促进孢子萌发和增加其产孢子能力,但丁香酸对病原菌生长还不明确,所以,很显然,酚酸类物质对植物的自毒作用也是促进连作障碍发生的重要因素[21, 26, 27]。
综上所述,尖孢镰刀菌侵染后,植物与病原菌的相互作用使得植物体内抑菌物质和促菌物质都会相应的增加,如叶片氨基酸含量显著增加。其中大多数氨基酸为促菌氨基酸,典型的如缬氨酸、组氨酸和异亮氨酸等。而一些抑菌氨基酸如丝氨酸、赖氨酸、精氨酸等也显示增加,同时叶片中有机羧酸的显著积累,说明香蕉植株对病害有一定的抗性。氨基酸、有机酸和酚酸的种类和数量与植物对病原菌的抗性密切相关,阐明三者之间的关系深入研究及有机酚酸累积的抑菌或促菌作用有待深入研究。
| [1] | Leong S K, Latiffah Z, Baharuddin S. Molecular characterization of Fusarium oxysporum F. Sp. Cubenseof banana. American Journal of Applied Sciences, 2009, 6(7): 1301-1307. |
| [2] | 张志红, 彭桂香, 李华兴, 蔡燕飞, 张新明, 赵兰凤. 生物肥与甲壳素和恶霉灵配施对香蕉枯萎病的防治效果. 生态学报, 2011, 31(4): 1149-1156. |
| [3] | Subramaniam S, Maziah M, Sariah M, Puad M P, Xavier R. Bioassay method for testing Fusarium wilt disease tolerance in transgenic banana. Scientia Horticulturae, 2006, 108(4): 378-389. |
| [4] | Dong X, Ling N, Wang M, Shen Q R, Guo S W. Fusaric acid is a crucial factor in the disturbance of leaf water imbalance in Fusarium-infected banana plants. Plant Physiology and Biochemistry, 2012, 60: 171-179. |
| [5] | Di Pietro A, Madrid M P, Caracuel Z, Delgado-Jarana J, Roncero M I G. Fusarium oxysporum: exploring the molecular arsenal of a vascular wilt fungus. Molecular Plant Pathology, 2003, 4(5): 315-325. |
| [6] | Knogge W. Fungal infection of plants. The Plant Cell, 1996, 8(10): 1711-1722. |
| [7] | Baker R A, Nemec S. Soybean sudden death syndrome: isolation and identification of a new phytotoxin from cultures of the causal agent, Fusarium solani. Phytopathology, 1994, 84: 1144-1144. |
| [8] | 韩雪, 潘凯, 吴凤芝. 不同抗性黄瓜品种根系分泌物对枯萎病病原菌的影响. 中国蔬菜, 2006, (5): 13-15. |
| [9] | 袁虹霞, 李洪连, 王烨, 房卫平, 王振跃. 棉花不同抗性品种根系分泌物分析及其对黄萎病菌的影响. 植物病理学报, 2002, 32(2): 127-131. |
| [10] | 毛达如. 近代植物营养科学的方法论. 植物营养与肥料学报, 1994, (1): 1-5. |
| [11] | Kim M Y, Chung I M, Lee S J, Ahn J K, Kim E H, Kim M J, Kim S L, Moon H I, Ro H M, Kang E Y, Seo S H, Song H K. Comparison of free amino acid, carbohydrates concentrations in Korean edible and medicinal mushrooms. Food Chemistry, 2009, 113(2): 386-393. |
| [12] | Wang J F, Zhou Y, Zhou C X, Shen Q R, Putheti R. Effects of NH4+-N/NO3-N ratios on growth, nitrate uptake and organic acid levels of spinach (Spinacia oleraceaL.). African Journal of Biotechnology, 2009, 8(15): 3597-3602. |
| [13] | Ling N, Raza W, Ma J H, Huang Q W, Shen Q R. Identification and role of organic acids in watermelon root exudates for recruiting Paenibacillus polymyxa SQR-21 in the rhizosphere. European Journal of Soil Biology, 2011, 47(6): 374-379. |
| [14] | Ling N, Huang Q W, Guo S W, Shen Q R. Paenibacillus polymyxa SQR-21 systemically affects root exudates of watermelon to decrease the conidial germination of Fusarium oxysporumf. sp. niveum. Plant and Soil, 2011, 341(1/2): 485-493. |
| [15] | 姬华伟, 郑青松, 董鲜, 周金燕, 沈其荣, 郭世伟. 铜、锌元素对香蕉枯萎病的防治效果与机理. 园艺学报, 2012, 39(6): 1064-1072. |
| [16] | Bouizgarne B, El-Maarouf-Bouteau H, Frankart C, Reboutier D, Madiona K, Pennarun A M, Monestiez M, Trouverie J, Amiar Z, Briand J, Brault M, Rona J P, Ouhdouch Y, El Hadrami I, Bouteau F. Early physiological responses of Arabidopsis thalianacells to fusaric acid: toxic and signalling effects. New Phytologist, 2006, 169(1): 209-218. |
| [17] | Mepsted R, Flood J, Cooper R M. Fusariumwilt of oil palm II. Stunting as a mechanism to reduce water stress. Physiological and Molecular Plant Pathology, 1995, 46(5): 373-387. |
| [18] | 潘凯, 吴凤芝. 枯萎病不同抗性黄瓜 (Cucumis sativus L.) 根系分泌物氨基酸组分与抗病的相关性. 生态学报, 2007, 27(5): 1945-1950. |
| [19] | 甄文超, 王晓燕, 曹克强, 靳增军. 草莓根系分泌物和腐解物中氨基酸的检测及其化感作用研究. 河北农业大学学报, 2004, 27(2): 76-80. |
| [20] | Michielse C B, Rep M. Pathogen profile update: Fusarium oxysporum. Molecular Plant Pathology, 2009, 10(3): 311-324. |
| [21] | 周宝利, 陈志霞, 杜亮, 谢玉宏, 叶雪凌. 不同抗病性茄子根系分泌物对黄萎菌的化感作用. 生态学报, 2011, 31(14): 3964-3972. |
| [22] | Ling N, Raza W, Ma J H, Huang Q W, Shen Q R. Identification and role of organic acids in watermelon root exudates for recruiting Paenibacillus polymyxa SQR-21 in the rhizosphere. European Journal of Soil Biology, 2011, 47(6): 374-379. |
| [23] | de Ascensao A R F D C, Dubery I A. Soluble and wall-bound phenolics and phenolic polymers in Musa acuminata roots exposed to elicitors from Fusarium oxysporum f. sp. cubense. Phytochemistry, 2003, 63(6): 679-686. |
| [24] | Wu H S, Raza W, Fan J Q, Sun Y G, Bao W, Shen Q R. Cinnamic acid inhibits growth but stimulates production of pathogenesis factors by in vitro cultures of Fusarium oxysporumf. sp. niveum. Journal of Agricultural and Food Chemistry, 2008, 56(4): 1316-1321. |
| [25] | Wu H S, Raza W, Liu D Y, Wu C L, Mao Z S, Xu Y C, Shen Q R. Allelopathic impact of artificially applied coumarin on Fusarium oxysporum f. sp. niveum. World Journal of Microbiology and Biotechnology, 2008, 24(8): 1297-1304. |
| [26] | 郝文雅, 冉炜, 沈其荣, 任丽轩. 西瓜、水稻根分泌物及酚酸类物质对西瓜专化型尖孢镰刀菌的影响. 中国农业科学, 2010, 43(12): 2443-2452. |
| [27] | 黄玉茜, 韩立思, 杨劲峰, 王月, 韩晓日. 花生植株和土壤水浸液自毒作用研究及土壤中自毒物质检测. 生态学报, 2012, 32(19): 6023-6032. |
 2015, Vol. 35
2015, Vol. 35




