文章信息
- 陈启东, 邓孺孺, 秦雁, 熊龙海, 何颖清
- CHEN Qidong, DENG Ruru, QIN Yan, XIONG Longhai, HE Yingqing
- 不同生长状态珊瑚光谱特征
- Analysis of spectral characteristics of coral under different growth patterns
- 生态学报, 2015, 35(10): 3394-3402
- Acta Ecologica Sinica, 2015, 35(10): 3394-3402
- http://dx.doi.org/10.5846/stxb201306261783
-
文章历史
- 收稿日期:2013-06-26
- 网络出版日期:2014-05-30
2. 珠江水利科学研究院, 广州 510611
2. Pearl River Hydraulic Research Institute, Guangzhou 510611, China
珊瑚礁大面积覆盖且生长在清澈浅海水域,遥感技术是调查和监测珊瑚礁结构组成的一种有效手段[1]。由于高生物多样性以及复杂的形态异质性,这些重要的生态系统在遥感监测时会遇到光谱识别困难。珊瑚礁栖底物质反射光谱在光学上相似,高光谱分辨率传感器才可能感知这些细微的差异[2]。近年来也有大量将高光谱技术应用于珊瑚礁生态环境领域的研究[2, 3, 4, 5, 6, 7, 8],Holden[2]现场测量133条不同状态珊瑚的光谱,对数据进行统计分析得出珊瑚形态没有光谱差异,但珊瑚的健康程度影响光谱。Hochberg等[7, 8]测量了12种珊瑚礁栖底物质的光谱(400—700 nm,1 nm间隔),指出珊瑚、海藻的反射率值都比较低;沙的反射率值最高,缺少峰谷特征,最容易与其它物质区分。这些研究结果表明珊瑚的反射光谱有共同的特征,可通过遥感手段从其它栖底物质中区分出珊瑚。目前对珊瑚光谱测量分析还远远不足,利用光谱识别珊瑚礁组成部分大多集中在生态层次如珊瑚、海草、海藻和钙质沙等,较少研究例如硬石珊瑚光谱在物种层次上是否可区分。
珊瑚的光谱特性及其变化均较为复杂,甚至同种珊瑚的光谱也存在明显差异,充分理解珊瑚光谱总体趋势和变异原因是进行光谱识别的关键。由于测量方法、数据质量不一致及缺乏因果关系的光谱环境,判别不同生长状态珊瑚光谱特征存在一些不确定性。本文采用统一的测量方法对西沙群岛常见的健康、白化珊瑚以及藻类覆盖的死珊瑚光谱进行测量,旨在分析石珊瑚光谱特征和不同状态的光谱差异,并探讨其特征光谱的成因。目的是确定根据它们的光学特征能否准确地被识别,寻找区分它们的敏感波段,建立珊瑚礁生长状态遥感判别方法,为今后珊瑚礁定量遥感提供依据。
1 研究区选择在海南省三沙市西沙群岛开展实验测量。西沙群岛珊瑚礁生态系统是我国最具代表性的珊瑚礁生态系统之一,生态系统结构最为完整,造礁石珊瑚种类约占我国石珊瑚种类的3/4。目前也面临着荒漠化和特色海洋生物资源濒危的问题,而且随着未来三沙市人类活动的加强,对研究区珊瑚礁生态系统的监测和保护工作显得尤为重要。出于实际野外数据采集的可行性,选取其中的永兴岛、石岛、西沙洲、赵述岛、北岛、南沙洲和银砾滩附近礁盘作为样品采集区。采样点位置如图 1所示。

|
| 图 1 研究区及采样点位置 Fig.1 Location of study area and sampling stations |
珊瑚光谱测量方法目前尚无一种通用的标准,常见有水表测量法和水下测量法[9],水下测量法在原位状态下进行,测量时珊瑚生态习性保持完全一致,但水下测量的入射光场常受到水表波浪以及光衰减等影响而不稳定,特别在浅水区常出现光闪烁现象导致测量误差很大。本文采取的是水表测量法,潜水采集珊瑚样品取出水面,立即在船上进行光谱测量。采用荷兰Avantes公司开发生产的AvaField便携式野外双通道光谱仪,测量光谱范围为200—1100 nm,光谱分辨率为2.4 nm,光谱采样间隔为0.6 nm,视场角为25°,实验前对仪器及参考板进行严格标定。野外光谱测量的具体时间为2012年5月,测试时间一般选择在当地时间10:00—14:00进行,与卫星传感器过顶的时间基本相同或相近。珊瑚样品大小一般在5—30 cm,在测量过程中保持样品湿润,并保证仪器视场角均落在珊瑚表面。另外为了模拟比较珊瑚死亡过程中光谱的变化,分别在采样后5d和1个月后再进行1次光谱测量。
物体反射率是反射辐射通量占入射辐射通量的比例,是波长的函数。测量时光谱仪两个光纤探头分别近垂直对准珊瑚样品和参考板,同时获得两者的反射光能量,通过比值计算得到目标物体反射率(式1)。使用双通道光谱仪可以有效地避免自然阳光的波动导致测量误差,增加数据的可靠性。
式中,Lc、Lp分别为珊瑚样品和参考板的反射光辐亮度,由光谱仪测量得到;Rc、Rp分别为珊瑚样品和参考板的反射率,Rp经过计量部门标定是已知值,故可算出样品反射率Rc。
实测光谱数据在波长350 nm之前的紫外波段噪声很大,900 nm之后由于水汽吸收的影响,有些值不尽合理予以剔除。350—900 nm数据质量较好,对合理值取平均,同时将反射率插值为波长间隔1 nm,得到该珊瑚的光谱曲线。
2.2 数据分析方法光谱曲线间的差异体现在反射率大小和波形上。为了确定珊瑚礁生长状态遥感的可行性和探寻识别的敏感波段,对光谱数据进行相关分析,主要从典型珊瑚反射率、主成分分析和导数光谱3个方面进行。主成分分析检测光谱在反射率大小上的区别;光谱导数分析可以更仔细地检查特定波长的光谱差异,增加一些类别的可分性。
主成分分析作为数据降维技术,是一种识别数据主导模式的方法。可以统计分析珊瑚种内和种群间的光谱差异,找出各类型最有代表性的光谱,从而判断各类型间光谱是否可区分。当种内所有光谱有相似特征时,大多数方差保留在第一成分中。相对于使用平均值或主观选择代表性的光谱,主成分是更有效的。
导数光谱可以增强光谱曲线在坡度上的微小差别,突出反射光谱中的特征,解决很多定量分析问题,相比比值法和差异法更有效。计算光谱导数的近似方法是将连续光谱值的差除以它们的波长间隔 (式2—式3)。一阶导数反映光谱曲线的变化率信息,而二阶导数揭示曲线凹凸形状信息。波长λi处反射率的一阶导数FDR(λi)和二阶导数DDR(λi):
式中,R(λi)表示波长λi处的反射率。
3 结果与分析选用几种常见造礁石珊瑚,有健康杯形珊瑚(Pocillopora verrucosa)、健康和白化鹿角珊瑚(Acropora brueggemanni)、健康和白化蜂巢珊瑚(Favia speciosa),块状白化珊瑚(未定种)。这里健康和白化是通过人工判定的典型状态。以下分别对典型健康珊瑚、白化珊瑚以及明显藻类覆盖死珊瑚的光谱特征进行分析,在此基础上应用更广泛数据进行可分性分析及判别准则确立。
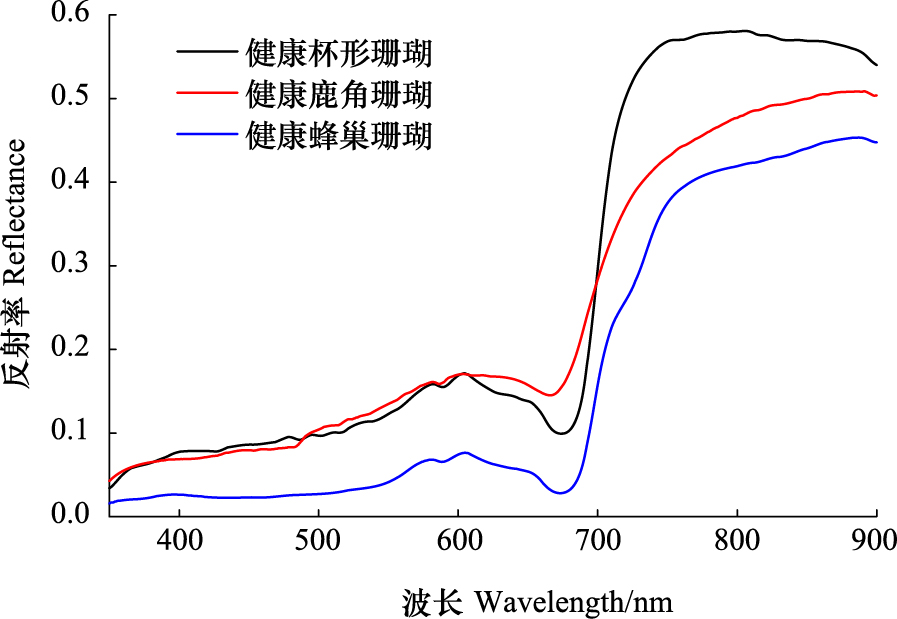
3.1 健康珊瑚光谱特征3种健康珊瑚光谱曲线有显著差异,但也有共同特征(图 2):曲线形状相似,可见光反射率值均较低,其中蓝绿波段更低,主要是共生藻光合作用吸收的结果;在反射率光谱的675 nm波段都有明显的由于色素吸收引起的谱形凹陷;在700 nm后的红边波段,反射率急剧上升增加数倍;近红外强反射,一般都在30%以上甚至达60%,高值表明缺乏吸收或存在活跃的荧光。该图中杯形珊瑚、蜂巢珊瑚表现明显的三重峰模式,这种模式Myers等[5]也曾发表过评论。其特点是350—550 nm低反射率和近575、605和650 nm有反射峰。鹿角珊瑚这3个反射峰不太突出。总体来说,杯形珊瑚和蜂巢珊瑚光谱形状比较相似,但光谱值大小有明显差异,可见光波段相差一倍有余;红边区域差异明显,杯形珊瑚光谱增幅最大,鹿角珊瑚较小,675 nm的吸收峰提前到665 nm且吸收峰不深,蜂巢珊瑚增幅先快后慢。
|
| 图 2 典型健康珊瑚光谱曲线 Fig.2 Spectral curve of typical healthy corals |
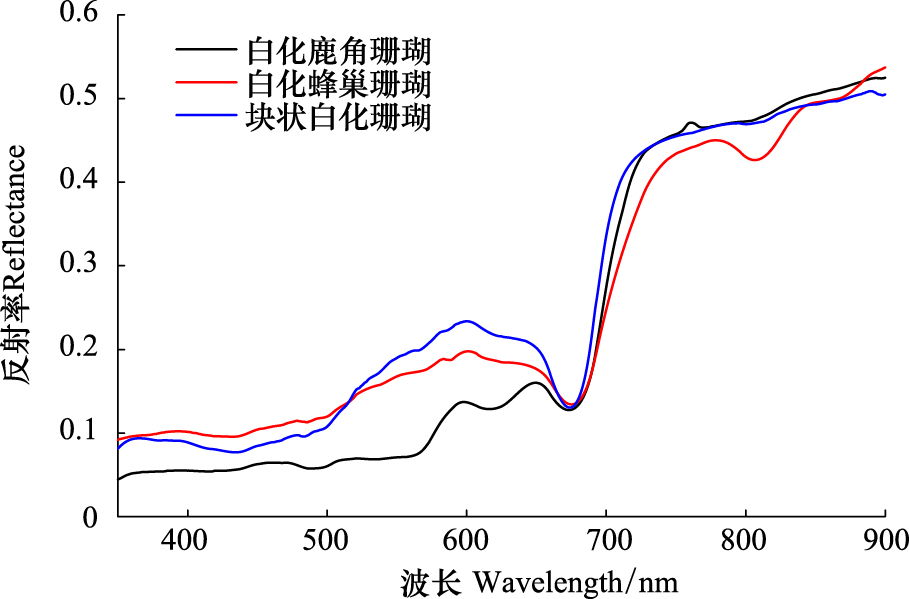
白化事件中色素或共生的虫黄藻损失导致珊瑚颜色变白,在光谱上会有反映。如图 3现场测量的3条白化珊瑚光谱,块状白化珊瑚在400—500 nm曲线下凹,500—600 nm曲线梯度较大并在600 nm达极大值约24%。白化蜂巢珊瑚与图 2健康的相比光谱增幅明显,675 nm反射率值增加了4倍;500—550 nm曲线增幅较大,575 nm处反射峰已不明显,在810 nm有明显的吸收峰;观察白化鹿角珊瑚表面有明显藻类覆盖,受藻类吸收影响反射率较低。总体来说,珊瑚白化后可见光反射率大幅升高,波形变的简单平滑,在500—600 nm曲线梯度增大;近红外变化不大甚至降低,这表明该波段从藻类反射的光可能比从组织或骨架反射的更多。
|
| 图 3 白化珊瑚光谱曲线 Fig.3 Spectral curve of bleached corals |
为了模拟珊瑚死亡过程中光谱的变化,以杯形珊瑚为例,对比采样5d和1个月后测量的光谱,图 4是3次测量的曲线及其二阶导数光谱。虽然跟真实水下白化珊瑚有区别,但可以避开藻类覆盖等环境条件的干扰,对理解珊瑚白化过程中变化及成因是有用的。可见光波段3条曲线整体依次提高,波形逐渐变得简单平直。相比现场测量,5d后测量的曲线在500—700 nm有明显提高,其中550—650 nm曲线平坦,是一个宽高原峰值,575和605 nm处反射峰不明显,650 nm处反射峰仍然保留;675 nm附近吸收峰也仍然存在但强度明显减弱,且提前到670 nm,出现红边蓝移现象。1个月后珊瑚完全死亡后测量的曲线除了在675 nm附近还留有少许吸收峰外,其它形状几乎呈直线,随波长递增,与碳酸钙骨架光谱接近。从导数光谱中也看出,3次测量中波形起伏逐渐变得平缓简单,近675 nm处吸收峰值也依次减小,且此峰位置也依次前移。

|
| 图 4 3次测量的杯形珊瑚光谱 Fig.4 Spectral curve of Pocillopora with three measurements |
珊瑚死亡后,表面容易被海藻覆盖,改变珊瑚表面的反射光谱。藻类覆盖的死珊瑚光谱与藻类类型及覆盖比例有关。图 3中白化鹿角珊瑚由于表面明显有藻类覆盖,在550—650 nm光谱形状与其它珊瑚不同,600和650 nm处是明显波峰,蓝绿波段反射率明显低于其它白化珊瑚;在570 nm处有个吸收峰,跟藻红蛋白在此处强吸收特征相吻合,推测曲线中含有了红藻光谱信息。
3次测量的白化鹿角珊瑚光谱曲线及二阶导数如图 5,现场测量的曲线波形丰富,跟健康珊瑚光谱相似;随着时间推移,表面覆盖藻类死亡或丢失,光谱曲线大幅增高,吸收峰逐渐趋于不明显;一个月后测量的样品,藻类几乎完全死亡,曲线随波长递增且反射率值明显较大,是珊瑚本底碳酸钙骨架光谱。表明珊瑚光谱反射率特性主要是由表面物质吸收作用的结果,而吸收强度与含有的藻类种类和数量密切相关。从光谱上虽然比较容易区分纯白化和健康珊瑚,实际上珊瑚死亡后,白色的骨骼持续时间很短,表面会被海藻快速覆盖重新引起色素沉着,光谱可能与健康珊瑚类似。因此,不同状态珊瑚不再是浅显的可区分,甚至常常造成误判。应用高光谱遥感定量评估珊瑚白化的程度,需要仔细检查光谱曲线,寻找可分离的判定准则。

|
| 图 5 3次测量的白化鹿角珊瑚光谱 Fig.5 Spectral curve of Acropora with three measurements |
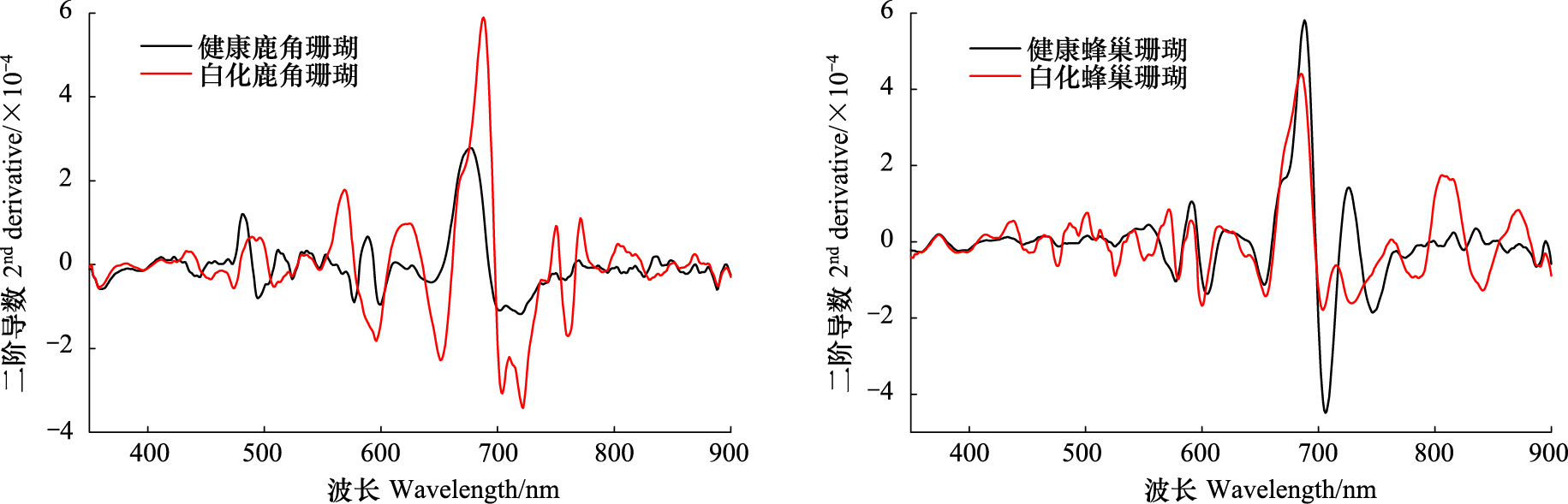
选取现场测量的同物种健康/白化鹿角珊瑚以及健康/白化蜂巢珊瑚光谱,分别计算二阶导数光谱并通过均值滤波处理,结果如图 6。二阶导数定量分析光谱曲线的相对曲率,检查光谱形状并确定曲线峰谷变化的波长位置,帮助引导波段的选择和遥感监测的判别准则。这4条导数光谱波形起伏都比较显著,共同的特征是在350—430 nm和890 nm处曲线几乎一致,其它波段波形差异明显。这两物种珊瑚,健康珊瑚共有的波峰谷波长有525、575、590和605 nm;白化珊瑚共有的波峰谷波长有475、570、655、686和705 nm。导数分析显示,白化珊瑚在430—440 nm,490—500 nm,564—577 nm,800—810 nm,860—880 nm波段是波峰且值为正,在830—843 nm之间有波谷值为负;而健康珊瑚刚相反。根据这些健康珊瑚与非健康珊瑚光谱特征,采用高光谱数据可被区分。
|
| 图 6 二阶导数光谱曲线 Fig.6 Second derivative spectra curve |
以上的分析针对选取的典型珊瑚样品光谱,区分健康和非健康珊瑚还是比较容易实现的,在更广泛的光谱数据中是否同样适用需有待检验。明显被藻类覆盖的死珊瑚光谱特征发生了变化,故和纯白化珊瑚分开单独成一类。根据人工判别将测量的120条光谱数据分成健康珊瑚、白化珊瑚和明显藻类覆盖的死珊瑚3个数据集。数据集间的光谱差异大于数据集内光谱差异,珊瑚状态的识别才可持续[10]。利用SPSS统计软件分别对这3个数据集进行主成分分析,检验光谱差异及是否可分离。考虑到实际应用中红外波段受水体衰减难以识别光谱差异,为避免这些数据在主成分分析中干扰,只选用了700 nm以内的波段。结果表明大多数的方差在第一主成分中解释,分别是健康珊瑚90%,白化珊瑚94%,明显藻类覆盖97%,分配给测定光谱的负荷都非常高,表明数据集内光谱变化小。所以第一主成分可以被认为是在数据集内的代表性光谱。使用最高载荷的第一成分计算的组分光谱如图 7,看出3种成分光谱有明显的差异,而这种差异不能归因于偶然,确认不同生长状态珊瑚光谱间有差异,可以建立相应的判别准则进行区分。

|
| 图 7 三类珊瑚第一主成分光谱 Fig.7 The first principal component spectra of three types of coral |
由于计算的组分光谱是假设的,在现实中可能不会存在,根据实测光谱建立判别准则。选取其中的58条光谱曲线,反复实验比较其导数光谱,寻找用于区分的波长范围。确定564—574 nm、520—530 nm和600—605 nm这三波段来区分,分3步骤进行,判别准则如表 1。为了测试这种识别技术的有效性,用余下的62条光谱数据进行验证,其中健康珊瑚、白化珊瑚和明显藻类覆盖的死珊瑚分别是28、27和7条。整体正确识别率优于80%。步骤一564—574 nm二阶导数为负分离出健康珊瑚,28条健康珊瑚曲线正确分出19条,有1条白化珊瑚错分成健康珊瑚;步骤二520—530 nm一阶导数大于0.0005分离出白化珊瑚,26条白化珊瑚曲线中有22条被正确分类;步骤三600—605 nm一阶导数均值为负,可以区分藻类覆盖面和余下的健康珊瑚。相对来说健康珊瑚识别准确率稍低,主要是由于珊瑚物种繁多光谱复杂,从健康珊瑚第一主成分中解释方差比例稍低也可看出。
| 步骤 Step |
判别准则Criteria | 分类Classification | 识别率Correctly identified | ||
| 健康珊瑚 Healthy |
白化珊瑚 Bleached |
藻类覆盖死珊瑚 Algae-covered |
|||
| 1 | 564—574 nm 二阶导数均值为负 | 分离出健康珊瑚 | 68%(19/28) | 4%(1/27) | 0(0/7) |
| 2 | 520—530 nm 一阶导数均值>0.0005 | 剩余曲线分出白化珊瑚 | 11%(1/9) | 92%(22/26) | 0(0/7) |
| 3 | 600—605 nm 一阶导数均值为负 | 剩余曲线分出藻类覆盖 | 25%(2/8) | 75%(3/4) | 100%(7/7) |
(1)使用比较全面的珊瑚光谱数据,主成分分析结果表明3种状态珊瑚光谱有明显差异。通过导数分析寻找判别敏感波段,最终选用3个窄波段范围564—574 nm、520—530 nm和600—605 nm。采用564—574 nm二阶导数为负判定是健康珊瑚,因为健康珊瑚一般在此波段是反射峰即二阶导数为负;而此波段藻类普遍是吸收峰,白化珊瑚曲线几乎是直线上升。珊瑚白化后由于共生藻吸收减少,500—550 nm光谱增幅很快也就是一阶导数值大,采用520—530 nm一阶导数均值大于某阈值为白化珊瑚,本文阈值0.0005是反复比较各种光谱得出。很多海藻包括常见的红藻、绿藻和褐藻光谱在595—600 nm附近有明显反射峰,600—625 nm曲线是下斜坡,故选取的600—605 nm一阶导数为负数判定藻类覆盖,而多数健康珊瑚在605 nm处是反射峰,在600—605 nm一阶导数为正。珊瑚光谱几乎所有的峰出现在狭窄的波长范围内,有时宽为20 nm,但通常为10 nm左右。选用的波段都在10 nm以内,经检验选用20 nm及以上的范围,精度会降到50%以下。充分理解珊瑚光谱的成因以及不同状态下光谱响应变化是光谱识别的关键。在缺乏因果关系的光谱环境中,光谱识别可能会得到不明确的结果[11]。Holden等[2]指出在582—686 nm是正斜率可判定表面覆盖藻类,但后来发现很多情况下是明显的负斜率[12]。数据显示褐藻满足这一判断,但红藻和绿藻不满足。Clark[6]和Holden[2, 13]都指出二阶导数可以区分健康珊瑚和死珊瑚,但他们的结果略有差异。前者指出536 nm和596 nm一阶导数值较低表示珊瑚已经死亡;而后者建议500—590 nm白化珊瑚一阶导数始终高于健康珊瑚。Holden[2]建议654—674 nm反射率的正斜率来辨别是钙质沙,这是由于缺少叶绿素a,如果钙质沙含有叶绿素a,这个判别的标准将可能失败。开发稳定的珊瑚和藻类的鉴别技术需要一个类似但更复杂的理解它们吸收和荧光对反射率的贡献。
(2)珊瑚光学特性主要受体内共生藻吸收的影响,其中共生虫黄藻在石珊瑚中普遍存在的,是一种光合甲藻[14],也是影响珊瑚光谱的重要因素。虫黄藻含有能直接参与光化学反应的叶绿素a及其它辅助色素[15]。有研究表明它们保持大致的相对浓度(叶绿素a(39%),多甲藻素(39%),叶绿素c(13%),甲藻黄素(7%),β-胡萝卜素(2%)),但绝对浓度高度可变[16]。这样虫黄藻色素对珊瑚光谱形状贡献是可预测的,但有不同的光谱反射率值大小。光谱形状主要由色素吸收决定,通过导数分析方便识别色素吸收峰特征[17]。如图 4健康杯形珊瑚导数光谱,427、470、634、665和690 nm的二阶导数峰非常显着,与主要色素吸收相关(427、665和690 nm是叶绿素a,470 nm是叶黄素,634 nm是叶绿素c2)。反射率值大小跟虫黄藻密度、体积和总色素含量等因素相关,取决于珊瑚种类和生长的环境条件。如不同光照条件色素密度会发生变化,低光强色素密度会增加,满足珊瑚生长能量的需要。另外珊瑚虫外胚层和内胚层组织以及一些物种的骨骼中也都可能含有光合色素[18]。每种色素源的变化都可能使珊瑚光谱形状和大小产生变化。虫黄藻、宿主组织和珊瑚骨架含有的色素构成了反射光谱的基础。
(3)珊瑚及海藻体内或多或少含有相同的光合色素[19],故光谱特征具有一定相似性,需要仔细检查光谱特征及原因分析,才可能持续的可区分。很多珊瑚在550—600 nm有反射峰,跟此处多甲藻-叶绿素复合物的吸光度最小相关[20]。650—690 nm光谱曲线斜率依赖于叶绿素a浓度,据此可以从含有叶绿素a的栖底生物(如藻类,珊瑚)中辨别没有藻成分的钙质沙。红藻可以通过体内的藻红蛋白在570 nm处强吸收峰的特征来辨别。Kleppel等[21]发现非白化珊瑚叶绿素c、多甲藻素和黄藻素分别是白化珊瑚的35、17和20倍,所以通常白化珊瑚反射率值更高和光谱形状光滑,原因可能是损失虫黄藻光合色素暴露了底层白色碳酸钙骨架,藻类吸收作用减弱,珊瑚组织(通过散射和荧光)改变了从骨架反射的光。分析这些光谱反射率的变化,可以在广泛范围内检测白化珊瑚。但如果海藻覆盖死珊瑚表面,海藻和虫黄藻都普遍存在叶绿素a,使用叶绿素a区别白化珊瑚或最近死去的珊瑚可能变得困难。虫黄藻含有独特的多甲藻素,可根据白化珊瑚多甲藻素浓度降低,通过500—600 nm的光谱来区分白化和健康珊瑚。本文的判定准则也根据这个特征。
(4)除了色素吸收,荧光在特定情况下有助于反射光谱。如图 4健康杯形珊瑚导数光谱,除了前面提到的由于色素吸收导致的二阶导数峰,在450—600 nm还有若干跟荧光有关的峰值。多数健康珊瑚在 680—685 nm有明显的叶绿素荧光峰,还有显着的<600 nm的荧光峰。由于虫黄藻不发出波长<675 nm的荧光,因此珊瑚宿主组织可能是较短波长荧光的来源,有研究发现在蓝、绿、橙和黄色波段的荧光[22]。450—600 nm珊瑚的宽荧光峰是多种色素激发的,其中486和515 nm荧光峰来源可能是胆蛋白质,575 nm可能是藻红蛋白[22, 23]。很多健康珊瑚呈现出575 nm附近的反射峰,荧光可能是其原因,但还没有证实是哪种色素,除了藻红蛋白,珊瑚宿主组织的荧光蛋白(FPs)也会导致约570 nm处的峰值。
5 结论本文选取西沙群岛典型珊瑚礁作为数据采集样区,对多物种不同生长状态的硬石珊瑚样品进行了反射率光谱测量,获取了丰富的实地测量数据。利用主成分和导数分析方法对珊瑚光谱特征及其成因作了分析和探讨,建立珊瑚生长状态高光谱遥感判别准则。
(1)健康珊瑚由于共生虫黄藻吸收,可见光波段反射率值均较低,光谱曲线起伏变化丰富,很多种类保持相似形状,在575、605和650 nm都呈现反射峰;珊瑚白化后损失共生藻,吸收作用减弱及珊瑚组织散射使可见光波段特别是500—650 nm反射率大幅升高;藻类覆盖的死珊瑚,重新引起色素沉着,可能会与健康珊瑚光谱相似,可利用虫黄藻含有独特的多甲藻素这一特征进行辨别。
(2)通过主成分和导数光谱分析方法,在统计学上验证3种状态珊瑚的可分性,确定可通过564—574 nm、520—530 nm和600—605 nm波段组合来识别,判别准则精度优于80%,误判的主要来源是种内珊瑚反射率差异。
(3)尽管在遥感应用中还面临诸多困难,然而这项工作提供精细尺度的珊瑚光谱分析,对传感器波段设计和珊瑚礁生态系统监测的意义。需要不断丰富光谱数据,建立全面的珊瑚礁栖底物质光谱数据库,不仅应用于遥感监测,在光合作用和辐射传输模型等研究方面都有用。
目前研究的缺点是光谱测量时探头视场范围内藻类覆盖类型和比例没有确认,光谱响应与藻类和珊瑚基底数量比值有关,故还不能定量评价藻类覆盖对光谱的影响。
| [1] | Mumby P J, Green E P, Edwards A J, Clark, C D. The cost-effectiveness of remote sensing for tropical coastal resources assessment and management. Journal of Environmental Management, 1999, 55(3): 157-166. |
| [2] | Holden H M, LeDrew E F. Hyperspectral identification of coral reef features. International Journal of Remote Sensing, 1999, 20(13): 2545-2563. |
| [3] | Hedley J D, Mumby P J, Joyce K E, Phinn S R. Spectral unmixing of coral reef benthos under ideal conditions. Coral Reefs, 2004, 23(1): 60-73. |
| [4] | Hedley J D, Roelfsema C M, Phinn S R, Mumby P J. Environmental and sensor limitations in optical remote sensing of coral reefs: implications for monitoring and sensor design. Remote Sensing, 2012, 4(1): 271-302. |
| [5] | Myers M R, Hardy J T, Mazel C H, Dustan P. Optical spectra and pigmentation of Caribbean reef corals and macroalgae. Coral Reefs, 1999, 18(2): 179-186. |
| [6] | Clark C D, Mumby P J, Chisholm J R M, Jaubert J, Andrefouet S. Spectral discrimination of coral mortality states following a severe bleaching event. International Journal of Remote Sensing, 2000, 21(11): 2321-2327. |
| [7] | Hochberg E J, Atkinson M J. Capabilities of remote sensors to classify coral, algae, and sand as pure and mixed spectra. Remote Sensing of Environment, 2003, 85(2): 174-189. |
| [8] | Hochberg E J, Atkinson M J, Apprill A, Andréfout S. Spectral reflectance of coral. Coral Reefs, 2004, 23(1): 84-95. |
| [9] | 李京, 陈云浩, 刘志刚. 海岛与海岸带环境遥感. 北京: 科学出版社, 2010: 73-73. |
| [10] | Kutser T, Jupp D L. On the possibility of mapping living corals to the species level based on their optical signatures. Estuarine, Coastal and Shelf Science, 2006, 69: 607-614. |
| [11] | Hedley J D, Mumby P J B. Biological and remote sensing perspectives of pigmentation in coral reef organisms. Advances in Marine Biology, 2002, 43(3/4): 277-317. |
| [12] | Dan L B, W, Dustan P, Mazel C H, Stamnes K. Spectral signatures of coral reefs: Features from space. Remote Sensing of Environment, 2001, 75(1): 127-137. |
| [13] | Holden H, LeDrew E. Spectral discrimination of healthy and non-healthy corals based on cluster analysis, principal components analysis, and derivative spectroscopy. Remote Sensing of Environment, 1998, 65(2): 217-224. |
| [14] | Torres-Pérez J L, Guild L S, Armstrong R A. Hyperspectral distinction of two Caribbean shallow-water corals based on their pigments and corresponding reflectance. Remote Sensing, 2012, 4(12): 3813-3832. |
| [15] | 李淑, 余克服. 珊瑚礁白化研究进展. 生态学报, 2007, 27(5): 2059-2069. |
| [16] | Gil-Turnes S, Corredor J. Studies of the photosynthetic pigments of zooxanthellae in Carribbean hermatypic corals//Gomez E D, Birkeland C E, eds. Proceedings of the Fourth International Coral Reef Symposium. Manila, Philippines: University of the Philippines, 1981: 51-54. |
| [17] | Polerecky L, Bissett A, Al-Najjar M, Faerber P, Osmers H, Suci P A, Stoodley P, de Beer D. Modular spectral imaging system for discrimination of pigments in cells and microbial communities. Applied and Environmental Microbiology, 2009, 75(3): 758-771. |
| [18] | Dove S G, Takabayashi M, Hoegh-Guldberg O. Isolation and partial characterization of the pink and blue pigments of Pocilloporid and Acroporid corals. Biological Bulletin, 1995, 189(3): 288-297. |
| [19] | 王圆圆, 刘志刚, 李京, 陈云浩. 珊瑚礁遥感研究进展. 地球科学进展, 2007, 12(4): 396-402. |
| [20] | Prézelin B, Ley A C, Haxo F T. Effects of growth irradiance on the photosynthetic action spectra of the marine dinoflagellate, Glenodinium sp. Planta, 1976, 130(3): 251-256. |
| [21] | Kleppel G S, Dodge R E, Reese C J. Changes in pigmentation associated with the bleaching of stony corals. Limnology and Oceanography, 1989, 34(7): 1331-1335. |
| [22] | Mazel C H. Spectral measurements of fluorescence emission in Caribbean cnidarians. Marine Ecology Progress Series, 1995, 120: 185-191. |
| [23] | Mazel C H. Coral fluorescence characteristics: excitation/emission spectra, fluorescence efficiences, and contribution to apparent reflectance. SPIE Proceedings, 1997, 2963: 240-245. |
 2015, Vol. 35
2015, Vol. 35







