文章信息
- 郭建国, 赵龙浩, 徐丹, 孙野青
- GUO Jianguo, ZHAO Longhao, XU Dan, SUN Yeqing
- 人工湿地处理造纸废水后细菌群落结构变化
- The bacterial community changes after papermaking wastewater treatment with constructed wetlands
- 生态学报, 2014, 34(8): 2095-2101
- Acta Ecologica Sinica, 2014, 34(8): 2095-2101
- http://dx.doi.org/10.5846/stxb201307011813
-
文章历史
- 收稿日期:2013-7-1
- 修订日期:2014-3-26
人工湿地是一类人工建造、模仿自然湿地的综合性生态体系[1],通过对自然湿地的模拟,利用人造生态系统中的物理、化学和生物的协同作用,可以促进废水中污染物质良性循环,实现对污水的净化,防止环境的再污染,获得污水处理与资源化的最佳效益。人工湿地作为一种低成本、高效率的手段早在20世纪初就开始被应用于污水的处理,目前已经被广泛用于各种污水处理;如重金属排放工业污水、生活污水、造纸污水和畜牧业废水等[2, 3, 4, 5, 6, 7, 8, 9, 10, 11]。在人工湿地的去污过程中,植物、基质和微生物共同发挥了重要的作用,其中微生物的作用最大[12, 13],是降解水体中污染物的主力军。
目前,关于人工湿地微生物的研究多集中于人工湿地基质中的不同位置,不同深度微生物群落的结构及随时间的动态演变过程[13, 14],用于探索人工湿地中稳定的微生物群落的形成规律。人工湿地处理的工业污水,大多关注于其中污染物的含量,如COD,对于排入环境的水样中微生物群落结构的研究较少,对人工湿地处理造纸污水后的微生物群落的研究更少。
造纸行业为全世界第五大能源耗费产业,也是需水量最多的行业,能够造成严重的河流污染问题,因此如何处理和净化造纸污水已经越来越受到重视。但是污水排放过程中的微生物的危害并没有引起太大关注。在微生物监测中,通常选择大肠杆菌,产气荚膜梭菌,沙门氏菌等一些生活污水中的代表性微生物,这些微生物在工业污水中有的并不具有代表性,而其他的一些代表微生物的危害性不容忽视。所以,本论文结合人工湿地对造纸污水处理后水质的情况和细菌群落的变化来研究人工湿地在污染物和病原微生物去除的双重作用,为今后人工湿地作为处理工业污水和降低病原微生物的环境排放提供有效可靠的依据。
1 材料与方法 1.1 实验材料本研究的水样于2012年8月采自辽宁省锦州市金城造纸厂排污口和人工湿地处理后的出水口。将排污口水样编号为PWK,出水口水样编号为CSK。该人工湿地为水平潜流湿地,基质填料为砾石,占地10hm2,处理规模2t4/d,主要的挺水植物为茭白、芦苇、香蒲。企业排放的污水在厂区内进行处理后,经过约2km管线输送至潜流湿地处理区的提升泵站,将污水由泵提升至潜流湿地去除多种污染物,潜流湿地出水进入渠塘湿地,最后排入大凌河。
1.2 实验方法 1.2.1 水样理化因素的测定DO由溶氧仪雷磁GTB-607A测定,pH由PH计雷磁THB-1测定,盐度S由盐度计测定,总氮、氨氮、总磷、磷酸盐、化学需氧量的测定参照《水质分析方法国家标准汇编》(1996,ISBN:7506612801)中提供的方法进行。
1.2.2 DNA的提取水样经300目的无菌纱布过滤除去大型颗粒和杂质,取 300ml,使用真空泵将水样经0.22um的硝酸纤维素膜过滤,将滤纸剪碎后,参照《分子克隆实验指南》CTAB法提取DNA。
1.2.3 变性梯度凝胶电泳(DGGE)对DNA浓度定量,以提取的水样微生物DNA为模板,用引物对U968-GC-F(5′CGCCCGGG GCGCGCCCCGGGCGGGGCGGGGGCAGGGGG GAACGCGAAGAACCTTAC3′)和L1401-R(5'CGGTGTGTACAAGACCC3′)扩增16SrDNA的V6-V8区,94℃ 5min,(94℃ 30s,55℃ 30s,72℃ 1min)30 cycles,72℃ 10min,4℃保存。PCR产物定量到400 ng进行变性梯度凝胶电泳,120V 17h,60℃保温,聚丙烯酰胺凝胶的浓度为8%,变性浓度为45%—65%。电泳结束后,进行硝酸银染色,然后利用UVP扫描仪进行扫描成像。
1.2.4 克隆测序对胶上的主要条带利用PAGE胶回收试剂盒(BIOMIGA)进行胶回收,然后利用引物B968(5′AACGCGAAGAACCTTAC3′),L1401-R进行条带扩增,对目的条带利用琼脂糖胶回收试剂盒(TIANGEN)回收,回收产物利用DNA Ligation Kit Ver.2.1(TAKARA)进行PMD18 T-vector的连接和转化,验证的阳性克隆送去Invitrogen北京分公司进行测序。
1.3 数据分析统计数据利用SPSS处理,DGGE图谱利用Quantity one对主要条带进行灰度分析,导出相应的灰度值,用于微生物多样性指数和均匀度指数的计算。测序结果已上传到NCBI数据库中,GenBank编号为:KF305475-KF305491。
2 结果与分析 2.1 人工湿地处理后的水质评价和主要污染物的检测对造纸厂排污口(PWK)和人工湿地出水口(CSK)两处水样的主要水质指标进行了测定,结果见表 1。结果表明人工湿地对污染物有较好的去除作用,水质有所改善。
|
样品
Sample | 常规指标
Conventional index | 污染物含量/(mg/L)
Concentration of pollutants | ||||||
| DO | PH | S | TN | NH+4-N | TP | PO3-P | COD | |
| 造纸厂排污口PWK | 2.35 | 6.76 | 1.23 | 3.20±0.09 | 5.86 ±1.16 | 1.49±0.08 | 0.093 ±0.010 | 141±4.6 |
| 人工湿地出水口CSK | 5.84 | 7.71 | 0.61 | 0.93± 0.10 | 1.36 ±0.10 | 0.98 ±0.09 | 0.063±0.010 | 47±3.6 |
| 去除率Removal rate/% | 70.83 | 76.79 | 34.55 | 32.26 | ||||
利用DGGE技术对造纸厂排污口(PWK)和人工湿地出水口(CSK)两处水样的微生物群落的结构进行了分析,每个采样点设两个重复样,如图 1所示,PWK样本有12条明显的条带(P1-12),CSK样本有6条明显的条带(P2,C1-5),通过比较各条带的位置发现两者之间仅有P2条带位置相同,人工湿地处理后微生物群落图谱改变。

|
| 图1 人工湿地处理前后水中微生物的图谱分析 Fig. 1, The profile of microbe in the wasterwater before and after treatment with aritficial wetland |
进一步对造纸厂排污口(PWK)和人工湿地出水口(CSK)两处水样的微生物群落进行分析如表 2,与排污口相比,出水口中微生物Shannon-Wiener′s指数、物种多度和均匀度降低,微生物结构趋于简单化,这些结果提示人工湿地处理后污染物的种类减少,导致参与污染物降解的微生物种类减少。
| 样品Sample | 多样性H | 物种多度S | 均匀度E |
| PWK | 3.7694 | 51 | 0.9587 |
| CSK | 3.1240 | 28 | 0.9375 |
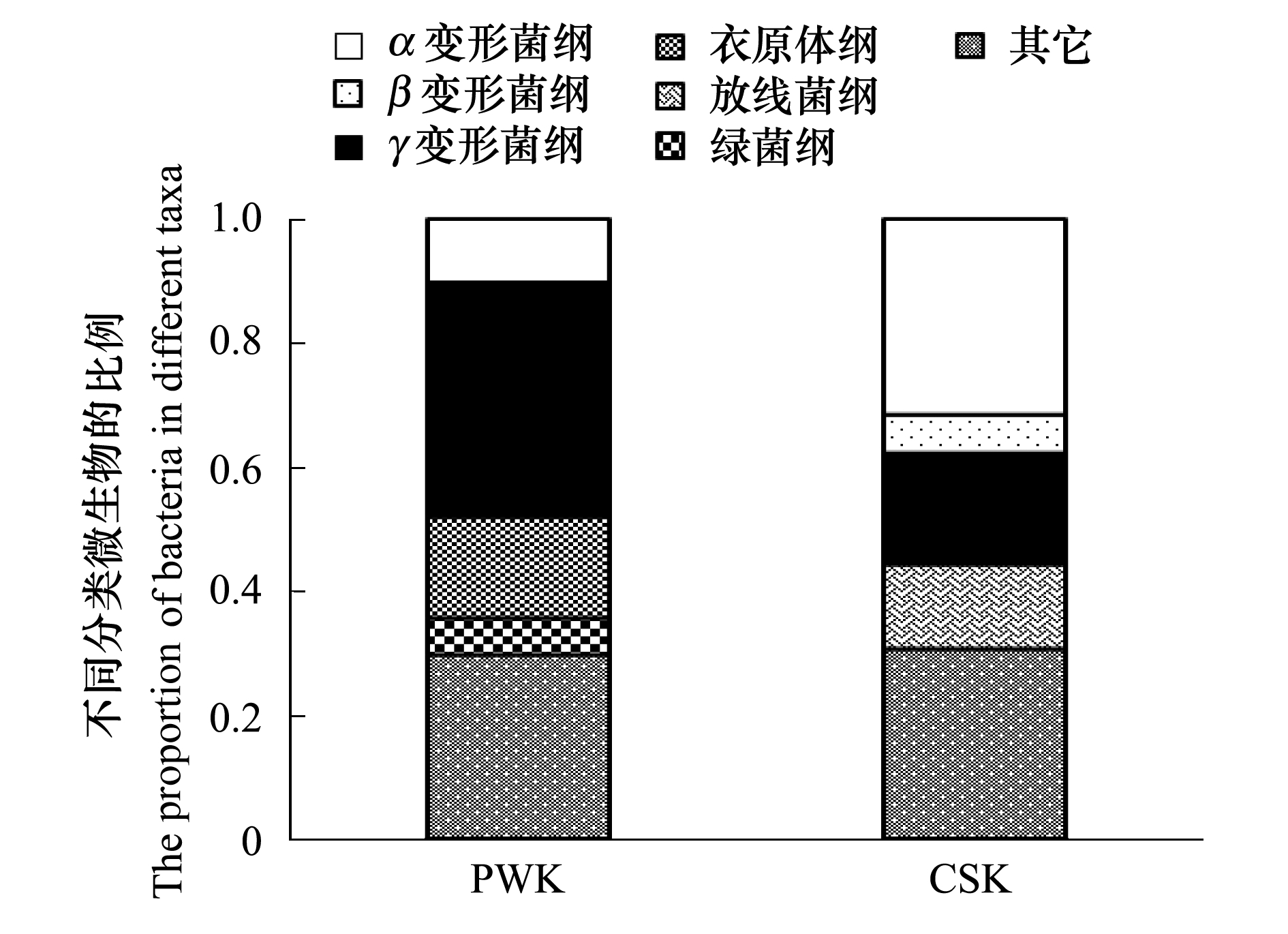
主要条带经克隆测序序列比对,分析发现17种微生物中,12个属于变形菌门。人工湿地处理前的造纸污水中以γ变形菌和衣原体为主要菌群,处理后主要以α变形菌为主,γ变形菌比例降低(如图 2),人工湿地处理后微生物种群分布发生改变。
|
| 图2 人工湿地处理前后的微生物种群分布比例情况 Fig.2 The percentage of different classes of microbe in the sample PWK and CSK |
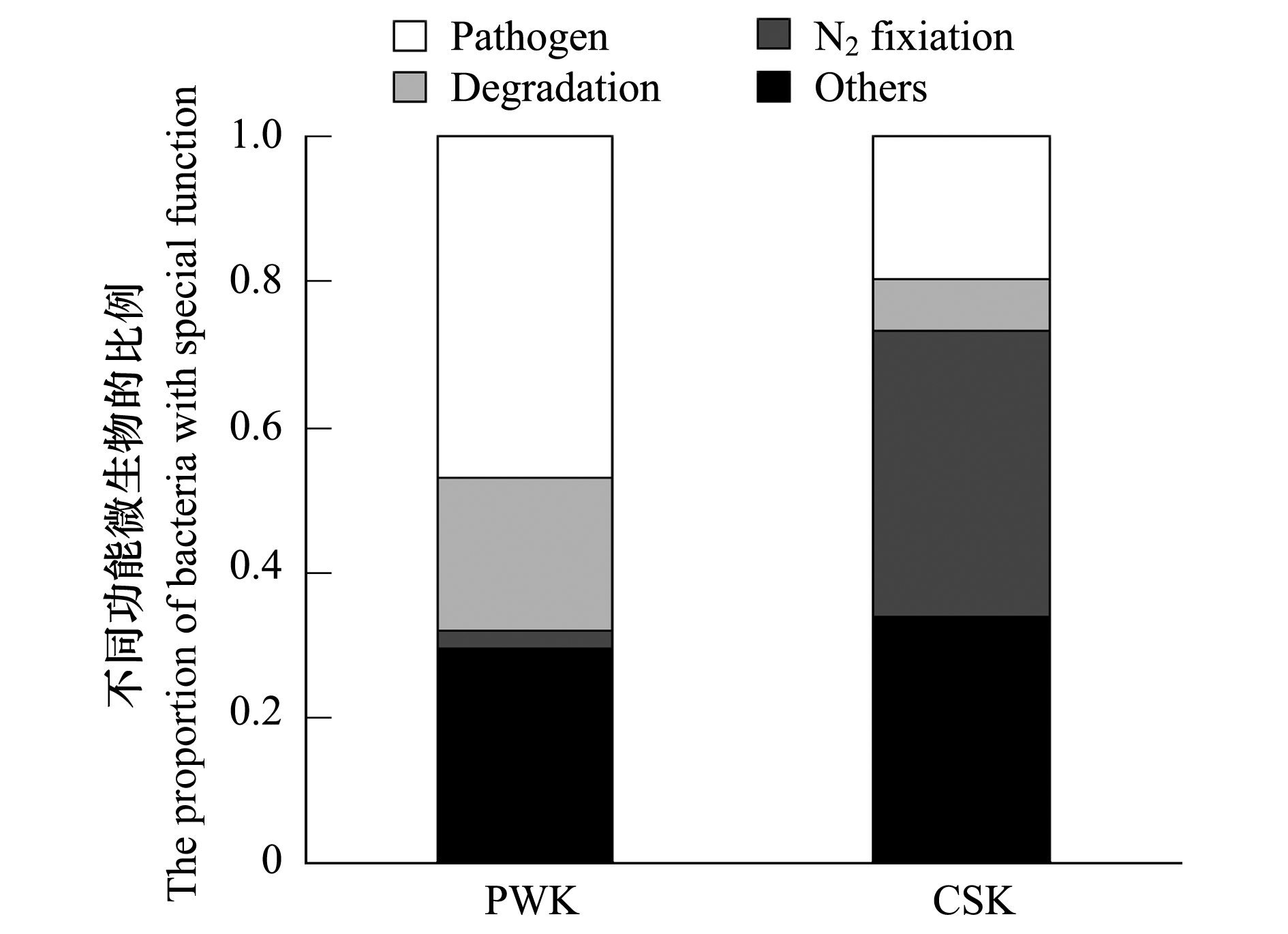
已鉴定的微生物根据功能主要分为三类:致病作用(Pathogen)、固氮作用(N2 fixation)和降解作用(Degradation)。如图 3所示,在造纸厂排污口(PWK),微生物主要以致病菌和降解菌为主;而在人工湿地出水口中,环境友好的固氮菌为主要优势菌,具有致病作用的细菌比例明显下降。
|
| 图3 人工湿地处理前后的不同功能细菌分布比例情况 Fig.3 The percentage of different bacteria according to their function in the sample PWK and CSK |
经鉴定发现在造纸污水中存在较多的污染物 降解菌和致病菌,而在出水口中这类微生物的比重 较低。在造纸厂排污口处中,Thioalkalivibrio为硫氧化细菌,参与反硝化过程[15];Dehalococcoides可以在氯乙烯和三氯乙烯污染的环境中大量富集[16],为脱氯细菌,在欧洲六氯苯污染的河流中,发挥了重要的脱氯作用[17];Hyphomicrobium可降解氯甲烷[18, 19],农药甲胺磷[20]。其中的致病菌和人类疾病的发生关系密切,Legionella具有耐受青霉素的特性,是第一种被发现的细胞内的细菌病原体,可以引起一种高致死性肺炎[21];Klebsiella可以引起呼吸疾病、肝脓肿、肠道疾病和骨髓炎等[22, 23, 24, 25];Parachlamydia可以引起角膜炎和肺炎[26, 27]。
在人工湿地出水口处,Mesorhizobium,Rhizobium为植物共生固氮菌[28, 29, 30],广泛存在于土壤中,与豆科植物共生,形成根瘤,有利于植物固氮。Variovorax存在于微量污染的环境中,以可溶性有机物为碳源,通过环羟基化降解农药高香草酸[31],选择性除草剂利谷隆[32],三氯乙烯[33],它们可以与植物和其他微生物相互作用,促进生态修复过程[34]。Rhodobacter是一种革兰氏阴性菌,它们广泛的存在于淡水和高盐环境下,代谢功能复杂。Cryobacterium主要从冰川和冰川土壤中分离得到[35],功能研究较少。
|
位置
Site | 条带
Band | NCBI序列号
Accession | 种属
Genus | 相似度/%
Similarity | 参与过程
Process | 与人类疾病的关系
Human diseases |
| PWK | P1 | NR_041321 | Legionella | 88 | 肺炎,呼吸道疾病 | |
| P2 | NR_074791 | Klebsiella | 99 | 肺炎,败血症等 | ||
| P3 | NR_074231 | Legionella | 91 | 肺炎,呼吸道疾病 | ||
| P4 | NR_074271 | Protochlamydia | 94 | 人眼、泌尿生殖道呼吸道,肠道疾病 | ||
| P5 | NR_074972 | Thioalkalivibrio | 91 | 参与反硝化过程 | ||
| P6 | NR_074271 | Parachlamydia | 91 | 人眼、泌尿生殖道、呼吸道,肠道疾病 | ||
| P7 | NR_102515 | Dehalococcoides | 82 | 脱氯作用 | ||
| P8 | NR_044952 | Legionella | 96 | 急性呼吸道传染病 | ||
| P9 | NR_044955 | Legionella | 97 | 急性呼吸道传染病 | ||
| P10 | NR_044955 | Legionella | 97 | 急性呼吸道传染病 | ||
| P11 | NR_026426 | Mesorhizobium | 99 | 固氮 | ||
| P12 | NR_025082 | Hyphomicrobium | 96 | 降解含甲基团化合物 | ||
| CSK | C1 | NR_074646 | Variovorax | 99 | 处理苯酚的废水 | |
| C2 | NR_074504 | Rhizobium | 97 | 共生固氮 | ||
| C3 | NR_044216 | Rhizobium | 99 | 固氮 | ||
| C4 | NR_042564 | Rhodobacter | 96 | 广泛存在水环境 | ||
| C5 | NR_042170 | Cryobacterium | 97 | 利用多种碳、氮 |
随着环境保护的迅速发展,人工湿地以其独到的优越性受到了越来越多的关注,已经普遍地应用于各种污水的处理。本研究中的人工湿地位于辽宁省锦州凌海市金城造纸厂污水处理区,植物以中国北方用于处理污水的适用物种芦苇、茭白和香蒲为主,它们根系发达,耐污能力强,去污效果好,适应当地环境。本研究结果显示人工湿地可以改善造纸污水的水质,对TN和TP都有较好的去除率,COD降低66.59%,说明该潜流人工湿地对于造纸污水中污染物的去除有很好的效果。这与湿地植物的交替种植,植物根系的吸附、分解和转化作用有关。在主要污染物中TN的去除率最高,与湿地中的微生物在氮的转化和去除过程中的硝化/反硝化作用有关[36, 37],人工湿地基质中形成了有效的降解污染物的微生物菌群。
微生物群落研究表明,在造纸污水中含有与污染物降解有关的微生物,如Dehalococcoides和 Hyphomicrobium,提示污水中有机污染物的存在。而且在造纸污水中致病性细菌达50%以上,如Legionella、Klebsiella、Parachlamydia。特别是Legionella大量存在,可以引起致死性的肺炎,该病菌与1976年在美国发生的肺炎大爆发密切相关[38]。它们排入环境中不仅污染水体,而且对食物链中营养级较高的动物危害较大,甚至可以造成人类传染性疾病大规模爆发,这些微生物种类与工业类型,生产工艺有很大关系,它们并不包含在常规的生活污水微生物监测种类中,如总大肠菌群、粪大肠菌群、粪链球菌、大肠杆菌、产气荚膜梭菌、沙门氏菌等[39]。所以,在工业病原微生物的监测方面还需要大量的研究。
在经过人工湿地处理后,微生物群落的结构发生了很大的变化,主要微生物由γ变形菌和衣原体变为α变形菌,处理后水样中大量致病菌被去除了。微生物的去除由人工湿地中化学、物理及生物作用共同完成的[40]。夏季温度适宜,系统中植物的生理生化活性较高,植物根系对于微生物的沉积和去除有很大作用。沉积作用是人工湿地中病原微生物去除的最主要途径[41]。该人工湿地的基质为砾石,已有研究表明较小粒径的砾石滤料可以在滤池中截留住微生物。污水进入人工湿地后,水中含有的微生物会粘附于悬浮固体颗粒或悬浮于水体中,通过与基质相互作用与水体分离。分离的微生物的聚集形成生物膜,其中具有降解能力的微生物在其中发挥降解功能,这也是砾石滤池去除污染物的主要途径。存活的微生物可能从固体基质中释放,滞留在生物膜上或基质间隙水中,或者重新返回水体[42]。沿着污水流经湿地的径迹,污染物的种类和浓度不断降低,污水中原有的微生物经过吸附解吸过程不断与周围其他微生物发生竞争作用。在竞争过程中,由于原有环境的改变,不适应环境的微生物多数会死亡,被周围适应环境的微生物替代。所以,水体中微生物的组成可以反映水质的状况。人工湿地处理造纸污水后水中多为环境友好的固氮菌和小部分致病菌,这也表明水质有所改善。
工业污染物种类繁多,常规的理化指标不能反映所有的污染物情况,而且需要投入巨大的资金和精力,有时具有局限性,而微生物群落结构的研究在一定程度上可以弥补这一不足,环境中的微生物组成可以与理化指标共同反映水质状况。本研究的结论也证实了这一点。
本研究主要对人工湿地处理造纸污水中微生物群落的影响进行了研究,还有必要开展对其他工业污水中的微生物群落的研究,扩展微生物在评价污水处理系统对污染物和致病菌的双重去除作用[43]。值得重视的是,人工湿地处理后的水中依然存在可以引起呼吸疾病、肝脓肿、肠道疾病的致病菌,如Klebsiella细菌,它们提醒人们应该关注工业污水排放过程中的致病微生物的监测和致病微生物的排放控制,这样可以防止污水在环境中引起生态风险。
| [1] | Stottmeister U, Wiessner A, Kuschk P, Kappelmeyer U, Kastner M, Bederski O, Muller R A, Moormann H. Effects of plants and microorganisms in constructed wetlands for wastewater treatment. Biotechnol Adv, 2003, 22(1/2):93-117. |
| [2] | Lim P E, Mak K Y, Mohamed N, Noor A M. Removal and speciation of heavy metals along the treatment path of wastewater in subsurface-flow constructed wetlands. Water Sci Technol, 2003, 48(5):307-313. |
| [3] | Lian J J, Xu S G, Zhang Y M, Han C W. Molybdenum(VI) removal by using constructed wetlands with different filter media and plants. Water Sci Technol, 2013, 67(8):1859-1866. |
| [4] | Richter A Y, Weaver R W. Treatment of domestic wastewater by subsurface flow constructed wetlands filled with gravel and tire chip media. Environ Technol, 2003, 24(12):1561-1567. |
| [5] | Mburu N, Tebitendwa S M, van Bruggen J J, Rousseau D P, Lens P N. Performance comparison and economics analysis of waste stabilization ponds and horizontal subsurface flow constructed wetlands treating domestic wastewater: A case study of the Juja sewage treatment works. J Environ Manage, 2013, 128C: 220-225. |
| [6] | He J T, Wu S B.Application Prospect of Constructed Wetland for Pulp and Paper Wastewater Treatment. Paper science & technology, 2006, 25(1):41-44. |
| [7] | Fan L W, Lu Z X, Hai R T. Treatment of Purp and Paper Wastewater by Constructed Wetland Technic. China Pulp and Paper, 2010, 29(11):37-42. |
| [8] | Ding C, Yang T Y, Yu Q, Li Z X, Yang C S. Treatment of 1, 2-dichlorobenzene in wastewater by using horizontal subsurface flow constructed wetlands. Huan Jing Ke Xue, 2011, 32(9):2582-2587. |
| [9] | Casas-Zapata J C, Rios K, Florville-Alejandre T R, Morato J, Penuela G. Influence of chlorothalonil on the removal of organic matter in horizontal subsurface flow constructed wetlands. J Environ Sci Health B, 2013, 48(2):122-132. |
| [10] | Langergraber G. Are constructed treatment wetlands sustainable sanitation solutions? Water Sci Technol, 2013, 67(10):2133-2140. |
| [11] | Zhao Y J, Cheng P, Pei X, Zhang H, Yan C, Wang S B. Performance of hybrid vertical up- and downflow subsurface flow constructed wetlands in treating synthetic high-strength wastewater. Environ Sci Pollut Res Int, 2013,20(7): 4886-4894 |
| [12] | Huang J, Zhao X F. Progress of Study on Microorganisms in the Constructed Wetland for Wastewater Treatment. Transactions of Oceanology and Limnology, 2012, 2:151-156. |
| [13] | Samso R, Garcia J. Bacteria distribution and dynamics in constructed wetlands based on modelling results. Sci Total Environ, 2013, 461-462C: 430-440. |
| [14] | Hench K R, Sexstone A J, Bissonnette G K. Heterotrophic community-level physiological profiles of domestic wastewater following treatment by small constructed subsurface flow wetlands. Water Environ Res, 2004, 76(5):468-473. |
| [15] | Sorokin D Y, Kuenen J G, Jetten M S. Denitrification at extremely high pH values by the alkaliphilic, obligately chemolithoautotrophic, sulfur-oxidizing bacterium Thioalkalivibrio denitrificans strain ALJD. Arch Microbiol, 2001, 175(2):94-101. |
| [16] | Duhamel M, Mo K, Edwards E A. Characterization of a highly enriched dehalococcoides-containing culture that grows on vinyl chloride and trichloroethene. Appl Environ Microbiol, 2004, 70(9):5538-5545. |
| [17] | Tas N, van Eekert M H, Wagner A, Schraa G, de Vos W M, Smidt H. Role of "Dehalococcoides" spp. in the anaerobic transformation of hexachlorobenzene in European rivers. Appl Environ Microbiol, 2011, 77(13):4437-4445. |
| [18] | McAnulla C, Woodall C A, McDonald I R, Studer A, Vuilleumier S, Leisinger T, Murrell J C. Chloromethane utilization gene cluster from Hyphomicrobium chloromethanicum strain CM2(T) and development of functional gene probes to detect halomethane-degrading bacteria. Appl Environ Microbiol, 2001, 67(1):307-316. |
| [19] | Duine J A, Frank J, Westerling J. Purification and properties of methanol dehydrogenase from Hyphomicrobium x. Biochim Biophys Acta, 1978, 524(2):277-287. |
| [20] | Wang L, Wen Y, Guo X, Wang G, Li S, Jiang J. Degradation of methamidophos by Hyphomicrobium species MAP-1 and the biochemical degradation pathway. Biodegradation, 2010, 21(4):513-523. |
| [21] | Diederen B M. Legionella spp. and Legionnaires′ disease. J Infect, 2008, 56(1):1-12. |
| [22] | Lee I A, Kim D H. Klebsiella pneumoniae increases the risk of inflammation and colitis in a murine model of intestinal bowel disease. Scand J Gastroenterol, 2011, 46(6):684-693. |
| [23] | Eisenberg G M, Flippin H F, Kayser H L, Nadel J, Sathavara S, Spivack A, Weiss W. Klebsiella in respiratory disease. Ann Intern Med, 1956, 45(6):1010-1026. |
| [24] | Kanhutu K N, Post J J, Clezy K R, Foo H Y. Community-acquired Klebsiella pneumoniae liver abscesses an “emerging disease” in Australia. Med J Aust, 2011, 194(7):374. |
| [25] | Hiran S, Vishwanathan K A. Klebsiella pneumoniae an emerging bacterial cause of osteomyelitis in sickle cell disease. J Assoc Physicians India, 1999, 47(6):637-638. |
| [26] | Richter M, Matheis F, Gonczi E, Aeby S, Spiess B, Greub G. Parachlamydia acanthamoebae in domestic cats with and without corneal disease. Vet Ophthalmol, 2010, 13(4):235-237. |
| [27] | Greub G, Boyadjiev I, La Scola B, Raoult D, Martin C. Serological hint suggesting that Parachlamydiaceae are agents of pneumonia in polytraumatized intensive care patients. Ann N Y Acad Sci, 2003, 990: 311-319. |
| [28] | Kaneko T, Nakamura Y, Sato S, Asamizu E, Kato T, Sasamoto S, Watanabe A, Idesawa K, Ishikawa A, Kawashima K et al. Complete genome structure of the nitrogen-fixing symbiotic bacterium Mesorhizobium loti. DNA Res, 2000, 7(6):331-338. |
| [29] | Tighe S W, de Lajudie P, Dipietro K, Lindstrom K, Nick G, Jarvis B D. Analysis of cellular fatty acids and phenotypic relationships of Agrobacterium, Bradyrhizobium, Mesorhizobium, Rhizobium and Sinorhizobium species using the Sherlock Microbial Identification System. Int J Syst Evol Microbiol, 2000, 50 (2): 787-801. |
| [30] | Spaink H P. Root nodulation and infection factors produced by rhizobial bacteria. Annu Rev Microbiol, 2000, 54: 257-288. |
| [31] | Allison N, Turner J E, Wait R. Degradation of homovanillate by a strain of Variovorax paradoxus via ring hydroxylation. FEMS Microbiol Lett, 1995, 134(2):213-219. |
| [32] | Dejonghe W, Berteloot E, Goris J, Boon N, Crul K, Maertens S, Hofte M, De Vos P, Verstraete W, Top E M. Synergistic degradation of linuron by a bacterial consortium and isolation of a single linuron-degrading variovorax strain. Appl Environ Microbiol, 2003, 69(3):1532-1541. |
| [33] | Futamata H, Nagano Y, Watanabe K, Hiraishi A. Unique kinetic properties of phenol-degrading variovorax strains responsible for efficient trichloroethylene degradation in a chemostat enrichment culture. Appl Environ Microbiol, 2005, 71(2):904-911. |
| [34] | Satola B, Wubbeler J H, Steinbuchel A. Metabolic characteristics of the species Variovorax paradoxus. Appl Microbiol Biotechnol, 2013, 97(2):541-560. |
| [35] | Zhang D C, Wang H X, Cui H L, Yang Y, Liu H C, Dong X Z, Zhou P J. Cryobacterium psychrotolerans sp. nov., a novel psychrotolerant bacterium isolated from the China No. 1 glacier. Int J Syst Evol Microbiol, 2007, 57(4):866-869. |
| [36] | Guo R M, Liu H H, Zhou L G, Pan D Y, Sun H B. Structure of Microorganisms in a Constructed Wetland and Nitrogen Removal. Jiangsu Environmental Science and Technology, 2006, 19(5):14-16. |
| [37] | Dai Y Y, Yang X P, Zhou L X. Effect of Reed Rhizosphere on Nitrogen and CODRemoval Efficiency in Subsurface Flow Constructed Wetlands. Environmental Science, 2008, 29(12):3387-3392. |
| [38] | Griffith M E, Lindquist D S, Benson R F, Thacker W L, Brenner D J, Wilkinson H W. First isolation of Legionella gormanii from human disease. J Clin Microbiol, 1988, 26(2):380-381. |
| [39] | Song Z W, Sun Q, Xu A L, Qian S C, Liu L L, Feng M X. Dynamic distribution and correlation analysis of indicator-and pathogenic microorganismsin a surface-flow constructed wetland. Chinese Journal of Ecology, 2013, 32(1):91-97. |
| [40] | Hench K R, Bissonnette G K, Sexstone A J, Coleman J G, Garbutt K, Skousen J G. Fate of physical, chemical, and microbial contaminants in domestic wastewater following treatment by small constructed wetlands. Water Res, 2003, 37(4):921-927. |
| [41] | George I, Petit M, Theate C, Servais P. Use of rapid enzymatic assays to study the distribution of faecal coliforms in the Seine river (France). Water Sci Technol, 2001, 43(12):77-80. |
| [42] | Hendricks C W. Increased recovery rate of salmonellae from stream bottom sediments versus surface waters. Appl Microbiol, 1971, 21(2):379-380. |
| [43] | McCarthy G, Lawlor P G, Harrington C, Gardiner G E. Microbial removal from the separated liquid fraction of anaerobically digested pig manure in meso-scale integrated constructed wetlands. Bioresour Technol, 2011, 102(20):9425-9431. |
| [6] | 贺进涛, 武书彬. 人工湿地处理造纸废水的应用前景. 造纸科学与技术, 2006, 25(1):41-44. |
| [7] | 范立维, 卢泽湘, 海热提. 造纸废水的人工湿地处理工艺分析. 中国造纸, 2010, 29(11):37-42. |
| [12] | 黄健, 赵晓芬. 微生物在人工湿地污水处理中的研究进展. 海洋湖沼通报, 2012, 02:151-156. |
| [36] | 郭如美, 刘汉湖, 周立刚, 潘道永, 孙红波. 潜流式人工湿地微生物群落结构及脱氮效果的研究. 江苏环境科技, 2006, 19(5):14-16. |
| [37] | 戴媛媛, 杨新萍, 周立祥. 芦苇根际微环境对潜流人工湿地氮与COD去除性能的影响. 环境科学, 2008, 29(12):3387-3392. |
| [39] | 宋志文, 孙群, 徐爱玲, 钱生财, 刘伶俐, 冯梦雪. 人工湿地中指示与病原微生物动态分布及相关性分析. 生态学杂志, 2013, 32(1):91-97. |
 2014, Vol. 34
2014, Vol. 34




