文章信息
- 陶巧静, 付涛, 项锡娜, 李波, 吴月燕, 周伟军
- TAO Qiaojing, FU Tao, XIANG Xina, LI Bo, WU Yueyan, ZHOU Weijun
- 模拟酸雨对西洋杜鹃生理生态特性的影响
- Effects of simulated acid rain on the physiological and ecological characteristics of Rhododendron hybridum
- 生态学报, 2014, 34(8): 2020-2027
- Acta Ecologica Sinica, 2014, 34(8): 2020-2027
- http://dx.doi.org/10.5846/stxb2013060915311531
-
文章历史
- 收稿日期:2013-6-9
- 修订日期:2013-12-3
2. 浙江大学 农业与生物技术学院, 杭州 310058;
3. 上海海洋大学 水产与生命学院, 上海 201306
2. College of Agriculture and Biotechnology, Zhejiang University, Hangzhou 310058, Zhejiang, China;
3. College of Fisheries and Life, Shanghai Ocean University, Shanghai 201306, China
酸雨是指pH值小于5.6的雨水,也包括雪、雾、冰雹等其他形式的酸性降水[1]。我国自20世纪70年代首次发现酸雨,近年来随着经济的发展,受酸雨影响的面积逐年扩大,危害越来越严重。目前,酸雨已成为威胁人类生存的三大环境问题之一,对植物的伤害也受到国内外学者的广泛关注。研究表明,酸雨会影响植物的株高和地径,破坏叶片的上皮细胞,增加细胞膜的透性,改变叶肉细胞中细胞器的结构,导致植物叶片产生可见伤害,还可以改变植物体内酶的活性,影响植物正常的光合生理功能[2, 3, 4, 5, 6]。不同类型植物对不同酸度酸雨胁迫的反应敏感性不同。园林绿化植物是改善城市环境、维护生态平衡的重要物质基础,城市区域也往往是酸雨的频发区,因此研究酸雨对园林植物生长的伤害效应和有关生理过程的变化,将有助于了解生理代谢机制和反应敏感性,为工程应用和栽培管理提供依据。
西洋杜鹃(Rhododendron hybridum)简称西鹃,别名比利时杜鹃,是杜鹃花科的常绿小灌木,属杜鹃花中生态应用较广的一类,也是世界盆栽花卉生产的主要种类之一[7]。西洋杜鹃是宁波市重要的绿化植物,而宁波又是我国酸雨污染较严重的地区之一。目前关于模拟酸雨对园林植物影响的研究有较多报道,但酸雨对西洋杜鹃的影响国内外还少有研究,本文通过模拟酸雨对西洋杜鹃生理生态特性影响的研究,探讨其对酸雨的敏感性及耐受能力,以期为西洋杜鹃在宁波市以及其它相似环境地区的推广提供理论依据,为城市生态建设中绿化树种的选择提供参考。
1 材料与方法 1.1 试验材料试验于2012年10月至2012年12月在浙江万里学院实验室内进行。试验材料来源于宁波市北仑区柴桥镇杜鹃花基地。选择一批生长一致、株高约40—50 cm的3年生西洋杜鹃“紫金冠”品种,移栽于高25 cm、直径20 cm的塑料花盆中,采用人工基质培养(泥炭 ∶ 砻糠=3 ∶ 1,体积比)。每盆基质为1450 g,含有机质49.3 mg/kg,碱解氮41.1 mg/kg,速效磷8.2 mg/kg,速效钾85.2 mg/kg,pH值5.6,定植前基质中一次性施入缓释肥(N ∶ P ∶ K为17 ∶ 17 ∶ 7)1.5 kg/m3。每盆种植1株,常规管理,随机分成5个组,每组3个重复,进行模拟酸雨处理。
1.2 试验设计与方法根据中国浙江地区酸雨主要以硫酸根为主的特点并参照有关宁波地区酸雨资料[8, 9],用分析纯H2SO4和HNO3配制体积比6 ∶ 1的酸雨母液,然后将适量母液用蒸馏水稀释成pH值分别为2.0、3.0、4.3、5.6的酸雨供试液,以自来水(pH值6.5)作为对照,用PB-21型pH计进行标定。酸雨喷洒采用小型喷雾器喷雾法,于定栽3周待植株恢复正常生长后(10月24日)开始喷洒,每隔7 d喷1次,持续两个月,期间进行常规管理,每次均喷至叶片滴液为度。为防止相互干扰,不同处理梯度之间分开喷施酸雨,并用薄膜遮盖盆土防止酸雨渗透入土,喷施酸雨后浇水要隔天进行。
试验于10月23日处理前进行第1次测定作为初始值。采样时每个处理随机选取3—4株西洋杜鹃的中部功能叶片,分别测定杜鹃叶片的丙二醛含量(MDA)、可溶性蛋白含量、过氧化氢酶(CAT)、过氧化物酶(POD)、超氧化物歧化酶(SOD)活性以及叶绿素含量。分别于处理30 d胁迫中期(2012年11月24号)和60 d胁迫晚期(2012年12月24日)时进行第2次和第3次测定。第3次测定时还需观察各处理间叶片的形态特征、测定其受害百分率,并测定光合作用相关指标。以上各指标均重复取样3次进行测定。
1.3 测定指标及方法 1.3.1 叶片形态特征的观测处理结束后,观察各处理西洋杜鹃叶片形态特征并采用混合采样法选取50张叶片,使用万深LA-S系列植物图像分析系统处理得到受害叶片面积占测量叶片总面积的百分比,从而得出叶片受害百分率。
1.3.2 叶片光合特性的测定采用ECA-PB0402光合测定仪于2012年12月下旬酸雨处理结束后测定植株中部功能叶片的光合速率、蒸腾速率、气孔导度、胞间CO2浓度和水分利用率等,测定时间为10:00至14:00阳光充足时。
1.3.3 西洋杜鹃生理生化特性测定使用SPAD-502叶绿素仪直接测定植株中部功能叶片的叶绿素含量。丙二醛含量的测定采用硫代巴比妥酸比色法[10];可溶性蛋白的测定采用考马斯亮蓝G-250染色法[11]。过氧化氢酶(CAT)活性的测定采用紫外吸收法[12];过氧化物酶(POD)活性的测定采用愈创木酚比色法[13];超氧化物歧化酶(SOD)的测定采用氮蓝四唑(NBT)法[14]。
试验数据采用Excel和DPS 9.50软件进行统计分析。
2 结果与分析 2.1 模拟酸雨对西洋杜鹃叶片形态的影响表 1为西洋杜鹃叶片在不同pH值模拟酸雨胁迫下形态特征的变化。结果表明,对照与pH值5.6的处理差异不大,其叶片生长正常,叶色浓绿,叶片脱落少,属于自然现象。pH值4.3的处理部分叶片仍为绿色,但叶尖出现极少量卷曲,说明模拟酸雨开始对其产生影响,但仍能正常生长。随着酸度加大,模拟酸雨对西洋杜鹃的伤害明显增加,pH值3.0的处理已出现叶片泛黄、部分卷曲萎焉现象,至pH值2.0的处理其叶片明显变红、卷曲,叶缘枯萎,落叶很多,生长受阻。另外,随着模拟酸雨酸性的增加,西洋杜鹃叶片的受害百分率也明显增大。对照与pH值5.6的处理其叶片基本无受害,pH值4.3的处理有极小量的受害,pH值3.0和pH值2.0的处理叶片明显受害,分别达到了15.6%和32.5%。
|
pH处理
pH Treatment | 叶片颜色
Leaf color | 叶片形状
Leaf shape | 叶片脱落
Leaf abscission | 叶片受害百分率/%
Leaf injury percentage |
| 表中数据为平均值±标准误,不同小写字母表示不同处理间差异显著(P≤0.05) | ||||
| 2.0 | 变红 | 卷曲、叶缘枯萎 | 较多 | 32.53±0.38 a |
| 3.0 | 泛黄 | 卷曲萎焉 | 一般 | 15.63±0.15 b |
| 4.3 | 正常,绿色 | 极少量卷曲 | 较少 | 3.50±0.21 c |
| 5.6 | 正常,浓绿 | 正常 | 少 | 0.57±0.12 d |
| ck(6.5) | 正常,浓绿 | 正常 | 少 | 1.03±0.18 d |
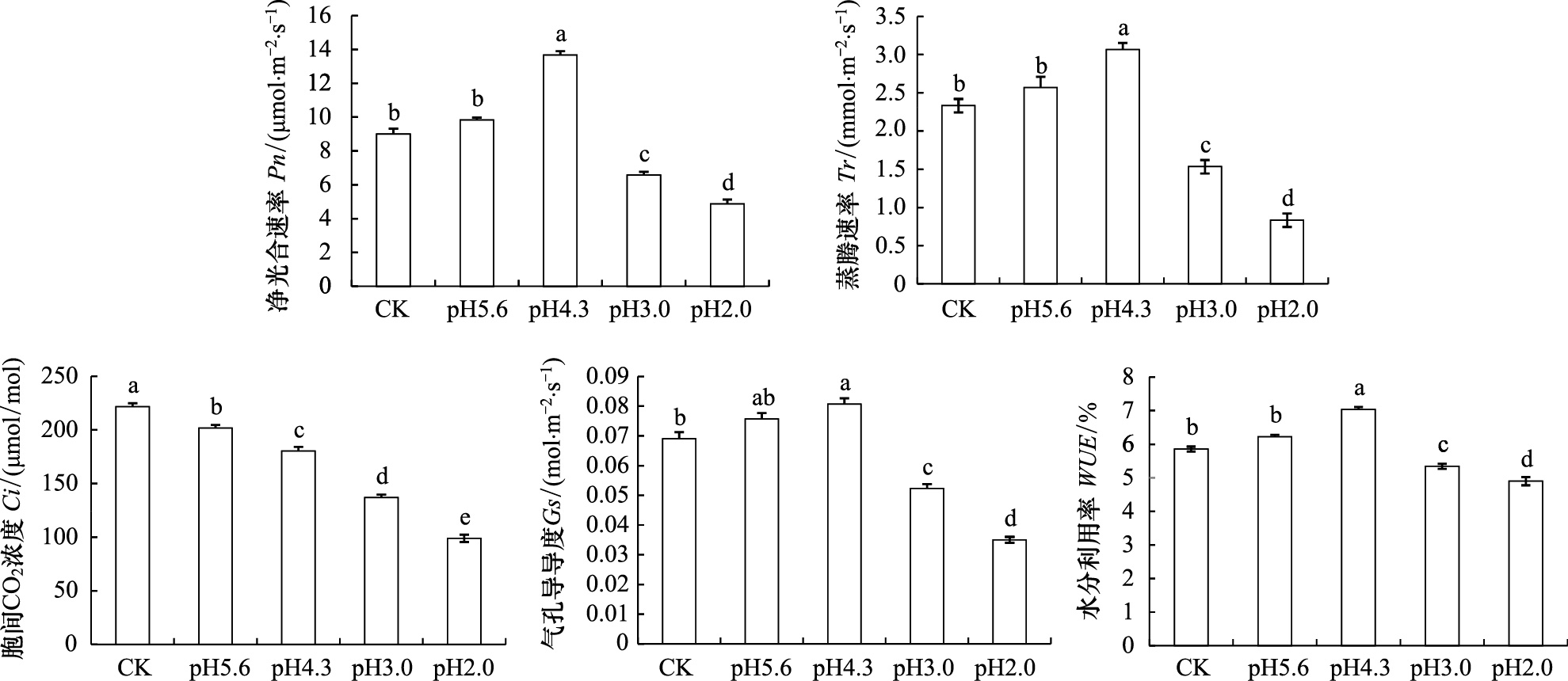
图 1为不同酸雨强度处理后对西洋杜鹃光合特性中多个指标的影响。由图可知pH值5.6的处理和对照差异不显著,净光合速率(Pn)、蒸腾速率(Tr)、气孔导度(Gs)及水分利用率(WUE)等指标均大于对照,但差异不显著;而pH值4.3的处理其净光合速率、蒸腾速率、气孔导度及水分利用率等光合特性均显著高于对照;随着酸度的进一步增强,胁迫增大,其光合特性也明显下降,pH值3.0的处理显著低于对照且pH值2.0的处理进一步降低。结果表明,弱酸性环境促进了西洋杜鹃的光合作用,其净光合速率、蒸腾速率、气孔导度及水分利用率等都显著提高,这可能是因为西洋杜鹃为了适应逆境作出的抗逆反应,从而增强了其光合特性;但酸性过强导致伤害过大,抑制了其光合作用。另外,西洋杜鹃的胞间CO2浓度(Ci)随着酸性增加而减少,表明酸雨胁迫会造成一定的影响,且随酸性增强影响显著。
|
| 图 1 不同模拟酸雨处理对西洋杜鹃光合特性的影响 Fig. 1 Effects of simulated acid rain on photosynthetic characteristics of Rhododendron hybridum 不同小写字母表示在P≤0.05水平上具有显著差异 |
如图 2所示,西洋杜鹃叶片的叶绿素含量随着模拟酸雨处理酸性的增强而减少,且随着处理时间的增加,各处理的叶绿素含量下降增大。对照与pH值5.6的处理差异不大,其处理前后的叶绿素含量变化也很小,pH值4.3的处理从处理中期开始出现一定的差异,随着pH值的降低及处理时间的增加其差异更加显著。结果表明,模拟酸雨对西洋杜鹃叶片叶绿素的影响显著,这可能是因为模拟酸雨中的酸性离子影响了叶绿素的合成与分解。

|
| 图 2 不同模拟酸雨处理对西洋杜鹃叶绿素含量的影响 Fig. 2 Effects of simulated acid rain on chlorophyll content in Rhododendron hybridum leaves |
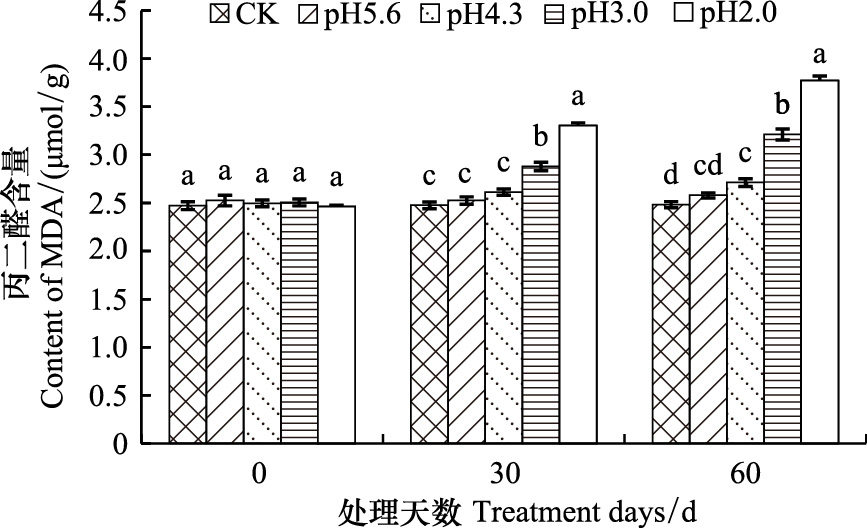
由图 3可知,随着酸性增强和处理时间的延长,西洋杜鹃叶片中的丙二醛含量逐渐增加且差异逐渐增大。处理30 d左右,pH值5.6,pH值4.3,pH值3.0和pH值2.0处理的丙二醛含量分别比对照增加了2.0%,5.5%,16.3%和33.4%。处理60 d左右,pH值5.6,pH值4.3,pH值3.0和pH值2.0处理的丙二醛含量分别比对照增加3.9%,9.3%,29.4%和51.9%。植物叶片中丙二醛含量的增加与膜透性破坏有关[15],MDA积累越多说明植物受伤害越重,其抗性就越差。结果表明随着模拟酸雨酸性的增强,西洋杜鹃叶片受害程度逐渐加深。
|
| 图 3 不同模拟酸雨处理对西洋杜鹃叶片丙二醛含量的影响 Fig. 3 Effects of simulated acid rain on MDA content in Rhododendron hybridum leaves |
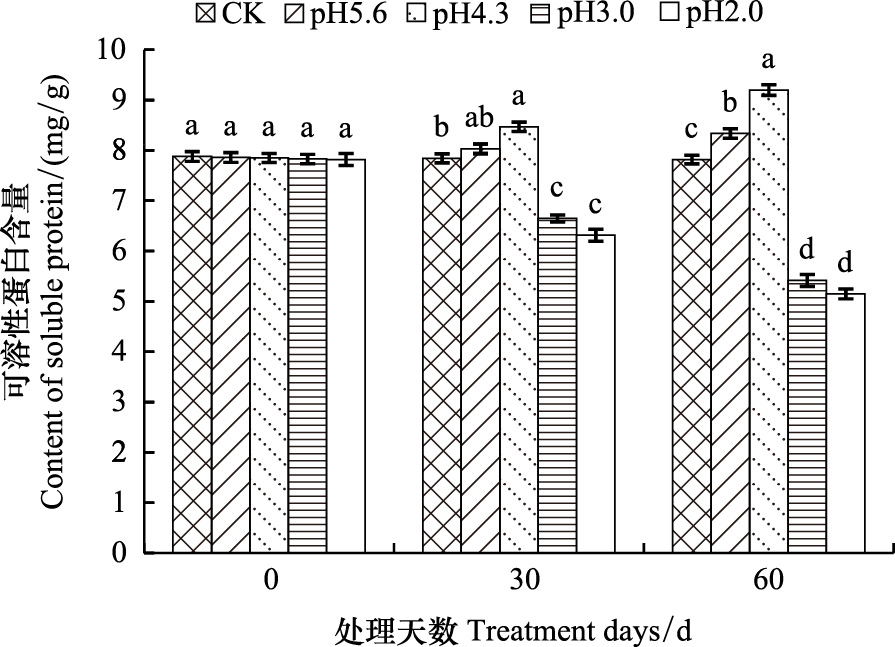
在一定的胁迫条件下,植物体内蛋白质含量的提高是植物对逆境胁迫适应的一种表现,可作为植物相对抗性的一种指标[16]。由图 4可以看出,随着模拟酸雨酸性的增加,西洋杜鹃叶片中可溶性蛋白的含量呈先升后降的趋势,且随处理时间的延长其变化增大。与对照相比,处理30 d左右时pH值5.6和pH值4.3的处理其可溶性蛋白含量分别增加2.4%和8.0%,而pH值3.0和pH值2.0的处理分别减少了15.2%和19.5%;处理60 d左右时pH值5.6,pH值4.3的处理其可溶性蛋白含量增加了6.6%和17.6%,而pH值3.0和pH值2.0处理则分别减少了30.7%和34.1%。西洋杜鹃在pH值4.3的模拟酸雨处理下明显提高了其可溶性蛋白含量表明其能对pH值4.3的模拟酸雨产生较大抗性,而pH值3.0和pH值2.0处理下其可溶性蛋白明显降低表明高强度的酸雨破坏了西洋杜鹃的组织结构,抑制了其蛋白质的合成。
|
| 图 4 不同模拟酸雨处理对西洋杜鹃可溶性蛋白含量的影响 Fig. 4 Effects of simulated acid rain on soluable protein content in Rhododendron hybridum leaves |
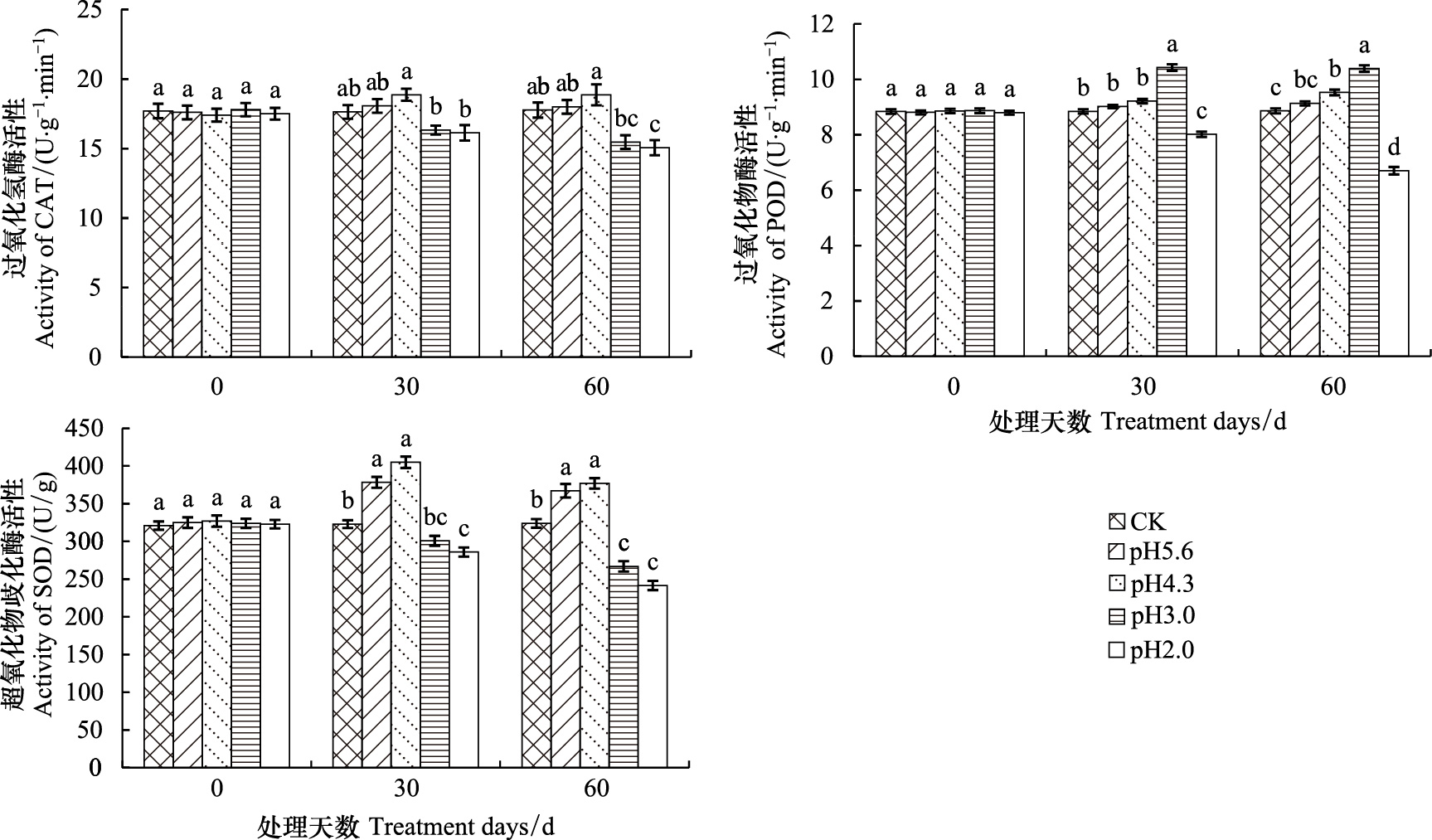
CAT、POD、SOD是生物体内重要的活性氧清除酶,在消除超氧化物自由基、减轻脂质过氧化作用和膜伤害方面起重要作用[17]。如图 5所示,pH值5.6和pH值4.3处理的西洋杜鹃CAT活性比对照略有增加,但差异不显著,而pH值3.0和pH值2.0的处理与对照相比有所减少,且随着处理时间延长减少明显。SOD酶活性的变化与CAT的变化相似,但变化更为明显,差异也更为显著(图 5)。处理30 d左右时pH值5.6和pH值4.3的处理其SOD活性比对照分别增加17.1%和25.4%,而pH值3.0和pH值2.0的处理却比对照分别下降6.8%和11.5%;处理60 d左右时pH值5.6和pH值4.3的处理其SOD活性比30 d左右时略有减少,pH值3.0和pH值2.0的处理与对照相比则下降更加明显,达到了17.6%和25.4%。POD酶活性的变化与CAT、SOD略有不同,表现为pH值5.6和pH值4.3的处理与对照差异不明显,而pH值3.0的处理其POD活性明显高于对照,pH值2.0的处理则明显低于对照,且随时间增加变化增大(图 5)。结果显示,在低酸度模拟酸雨下西洋杜鹃CAT、POD、SOD酶活性都增加了表明其抗性增强了,能适应该酸雨胁迫,而强酸度胁迫下其CAT、POD、SOD酶活性降低表明该浓度模拟酸雨对西洋杜鹃造成了一些不可逆的伤害,破坏了酶的合成。
|
| 图 5 不同模拟酸雨处理后西洋杜鹃抗氧化酶活性的变化 Fig. 5 Change of antioxidant enzyme activities in R. hybridum leaves with different simulated acid rain treatments |
研究表明,酸雨对许多植物叶片产生伤害的临界点在pH值=3.5,对植物生长和生物量影响的酸雨临界点在pH值=3.0—2.0,而植物的形态结构特点和生物学特性决定了其对酸雨所造成的伤害的自身恢复功能和抗性[18, 19]。从西洋杜鹃叶片结构上看,西洋杜鹃叶表被有较多的绒毛,表面较为光滑,可以减少模拟酸雨液滴在叶片上的接触与停留时间,减少酸性离子的侵入,提高了西洋杜鹃对酸雨的抗性。另外,西洋杜鹃喜好偏酸性土壤。本实验也表明,随着酸雨酸度的增大,特别是在较重酸雨(pH值≤3.0)胁迫下,西洋杜鹃的叶片才出现较多的黄斑及落叶等,说明西洋杜鹃对酸雨具有较高的抗性。
酸雨伤害植物的主要机理在于酸雨降低了膜保护酶的活性以及膜保护物质的含量,使活性氧代谢平衡失调,相对过剩的活性氧或氧自由基启动并加强了膜质过氧化作用而使植物受害[20, 21]。本实验表明:在模拟酸雨胁迫下,西洋杜鹃叶片中MDA含量随胁迫强度的增加而增大,说明酸雨胁迫引起了西洋杜鹃的膜质过氧化加剧。通过对在酸雨胁迫下西洋杜鹃叶片中的CAT、POD、SOD活性的影响结果以及这3种保护酶活性与MDA含量之间的相关程度分析判断,造成西洋杜鹃膜质过氧化加剧的主要原因是由于酸雨胁迫产生的自由基离子使抗氧化酶系统的协调作用失衡,从而使CAT、POD和SOD清除活性氧的能力降低,导致了活性氧的进一步积累,最终造成细胞质膜透性增大,膜功能受损,甚至引发叶绿体结构破坏,使叶片叶绿素含量下降,进而影响光合代谢,致使净光合速率下降。同时应注意到,POD 作为一种保护酶,在本实验中其活性的持续增强似乎并未起到有效缓解活性氧的伤害作用,其原因可能与它的双重作用有关,POD不仅参与消除羟基自由基也在逆境加强后及叶片衰老初期参与活性氧的生成和叶绿素的降解,并引发膜脂过氧化作用[22]。
酸雨对植物膜系统的损伤必然会引起光合器官的伤害和功能的下降[23, 24]。叶绿体是植物光合作用的场所,也是细胞对胁迫生境最敏感的细胞器,其含量受各种胁迫条件的影响,在本实验中,西洋杜鹃叶绿素含量随模拟酸雨胁迫的增强而逐渐减少,表明模拟酸雨对西洋杜鹃叶片叶绿素的影响较大。实验也表明,气孔对环境变化的协同响应是西洋杜鹃在酸雨胁迫条件下叶片净光合速率变化的主导因子。对照和处理的叶片净光合速率和气孔导度之间均存在高度的线性相关性,而且在pH值≤3.0时西洋杜鹃叶片Pn、Tr、Gs及Ci都明显降低,表明植物受胁迫明显加重。另外,Gs的变化还影响其他参数的变化:Gs的降低减少了CO2的进入,同时还影响了叶片的Tr,Gs低则Tr低,进而也影响了西洋杜鹃叶片对水分的利用效率,这是导致西洋杜鹃光合速率降低的一个重要原因。而且西洋杜鹃在Pn下降过程中,Gs下降并伴随着Ci降低,按照Farquhar等[25]的理论,西洋杜鹃净光合速率降低属于气孔限制型。
可溶性蛋白质参与调节植物细胞的渗透势,在一定的逆境胁迫下,植物体内蛋白质含量的增加是植物对逆境适应的一种表现[26]。试验中西洋杜鹃可溶性蛋白的含量随酸雨强度增加先增后减,表明西洋杜鹃能适应一定程度的酸雨胁迫。酸雨减少了植物蛋白质的含量,其原因一方面可能是酸雨抑制了蛋白质的合成,另一方面可能是酸雨胁迫阻抑了植物的氮代谢[27, 28]。
综上所述,在本试验中西洋杜鹃在较重酸雨(pH值≤3.0)胁迫下,其生理生化特性受到明显影响:叶片发黄、落叶增多,叶片MDA含量显著增加,可溶性蛋白含量、CAT和SOD酶活性显著下降而POD活性明显增加,同时叶绿素含量减少,光合速率和水分利用率等均显著下降。因此综合各项生理评价指标认为pH值≤3.0是酸雨对西洋杜鹃产生隐性伤害的临界点(或阈值)。西洋杜鹃喜半阴、凉爽、湿润的环境,喜好酸性土壤,是典型的酸性花卉,常作为盆栽在全国广泛栽培,但目前地栽较少,只有浙江宁波、福建漳平等地有地栽西洋杜鹃[29]。据调查,我国华东各省的酸雨污染情况比较严峻,大部分地区降水的pH值小于4.0,甚至达到pH值2.0,且酸雨的范围也逐渐扩大[30]。由此可见宁波虽处于酸雨受害较重区但仍适合西洋杜鹃栽培,因此西洋杜鹃可作为酸雨灾害较重地区园林绿化及植被构建的物种之一。
| [1] | Deng W, Liu R H, Xiong J W, Chen H B, Tian H W, Du Z X. Research progress of acid rain in china. Meteorological and Environmental Sciences, 2009, 32(1): 82-87. |
| [2] | Chen X L, He D J, Hong W, Liu Y S, Bian L L, Wang Y T. Research advance in acid rain injury mechanism to garden plants. Subtropical Agriculture Research, 2007, 2(2): 99-103. |
| [3] | Wang Y J, Deng S H, Jiang J, Shang H, Lin B, Sun Y Q, Hu X M. Effects of acid rain on photosynthesis and antioxidant enzyme activity of H. mitabilis L. seedlings. Acta Agriculturae Nucleatae Sinica, 2011, 25(3): 588-593. |
| [4] | Ková?ik J, Klejdus B, Ba?kor M, ?tork F, Hedbavny J. Physiological responses of root-less epiphytic plants to acid rain. Ecotoxicology, 2011, 20(2): 348-357. |
| [5] | Liu J F, Yang C, Wang M Y. Effect of simulated acid rain on physiological characteristics in Taxus chinensis var. Mairei. Chinese Journal of Tropical Crops, 2012, 33(6): 1046-1050. |
| [6] | Lu M J, Jiang H, Li W, Yu S Q, Zeng B, Jiang F W, Li J, Jin Q. Effect of simulated acid rain on growth and photosynthetic physiology of Machilus pauhoi. Acta Ecologica Sinica, 2009, 29(11): 5986-5994. |
| [7] | Kuang Z Y, Zhang Y J. Cultivation techniques of Belgium azaleas in intelligent greenhouse. Modern Agricultural Sciences and Technology, 2007, (22): 33-33. |
| [8] | Li Y Q, Chen S Y, Xu N B, Zhu L B. Current situation of acid rain in Ningbo city. Jiangsu Environmental Science and Technology, 1997, (4): 28-31. |
| [9] | Li Z Y. Pollution Characteristic of Acid Precipitation in Zhejiang and its Multi-Dimension Analysis[D]. Hangzhou: Zhejiang University, 2004. |
| [10] | Li H S. Principle and Technology of Plant Physiological and Biochemical Experiments. Beijing: Higher Education Press, 2000. |
| [11] | Kong X S, Yi X F. Experiment Technology of Plant Physiology. Beijing: China Agriculture Press, 2008: 160-162. |
| [12] | Shim I S, Momose Y, Yamamoto A, Kim D W, Usui K. Inhibition of catalase activity by oxidative stress and its relationship to salicylic acid accumulation in plants. Plant Growth Regulation, 2003, 39(3): 285-292. |
| [13] | Wu Y X, von Tiedemann A. Impact of fungicides on active oxygen species and antioxidant enzymes in spring barley (Hordeum vulgare L.) exposed to ozone. Environmental Pollution, 2002, 116(1): 37-47. |
| [14] | Vuleta A, Tuci? B. Thermal dependence of the antioxidant enzymes superoxide dismutase, catalase, and peroxidase in foliage of Iris pumila L. Archives of Biological Sciences, 2009, 61(3): 441-446. |
| [15] | Filek M, Walas S, Mrowiec H, Rudolphy-Skórska E, Sieprawska A, Biesaga-Ko?cielniak J. Membrane permeability and micro-and macroelement accumulation in spring wheat cultivars during the short-term effect of salinity-and PEG-induced water stress. Acta Physiologiae Plantarum, 2012, 34(3): 985-995. |
| [16] | Fang Z H, Dong K H. Effects of NaCl stress on soluble protein contents and soluble carbohydrate contents of Artemisia anethifolia. Chinese Agricultural Science Bulletin, 2010, 26(16): 147-149. |
| [17] | Wang W B, Kim Y H, Lee H S, Kim K Y, Deng X P, Kwak S S. Analysis of antioxidant enzyme activity during germination of alfalfa under salt and drought stresses. Plant Physiology and Biochemistry, 2009, 47(7): 570-577. |
| [18] | Qi Z M, Wang X D, Song G Y. The research progress of the effect of acid rain on plant. World Science Technology Research and Development, 2004, 26(2): 36-41. |
| [19] | Li Z G, Jiang W B, Weng M L, Jiang W. Physiologic responses and sensitivity of six garden plants to simulated acid rain. Acta Horticulturae Sinica, 2011, 38(3): 512-518. |
| [20] | Zhao D, Pan Y Z, Deng S H, Shang H, Wang F, Chen R. Effects of simulated acid rain on physiological and ecological characteristics of Camellia sasanqua. Scientia Agricultura Sinica, 2010, 43(15): 3191-3198. |
| [21] | Liu E U, Liu C P. Effects of simulated acid rain on the antioxidative system in Cinnamomum philippinense seedlings. Water, Air, and Soil Pollution, 2011, 215(1/4): 127-135. |
| [22] | Ke S S, Yang M W. Effects of water stress on antioxidant system and lipid peroxidation in leaves of Rhododendron fortunei. Acta Horticulturae Sinica, 2007, 34(5): 1217-1222. |
| [23] | Wen K J, Liang C J, Wang L H, Hu G, Zhou Q. Combined effects of lanthanumion and acid rain on growth, photosynthesis and chloroplast ultrastructure in soybean seedlings. Chemosphere, 2011, 84(5): 601-608. |
| [24] | Tian D L, Fu X P, Fang X, Xiang W H. Effect of simulated acid rain on photosynthetic characteristics in Cinnamomum camphora seedlings. Scientia Silvae Sinicae, 2007, 43(8): 29-35. |
| [25] | Farquhar G D, Sharkey T D. Stomatal conductance and photosynthesis. Annual Reviews of Plant Physiology, 1982, 33(1): 317-345 |
| [26] | Amini F, Ehsanpour A A. Soluble proteins, proline, carbohydrates and Na+/k+ changes in two tomato (Lycopersicon esculentum Mill.) cultivars under in vitro salt stress. American Journal of Biochemistry and Biotechnology, 2005, 1(4): 212-216. |
| [27] | Liang J, Mai B R, Zheng Y F, Li L, Tang X Y, Wu R J. Effects of simulated acid rain on the growth, yield and quality of rape. Acta Ecologica Sinica, 2008, 28(1): 275-283. |
| [28] | Liu T W, Fu B, Niu L, Chen, J, Wang W H, He J X, Pei Z M, Zheng H L. Comparative proteomic analysis of proteins in response to simulated acid rain in Arabidopsis. Journal of Proteome Research, 2011, 10(5): 2579-2589. |
| [29] | Zhang X B. Study on Growth Dynamics and Cultivation Technology of Rhododendron Hybridum Hort. in Guiyang. Guiyang: Guizhou Normal University, 2006. |
| [30] | Xiao Y, Huang J C, Liu S X, Yang W Z, Guo D S, Zhu L Z. Inhibitory effects of simulated acid rain on the growth of 12 garden plant species and their physiological response to it. Journal of Southwest Agricultural University: Natural Science Edition, 2004, 26(3): 270-273, 276-276. |
| [1] | 邓伟, 刘荣花, 熊杰伟, 陈海波, 田宏伟, 杜子璇. 当前国内外酸雨研究进展. 气象与环境科学, 2009, 32(1): 82-87. |
| [2] | 陈笑玲, 何东进, 洪伟, 刘勇生, 卞莉莉, 王彦涛. 酸雨胁迫对园林植物伤害机理的研究进展. 亚热带农业研究, 2007, 2(2): 99-103. |
| [3] | 王应军, 邓仕槐, 姜静, 尚鹤, 林波, 孙亚琴, 胡晓梅. 酸雨对木芙蓉幼苗光合作用及抗氧化酶活性的影响. 核农学报, 2011, 25(3): 588-593. |
| [5] | 刘建福, 杨晨, 王明元. 模拟酸雨对南方红豆杉生理特性的影响. 热带作物学报, 2012, 33(6): 1046-1050. |
| [6] | 鲁美娟, 江洪, 李巍, 余树全, 曾波, 蒋馥蔚, 李佳, 金清. 模拟酸雨对刨花楠幼苗生长和光合生理的影响. 生态学报, 2009, 29(11): 5986-5994. |
| [7] | 邝作玉, 张严君. 比利时杜鹃花智能温室栽培技术. 现代农业科技, 2007, (22): 33-33. |
| [8] | 李应群, 陈尚玉, 徐能斌, 朱丽波. 宁波市区酸雨现状. 江苏环境科技, 1997, (4): 28-31. |
| [9] | 李震宇. 浙江降水污染的特征和多维分析 [D]. 杭州: 浙江大学, 2004. |
| [10] | 李合生. 植物生理生化实验原理和技术. 北京: 高等教育出版社, 2000. |
| [11] | 孔祥生, 易现峰. 植物生理学实验技术. 北京: 中国农业出版社, 2008: 160-162. |
| [16] | 方志红, 董宽虎. NaCl胁迫对碱蒿可溶性糖和可溶性蛋白含量的影响. 中国农学通报, 2010, 26(16): 147-149. |
| [18] | 齐泽民, 王玄德, 宋光煜. 酸雨对植物影响的研究进展. 世界科技研究与发展, 2004, 26(2): 36-41. |
| [19] | 李志国, 姜卫兵, 翁忙玲, 姜武. 常绿阔叶园林6树种(品种)对模拟酸雨的生理响应及敏感性. 园艺学报, 2011, 38(3): 512-518. |
| [20] | 赵栋, 潘远智, 邓仕魁, 尚鹤, 王芳, 陈睿. 模拟酸雨对茶梅生理生态特性的影响. 中国农业科学, 2010, 43(15): 3191-3198. |
| [22] | 柯世省, 杨敏文. 水分胁迫对云锦杜鹃抗氧化系统和脂类过氧化的影响. 园艺学报, 2007, 34(5): 1217-1222. |
| [24] | 田大伦, 付晓萍, 方晰, 项文化. 模拟酸雨对樟树幼苗光合特性的影响. 林业科学,2007, 43(8): 29-35. |
| [27] | 梁骏, 麦博儒, 郑有飞, 李璐, 唐信英, 吴荣军. 模拟酸雨对油菜(Brassica napus L.)生长、产量及品质的影响. 生态学报, 2008, 28(1): 275-283. |
| [29] | 张轩波. 比利时杜鹃生长规律及栽培技术研究——以贵阳市为例 [D]. 贵阳: 贵州师范大学, 2006. |
| [30] | 肖艳, 黄建昌, 刘少娴, 杨伟钊, 郭冬升, 朱凌志. 模拟酸雨对12 种园林植物的伤害及敏感性反应. 西南农业大学学报: 自然科学版, 2004, 26(3): 270-273, 276-276. |
 2014, Vol. 34
2014, Vol. 34




