文章信息
- 贾婷婷, 毛亮, 郭正刚
- JIA Tingting, MAO Liang, GUO Zhenggang
- 高原鼠兔有效洞穴密度对青藏高原高寒草甸群落植物生态位的影响
- Effect of available burrow densities of plateau pika (Ochotona curzoniae) on plant niche of alpine meadow communities in the Qinghai-Tibet Plateau
- 生态学报, 2014, 34(4): 869-877
- Acta Ecologica Sinica, 2014, 34(4): 869-877
- http://dx.doi.org/10.5846/stxb201305050926
-
文章历史
- 收稿日期:2013-5-5
- 修订日期:2013-10-15
高原鼠兔(Ochotona curzoniae)是青藏高原高寒草甸生态系统的关键种[1],这种特有的小型哺乳动物在高寒草甸生态系统中的作用随其种群密度而发生明显变化[2]。当高原鼠兔密度适宜时,其通过采食和挖掘活动传播和扩散植物种子[3],改善土壤通透性,提高土壤水分涵养能力[4],优化高寒草甸植物群落,增加物种多样性和可食牧草生物量[5]。但当高原鼠兔密度极度扩展且超过高寒草甸生态系统承载力的范畴时,则会引起土壤和草甸植被退化,土壤养分随地表径流流失,优势种植物和主要伴生种发生更替[6],说明高寒草甸群落内植物种群的地位和作用随高原鼠兔密度变化而需要做出适应性应答,以适应变化后的新环境,而植物群落内种群的作用和地位通常反映了植物种群的生态位。因此研究高寒草甸植物群落内种群生态位随高原鼠兔密度变化的特征,有助于全面解析高原鼠兔密度变化时植物种群间的相互关系,从而一定程度上可以揭示草甸植物群落的演变方向。
目前高寒草甸植物群落对高原鼠兔密度变化的响应的研究主要集中于草甸植物群落数量特征的变化,刘伟等[7]认为高原鼠兔活动有利于增加群落内的物种丰富度,但一程度上减少了地上生物量。张军[8]研究青藏高原东北部高寒草甸群落内优势种变化特征时发现,优势种垂穗披碱草随高原鼠兔密度增加出现由低到高极显著线形负相关关系,Guo等[9]报道,适量的高原鼠兔能够增加高寒草甸群落内优良牧草比例,优化草甸品质,而高原鼠兔密度过大时则使草甸品质劣化,产量下降。上述研究从表观特征方面分析植物群落特征对高原鼠兔密度变化的响应,没有关注到草甸群落内植物生态位随高原鼠兔密度增减的变化规律,不能全面阐明各个植物种群地位和作用随高原鼠兔密度变化的更替过程。因此,本研究通过调查不同高原鼠兔活动强度下高寒草甸群落内的植物种群生态位的变化特征,以期阐明高寒草甸群落内植物种群地位和作用随高原鼠兔活动强度变化规律,对全面阐明高原鼠兔影响草甸群落的演变方向提供科学依据。
1 研究地区概况与方法 1.1 研究地区概况研究地区位于青藏高原东部,行政隶属于甘肃省甘南自治州玛曲县,北纬33°06′30″—34°30′15″,东经100°40′45″—102°29′00″,海拔3300—4806 m。气候为高原湿润气候,年均温度1.2 ℃,1月平均温度-10 ℃,7月平均温度11.7 ℃。年降水量为564 mm,主要集中于5—9月,年蒸发量1000—1500 mm。全年日照时数2613.9 h,年内霜期大于270 d,无绝对无霜期。土壤为亚高山草甸土,表层有5—10 cm草皮层,有机质含量可达10%—15%。植被类型主要是高寒草甸,以莎草科嵩草属的高山嵩草(Kobresia pygmaea)为优势种[8],主要伴生种为毛茛科银莲花属的钝裂银莲花(Anemone obtusiloba)和小花草玉梅(A. rivularis)、蔷薇科委陵菜属的鹅绒萎陵菜(Potentilla anserina)和莓叶萎陵菜(P. fragarioides)、菊科垂头菊属的条叶垂头菊(Cremanthodium lineare)。全县受鼠害危害的草地面积占总草地面积的比例30%左右,其中高原鼠兔是主要的危害鼠类,自20世纪70年代以来,高原鼠兔危害面积逐渐加大,单位面积有效洞穴数量逐渐增加[8],已经严重威胁高寒草甸生态系统的健康。
1.2 研究方法 1.2.1 试验设计和野外调查高原鼠兔具有选择采食、家族营居生活和运动迁移的特征,直接测定其密度具有较大难度。目前经常采用高原鼠兔有效鼠洞口数间接代替高原鼠兔密度,分析高原鼠兔密度变化对高寒草甸植物群落和土壤的影响[4, 6, 9]。2012年5月在玛曲县阿孜站地势相对一致的地块,选取了36个25 m×25 m (625m2) 的样地,并将每个样地四角采用螺丝刀标记,然后用堵洞法测定各样地的有效洞口数,即每天17:00点将样地内所有高原鼠兔洞口填埋,翌日早上查数每个样地洞口数,下午继续填埋,连续3 d,将3 d内的平均值被刨开的洞口数作为样地的有效洞口数。然后调查每个样地的有效洞口数、裸斑面积比例和草丛高度,并以这3个因子为变量将36个样地聚成4个类群,求出各个类群有效洞口的平均值,其分别为10(10±3)、15(15±2)、21(21±3)、31(31±4),以这些平均值为基准设置高原鼠兔有效洞穴梯度,每个梯度选择3个样地作为研究样地,组成3次重复,其余24个样地不做任何观测。然后将选择的样地围栏,避免放牧对高原鼠兔作用的影响。在每个样地采用“W”型布设5 个1 m×1 m的观测样方,样方间隔约8 m,尽量使其保持在周围洞口的中间位置,并对样方做出标记。2012年8月中旬进行样方调查,统计样方内植物种类、高度、频度、盖度等。
1.2.2 指标计算(1)重要值
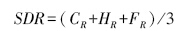
式中,SDR是每个植物种在样方内的重要值,CR表示相对盖度;HR表示相对高度;FR表示相对频度值。
(2)生态位宽度[10]
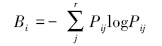
式中,Bi为种i生态位宽度,Pij为种i对第j个样方的各种资源利用占它对全部样方各种资源利用频度,Pij=nij/Ni,而Ni=∑rjnij, nij为种i在资源j上的优势度,即样方中物种的重要值,r为样方数,其值域为[0,logr]。Bi值越大,说明生态位越宽,该种利用的资源总量越多,竞争力越强。
(3)生态位重叠[11]
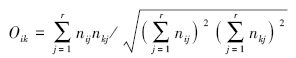
式中,Oik为物种i与物种k的生态位重叠值,nij和nkj为物种i和物种k在样方j上的优势度,即物种i与物种k在样方j的重要值,r为样方数,其值域为[0, 1]。
1.3 数据分析采用Excel 2003进行数据处理和制图。
2 结果 2.1 有效洞穴密度对草甸植物群落组成及其重要值的影响有效洞穴密度对高寒草甸群落物种具有明显的影响,样方内植物物种数介于10—15,整体表现为随有效洞穴密度增加而逐渐增多,至31 个/625m2物种数最多(表 1)。高原鼠兔有效洞穴密度从10 个/625m2增至31 个/625m2的过程中,高寒草甸植物群落优势种没有发生变化,均为高山嵩草,但主要伴生种和少见种发生了一定程度的更替,总体表现为豆科植物和毒杂草增多。有效洞穴密度10 个/625m2增至15 个/625m2时,主要伴生种除小花草玉梅保留外,青藏苔草(Carex moorcroftii)和秦艽(Gentiana macrophylla)被钝裂银莲花、鹅绒委陵菜、莓叶委陵菜所代替,此时豆科植物米口袋(Gueldenstaedtia verna)出现;有效洞穴密度增至21 个/625m2时,主要伴生种出现了矮火绒草(Leontopodium nanum)和莓叶委陵菜,但有效洞穴密度达到31 个/625m2,主要伴生种和21 个/625m2时基本一致,且出现了豆科植物蓝花棘豆(Oxytropis coerulea)和雪地黄芪(Astragalus nivalis)。
|
种号
Species number | 物种
Species |
有效洞穴密度/(个/625m2)
Available burrow densities | |||
| 10 | 15 | 21 | 31 | ||
| “—”表示此物种在该样方中未出现 | |||||
| S1 | 高山嵩草Kobresia pygmaea | 0.143 | 0.190 | 0.151 | 0.128 |
| S2 | 钝裂银莲花Anemone obtusiloba | 0.052 | 0.060 | 0.058 | 0.045 |
| S3 | 鹅绒委陵菜Potentilla anserina | 0.053 | 0.054 | 0.048 | 0.051 |
| S4 | 莓叶委陵菜P. fragarioides | 0.056 | 0.054 | 0.065 | 0.064 |
| S5 | 条叶垂头菊Cremanthodium lineare | 0.065 | 0.043 | 0.039 | 0.046 |
| S6 | 小花草玉梅A. rivularis | 0.084 | 0.075 | 0.058 | 0.050 |
| S7 | 青藏苔草Carex moorcroftii | 0.090 | — | 0.095 | 0.079 |
| S8 | 条叶银莲花A. trullifolia | 0.047 | — | 0.038 | 0.038 |
| S9 | 秦艽Gentiana macrophylla | 0.067 | 0.047 | — | 0.050 |
| S10 | 乳浆大戟Euphorbia esula | — | 0.047 | 0.035 | 0.044 |
| S11 | 矮火绒草Leontopodium nanum | — | 0.053 | 0.071 | 0.066 |
| S12 | 兰石草Lancea tibetica | — | 0.046 | — | 0.025 |
| S13 | 棱子芹Pleurospermum camtschaticum | 0.029 | — | — | — |
| S14 | 圆叶筋骨草Ajuga ovalifolia | — | 0.038 | — | — |
| S15 | 米口袋Gueldenstaedtia verna | — | 0.029 | — | — |
| S16 | 小米草Euphrasia pectinata | — | — | — | 0.044 |
| S17 | 雪地黄芪Astragalus nivalis | — | — | — | 0.025 |
| S18 | 蓝花棘豆Oxytropis coerulea | — | — | — | 0.031 |
优势种高山嵩草的重要值随高原鼠兔有效洞穴密度增加呈单峰式趋势,在有效洞穴为15 个/625m2时最大,而在31 个/625m2时最小,说明优势种在高寒草甸群落内的地位和作用随有效洞穴密度增加表现为先加强后减弱的趋势。主要伴生种钝裂银莲花重要值变化过程趋同于优势种高山嵩草,但伴生种鹅绒委陵菜和莓叶委陵菜重要值变化过程均不趋同于钝裂银莲花,两者间又出现分异,鹅绒委陵菜的重要值在有效洞穴密度小于15 个/625m2生境内要大于有效洞穴密度大于21 个/625m2的生境内,但莓叶委陵菜的重要值恰好相反。条叶垂头菊的重要值随有效洞穴密度增加而先降低后升高,在21 个/625m2时最低。小花草玉梅的重要值随有效洞穴密度增加而逐渐降低,在31 个/625m2时最小。这说明高原鼠兔密度变化严重影响高寒草甸群落内不同种群的优势度,且变化过程趋异。
2.2 有效洞穴密度对草甸群落内植物种群生态位宽度的影响高原鼠兔有效洞穴密度对植物种群生态位宽度存在一定的影响,高寒草甸群落内各种植物种群利用资源秩序重新配置。当有效洞穴密度小于或等于21 个/625m2时,优势种高山嵩草生态位宽度在所有的植物种群中占据第一,说明其利用资源的能力最高,而当高原鼠兔洞穴密度增至31 个/625m2时,其生态位宽度降至并列第三,低于小米草(Euphrasia pectinata)和钝裂银莲花,等同于小花草玉梅和乳浆大戟(Euphorbia esula)(表 2)。钝裂银莲花生态位宽度随有效洞穴密度增加表现先降低后升高,在有效洞穴密度为15 个/625m2时最低,说明此种生境内钝裂银莲花利用能力最低,然而鹅绒委陵菜生态位宽度随有效洞穴密度增加表现为先升高后降低,在有效洞穴密度为15 个/625m2时最高,说明其利用资源的能力最大。有效洞穴密度小于15 个/625m2时,小花草玉梅生态位宽度小于0.470,而有效洞穴密度大于21 个/625m2时,其高于0.470,说明小花草玉梅生态位随有效洞穴密度增加而具有资源利用能力增强的态势。有效洞穴密度为10 个/625m2时,高寒草甸群落内没有矮火绒草和乳浆大戟,但当有效洞穴密度大于或等于15 个/625m2时,高寒草甸群落内均有矮火绒草和乳浆大戟种群分布,在有效洞穴密度介于15 个/625m2和21 个/625m2时,其生态位宽度较小,但到31 个/625m2时,其生态位宽度逐渐增加,说明其种群生存能力加强。
|
种号
Species number | 物种
Species |
有效洞穴密度/(个/625 m2)
Available burrow densities | |||
| 10 | 15 | 21 | 31 | ||
| S1 | 高山嵩草Kobresia pygmaea | 0.476 | 0.474 | 0.475 | 0.472 |
| S2 | 钝裂银莲花Anemone obtusiloba | 0.472 | 0.466 | 0.472 | 0.474 |
| S3 | 鹅绒委陵菜Potentilla anserina | 0.459 | 0.473 | 0.469 | 0.447 |
| S4 | 莓叶委陵菜P. fragarioides | 0.470 | 0.467 | 0.475 | 0.469 |
| S5 | 条叶垂头菊Cremanthodium lineare | 0.460 | 0.473 | 0.468 | 0.471 |
| S6 | 小花草玉梅A. rivularis | 0.465 | 0.457 | 0.475 | 0.472 |
| S7 | 青藏苔草Carex moorcroftii | 0.473 | — | 0.473 | 0.463 |
| S8 | 条叶银莲花A. trullifolia | 0.457 | — | 0.467 | 0.453 |
| S9 | 秦艽Gentiana macrophylla | 0.442 | 0.448 | 0.456 | |
| S10 | 乳浆大戟Euphorbia esula | — | 0.457 | 0.475 | 0.472 |
| S11 | 矮火绒草Leontopodium nanum | — | 0.447 | 0.467 | 0.460 |
| S12 | 兰石草Lancea tibetica | — | 0.462 | — | 0.459 |
| S13 | 棱子芹Pleurospermum camtschaticum | 0.456 | — | — | — |
| S14 | 圆叶筋骨草Ajuga ovalifolia | — | 0.473 | — | — |
| S15 | 米口袋Gueldenstaedtia verna | — | 0.471 | — | — |
| S16 | 小米草Euphrasia pectinata | — | — | — | 0.476 |
| S17 | 雪地黄芪Astragalus nivalis | — | — | — | 0.464 |
| S18 | 蓝花棘豆Oxytropis coerulea | — | — | — | 0.468 |
高寒草甸群落内种群间生态位重叠程度总体非常高,4个高原鼠兔有效洞穴密度下生态位重叠系数均大于0.900(表 3),说明种群间存在很大可能的竞争性。随高原鼠兔有效洞穴密度增加,种群间生态位重叠系数表现为先增加后降低,在21 个/625m2时最大,而在10 个/625m2时最小,到31 个/625m2时又有所降低。
| 有效洞穴密度Available burrow densities/(个/625 m2) | ||||
| 10 | 15 | 21 | 31 | |
| 平均生态位重叠值Average niche overlap | 0.946 | 0.953 | 0.976 | 0.957 |
高原鼠兔有效洞穴密度为10 个/625m2时,种群间生态位重叠系数介于0.880—0.992之间,其中高山嵩草和莓叶委陵菜的生态位重叠度最高(表 4),其系数为0.992;鹅绒委陵菜和莓叶委陵菜、高山嵩草和青藏苔草、高山嵩草和钝裂银莲花次之,分别为0.989、0.988、0.985;秦艽和棱子芹(Pleurospermum camtschaticum)重叠度最低,系数为0.880。与优势种高山嵩草生态位重叠度最高的是莓叶委陵菜,系数为0.992。说明此时优势种的主要竞争种群为莓叶委陵菜、青藏苔草和钝裂银莲花。
| S2 | S3 | S1 | S13 | S4 | S9 | S7 | S8 | S5 | S6 | |
| S2 | 1 | |||||||||
| S3 | 0.950 | 1 | ||||||||
| S1 | 0.985 | 0.981 | 1 | |||||||
| S13 | 0.924 | 0.952 | 0.963 | 1 | ||||||
| S4 | 0.973 | 0.989 | 0.992 | 0.952 | 1 | |||||
| S9 | 0.934 | 0.956 | 0.941 | 0.880 | 0.941 | 1 | ||||
| S7 | 0.979 | 0.953 | 0.988 | 0.969 | 0.975 | 0.904 | 1 | |||
| S8 | 0.944 | 0.954 | 0.965 | 0.956 | 0.952 | 0.951 | 0.969 | 1 | ||
| S5 | 0.974 | 0.966 | 0.970 | 0.932 | 0.977 | 0.964 | 0.966 | 0.972 | 1 | |
| S6 | 0.955 | 0.914 | 0.966 | 0.957 | 0.936 | 0.859 | 0.968 | 0.915 | 0.904 | 1 |
高原鼠兔有效洞穴密度为15 个/625m2时,生态位重叠度最高的是鹅绒委陵菜和条叶垂头菊,其系数为0.997(表 5),而高山嵩草和圆叶筋骨草(Ajuga ovalifolia)、条叶垂头菊和圆叶筋骨草、高山嵩草和条叶垂头菊次之,系数分别为0.993、0.992、0.989,秦艽和兰石草(Lancea tibetica)之间的生态位重叠度最低,系数为0.841。与优势种高山嵩草生态位重叠度最高的是圆叶筋骨草,系数为0.993。
| S2 | S3 | S1 | S11 | S12 | S4 | S15 | S9 | S10 | S5 | S6 | S14 | |
| S2 | 1 | |||||||||||
| S3 | 0.951 | 1 | ||||||||||
| S1 | 0.978 | 0.986 | 1 | |||||||||
| S11 | 0.929 | 0.924 | 0.964 | 1 | ||||||||
| S12 | 0.932 | 0.971 | 0.961 | 0.891 | 1 | |||||||
| S4 | 0.947 | 0.962 | 0.984 | 0.961 | 0.914 | 1 | ||||||
| S15 | 0.973 | 0.973 | 0.980 | 0.916 | 0.985 | 0.946 | 1 | |||||
| S9 | 0.962 | 0.910 | 0.953 | 0.945 | 0.841 | 0.957 | 0.897 | 1 | ||||
| S10 | 0.908 | 0.966 | 0.951 | 0.886 | 0.928 | 0.945 | 0.941 | 0.864 | 1 | |||
| S5 | 0.947 | 0.997 | 0.989 | 0.934 | 0.977 | 0.968 | 0.977 | 0.905 | 0.968 | 1 | ||
| S6 | 0.943 | 0.928 | 0.944 | 0.908 | 0.923 | 0.932 | 0.965 | 0.885 | 0.898 | 0.931 | 1 | |
| S14 | 0.964 | 0.989 | 0.993 | 0.956 | 0.967 | 0.971 | 0.981 | 0.924 | 0.970 | 0.992 | 0.951 | 1 |
高原鼠兔有效洞穴密度增至21 个/625m2时,生态位重叠度最高的是钝裂银莲花和青藏苔草,钝裂银莲花和小花草玉梅、小花草玉梅和青藏苔草、鹅绒委陵菜和乳浆大戟,均为0.995(表 6),乳浆大戟和小花草玉梅次之,系数为0.990,最低的是鹅绒委陵菜和条叶银莲花,系数为0.934。与优势种高山嵩草生态位重叠度最高的是乳浆大戟,其系数为0.988。
| S2 | S3 | S1 | S11 | S4 | S10 | S7 | S8 | S5 | S6 | |
| S2 | 1 | |||||||||
| S3 | 0.969 | 1 | ||||||||
| S1 | 0.981 | 0.975 | 1 | |||||||
| S11 | 0.980 | 0.955 | 0.971 | 1 | ||||||
| S4 | 0.974 | 0.964 | 0.984 | 0.963 | 1 | |||||
| S10 | 0.983 | 0.995 | 0.988 | 0.965 | 0.983 | 1 | ||||
| S7 | 0.995 | 0.971 | 0.977 | 0.977 | 0.978 | 0.985 | 1 | |||
| S8 | 0.971 | 0.934 | 0.975 | 0.958 | 0.980 | 0.956 | 0.977 | 1 | ||
| S5 | 0.972 | 0.980 | 0.985 | 0.966 | 0.965 | 0.979 | 0.963 | 0.956 | 1 | |
| S6 | 0.995 | 0.981 | 0.986 | 0.981 | 0.979 | 0.990 | 0.995 | 0.979 | 0.984 | 1 |
高原鼠兔有效洞穴密度达31 个/625m2时,生态位重叠度最高的是钝裂银莲花和小米草,其系数为0.997(表 7)。乳浆大戟和小米草、高山嵩草和条叶垂头菊、小花草玉梅和小米草次之,分别为0.996、0.995、0.995,生态位重叠度最低的是条叶银莲花和兰石草,其系数为0.866。与优势种高山嵩草生态位重叠度最高的是条叶垂头菊,其系数为0.995。
| S2 | S3 | S1 | S17 | S11 | S18 | S12 | S4 | S9 | S10 | S7 | S8 | S5 | S6 | S16 | |
| S2 | 1 | ||||||||||||||
| S3 | 0.950 | 1 | |||||||||||||
| S1 | 0.993 | 0.958 | 1 | ||||||||||||
| S17 | 0.963 | 0.911 | 0.978 | 1 | |||||||||||
| S11 | 0.939 | 0.891 | 0.961 | 0.963 | 1 | ||||||||||
| S18 | 0.961 | 0.898 | 0.964 | 0.986 | 0.966 | 1 | |||||||||
| S12 | 0.954 | 0.901 | 0.973 | 0.945 | 0.981 | 0.932 | 1 | ||||||||
| S4 | 0.993 | 0.918 | 0.978 | 0.956 | 0.910 | 0.953 | 0.927 | 1 | |||||||
| S9 | 0.976 | 0.937 | 0.984 | 0.941 | 0.926 | 0.908 | 0.971 | 0.961 | 1 | ||||||
| S10 | 0.993 | 0.941 | 0.990 | 0.983 | 0.939 | 0.977 | 0.939 | 0.991 | 0.960 | 1 | |||||
| S7 | 0.989 | 0.925 | 0.975 | 0.934 | 0.891 | 0.919 | 0.929 | 0.993 | 0.978 | 0.978 | 1 | ||||
| S8 | 0.945 | 0.938 | 0.948 | 0.967 | 0.898 | 0.964 | 0.866 | 0.940 | 0.889 | 0.971 | 0.912 | 1 | |||
| S5 | 0.984 | 0.953 | 0.995 | 0.966 | 0.976 | 0.958 | 0.988 | 0.960 | 0.981 | 0.924 | 0.959 | 0.924 | 1 | ||
| S6 | 0.987 | 0.969 | 0.983 | 0.963 | 0.940 | 0.972 | 0.930 | 0.972 | 0.942 | 0.988 | 0.958 | 0.973 | 0.975 | 1 | |
| S16 | 0.997 | 0.957 | 0.994 | 0.975 | 0.953 | 0.976 | 0.954 | 0.986 | 0.965 | 0.996 | 0.975 | 0.963 | 0.986 | 0.995 | 1 |
高原鼠兔一方面通过直接啃食行为而影响高寒草甸植物的正常生长发育,另一方面通过挖掘活动而间接影响高寒草甸植物的生理特性[12, 13],因此随着高原鼠兔有效洞穴密度变化,高寒草甸植物群落组分会发生相应的调整[1],以实现生态系统的再平 衡。本研究结果表明,随高原鼠兔有效洞穴密度增 加,样方内出现的植物种数逐渐增多,说明高原鼠兔活动增加了高寒草甸植物群落的物种丰富度,但增加物种主要是有毒的乳浆大戟、圆叶筋骨草、蓝花棘豆,以及适口性差的矮火绒草和兰石草,草甸质量变劣,这与石红霄等人[14]在青海果洛地区的研究结果相似。然而值得注意的是随着有效洞穴密度增加,豆科类植物入侵的种类和比例有所增加,这一定程度上有助于提高土壤固持氮和碳的能力[15]。本研究发现,随着高原鼠兔有效洞穴密度从10 个/625m2时增至31 个/625m2过程中,高寒草甸植物群落的优势种均为高山嵩草,说明高山嵩草在群落中的主导地位并没有发生明显的改变,高寒草甸群落并没有变化为其他群落,群落内组分的变化属于群落内部波动的范畴,其变化主要发生群落内的伴生种,这与Guo等人[9]对青海果洛地区的研究结果趋同。
虽然高寒草甸群落没有随着有效洞穴密度增加而发生质的改变,演变成其他群落,但当高原鼠兔有效洞穴密度增加时群落优势种高山嵩草的重要值先增高后降低,说明高原鼠兔密度变化时优势种在群落内的地位也随之发生改变。优势种高山嵩草重要值在15 个/625m2时最大,说明适宜的有效洞穴密度强化了优势种在群落内的地位和作用,在31 个/625m2时最小,说明有效洞穴密度过大时优势种在群落内的地位和作用反而削弱。草甸群落优势种地位和作用随高原鼠兔有效洞穴密度变化而变化,势必联动的引起伴生种在群落内地位和作用的变化,这是因为高原鼠兔有效洞穴增加,意味着裸露鼠斑面积增加,高寒草甸生境异质性增加,一方面为原来处于竞争劣势,被抑制的物种创造了茁壮生长的机会,另外一方面,为一些机会主义者,如毒杂草入侵创造了条件,使草甸群落内物种间的竞争更为多样化,有可能出现物种利用资源方式的分化,客观上影响了优势种和主要伴生种获取资源的范围,如主要伴生种小花草玉梅的重要值随有效洞穴密度增加而逐渐降低,条叶垂头菊和乳浆大戟的重要值则随着有效洞穴密度增加而增加。
本研究结果表明,当高原鼠兔有效洞穴密度低于21 个/625m2时,优势种高山嵩草的生态位宽度在所有种群中均位居第一,而高原鼠兔有效洞穴密度增至31 个/625m2时,优势种高山嵩草的生态位宽度降至并列第三,这说明有效洞穴密度较小时,优势种的特化程度小,在竞争性利用各种资源的过程中,保持有较高的竞争力[16, 17, 18, 19],这是因为高山嵩草具有极强的克隆生长能力,它通过侧芽迅速生长形成致密的草皮,这提高了抵抗外界机械作用的能力[20],所以在有效洞穴密度从10 个/625m2上升到21 个/625m2时,高山嵩草的生态位宽度位居第一,当有效洞穴密度过大时,优势种特化程度增加,与其他物种的竞争能力逐渐下降,其竞争性利用资源的能力降低,这可能是改变后的生境已经逐渐不十分适配优势种的生长。高原鼠兔有效洞穴密度较低时,毒杂草生态位宽度较小,如秦艽仅为0.442,有些群落内未出现毒杂草如乳浆大戟和矮火绒草等,说明有效洞穴密度较低时毒杂草利用资源能力有限,主要受优势种较强的竞争力所抑制,随高原鼠兔有效洞穴密度升高时,毒杂草(如秦艽)的生态位宽度增大,群落内出现毒杂草如乳浆大戟和矮火绒草。
不同有效洞穴密度下物种间平均生态位重叠度总体较高,说明高原鼠兔活动强度的变化,迫使高寒草甸群落内植物种群重新配制他们间资源利用的过程和方式,以谋取最大利益,这客观上加剧了群落内种群间的竞争激烈程度[21],导致种群间的生态位重叠系数平均值大于0.900。在有效洞穴密度分别为10、15、21、31 个/625m2时,与优势种高山嵩草竞争力最大的物种分别为莓叶委陵菜、圆叶筋骨草、乳浆大戟、条叶垂头菊,这说明高原鼠兔活动强度的差异,决定了与优势种的主要竞争物种出现分异,当有效洞穴密度从10 个/625m2增加至31 个/625m2的过程中,竞争力最强的两个物种从高山嵩草和莓叶委陵菜变化为钝裂银莲花和小米草,竞争力最低的两个物种从秦艽和棱子芹演变为条叶银莲花和兰石草,说明当高原鼠兔有效洞穴密度为10 个/625m2时,高山嵩草是种群间竞争最激烈的一方,但当高原鼠兔有效洞穴密度超过或等于15 个/625m2时,优势种高山嵩草则没有出现在种群间竞争强度最激烈的双方。
综上所述,随高原鼠兔有效洞穴密度增加,高寒草甸群落组分、物种重要值、生态位宽度和生态位重叠值均发生一定程度的变化,样方内植物种数逐渐增多,但主要是豆科类和毒杂草,高山嵩草的重要值先增加后降低,在15 个/625m2下最高,说明其在群落内的地位和作用发生了显著变化;当高原鼠兔有效洞穴密度低于或等于21 个/625m2,优势种生态位宽度位居第一,当高原鼠兔有效洞穴密度达31 个/625m2时,其生态位宽度低于小米草和钝裂银莲花,等同于小花草玉梅和乳浆大戟;虽然不同高原鼠兔有效洞穴密度下,与优势种高山嵩草生态位重叠系数最大的物种不一样,当高原鼠兔有效洞穴密度为10 个/625m2时,高山嵩草是种群间竞争强度最大的一方,但当高原鼠兔有效洞穴密度超过或等于15 个/625m2时,高山嵩草则退出了种群间竞争强度最激烈的局面。
致谢: 兰州大学草地农业科技学院周杰,张晓黎,赵旭,陈龙参加野外调查工作,谨致谢忱。
| [1] | Smith A T, Foggin J M. The plateau pika (Ochotona curzoniae) is a keystone species for biodiversity on the Tibetan plateau. Animal Conservation, 1999, 344: 235-240. |
| [2] | Arthur A D, Pech R P, Davey C, Jiebu, Zhang Y M, Lin H. Livestock grazing, plateau pikas and the conservation of avian biodiversity on the Tibetan plateau. Biological Conservation, 2008, 141(8): 1972-1981. |
| [3] | Howe H F, Smallwood J. Ecology of seed dispersal. Annual Review of Ecology and Systematics, 1982, 13: 201-228. |
| [4] | Sun F D, Guo Z G, Shang Z H, Long R J. Effects of density of burrowing plateau pikas (Ochotona curzoniae) on soil physical and chemical properties of alpine meadow soil. Acta Pedologica Sinica, 2010, 47(2): 378-383. |
| [5] | Zhou X R, Guo Z G, Guo X H. The role of plateau pika and plateall zokor in alpine meadow. Pratacultural Science, 2010, 27(5): 38-44. |
| [6] | Guo Z G, Zhou X R, Hou Y. Effect of available burrow densities of plateau pika (Ochotona curzoniae) on soil physicochemical property of the bare land and vegetation land in the Qinghai-Tibetan Plateau. Acta Ecologica Sinica, 2012, 32(2): 104-110. |
| [7] | Liu W, Li L, Yan H Y, Sun H Q, Zhang L. Effects of burrowing activity of plateau pika (Ochotona curzoniae) on plant species richness and aboveground biomass. Acta Theriologica Sinica, 2012, 32(3): 216-220. |
| [8] | Zhang J. Population of Plateau Pika Response to Regulated Measures of Vegetation. Lanzhou: Lanzhou University, 2011. |
| [9] | Guo Z G, Li X F, Liu X Y, Zhou X R. Response of alpine meadow communities to burrow density changes of plateau pika (Ochotona curzoniae) in the Qinghai-Tibet Plateau. Acta Ecologica Sinica, 2012, 32(1): 44-49. |
| [10] | Levins R. Evolution in Changing Environments: Some Theoretical Explorations. Princeton: Princeton University Press, 1968. |
| [11] | Pianka E R. The structure of lizard communities. Annual Review of Ecology and Systematics, 1973, 4: 53-74. |
| [12] | Pech R P, Arthur A D, Zhang Y M, Lin H. Population dynamics and responses to management of plateau pikas Ochotona curzoniae. Journal of Applied Ecology, 2007, 44(3): 615-624. |
| [13] | Wesche K, Nadrowski K, Retzer V. Habitat engineering under dry conditions: the impact of pikas (Ochotona pallasi) on vegetation and site conditions in southern Mongolian steppes. Journal of Vegetation Science, 2007, 18(5): 665-674. |
| [14] | Shi H X, Yu J L. Influence of burrowing rodent density plots on the alpine Kobresia meadows structure and soil water content. Chinese Journal of Grassland, 2010, 344: 109-112, 116-116. |
| [15] | He N P, Han X G, Yu G R. Carbon and nitrogen sequestration rate in long-term fenced grasslands in Inner Mongolia, China. Acta Ecologica Sinica, 2011, 31(15): 4270-4276. |
| [16] | Hurlbert S H. The measurement of niche overlap and some relatives. Ecology, 1978, 59(1): 67-77. |
| [17] | Wang G, Zhao S L, Zhang P Y, Chen Q C. On the definition of niche and the improved formula for measuring niche overlap. Acta Ecologica Sinica, 1984, 4(2): 119-127. |
| [18] | Weider L J. Niche breadth and life history variation in a hybrid daphnia complex. Ecology, 1993, 74(3): 935-943. |
| [19] | Zhang J Y, Zhao H L, Zhang T H, Zhao X Y. Niche dynamics of main populations of plants communities in the restoring succession process in Horqin Sandy Land. Acta Ecologica Sinica, 2003, 23(12): 2741-2746. |
| [20] | Miehe G, Miehe S, Kaiser K, Liu J Q, Zhao X Q. Status and dynamics of the Kobresia pygmaea ecosystem on the Tibetan Plateau. AMBIO, 2008, 344: 258-265. |
| [21] | Spiex T A, Franklin J F, Klopsch M. Canopy gaps in Douglas-fir forests of the Cascade Mountains. Canadian Journal of Forest Research, 1990, 20(5): 649-658. |
| [4] | 孙飞达, 郭正刚, 尚占环, 龙瑞军. 高原鼠兔洞穴密度对高寒草甸土壤理化性质的影响. 土壤学报, 2010, 47(2): 378-383. |
| [5] | 周雪荣, 郭正刚, 郭兴华. 高原鼠兔和高原鼢鼠在高寒草甸中的作用. 草业科学, 2010, 27(5): 38-44. |
| [7] | 刘伟, 李里, 严红宇, 孙海群, 张莉. 高原鼠兔挖掘活动对植物种的丰富度和地上生物量的影响. 兽类学报, 2012, 32(3): 216-220. |
| [8] | 张军. 高原鼠兔种群数量对植被调控措施的响应 [D]. 兰州: 兰州大学, 2011. |
| [14] | 石红霄, 于健龙. 高原鼠兔洞口密度对高寒嵩草草甸植被及土壤水分的影响. 中国草地学报, 2010, 344: 109-112, 116-116. |
| [15] | 何念鹏, 韩兴国, 于贵瑞. 长期封育对不同类型草地碳贮量及其固持速率的影响. 生态学报, 2011, 31(15): 4270-4276. |
| [17] | 王刚, 赵松岭, 张鹏云, 陈庆诚. 关于生态位定义的探讨及生态位重叠计测公式改进的研究. 生态学报, 1984, 4(2): 119-127. |
| [19] | 张继义, 赵哈林, 张铜会, 赵学勇. 科尔沁沙地植物群落恢复演替系列种群生态位动态特征. 生态学报, 2003, 23(12): 2741-2746. |
| [20] | Miehe G, Miehe S, Kaiser K, 刘健全, 赵新全. 青藏高原高山嵩草 (Kobresia pygmaea) 生态系统的现状与动态. AMBIO-人类环境杂志, 2008, 344: 258-265. |
 2014, Vol.34
2014, Vol.34




