文章信息
- 邓华堂, 段辛斌, 刘绍平, 陈大庆
- DENG Huatang, DUAN Xinbin, LIU Shaoping, CHEN Daqing
- 大宁河下游主要鱼类营养结构的时空变化
- Temporal and spatial variations in the trophic structure of key species in downstream of the Daning River
- 生态学报, 2014, 34(23): 7110-7118
- Acta Ecologica Sinica, 2014, 34(23): 7110-7118
- http://dx.doi.org/10.5846/stxb201306091555
-
文章历史
- 收稿日期:2013-06-09
- 网络出版日期:2014-06-15
2. 中国水产科学研究院长江水产研究所, 农业部长江中上游渔业资源环境科学观测实验站, 武汉 430223
2. Scientific Observing and Experimental Station of fishery Resources and Environment in the Upper and Middle Reaches of the Yangtze River, Ministry of Agriculture; Yangtze River Fisheries Research Institute, Chinese Academy of Fishery Sciences, Wuhan 430223, China
阐明食物网结构是研究水生生态系统物质循环和能量流动的基础,传统定量研究食物网结构的方法主要是胃肠含物分析。随着技术的进步,稳定性同位素分析方法已经成为研究水生生态系统食物网结构与动力的重要手段之一[1, 2]。由于生物组织的各稳定同位素比值能代表相应的生物与非生物的多维生态空间信息[3, 4],由各稳定同位素值为坐标组成的“δ-空间”被定义为同位素生态位(isotopic niche)[5]。同位素生态位研究反映的是物种时空整合的数据[5],能够区分食物网中各物种营养位置中的细微差别[6, 7],因此同位素生态位的各种研究方法能够对个体、种群及群落特征分析提供新的研究思路和更为精确的研究结果。目前,最常用的是由δ13C-δ15N值双坐标图(bi-plots)组成的双维空间生态位[6, 8, 9]。Layman等根据形态生态学研究中物种形态指标方法提出双标图中6个营养结构的同位素量化指标[6]。Hoeinghaus认为,由于这些指标并未考虑基础碳源的同位素值和同位素值的标准化问题,可能并不适用大多数食物网研究[10]。然而,通过合理的采样及修正策略[11],这些指标已应用于描述个体生态位宽度[12, 13]和群落特征[6] 研究中。通过引入统计学概念与方法,新增了量化指标[8, 9]及指标的误差分析[14],能提高研究结果的准确性。
基于各种同位素值量化的生态指标不仅能够用于描述物种水平的生态位宽度和重叠度,还能评估各种因素对物种生态位宽度影响或食物网特征变化的影响[6, 12, 15]。目前,同位素生态指标已应用于物种的引入和生态修复等对生态系统影响的研究中[16, 17]。而国内尚无关于三峡库区大宁河鱼类营养结构特征及其时空变化的稳定同位素研究。
大宁河位于巫山以东,是长江上游最重要的支流之一,鱼类资源丰富[18]。三峡水库蓄水后,由于生态环境的改变,大宁河鱼类组成发生变化[18, 19]。加之大宁河流域正开展增殖放流等生态修复措施,目前需要了解大宁河主要鱼类群落营养结构的时空变化规律,开展以上因素对大宁河鱼类营养结构产生的影响研究。本文的研究目的是利用碳、氮稳定性同位素技术研究探讨大宁河不同水位时期及不同地点主要鱼类群落食物网营养结构变化特征,为进一步评估不同的调控措施对大宁河渔业生态系统各指标变化的研究奠定基础,最终为增殖放流的物种确定、增殖放流的效果评价等生态调控技术措施提供理论依据。
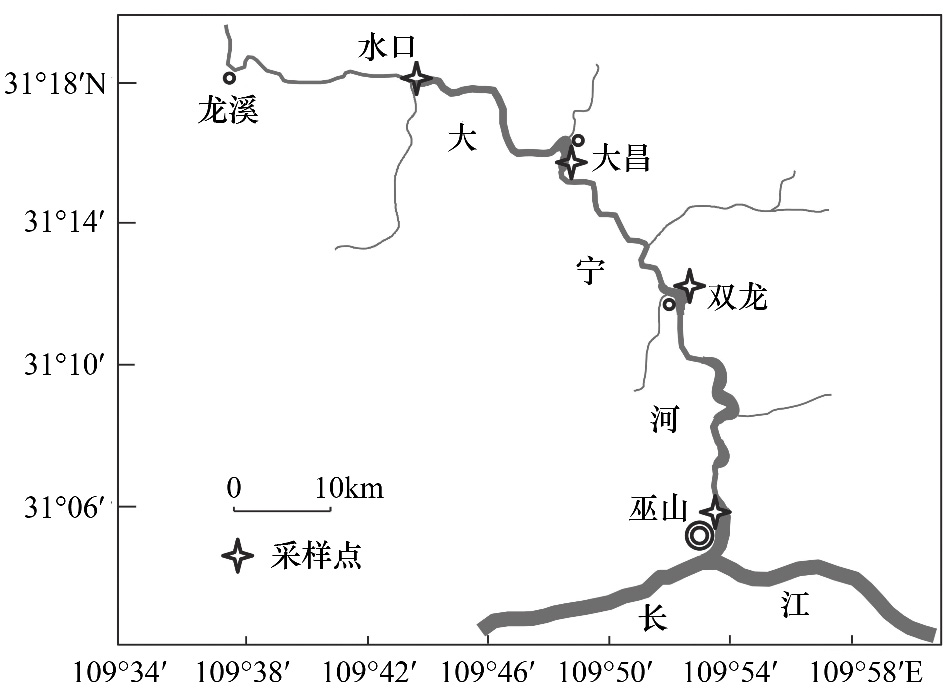
1 研究方法 1.1 研究区域与时间本文研究水域为三峡库区蓄水后大宁河巫山-水口段静水水域,长约40 km,河面狭窄,平均宽度约 60 m,该河段水文状况复杂,鱼类资源丰富[19]。本研究于2011年5月(低水位时期,水位145 m)和10月(高水位时期,水位170 m)在大宁河巫山-水口静水江段开展采样工作(图 1)。鱼类样本主要是通过三层刺网、地笼和板罾网获得。鱼类采样点设置为巫山和大昌,两点相距约30 km。颗粒有机物(POM)采样点设置为巫山(0 km距河口)、双龙(14 km)、大昌(30 km)、水口(40 km)(图 1)。
|
| 图 1 采样点分布图 Fig.1 Map of Daning River and location of sampling sites |
在两个采样点共采集鱼类24种共88尾。鱼类取其背部肌肉,在70 ℃下连续烘干至恒重,使用研钵研碎成均匀粉末,干燥保存。POM样品在各采样点采上中下层水混合,抽滤到预先灼烧的 Whatman GF /C纤维滤膜上获得,用去离子水冲洗后,于60 ℃烘干24 h至恒重,用锡箔纸包裹后保存[20]。
所有样品的稳定性同位素比值测定均使用Flash EA1112 HT 元素分析仪和DELTA V Advantage 同位素比率质谱仪(中国林业科学院)进行。碳氮稳定性同位数分析分别采用国际标准物质PDB(Pee Dee Belnite)和标准大气氮对比。测定精度δ13C<0.1‰,δ15N<0. 2‰。
1.3 数据计算与统计分析δ13C-δ15N值双坐标图中6个指标为氮值范围NR(δ15N range)、碳值范围CR(δ13C range)、总面积TA(Total area)、平均离心距离CD(Mean distance to centroid)、平均最邻近距离NND(Mean nearest neighbor distance)、最邻近距离标准差SDNND(Standard deviation of nearest neighbor distance)。各指标计算参考Layman等[6],其中 TA为各物种在δ13C-δ15N值双坐标图中组成多边形面积(convex hull area),其值采用ArcGIS 9.3计算[12]。
采用配对双样本t检验,对不同采样站点、不同水位时期的同种鱼类稳定性同位素值进行差异分析。对上述统计分析均通过SPSS16.0软件完成,图像处理采用CorelDRAW 12.0软件。实验数据用平均数±标准差(Mean±SD)表示。
2 结果与分析 2.1 大宁河下游主要鱼类种类组成2011年,在大宁河两个采样点种共调查到鱼类39种,隶属于5目10科33属,其中鲤形目25属28种,鲇形目4属7种,鲈形目2属2种,合鳃鱼目、鲑形目各1属1种。鲤科鱼类在大宁河下游占优势,共22属25种,占总种数的64.10%。
巫山采样点共调查到鱼类37种,其中5月32种,10月23种,大昌采样点共调查到鱼类29种,其中5月26种,10月21种。在大宁河静水江段优势种主要包括鲤(Cyprinus carpio)、鲇(Silurus asotus)、翘嘴鲌(Culter alburnus)、大眼鳜(Siniperca kneri)、贝氏 (Hemiculter bleekeri)、 (Hemiculter leucisculus)、鱤(Elopichthys bambusa)、鲢(Hypophthalmichthys molitrix)、鳙(Aristichthys nobilis)、鲫(Carassius auratus)、瓦氏黄颡鱼(Pseudobagrus vachellii)、光泽黄颡鱼(Peltevbagrus nitidus)、草鱼(Ctenopharyngodon idella)、胭脂鱼(Myxocyprinus asiaticus)、长吻鮠(Leiocassis longirostris)、兴凯鱊(Acanthorhodeus chankaensis)、太湖新银鱼(Neosalanx taihuensis)、蛇鮈(Saurogobio dabryi)、子陵吻鰕虎鱼(Rhinogobius giurinus)等。其中鲢、鳙、草鱼、胭脂鱼、长吻鮠为大宁河主要增殖放流经济物种。
2.2 碳、氮稳定性同位素组成及其变化特征测定大宁河静水水域4个采样点颗粒有机物(POM)样品δ13C、δ15N值,其中δ13C值范围为-29.08‰—-21.82‰,均值为(-25.27±2.61)‰,δ15N值范围在3.99‰—7.06‰之间,均值为(4.68±1.30)‰(表 1)。δ13C值与河口距离有极显著负相关性(R 2=0.9638,P=0.00<0.01),随河口距离而减小,而氮值与河口距离无显著相关性(R2= 0.4546,P=0.14>0.05)。
|
采样点
Sampling site | (δ13C±SD)/‰ | (δ15N±SD)/‰ | n |
| 水口 | -29.08 | 3.99 | 1 |
| 大昌 | -26.23±0.68 | 4.21±0.70 | 2 |
| 双龙 | -25.30 | 3.58 | 1 |
| 巫山 | -22.40±0.81 | 6.05±1.43 | 2 |
| 平均Average | -25.27±2.61 | 4.68±1.30 | 6 |
不同水位时期、不同地点鱼类样品碳、氮稳定性同位素比值见表 2、表 3。鱼类δ13C值范围在-29.74‰(太湖新银鱼Neosalanx taihuensis)—-16.61‰(草鱼Ctenopharyngodon idella)之间,相差达13.14‰(表 2),δ15N值范围在4.54‰(鲢Hypophthalmichthys molitrix)—17.51‰(铜鱼Coreius heterodon)之间,相差达12.96‰(表 3)。5月δ13C值范围为-29.74‰(太湖新银鱼)—-17.86‰(鲤Cyprinus carpio),δ15N值范围为4.54‰(鲢)—12.91%(蒙古鲌Culter mongolicus);10月δ13C值范围为-26.32(鳙Aristichthys nobilis)—-16.61‰(草鱼),δ15N值范围为 6.63(草鱼)—17.51‰(铜鱼)。
|
种类
Species | 体长范围/mm
Body length range | (δ13C±SD)/‰ | |||||
| 5月 May | 10月 October | ||||||
| 巫山 | 大昌 | n | 巫山 | 大昌 | n | ||
| 鳊Parabramis pekinensis | 245—250 | -20.36±2.69 | 2 | ||||
| 贝氏 Hemiculter bleekeri | 143—182 | -23.19 | -23.47 | 2 | -25.94 | 1 | |
| 粗唇鮠Pseudobagrus crassilabris | 190 | -24.30 | 1 | ||||
| 长吻鮠Leiocassis longirostris | 195—210 | -21.29±0.42 | 2 | ||||
| 草鱼Ctenopharyngodon idella | 175—251 | -22.57±1.44 | -22.54 | 3 | -18.65 | -18.76±3.04 | 3 |
| 赤眼鳟Squaliobarbus curriculus | 244—260 | -21.83 | 1 | -20.25 | 1 | ||
| 达氏鲌Culter dabryi dabryi | 230—302 | -22.57±0.56 | -23.92 | 3 | -24.10 | 1 | |
| 大眼鳜Siniperca kneri | 165—262 | -22.18±1.29 | -24.32 | 3 | -22.16±0.28 | -23.96±0.5 | 5 |
| 鳡Elopichthys bambusa | 106—270 | -23.41±0.25 | 3 | -22.63±1.27 | -25.87 | 3 | |
| 鲫Carassius auratus | 157—225 | -20.6±0.49 | -18.24 | 3 | -20.37±0.81 | 4 | |
| 鲤Cyprinus carpio | 190—220 | -19.67±2.55 | 2 | ||||
| 鲢Hypophthalmichthys molitrix | 148—342 | -26.76±1.61 | -26.26±1.16 | 6 | -23.63 | -25.94 | 2 |
| 蒙古鲌Culter mongolicus | 190—222 | -23.97±0.74 | 2 | -21.99 | 1 | ||
| 鲇Silurus asotus | 170—205 | -24.33±0.42 | -24.57 | 3 | |||
| 翘嘴鲌Culter alburnus | 223—490 | -23.32 | -25.48±0.1 | 3 | -22.72±0.03 | -24.62±0.34 | 5 |
| 似鳊Pseudobrama simoni | 115—150 | -22.73 | 1 | -23.63 | 1 | ||
| 蛇鮈Saurogobio dabryi | 135 | -25.93 | 1 | ||||
| 铜鱼Coreius heterodon | 220—231 | -24.37 | 1 | -25.77 | 1 | ||
| 团头鲂Megalobrama amblycephala | 220 | -23.50 | 1 | ||||
| 瓦氏黄颡鱼Pseudobagrus vachellii | 130—220 | -22.86±1.94 | -22.78 | 3 | -24.86 | -23.57±0.63 | 4 |
| 鳙Aristichthys nobilis | 210—312 | -24.55±1.08 | -27.49±0.29 | 4 | -25.77 | -26.32 | 2 |
| 银鮈Squalidus argentatus | 103 | -24.47 | 1 | ||||
| 太湖新银鱼Neosalanx taihuensis | -29.74 | 1 | |||||
| 胭脂鱼Myxocyprinus asiaticus | 162—163 | -20.67±0.27 | 2 | ||||
| 合计total | 29 | 18 | 47 | 17 | 24 | 41 | |
|
种类
Species | 体长范围/mm
Body length range | (δ13C±SD)/‰ | |||||
| 5月 May | 10月 October | ||||||
| 巫山 | 大昌 | n | 巫山 | 大昌 | n | ||
| 鳊Parabramis pekinensis | 245—250 | 7.77±0.75 | 2 | ||||
| 贝氏 Hemiculter bleekeri | 143—182 | 6.16 | 7.93 | 2 | 8.77 | 1 | |
| 粗唇鮠Pseudobagrus crassilabris | 190 | 10.18 | 1 | ||||
| 长吻鮠Leiocassis longirostris | 195—210 | 8.90±0.23 | 2 | ||||
| 草鱼Ctenopharyngodon idella | 175—251 | 4.59±0.01 | 6.26 | 3 | 9.37 | 7.62±1.4 | 3 |
| 赤眼鳟Squaliobarbus curriculus | 244—260 | 8.24 | 1 | 7.10 | 1 | ||
| 达氏鲌Culter dabryi dabryi | 230—302 | 10.47±0.01 | 9.80 | 3 | 11.06 | 1 | |
| 大眼鳜Siniperca kneri | 165—262 | 10.77±0.87 | 11.43 | 3 | 13.66±0.32 | 12.17±1.2 | 5 |
| 鳡Elopichthys bambusa | 106—270 | 10.37±0.48 | 3 | 12±0.67 | 10.25 | 3 | |
| 鲫Carassius auratus | 157—225 | 7.02±0.57 | 8.05 | 3 | 8.88±0.38 | 4 | |
| 鲤Cyprinus carpio | 190—220 | 5.76±0.57 | 2 | ||||
| 鲢Hypophthalmichthys molitrix | 148—342 | 7.93±2.3 | 7.37±1.26 | 6 | 8.40 | 8.80 | 2 |
| 蒙古鲌Culter mongolicus | 190—222 | 11.44±2.07 | 2 | 13.00 | 1 | ||
| 鲇Silurus asotus | 170—205 | 13.07±2.2 | 11.42 | 3 | |||
| 翘嘴鲌Culter alburnus | 223—490 | 11.78 | 10.43±0.15 | 3 | 12.49±0.64 | 11.53±1.42 | 5 |
| 似鳊Pseudobrama simoni | 115—150 | 9.30 | 1 | 7.62 | 1 | ||
| 蛇鮈Saurogobio dabryi | 135 | 10.60 | 1 | ||||
| 铜鱼Coreius heterodon | 220—231 | 12.03 | 1 | 17.51 | 1 | ||
| 团头鲂Megalobrama amblycephala | 220 | 5.29 | 1 | ||||
| 瓦氏黄颡鱼Pseudobagrus vachellii | 130—220 | 8.61±2.25 | 9.29 | 3 | 11.44 | 9.83±0.64 | 4 |
| 鳙Aristichthys nobilis | 210—312 | 8.12±2.54 | 6.34±0.81 | 4 | 9.19 | 8.62 | 2 |
| 银鮈Squalidus argentatus | 103 | 10.28 | 1 | ||||
| 太湖新银鱼Neosalanx taihuensis | 12.00 | 1 | |||||
| 胭脂鱼Myxocyprinus asiaticus | 162—163 | 9.14±0.22 | 2 | ||||
| 合计 total | 47 | 41 | |||||
选取同种类不同站点的鱼类碳、氮稳定性同位素值进行空间差异比较。配对双样本t检验结果表明(表 4),在5月,巫山站点与大昌站点δ13C值、δ15N值均无显著性差异(P>0.05);在10月时,不同站点间δ13C值无显著性差异(t=2.15,P=0.069),而δ15N值有显著性差异(t=4.39,P=0.003)。同种类不同水位时期的碳氮稳定性同位素值时间差异比较结果表明(表 4),δ13C值在不同水位时期的各站点中均无显著性差异(P>0.05),δ15N值在不同水位时期的各站点中均存在显著性差异(P<0.05)。
|
对比项
Comparative items | 分类
Category | 种类数
NO. of species | δ13C | δ15N | ||||||
| 均数
Mean | 检验值
t value | 自由度
df | 显著性
Sig.(P) | 均数
Mean | 检验值
t value | 自由度
df | 显著性
Sig.(P) | |||
| 巫山-大昌 | 5月 | 9 | 0.65 | 1.19 | 8 | 0.267 | -0.16 | -0.37 | 8 | 0.721 |
| 10月 | 8 | 1.11 | 2.15 | 7 | 0.069 | 1.2 | 4.39 | 7 | 0.003 | |
| 5—10月 | 巫山 | 9 | -0.60 | -0.89 | 8 | 0.397 | -2.08 | -2.95 | 8 | 0.018 |
| 大昌 | 10 | 0.00 | 0.00 | 9 | 0.999 | -0.87 | -2.69 | 9 | 0.025 | |
对不同采样站点、不同水位时期的同种鱼组成的鱼类群落分析大宁河下游静水区域鱼类营养结构的时空变化情况。通过δ13C-δ15N值双坐标图计算6个生态学指标,各时期各站点的计算结果见图 2—图 5。前4个指标反应物种空间范围,代表群落营养多样性(trophic diversity);后两个指标反应物种相对位置,代表营养冗余(trophic redundancy)[6]。
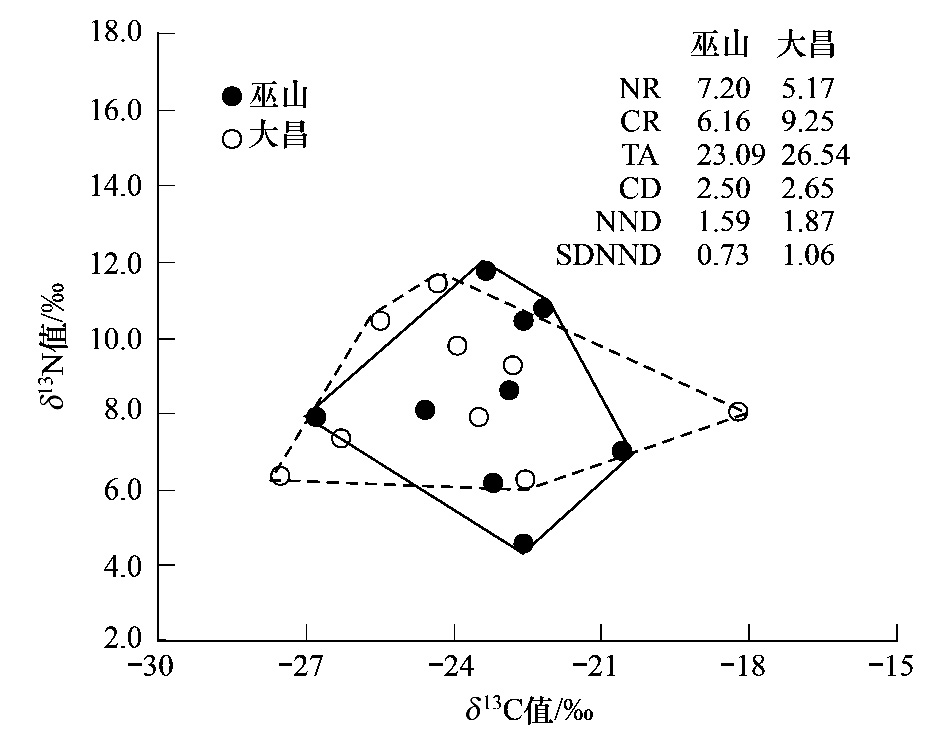
图 2所示,大昌鱼类群落的δ13C-δ15N总面积(TA值)较巫山大,表明在5月份,上游大昌TA值所代表鱼类群落的生态位总空间较巫山大。大昌鱼类群落的氮值范围(NR值)较小,碳值范围(CR值)较大,说明虽然大昌鱼类的营养长度(食物网垂直结构)较小,但其基础食物源多样性增加更为显著。大昌鱼类群落的平均离心距离(CD值)大于巫山,则表明大昌鱼类营养多样性的程度亦较巫山大。通过两个站点平均最邻近距离(NND)值的变化可见大昌食物网中各鱼类的营养位置差异较大,而巫山鱼类群落的最邻近距离标准差(SDNND)值较大,则说明巫山鱼类的营养生态位分布更加平均。
|
| 图 2 5月主要鱼类营养结构空间变化趋势 Fig.2 Spatial variations of trophic structure on the same selected species in May NR:氮值范围δ15N range;CR:碳值范围δ13C range;TA:总面积Total area;CD:平均离心距离 Mean distance to centroid;NND:平均最邻近距离Mean nearest neighbour distance;SDNND:最邻近距离标准差Standard deviation of mean nearest neighbour distance;实心点 Closed circles:5月巫山各种鱼类同位素值Isotope data of each species in May at Wushan sites;空心点Open circles:5月大昌各种鱼类同位素值Isotope data of each species in May at Dachang sites;实线和虚线多边形Solid and dashed outlines:鱼类群落在δ13C-δ15N双标图中总同位素生态位空间Total isotopic niche space of fish communities in δ13C-δ15N bi-plots |
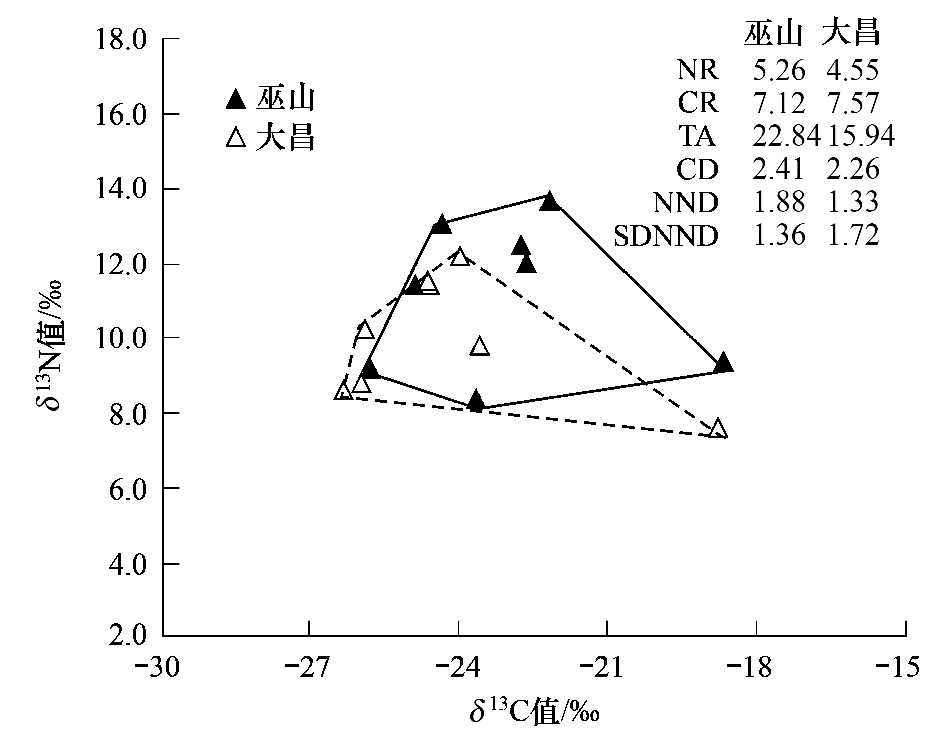
1 0月份,巫山与大昌的比较结果与5月有所不同(图 3)。大昌的生态位总空间明显小于巫山。大昌与巫山基础食物源多样性较为相似,但大昌鱼类的食物网垂直结构小于巫山,营养多样性程度亦较小。此时,大昌食物网中各鱼类的营养位置差异较小,但均匀程度不大。从图 3中也可以看出,此时巫山鱼类的营养位置高于大昌。
|
| 图 3 10月主要鱼类营养结构空间变化趋势 Fig.3 Spatial variations of trophic structure on the same selected species in October 实心三角Closed triangles:10月巫山各种鱼类同位素值Isotope data of each species in October at Wushan sites;空心三角Open triangles:10月大昌各种鱼类同位素值Isotope data of each species in October at Dachang sites |
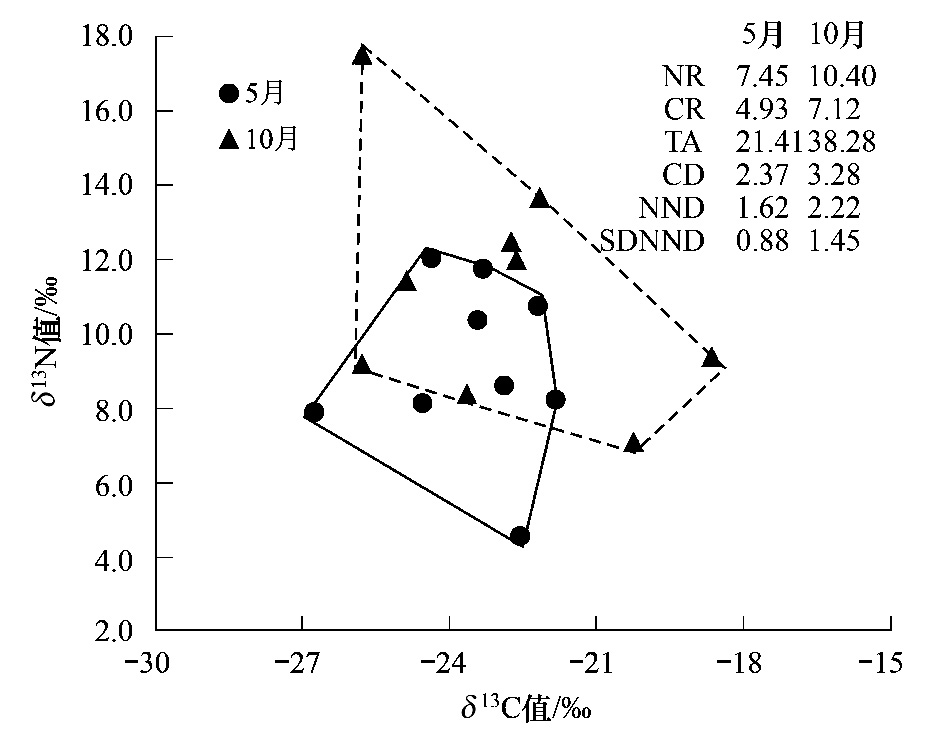
在巫山(图 4),高水位时期的生态位总空间明显大于低水位时期(10月TA值增加↑,下同),高水位时期鱼类基础食物源和营养长度均增加(CR↑、NR↑),鱼类营养多样性的程度亦增加明显(CD↑)。高水位时期,食物网中各鱼类间营养生态位的相似度较低,营养位置差异较大(NND↑),营养生态位分布程度不均匀(SDNND↑)。此时,高水位时期鱼类的营养位置高于低水位时期。
|
| 图 4 巫山主要鱼类营养结构时间变化趋势 Fig.4 Temporal variations of trophic structure on the same selected species in Wushan |
在大昌,各水位时期的变化趋势相反。由图 5所示,在高水位时期,生态位总空间、鱼类基础食物源和营养长度均下降(TA下降↓、CR↓、NR↓),鱼类营养多样性的程度变化不明显(CD值差异不大)。高水位时期鱼类的营养位置差异较小(NND↓),营养生态位分布程度更均匀(SDNND↓)。
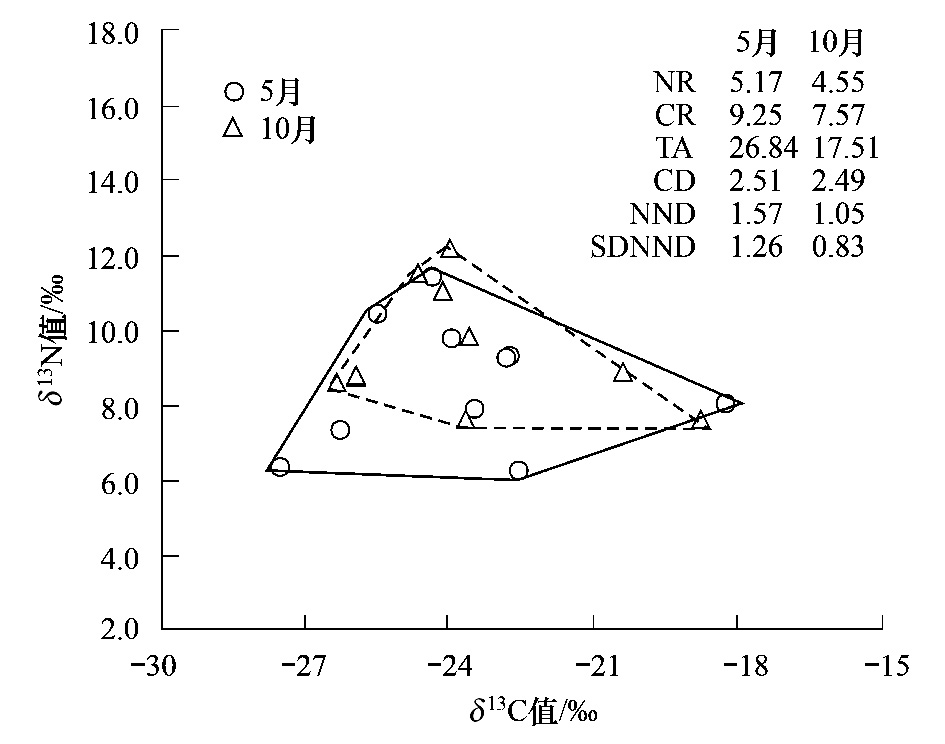
|
| 图 5 大昌主要鱼类营养结构时间变化趋势 Fig.5 Temporal variations of trophic structure on the same selected species in Dachang |
三峡库区蓄水后,大宁河在水口以下江段形成静水水域,河面增宽,深度增加,水体富营养化,曾多次爆发水华[21]。由于消落带多为峡谷岩石,河床平均水深达38.3 m[19],大宁河下游水草较少,浮游植物已成为水体的主要初级生产者[22],因此水体的浮游动植物及其他有机颗粒(POM)已成为主要的食物来源。虽然POM的δ13C值随着河口距离有极显著负相关性,但同种鱼类样品的δ13C值在不同采样点或不同水位时期并无明显差异,同时鱼类群落的CR值在不同月份和采样点均有很大差异,而CR值代表了食物网中基础食物碳源的多样性特征[6],表明大宁河下游鱼类仍具有多种食物来源,各种鱼类对基础食物源的选择有一定差异。目前大宁河食物碳来源及其时空变化尚不清楚,有待进一步研究。
鱼类样品的δ15N值随采样点的不同而出现一定程度的变化。在10月蓄水期,巫山样点的鱼类δ15N值明显大于大昌站,这可能与人为氮源输入的影响有关。由于人类活动氮的输入导致基准δ15N值升高[23],进而会影响食物网中生物δ15N值的升高[24]。巫山县城位于大宁河口,受工业废水、生活污水排放的影响,巫山POM的δ15N值为6.05‰,明显高于大昌的4.21%,因此巫山采样点中鱼类的δ15N值偏高。然而在5月巫山样点的鱼类δ15N值并非均高于大昌样点,可能与鱼类活动范围有关[25],鱼类在不同站点的来回运动会减少站点间的差异性[26]。在各采样点,5月鱼类δ15N值均显著小于10月,也可能不同水位时期的食物组成,以及水域环境和鱼类饵料生物的δ15N值季节变化有关[26]。由于尚未研究大宁河水域环境及饵料生物的δ15N值季节变化,因此出现这种结果的原因无法具体分析。另外,由于生物个体发育对其个体组织氮稳定性同位素值有一定影响[27, 28],虽然在采样过程中采集为大个体标本,减少了食性转变带来的误差,但研究样本体长还是存在一定的差异,已有研究表明,不同鱼类个体大小对δ15N值可能会存在一定影响[29]。
大宁河不同采样点的鱼类群落营养结构在不同水位时期的差异有所不同。在高水位时期,淹没的消落带会带入大量的潜在食物源,因此在巫山站,水位升高,使该水域食物源扩大,垂直营养长度增加,鱼类营养多样性以及营养位置差异程度明显增加(图 4)。但在大昌的鱼类群落营养结构中却出现相反的变化趋势。产生这种变化的原因可能是多方面的。Layman等研究表明,在资源未完全利用开发的生态系统中,引入冗余种不会引起群落营养多样性指标的改变,而营养多样性的程度和营养冗余指标反而会下降[6]。在加拿大的部分湖泊中,引入Micropterus dolomieu和Ambloplites rupestris两种鲈鱼后,导致湖鳟鱼的营养位置降低[30]。在亚北极区的湖泊中,引入Arctic charr鳟鱼后,群落营养结构的同位素量化指标均有不同幅度下降趋势[31]。大宁河下游形成静水后,水域空间增加,生态容量增加。虽然在蓄水期干流鱼类的大量进入支流[19],但相较于蓄水期增加的水域,现有的渔业资源量可能难以充分利用消落带及其他区域的食物源,没有食物竞争的压力使这些鱼类的食物选择不会发生改变[31]。因此可能存在的生态位空缺,以及单一饵料的丰富,都会使大昌的鱼类群落营养结构出现相反的变化趋势。
鱼类群落营养结构的时空变化并未显出处明显的规律性,也可能由以下几个方面的原因导致。首先,采样时间的选择。本次采样是在5月和10月,分别为水库水位下降期和蓄水期。水位的变动会造成生态系统的扰乱,环境扰乱可能会影响到河流中食物链的长度,并且与扰乱-资源联系程度和干扰的可预测性相关[32]。由于消落区环境不同,水位变动对巫山和大昌生态系统的影响是不同的,导致生态指标出现了不同变化趋势。其次,对比鱼类种类的选择。虽然在对比鱼种类的选择上考虑了各种食性的鱼类,但因同时能获取样品的种类较少,因此在鱼类群落营养结构的时空变化趋势上的分析,是不同的鱼类群落所组成,这也暗示了不同的鱼类群落结构在同一的生态系统中有不同变化动态。最后,样本量的大小[14]。不同鱼类的δ13C、δ15N值范围会影响群落各种生态指标值的计算[10]。各种鱼类是有一定的摄食宽度,因此获得一些鱼类同位素极端值能够更加准确的反映物种的生态宽度范围,最优的采样是能获得最大范围的值的样本[14]。例如本文中铜鱼的值显著较高,可能与铜鱼的分布范围有关。铜鱼仅能在巫山河口发现,其主要分布在长江干流水域,其摄食对象可能更加多样化,因此其摄食宽度增加也导致了群落生态宽度的增加。样本数量种类的限制,最终会影响鱼类群落营养变化趋势分析。
在本研究中,为了减少比较误差,鱼类样本的采集主要以体长相同的个体为主,以减少鱼类个体发育食性转变对同位素值的改变。因此文中生态指标中的计算值只能作为该水域特定鱼类群落结构不同水位时期、不同地点的比较分析。同时,文中生态指标值计算方法只能提供各估计点值,并没有取值范围,因此无法分析误差来源[14]。今后的研究中,需要增加研究水域各月份鱼类的种类和样本数量,并且采用合理的统计学方法,分析误差来源,才能更准确的阐述三峡水库水位变动对支流鱼类种群营养结构的影响,为支流乃至干流的水生生物保护与增殖提供理论依据。
致谢: 西南大学杨峰在样品采集过程中给予帮助;华中农业大学朱正伟在计算机软件应用方面给予帮助;中国林业科学院稳定同位素实验室柯渊老师对同位素测定提供帮助,特此致谢。
| [1] | Layman C A, Araujo M S, Boucek R, Hammerschlag-Peyer C M, Harrison E, Jud Z R, Matich P, Rosenblatt A E, Vaudo J J, Yeager L A, Post D M, Bearhop S. Applying stable isotopes to examine food-web structure: an overview of analytical tools. Biological Reviews, 2012, 87(3): 545-562. |
| [2] | Boecklen W J, Yarnes C T, Cook B A, James A C. On the use of stable isotopes in trophic ecology. Annual Review of Ecology Evolution and Systematics, 2011, 42(1): 411-440. |
| [3] | Post D M. Using stable isotopes to estimate trophic position: Models, methods, and assumptions. Ecology, 2002, 83(3):703-718. |
| [4] | West J B, Bowen G J, Cerling T E, Ehleringera J R. Stable isotopes as one of nature's ecological recorders. Trends in Ecology and Evolution, 2006, 21(7): 408-414. |
| [5] | Newsome S D, Martínez del Rio C, Bearhop S, Phillips D L. A niche for isotopic ecology. Frontiers in Ecology and the Environment, 2007, 5(8): 429-436. |
| [6] | Layman C A, Arrington D A, Montaña C G, Post D M. Can stable isotope ratios provide for community-wide measures of trophic structure? Ecology, 2007a, 88(1): 42-48. |
| [7] | Bearhop S, Adams C E, Waldron S, Fuller R A, Macleod H. Determining trophic niche width: a novel approach using stable isotope analysis. Journal of Animal Ecology, 2004, 73(5): 1007-1012. |
| [8] | Schmidt S N, Olden J D, Solomon C T, Vander Zanden M J. Quantitative approaches to the analysis of stable isotope food web data. Ecology, 2007, 88(11): 2793-2802. |
| [9] | Turner T F, Collyer M L, Krabbenhoft T J. A general hypothesis-testing framework for stable isotope ratios in ecological studies. Ecology, 2010, 91(8): 2227-2233. |
| [10] | Hoeinghaus D J, Zeug S C. Can stable isotope ratios provide for community-wide measures of trophic structure? Comment. Ecology, 2008, 89(8): 2353-2357. |
| [11] | Layman C A, Post D M. Can stable isotope ratios provide for community-wide measures of trophic structure? Reply. 2008, Ecology, 89(8): 2358-2359. |
| [12] | Layman C A, Quattrochi J P, Peyer C M, Allgeier J E. Niche width collapse in a resilient top predator following ecosystem fragmentation. Ecology Letters, 2007b, 10(10): 937-944. |
| [13] | Hammerschlag-Peyer C M, Yeager L A, Araújo M S, Layman C A. A hypothesis-testing framework for studies investigating ontogenetic niche shifts using stable isotope ratios. PloS One, 2011, 6 (11): e27104. |
| [14] | Jackson A L, Inger R, Parnell A C, Bearhop S. Comparing isotopic niche widths among and within communities: SIBER-stable isotope bayesian ellipses in R. Journal of Animal Ecology, 2011,80 (3): 595-602. |
| [15] | Quevedo M, Svanbäck R, Eklöv P. Intrapopulation niche partitioning in a generalist predator limits food web connectivity. Ecology, 2009, 90(8): 2263-2274. |
| [16] | Layman C A, Allgeier J E. Characterizing trophic ecology of generalist consumers: a case study of the invasive lionfish in The Bahamas. Marine Ecology Progress Series, 2012, 448:131-141. |
| [17] | Simonsen K A, Cowan J H. Effects of an inshore artificial reef on the trophic dynamics of three species of estuarine fish. Bulletin of Marine Science, 2013, 89(3): 657-676. |
| [18] | Wang Y M. Conservation Strategies of Fish Resources in Upper Reach of Yangtze River [D]. Wuhan, Institute of Hydrobiology, Chinese Academy of Sciences, 2004. |
| [19] | Wang K, Duan X B, Liu S P, Li Z H, Chen D Q. Survey on temporal and spatial distribution of fish in the Daning River. Acta Hydrobiologica Sinica, 2009, 33(3): 516-521. |
| [20] | Zeng Q F, Kong F X, Zhang E L, Qian S Q. Assessment of sample processing methods for stable isotope analysis of aquatic food webs. Journal of Lake Sciences, 2008, 20(1): 13-20. |
| [21] | Wang L P, Zheng B H, Zhang J L, Liu X A, Wu G Y. Effects on euthrophication and hydrodynamics of Daning River after impoundment of Three Gorges Reservoir. Journal of Lake Sciences, 2012, 24(2): 232-237. |
| [22] | Zhang J L, Zheng B H, Huang M S, Liu L S, Wang L P, Wu G Y. Seasonal variation of primary productivity in the Daning River backwater area. Journal of East China Normal University: Natural Science, 2011, 1(1): 1-11. |
| [23] | Cabana G, Rasmussen J B. Comparison of aquatic food chains using nitrogen isotopes. Proceedings of the National Academy of Sciences of the United States of America, 1996, 93(20): 10844-10847. |
| [24] | Bannon R O, Roman C T. Using stable isotopes to monitor anthropogenic nitrogen inputs to estuaries. Ecological Applications, 2008, 18(1): 22-30. |
| [25] | Li B, Wang Z J, Jin L, Jiang X, Xu D D, Liu X L, Chen D Q, Zhang Y G. Effects of anthropogenic nutrient input on organisms from different trophic levels in Hanfeng Lake: Evidence from stable carbon and nitrogen isotope analysis. Acta Ecologica Sinica, 2012, 32(5): 1519-1526. |
| [26] | Guzzo M M, Haffner G D, Legler N D, Rush S A, Fisk A T. Fifty years later: trophic ecology and niche overlap of a native and non-indigenous fish species in the western basin of Lake Erie. Biological Invasions, 2013, 15(8): 1695-1711. |
| [27] | Post D M. Individual variation in the timing of ontogenetic niche shifts in largemouth bass. Ecology, 2003, 84(5): 1298-1310. |
| [28] | Tibbets T M, Wheeless L A, Martínez del Rio C. Isotopic enrichment without change in diet: an ontogenetic shift in δ15N during insect metamorphosis. Functional Ecology, 2008, 22(1): 109-113. |
| [29] | Sweeting C J, Barry J, Barnes C, Polunin N V C, Jennings S. Effects of body size and environment on diet-tissue δ15N fractionation in fishes. Journal of Experimental Marine Biology and Ecology, 2007, 340(1): 1-10. |
| [30] | Vander Zanden M J, Casselman J M, Rasmussen J B. Stable isotope evidence for the food web consequences of species invasions in lakes. Nature, 1999, 401(6752): 464-467. |
| [31] | Murdoch A, Klein G, Doidge D W, Power M. Assessing the food web impacts of an anadromous Arctic charr introduction to a sub-Arctic watershed using stable isotopes. Fisheries Management and Ecology, 2013, 20(4): 302-314. |
| [32] | McHugh P A, McIntosh A R, Jellyman P G. Dual influences of ecosystem size and disturbance on food chain length in streams. Ecology Letters, 2010, 13(7): 881-890. |
| [18] | 王亚民. 长江上游鱼类资源保护对策[D]. 武汉: 中国科学院水生生物研究所, 2004. |
| [19] | 王珂, 段辛斌, 刘绍平, 李志华, 陈大庆. 三峡库区大宁河鱼类的时空分布特征. 水生生物学报, 2009, 33(3): 516-521. |
| [20] | 曾庆飞, 孔繁翔, 张恩楼, 钱善勤. 稳定同位素技术应用于水域食物网的方法学研究进展. 湖泊科学, 2008, 20(1): 13-20. |
| [21] | 王丽平, 郑丙辉, 张佳磊, 刘晓霭, 吴光应. 三峡水库蓄水后对支流大宁河富营养化特征及水动力的影响. 湖泊科学, 2012, 24(2): 232-237. |
| [22] | 张佳磊, 郑丙辉, 黄民生, 刘录三, 王丽平, 吴光应. 大宁河回水区初级生产力的季节变化. 华东师范大学学报: 自然科学版, 2011, 1(1): 1-11. |
| [25] | 李斌, 王志坚, 金丽, 江星, 徐丹丹, 刘晓蕾, 陈大庆, 张耀光. 人为营养物质输入对汉丰湖不同营养级生物的影响——稳定C、N同位素分析. 生态学报, 2012, 32(5): 1519-1526. |
 2014, Vol. 34
2014, Vol. 34




