文章信息
- 王娟, 朱道弘, 曾杨
- WANG Juan, ZHU Daohong, ZENG Yang
- 遗传和环境因素对曲脉姬蟋亚热带种群翅型分化的影响
- Effects of genetic and environmental factors on wing dimorphism in a subtropical population of Modicogryllus confirmatus Walker
- 生态学报, 2014, 34(22): 6606-6612
- Acta Ecologica Sinica, 2014, 34(22): 6606-6612
- http://dx.doi.org/10.5846/stxb201302070256
-
文章历史
- 收稿日期:2013-2-7
- 网络出版日期:2014-3-17
翅的出现使得昆虫获得了飞行能力,扩大了昆虫的分布范围和取食空间,同时有利于逃避天敌和寻求配偶等[1]。但研究发现在同一昆虫种群中同时存在具飞行能力的长翅型个体和不具备飞行能力的短翅型个体,即翅多型现象。这一现象存在于许多昆虫种类中,如小翅稻蝗Oxya yezoensis Shiraki[2],水稻褐飞虱Nilaparvata lugens Stl[3],沙蟋Gryllus firmus Scudder[4]等。
已有研究表明,昆虫翅多型现象受环境因子调控。这些环境因子主要包括光周期、温度、密度和营养条件。一般认为,翅型分化是昆虫对季节变化的一种适应[5],长光周期、夏季的高温条件诱使昆虫往长翅型方向分化,而短光周期和低温诱导短翅化。如东方长蝽Cavelirius saccharivorus Okajima[6]、褐飞虱 [1]、蟋蟀Pteronemobius nitidus Bolivar[7]等。蚜虫类由于早春寄主植物生长繁盛,因此经历冬季的低温条件会促使长翅型个体的产生[8]。栖息环境的恶化亦是导致昆虫产生迁飞、扩散的重要原因,因而食料条件恶化、若虫密度上升会诱导长翅个体大量出现。如褐飞虱、大豆蚜Aphis glycines Matsumura以及半翅目水黾科昆虫Microvelia horuvathi Lundlad和Microvelia douglasi Scott[7, 9, 10] 等。同时,昆虫的翅型分化亦受遗传控制,其遗传机制大体可分成两类。其一,受染色体上一对等位基因支配,符合孟德尔遗传规律。这种遗传机制在象甲[11]和拟步甲[12]等鞘翅目昆虫中较普遍,多数情况下短翅为显性。其二,翅多型现象受多个基因共同调控。大多数翅多型种类昆虫的翅型受多基因控制[13]。
一些昆虫的翅多型存在地理变异。如分布于日本冲绳的东方蝼蛄Gryllotalpa orientalis Burmeister种群无翅多型现象,而兵库种群存在翅多型现象,且受季节变化的影响[14]。Tanaka[15] 曾对曲脉姬蟋Modicogryllus confirmatus Walker的日本冲绳本岛(那霸)(26°14′N,127°41′E)、与那国岛(24°28′N,123°01′E)和石垣岛(24°20′N,124°10′E)种群的翅多型现象进行了研究,结果表明冲绳和那国岛种群翅型分化受光周期的影响,而石垣种群对光周期的变化不敏感。由于3种群所处纬度较为接近,气候条件相似,而推测石恒种群的这一特征可能来源于纬度更低地区的种群。因此,为进一步探讨曲脉姬蟋翅多型的地理变异是否具有纬度变化趋势,本文对分布于我国亚热带地区广西贺州(22.9°N,110.90 E)的曲脉姬蟋翅型分化与环境及遗传因子的相关性进行了研究。
1 材料与方法 1.1 供试虫源及饲养方法本研究的曲脉姬蟋若虫于2010年7月采自广西贺州的郊区林地(22.9°N,110.9°E)。将采集到的蟋蟀先置于25℃,LD12 ∶ 12h的人工气候室(宁波江南仪器厂,GX-HE302-300)饲养1代,实验室获得的第2代卵用于本研究。
饲养方法:若虫饲养于塑料容器中,容器顶部开口,并用纱网覆盖,有利于通风和透光,并可防止蟋蟀逃跑。在容器中放入几张折叠的滤纸,用以增加蟋蟀的活动空间。同时,在容器中放入装满水的塑料管(管口径4.3 cm,管长5.5cm),用脱脂棉塞紧,以此作为蟋蟀的水源,每3 d换1次水,保证清洁。每天给蟋蟀提供专门的昆虫饲料(Oriental Yeast Co.,Japan),保证饲料的新鲜。待成虫产卵时,塑料管中的脱脂棉可作为其产卵的基质,每4 d换1次脱脂棉收集卵,卵置于25℃下孵化。
1.2 恒定光周期对曲脉姬蟋翅型分化的影响将当日孵化的若虫置于25℃,密度为50只/容器(30 cm×17cm×19cm),设置光周期LD 8 ∶ 16 h、12 ∶ 12 h和16 ∶ 8 h 3个处理,每个处理饲养5个容器。直至羽化,分别统计不同光周期下成虫的长短翅型比。
1.3 变化光周期对曲脉姬蟋翅型分化的影响将当日孵化的若虫置于25℃,密度为50只/容器,光周期分别为LD 12 ∶ 12 h或LD 16 ∶ 8 h的条件下饲养。分别于孵化后第10、20、30、40和50d,将若虫由LD 12 ∶ 12 h转移至LD 16 ∶ 8 h,或由LD 16 ∶ 8 h转移至LD 12 ∶ 12 h。各处理转移2个容器。至成虫羽化时统计各处理成虫的长短翅型比。
1.4 温度对曲脉姬蟋翅型分化的影响将当日孵化的若虫置于LD 16 ∶ 8h,密度为50只/容器,设置温度25、30和35℃ 3个处理,每个处理饲养2个容器。直至羽化,分别统计不同温度条件下成虫的长短翅型比。
1.5 密度对曲脉姬蟋翅型分化的影响将当日孵化的若虫置于25℃,光周期为LD 16 ∶ 8 h,设置密度1、2、5、10和20只若虫/容器5个处理。单只饲养25个容器,2只/容器饲养20个容器,5、10和20只/容器各饲养15个容器。至成虫羽化时统计各密度下成虫的长短翅型比。
1.6 遗传对曲脉姬蟋翅型分化的影响刚孵化的若虫置于LD 16 ∶ 8 h,25℃,50只/容器条件下饲养。羽化当日,取长、短翅型成虫各15对分别饲养于2个不同容器中。收集不同翅型成虫所产卵粒,置于LD 16 ∶ 8 h,25℃条件下孵化。子代若虫饲养于LD 16 ∶ 8 h,25℃,50只/容器条件下,长、短翅型子代各饲养3个容器。至成虫羽化后,选长翅型子代若虫羽化的长翅型成虫和短翅型子代若虫羽化的短翅型成虫各15对分别饲养于2个不同容器中。如此对长、短翅型蟋蟀共筛选3代,分别统计每一代成虫的长短翅型比。取短翅型选拔系的F2代成虫,按长♀×长♂,长♀×短♂,短♀×长♂,短♀×短♂ 4种组合方式交配,各处理饲养15对。子代若虫置于LD 16 ∶ 8 h,25℃,50只/容器条件下饲养,分别饲养4个容器,至成虫羽化后统计不同处理下成虫的长短翅型比。
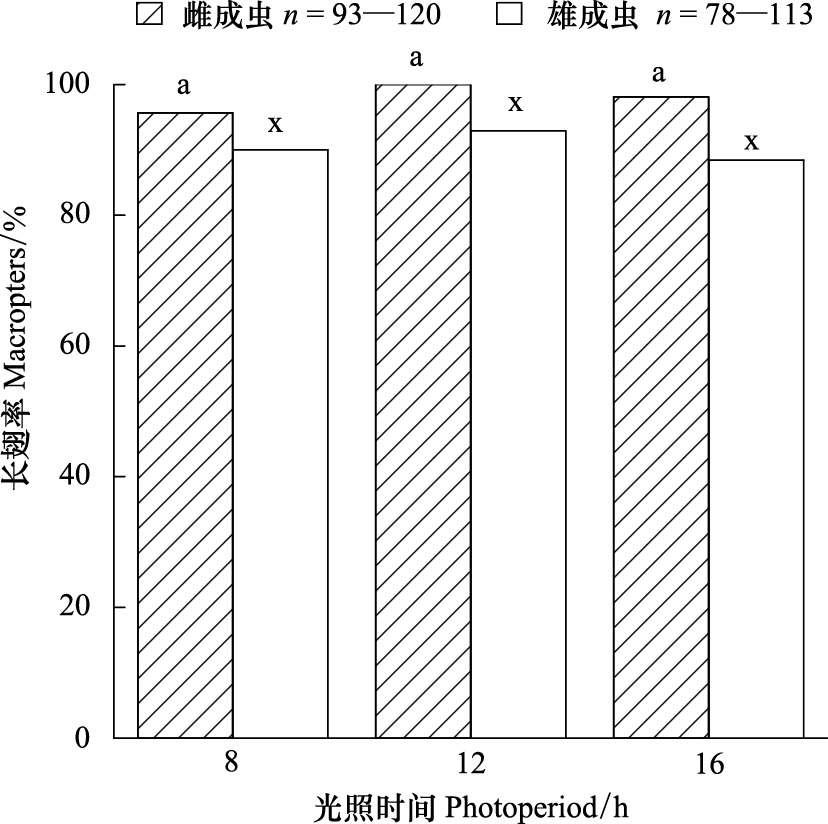
2 结果与分析不同光周期条件下,曲脉姬蟋的长翅率如图 1所示。雌成虫在光周期LD 8 ∶ 16 h、12 ∶ 12 h和16 ∶ 8h条件下的长翅率分别为95.7%、100%和98.1%,各处理间无显著性差异(χ2 = 5.85,df=2,P>0.05),可见恒定光周期对雌虫的翅型分化无影响。雄成虫在各光周期条件下的长翅率略低于雌成虫,分别为90%、92.92%和88.46%,彼此间亦无显著性差异(χ2= 1.2,df=2,P>0.05),表明恒定光周期对雄虫的翅型分化亦无影响。
|
| 图 1 恒定光周期对曲脉姬蟋翅型分化的影响 Fig. 1 Effect of constant photoperiod on wing differentiation of M. confirmatus Walker 相同字母表示相同性别的不同处理组间无显著性差异,χ2-test,P>0.05 |
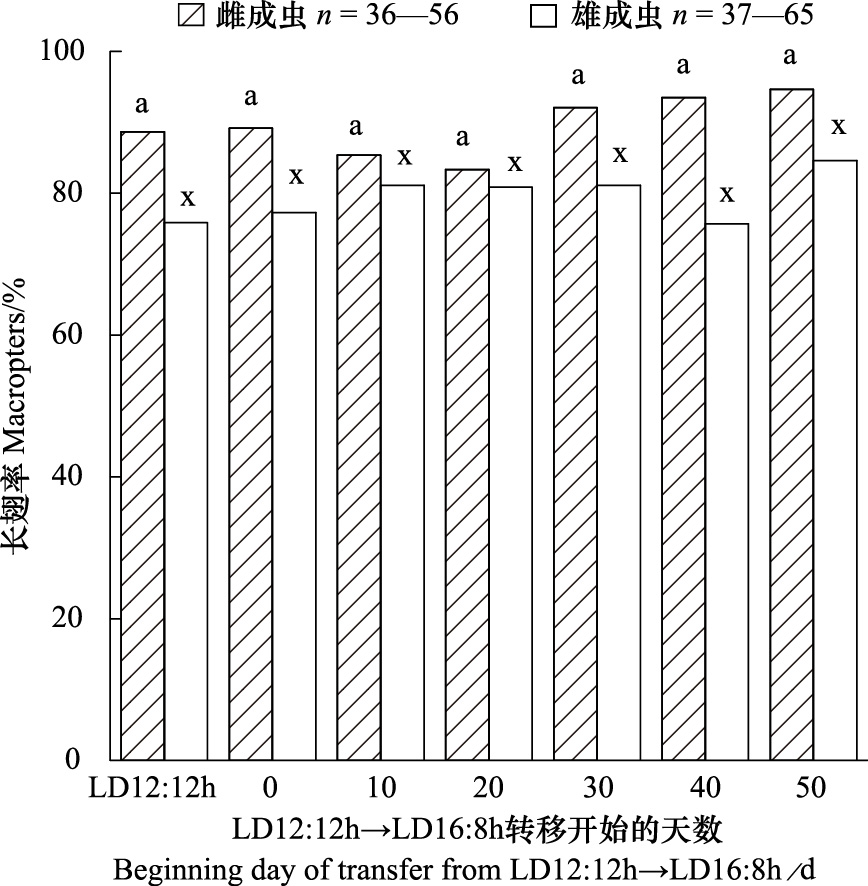
若虫于孵化后不同天数经历趋长和趋短光周期的变化,羽化成虫的长翅率如图 2、图 3所示。当若虫于孵化后第10、20、30、40、50天由光周期为LD 12 ∶ 12 h向LD 16 ∶ 8 h转移时,雌成虫的长翅率分别为89.19%、85.37%、83.33%、92.11%和93.48%,雄成虫的长翅率分别为77.27%、81.13%、80.85%、81.13%和75.68%(图 2),各处理下的雌、雄成虫的长翅率均无显著性差异(♀:χ2 = 3.39,df=4,P>0.05; ♂:χ2 = 0.86,df=4,P>0.05),表明趋长的光周期对曲脉姬蟋的翅型分化无影响。
|
| 图 2 趋长光周期对曲脉姬蟋翅型分化的影响 Fig. 2 Effect of increasing photoperiod on wing differentiation of M. confirmatus Walker 相同字母表示相同性别的不同处理组间无显著性差异,χ2-test,P>0.05 |
|
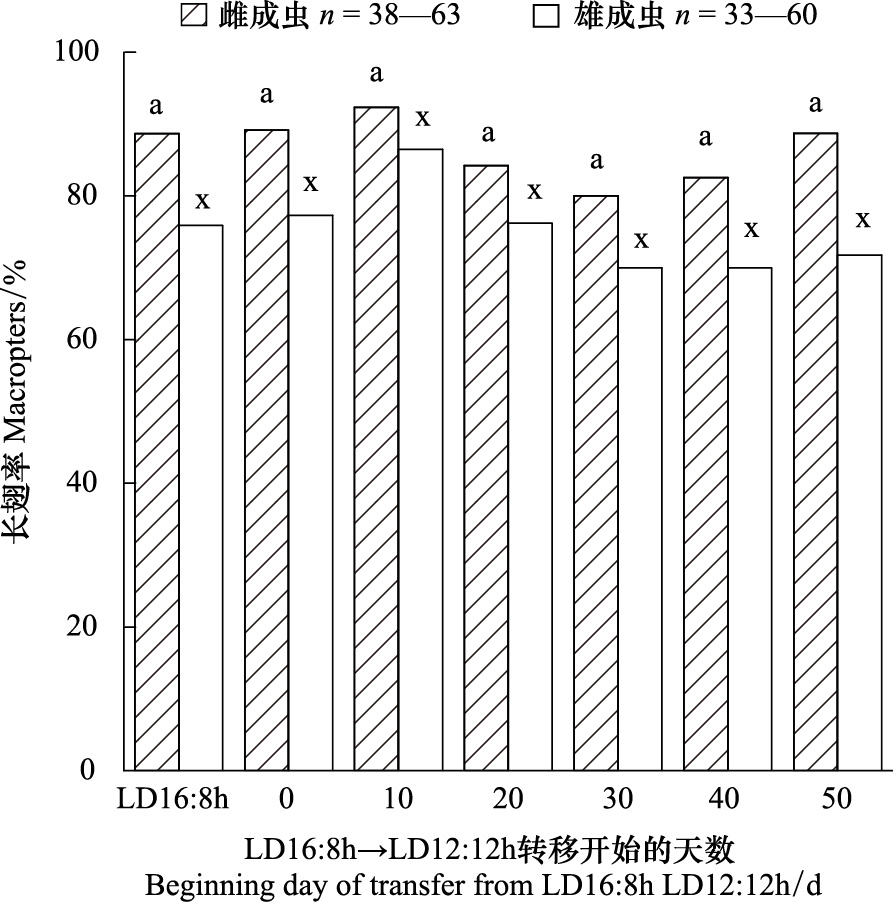
| 图 3 趋短光周期对曲脉姬蟋翅型分化的影响 Fig. 3 Effect of decreasing photoperiod on wing differentiation of M. confirmatus Walker 相同字母表示相同性别的不同处理组间无显著性差异,χ2-test,P>0.05 |
反向转移时,雌、雄成虫的长翅率亦较高,雌成虫的长翅率分别为89.19%、92.31%、84.21%、80%和82.54%,雄成虫的长翅率分别为77.27%、86.49%、76.19%、70%和70%(图 3),各处理下的雌、雄成虫的长翅率亦无显著性差异(♀:χ2 = 3.62,df=4,P>0.05; ♂:χ2 = 4.69,df=4,P>0.05),表明趋短的光周期对曲脉姬蟋的翅型分化亦无影响。
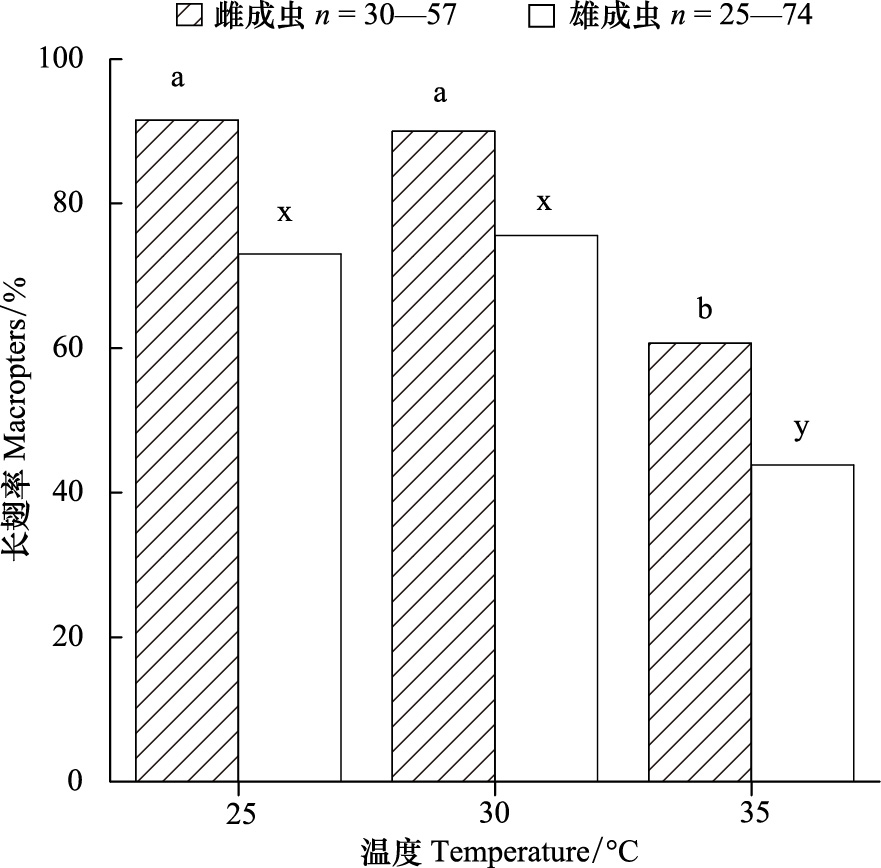
2.3 温度对曲脉姬蟋翅型分化的影响对若虫在温度分别为25、30、35℃条件下羽化成虫的长翅率调查结果如图 4所示。25℃和30℃条件下雌、雄成虫的长翅率均较高,雌成虫的长翅率分别为91.5%和90%,雄成虫的长翅率分别为73%和75.6%。二者均无显著性差异(♀:χ2 = 0.05,df=1,P>0.05; ♂:χ2 = 0.07,df=1,P>0.05)。当温度上升至35℃时,雌成虫的长翅率降低至60.65%,雄成虫的长翅率亦降低至43.8%,均显著低于其他两组温度下的长翅率(♀:χ2 =17.53,df=2,P<0.01; ♂:χ2 =14.75,df=2,P<0.01)。这说明正常范围内的温度变化对曲脉姬蟋翅型分化无影响,而极高温则促进其短翅化。
|
| 图 4 温度对曲脉姬蟋翅型分化的影响 Fig. 4 Effect of temperature on wing differentiation of M. confirmatus Walker 不同字母表示相同性别的不同处理组间存在显著性差异,χ2-test,P<0.05 |
对不同密度条件下羽化成虫的长翅率调查结果如图 5所示。当密度分别为1、2、5、10和20只/容器时,雌成虫的长翅率分别为100%、100%、96.97%、100%和100%,彼此间无显著性差异(χ2 = 3.87,df=4,P>0.05),说明密度对雌虫的翅型分化无影响。雄成虫的长翅率分别为100%、92.86%、96.97%、96.47%和98.31%,彼此间亦无显著性差异(χ2 = 1.47,df=4,P>0.05),可见密度对雄虫的翅型分化亦无影响。

|
| 图 5 密度对曲脉姬蟋翅型分化的影响 Fig. 5 Effect of density on wing differentiation of M. confirmatus Walker 相同字母表示相同性别的不同处理组间无显著性差异,χ2-test,P>0.05 |
为探究翅型分化是否受遗传影响,分别对长、短翅型蟋蟀进行了3代遗传选拔,结果如图 6所示。母代成虫的长翅率较高,雌、雄成虫分别为98.1%和88.5%。短翅型选拔系中,F1、F2和F3代雌成虫的长翅率分别为89.6%、64.6%、54.2%,雄成虫的长翅率分别为80.4%、47.1%、49.0%,F2和F3代雌、雄成虫的长翅率均显著低于母代(F2:♀:χ2 = 35.55,df=1,P<0.01; ♂:χ2 = 22.19,df=1,P<0.01; F3:♀:χ2 = 54.84,df=1,P<0.01; ♂:χ2 = 27.28,df=1,P<0.01)。长翅型选拔系中,F1、F2和 F3代雌、雄成虫的长翅率均极高,雌成虫的长翅率分别为97.9%、100%、98.7%,雄成虫的长翅率分别为90.1%、94.3%、92.3%,各代间雌、雄成虫的长翅率均无显著性差异(♀:χ2 = 1.79,df=3,P>0.05; ♂:χ2 = 1.65,df=3,P>0.05)。表明曲脉姬蟋的翅型分化受遗传调控。

|
| 图 6 遗传筛选对曲脉姬蟋子代长翅率的影响 Fig. 6 Effect of genetic selection on frequencies of macropters in progenies of M. confirmatus Walker *指长翅率显著高于未筛选的亲代长翅率,χ2-test,P<0.05 |
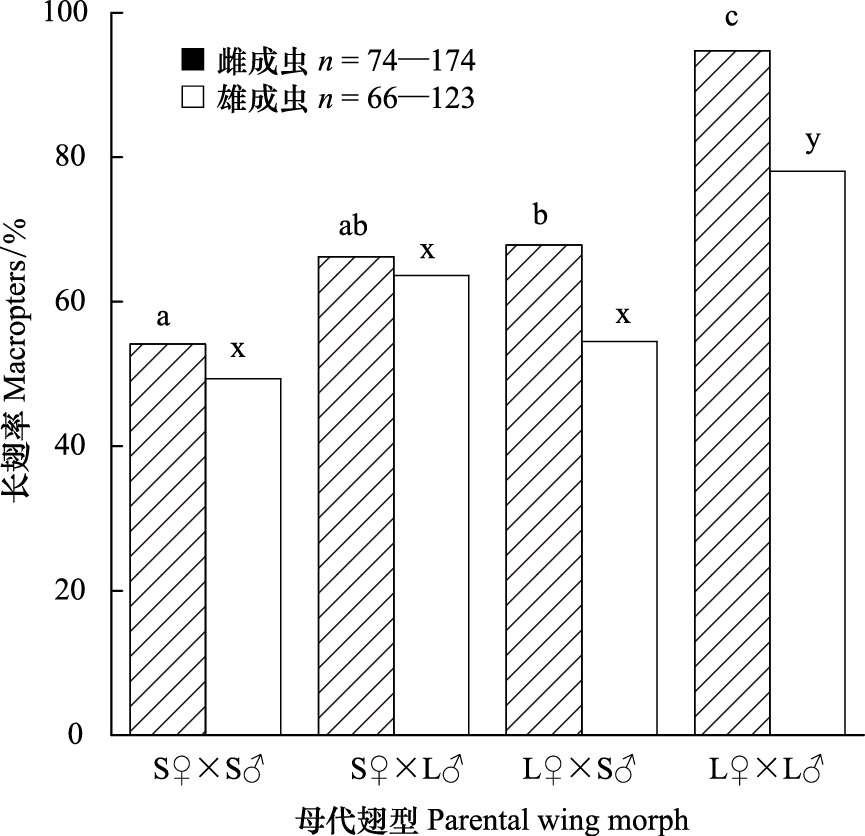
对短翅型选拔系的F2代成虫按不同翅型组合进行交配,调查了子代成虫的长翅率,结果如图 7所示。长翅型成虫交配(L♀×L♂)所产子代雌、雄成虫的长翅率分别为94.7%和78.1%,均显著高于短翅型成虫交配(S♀×S♂)子代雌、雄成虫的长翅率(♀:χ2 =34.70,df=1,P< 0.01; ♂:χ2 = 13.93,df=1,P< 0.01)。而长翅与短翅成虫交配(S♀×L♂或L♀×S♂)所产子代的长翅率则介于二者之间,S♀×L♂子代雌、雄成虫的长翅率分别为66.2%和63.6%;L♀×S♂子代雌、雄成虫的长翅率分别为67.8%和54.5%。不同翅型亲本所产子代的长翅率并不符合孟德尔遗传规律。表明曲脉姬蟋的翅型分化可能受多基因的共同调控。
|
| 图 7 不同翅型亲代交配的子代长翅率比较 Fig. 7 Comparison of macropterous rate in progenies of various crosses in M. confirmatus Walker 不同字母表示相同性别的不同处理组间存在显著性差异,χ2-test,P<0.05 |
一般认为,昆虫的翅型分化是对季节变化的一种适应机制,长光周期,高温的夏季条件促进其长翅化,短光周期,低温的秋季条件则诱导短翅化,如朱道弘对小翅稻蝗的研究结果表明,短光周期条件下,羽化成虫的短翅率为100%,而随着光周期的增加,短翅率逐渐降低[2]。然而,明显的季节变化主要存在于温带地区,对分布于季节变化不明显的亚热带地区翅二型昆虫而言,其翅型分化是否仍受光周期和温度的调控?Tanaka研究了日本亚热带地区曲脉姬蟋3种群翅型分化的光周期调控机制,结果表明冲绳本岛(26°14′N,127°41′E)和与那国岛(24°28′N,123°01′E)种群的翅型分化受光周期调控,而石垣岛(24°20′N,124°10′E)种群的翅型分化与光周期无关[15]。本项研究结果表明,我国亚热带广西种群的曲脉姬蟋翅型分化不受光周期调控,恒定或变化光周期条件下成虫的长翅率均较高。正常范围内的温度变化亦对其翅型分化无显著影响。因此,广西种群与纬度接近的日本石垣岛种群翅型分化的调控机制较为相似,说明了曲脉姬蟋翅型分化的调控机制具有明显的纬度变化趋势。另外,在35℃极高温的条件下,成虫的短翅率显著高于其他2个温度处理,这可能是高温的胁迫作用导致的短翅化。当环境条件超出正常范围,会对昆虫的生长发育产生胁迫作用,这种胁迫包括低温、高温、机械损伤等。有研究表明,环境胁迫可能会导致翅二型昆虫往短翅型分化,如一种蟋蟀Dianemobius fascipes Walker在人工摘除若虫附肢,低温和高温胁迫条件下,羽化成虫的短翅率显著升高[16]。
种群密度亦被认为是调节昆虫翅型分化的重要因子之一,密度的增加会导致长翅率上升,产生较多具有扩散能力的成虫,拓展到新的栖息地,从而调节种群的密度。这一现象存在于许多翅二型昆虫种类,如长颚斗蟋Velarifictorus asperses Walker[17]和一种螽斯Eobiana engelhardti subtropica Bey-Bienko [18] 等。然而,种群密度对昆虫翅型分化的调控机制并不一致,如一种蟋蟀Gryllus rubens Scudder在单独饲养时,羽化为长翅型成虫的比例较高,而群养条件下,羽化为短翅型成虫的比例较高[19]。Kisimoto[20]曾指出,热带型稻褐飞虱短翅率相当高,受密度影响不大,俞晓平[21]等亦发现热带国家如菲律宾的稻褐飞虱不同生物型在不同密度下均有很高的短翅率。本研究中,曲脉姬蟋广西种群的翅型分化对密度变化并不敏感,不同密度条件下,羽化成虫的长翅率无显著性差异,这与Kisimoto和俞晓平等的研究结果一致,然而不同的是,各密度条件下曲脉姬蟋的长翅率均高达90%以上。可知种群密度对昆虫翅型分化的影响机制较为复杂,不同昆虫种类间差异较大,导致这一现象的原因仍需进一步研究。
有研究表明,昆虫的翅型分化受环境因子和遗传的共同调控。Roff曾对沙蟋G. firmus Zera和Denno翅型分化的遗传率进行了研究,结果表明其遗传率为0.7[22],说明了遗传对昆虫的翅型分化具有显著的调控作用。王群等[23]对不同翅型褐飞虱成虫进行了杂交实验,结果表明不同亲本组合的子代长翅率具有显著差异,亦说明了昆虫的翅型分化受遗传的调控。然而,Iwanaga等和俞晓平等经遗传杂交试验,均发现稻褐飞虱短翅型雌成虫是由1对显性基因控制,雄虫翅型分化不遵循遗传分离规律[21, 24]。Tojo[25]用遗传纯系杂交试验发现,稻褐飞虱成虫翅型是由多基因控制的,其中的2个基因位于常染色体的同1个位点上。而诸冈直[26]却认为稻褐飞虱的翅型分化取决于2对基因。可见,昆虫翅型分化的遗传调控机制较为复杂,需要进一步的研究论证。本研究对分布于我国广西境内的曲脉姬蟋种群进行了长、短翅型的3代选拔,结果表明往短翅型选拔时,F2和F3代雌、雄成虫的短翅率均显著高于母代。而不同翅型成虫交配所产子代的长翅率并不符合孟德尔遗传规律,说明曲脉姬蟋的翅型分化可能受多基因的共同调控。这一结果与Tanaka[15]对与那国岛的曲脉姬蟋种群的研究结果一致,进一步验证了曲脉姬蟋翅型分化受多基因共同调控的推测。
| [1] | Zhu D H. Regulatory mechanism and evolution of insect wing polymorphism. Chinese Bulletin of Entomology, 2009, 46(1):11-16. |
| [2] | Zhu D H. The wing polymorphism in rice grasshopper, Oxya yezoensi Shiraki (Orthopera:Catantopidae). Acta Ecologica Sinica, 2001, 21(4):624-628. |
| [3] | Kiyoko M, Nakasuji F. Effects of day length and density on development and wing form of the small brown planthopper Laodelphax striatellus (Hemiptera:Delphacidae). Applied Entomology and Zoology, 1991, 26(4):557-561. |
| [4] | Zhang B C, Zhao Z W. The regulatory mechanisms of the wing-polymorphism in Gryllus firmus. Chinese Bulletin of Entomology, 2009, 46(1):5-11. |
| [5] | Briceño R D, Eberhard W G. Genetic and environmental effects on wing polymorphisms in two tropical earwigs (Dermaptera:Labiidae). Ecologia, 1987, 74(2):253-255. |
| [6] | Fujisaki K. Wing form determination and sensitivity of stages to environmental factors in the oriental chinch bug, Cavelerius saccharivorus. Applied Entomology and Zoology, 1989, 24(3):287-294. |
| [7] | Lu L H, Chen R L. Study on the production of alatae in soybean aphid, Aphis glycines. Acta Entomologica Sinica, 1993, 36(2):143-149. |
| [8] | Roff D A. The evolution of wing dimorphism in insects. Evolution, 1986, 40(5):1009-1020. |
| [9] | Muraji M, Nakasuji F. Comparative studies on life history traits of three wing dimorphic water bugs Microvelia spp. Westwood (Heteroptera:Valiidae). Researches on Population Ecology, 1988, 30(2):315-327. |
| [10] | Dai H G, Wu X Y, Yang Y H. Regulative mechanism of wing-polymorphism of insects. Entomological Journal of East China, 1997, 6(1):99-103. |
| [11] | Jackson D L. The inheritance of long and short wings in the weevil Sitona hispidula with a discussion of wing reduction among beetles. Transactions of the Royal Society of Edinburgh, 1928, 55(3):665-735. |
| [12] | Aukema B. Wing-length determination in two Wing-dimorphic Calathusspecies (Coleoptera:Carabidae). Hereditas, 1990, 113(3):189-202. |
| [13] | Zera A J, Tiebel K C. Differences in juvenile hormone esterase activity between presumptive macropterous and brachypterous Gryllus rubens, Implications to the hormonal control of wing polymorphism. Journal of Insect Physiology, 1989, 35(1):7-18. |
| [14] | Endo C, Ikeda Y, Saton A. Variation in wing dimorphism of oriental mole cricket Gryllotalpa orientalis:comparative study in Okinawa and Hyogo populations. Entomological Science, 2011, 14(1):103-105. |
| [15] | Suzuki Y, Tanaka S. Environmental and genetic control of wing morph determination in three subtropical populations of a cricket, Modicogrgllus confirmatus (Orthoptera; Gryllidae). Japanese Journal of Entomology, 1996, 64(4):896-909. |
| [16] | Shimizu T, Masaki S. Injury causes microptery in the ground cricket, Dianemobius fascipes. Journal of Insect Physiology, 1993, 39(12):1021-1027. |
| [17] | Zeng Y, Zhu D H, Zhao L Q. Effects of environmental factors on wing differentiation in Velarifictorus asperses Walker. Acta Ecologica Sinica, 2010, 30(21):6001-6008. |
| [18] | Higaki M, Ando Y. Effect of crowding and photoperiod on wing morph and egg production in Eobiana engelhardti subtropica. Applied Entomology and Zoology, 2003, 38(3):321-325. |
| [19] | Zera A J, Tiebel K C. Brachypterizing effect of group rearing, juvenile hormone Ⅲ and methoprene in the wing dimorphic cricket, Gryllus rubens. Journal of Insect Physiology, 1988, 34(6):489-498. |
| [20] | Kismoto R. Studies on the polymorphism and its role playing in the population growth of planthopper, Nilaparvata lugens (stål). Bulletin of the Shikoku National Agricultural Experiment Station, 1965, 13:1-106. |
| [21] | Yu X P, Lu Z X, Wu G R, Tao L Y, Zhang Z T. Studies on the immigration and the wing-form development of brown planthopper, Nilaparvata lugens (Stål). Acta Ecologica Sinica, 1997, 40(S1):128-134. |
| [22] | Roff D A, Simons A M. The quantitative genetics of wing dimorphism under laboratory and 'field'conditions in the cricket Gryllus pennsylvonicus. Heredity, 1997, 78(3):235-240. |
| [23] | Wang Q, Du J G, Cheng X N. genetic studies on wing dimorphism of brown planthopper, Nilaparvata lugens (Homoptera:Delphacidae). Acta Ecologica Sinica, 1997, 40(4):343-348. |
| [24] | Iwanaga K, Tojo S, Nagata T. Immigration of the brown planthopper, Nilaparvata lugens, exhibiting various responses to density in relation to wing morphism. Entomologia Experimentalis et Applicata, 1985, 38(2):101-108. |
| [25] | Tojo S. Genetic background of insect migration//Proceedings of the International Seminar on Migration and Dispersal of Agricultural Insects. Tsukuba:National Institute of Agro-Environmental Science, 1991:9-21. |
| [1] | 朱道弘. 昆虫翅型分化的调控及翅多型性的进化. 昆虫知识, 2009, 46(1):11-16. |
| [2] | 朱道弘. 小翅稻蝗(Oxya yezoensis Shiraki)翅多型现象浅释. 生态学报, 2001, 21(4):624-628. |
| [4] | 张保常, 赵章武. 沙蟋翅多型性的调控机理. 昆虫知识, 2009, 46(1):5-11. |
| [7] | 吕利华, 陈瑞鹿. 大豆蚜有翅蚜产生的原因. 昆虫学报, 1993, 36(2):143-149. |
| [10] | 戴华国, 吴小毅, 杨亦桦. 昆虫翅多型现象的控制机理. 华东昆虫学报, 1997, 6(1):99-103. |
| [17] | 曾杨, 朱道弘, 赵吕权. 环境因素对长颚斗蟋翅型分化的影响. 生态学报, 2010, 30(21):6001-6008. |
| [21] | 俞晓平, 吕仲贤, 巫国瑞, 陶林勇, 张志涛. 褐飞虱的迁入和翅型分化规律研究. 昆虫学报, 1997, 40(增):128-134. |
| [23] | 王群, 杜建光, 程遐年. 褐飞虱翅型分化遗传规律的研究. 昆虫学报, 1997, 40(4):343-348. |
| [26] | 诸冈直. トビイロウンカにおける翅长变异の遗传の制御. 个体群生态学会会报(日文), 1992, 49:12-14. |
 2014, Vol. 34
2014, Vol. 34




