文章信息
- 邢星, 陈辉, 朱建佳, 陈同同
- XING Xing, CHEN Hui, ZHU Jianjia, CHEN Tongtong
- 柴达木盆地诺木洪地区5种优势荒漠植物水分来源
- Water sources of five dominant desert plant species in Nuomuhong area of Qaidam Basin
- 生态学报, 2014, 34(21): 6277-6286
- Acta Ecologica Sinica, 2014, 34(21): 6277-6286
- http://dx.doi.org/10.5846/stxb201310092427
-
文章历史
- 收稿日期:2013-10-9
- 修订日期:2014-5-29
2. 中国科学院地理科学与资源研究所, 北京 100101
2. Institute of Geographic Sciences and Natural Resources Research, Chinese Academy of Sciences, Beijing 100101, China
水分是维持植物生命系统的重要物质,水分来源的选择便成为植物生命周期中的重要选择过程。植物水分来源包括地下水、地表水、土壤水等等,但是大气降水却是这些水分的最终来源[1]。虽然植物所吸收利用的水分均来自于降水,但是由于蒸发因素、海拔高度差异、蓄水层地质特征、土壤对水分吸收溶解浓度的差异等因素,都会造成水中δ18O、δD的不同[2, 3]。
有研究认为,水分在从根系到叶片的蒸腾作用下会在叶片中产生同位素的富集[4],少部分排盐的盐生植物根系会在从土壤吸收水分的过程中发生同位素的分馏[5],但大多数植物在这一过程中水分的氢氧同位素不会发生分馏[6, 7, 8]。而且,水分在植物茎中向上传递的过程中,利用木质部的运输,不存在稳定同位素分馏的现象[9]。因此,通过对比植物茎木质部与各个来源水分的δ18O、δD值,便可以找出该种植物是运用何种来源的水分进行生长[10],为利用稳定性同位素来分析植物水分来源提供了理论基础。
稳定同位素技术到20世纪70年代才应用到生态学领域,该项技术在确定植物群落水分来源方面得到了广泛的应用,近年来许多学者致力于对干旱区植物水分来源研究。新的研究发现:干旱区不同海拔梯度条件下乔木、灌木都有不同程度的利用夏季降水的状况[11]。研究发现:灌溉前后幼龄柽柳表现出对水源利用的转换,而成年柽柳则对灌溉反映不敏感[12]。降水较多的样地,植物更倾向于利用浅层土壤水[13];气候越干旱,植物越倾向于利用深层土壤水以及地下水[14]。也有研究认为,不同季节植物对水源的利用比例也存在转换[15, 16]。但是地处青藏高原的柴达木盆地,荒漠生态系统对全球变化具有敏感响应和强烈影响[17],至今也未见对柴达木盆地植物水分来源报道,并且在以往的研究中,并没有注意到河水、降水对植物水分来源的影响。柴达木盆地优势植物在整个生长季对不同水源的利用比例如何,生长季初期和末期水分利用比例是否一致以及优势种之间是否存在水源竞争等问题也并未知晓。
本文对柴达木盆地东部诺木洪地区5种荒漠植物水分来源进行定量分析,通过荒漠植物水分利用的总体特征、季节规律和物种间的差别,研究柴达木盆地植物水分利用机理,探讨干旱地区植物适应环境策略,为我国干旱半干旱地区荒漠生态系统的维护和稳定提供基础理论依据。
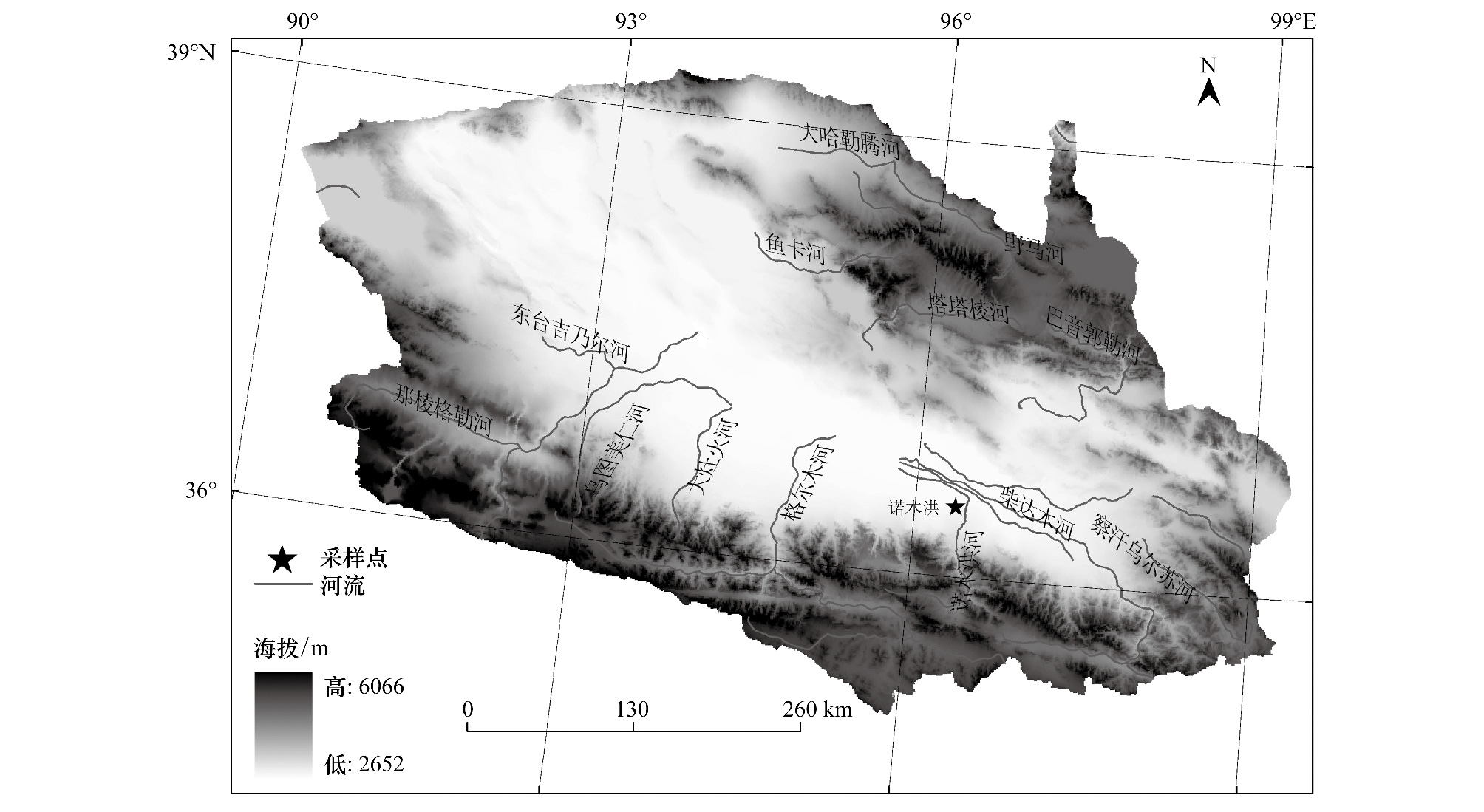
1 材料和方法 1.1 研究区概况研究区位于我国青藏高原东北部,青海省海西蒙古族藏族自治州都兰县境内(图 1)。属于高原大陆性气候,平均海拔较高,气候干旱,生长季较短,集中在每年的6—9月。根据全国气象站点的逐日数据计算得出研究区56年(1957—2012)平均气温4.9 ℃,多年平均降水量43.5 mm。2010年均温6.2 ℃,植物生长季6—9月降水量分别为81、17.2、19、14.8 mm,生长季降水总量为132.0 mm,占年降水量(149.0 mm)的88.6%,蒸发量2800 mm远大于降水量。土壤多以荒漠土壤为主,植被则以抗旱能力好的荒漠灌丛为主。诺木洪样地采样点位于: 36°22′49.26″ N,96°24′36.06″ E,海拔2858 m。
|
| 图 1 研究区及采样点位置图 Fig. 1 Location of the study area and the sampling site |
植物样品包括当地所有优势种:驼绒藜(Ceratoides latens)、白刺(Nitraria tangutorum)、麻黄(Ephedra sinica)、柽柳(Tamarix ramosissima)、沙拐枣(Calligonum mongolicum)。
2010年6—9月每15d采集1次样品,采样开始时间为6月15日,结束时间为9月30日。为了尽量减少光照强度等外界条件对同位素分析结果的影响,采样过程保证在9:00到11:00间完成。在样地选择生长状况较良好、高度较为一致的植株作为植物茎样品的采集对象。选取5棵有代表性的驼绒藜、白刺、麻黄、柽柳、沙拐枣,在朝向一致的大枝条上选取一根小的树枝,截取直径0.2 cm左右的栓质化小茎,快速装入已经准备好的4 mL螺纹玻璃样品瓶中,拧紧瓶盖。在上述植物分布的样点附近选择地势相对均一的地方挖3个1 m深的土壤剖面,分别采集0—10 cm、10—30 cm、30—50 cm、50—70 cm、70—90 cm土层的土壤,装入4 mL螺纹样品瓶中,拧紧瓶盖。植物取样同时收集距离取样点最近的24 m深井井水代表样点的地下水。该井位于36°25′48″ N,96°24′36″ E,距离采样点大约5.6 km。采集样地附近河水,搅动表层水以保证样品的均质性。收集取样前最近一次降水,装入取样瓶中。所有样品均取3个重复,用封口膜密封冷藏保存,共采集样品306个。
1.2.2 样品分析先使用低温真空抽提法抽提植物茎和土壤样品中的水分,过0.22 μm滤纸后放入2 mL样品瓶。水样直接过0.22 μm滤纸放入2 mL样品瓶待测。本次实验中全部水样使用Picarro L2130-i 超高精度液态水和水汽同位素分析仪进行同位素的测定。液态水测量的典型精度δ18O为 0.011‰;δD为0.038‰。该仪器自带ChemCorrect有机污染物校验软件可以通过光谱分析对不同污染物进行标记,从而得出该结果是否可靠。存在有机污染的全部植物茎样品以及部分土壤样品在中国科学院地理科学与资源研究所同位素质谱仪Finnegan MAT-253分析。分析得出的δD、δ18O是同标准平均海洋水SMOW的千分差。
δX=[R样品/R标准-1] ×1000
式中,R样品为待测样品的氢或氧同位素自然丰度比,R标准为标准海洋水SMOW的氢或氧同位素自然丰度比。随机抽取诺木洪地区无有机污染的样品17个同时用Picarro和质谱仪测定,测定结果采用Anova单因素方差分析显示:δ18O和δD均值分别为-6.577‰、-6.173‰和-58.118‰、-53.253‰,两种测定方法结果无显著性差异(P>0.05)。土壤含水量使用Decagon公司Em50\\Em50R仪器进行测定。
1.2.3 数据分析不同土壤层含水量以及土壤水δ18O的差异用SPSS 17.0统计软件进行分析。不同水源对植物的贡献率用多源线性混合模型(IsoSource)分析,计算时增幅为1%,不确定水平为0.1%。
2 结果与讨论 2.1 诺木洪降水同位素特征Craig[18]根据全球降水中氢氧同位素存在的线性关系,通过计算得出全球尺度下二者之间的关系,将其定义为大气水线(Meteoric Water Line,即MWL):δD=8δ18O+10。Dansgaard提出过量氘(deuterium excess)的概念:d=δD-8δ18O。d值在全球尺度下为10,即全球尺度下大气水线的截距。过量氘反映了降水形成时局部地理要素,以及海水蒸发时的条件,因此比较普遍地运用到降雨水汽来源的研究中。
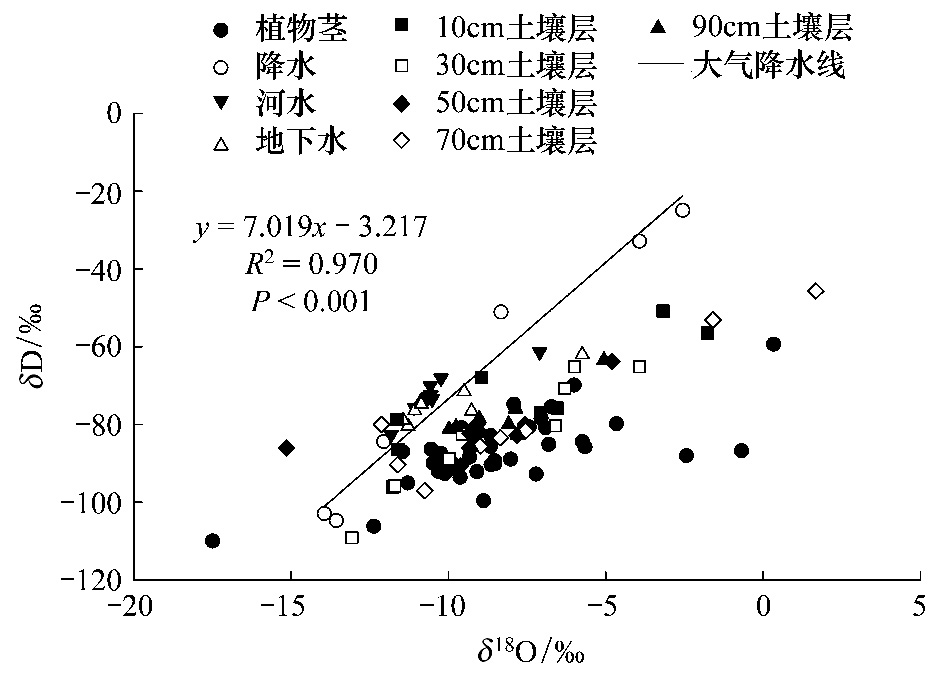
根据测得的诺木洪降水样品中稳定性氢氧同位素的值,得出该地大气水线y=7.019x-3.217(R2=0.970,P<0.001) (图 2),斜率为7.019,截距为-3.217,斜率小于全球平均值说明该地区气候干燥,截距呈现负值说明该地区气温高、湿度低。对诺木洪地区进行过量氘计算,均值为(5.674±3.18)‰,低于大部分地区雨水d值(10‰左右)说明本地夏季水汽辐合较强,在干燥气候条件下形成降雨,水滴降落过程蒸发强烈。通过对诺木洪地区植物茎、河水、分层土壤水中δD—δ18O分布点与该样地大气降水线进行比较,分析结果表明:由于地下水位较浅,河水入渗量较大,地下水、河水δ18O值偏小,均位于大气降水线的上方[19]。土壤水、植物水的δ18O、δD值多位于该地大气降水线右下方,说明该地区存在强烈的蒸发作用,和降水相比重同位素富集明显。图中土壤水、地下水、河水除少量点距离大气降水线较远外,其余都分布于大气降水线附近,说明诺木洪地区降水对土壤水、地下水、河水等都有补给作用[20]。
|
| 图 2 诺木洪植物茎水以及各种水分来源δD—δ18O与当地大气降水线关系比较 Fig. 2 Relations between δD and δ18O values of plant stem water,precipitation,soil water,river water,groundwater,and local meteoric water line |
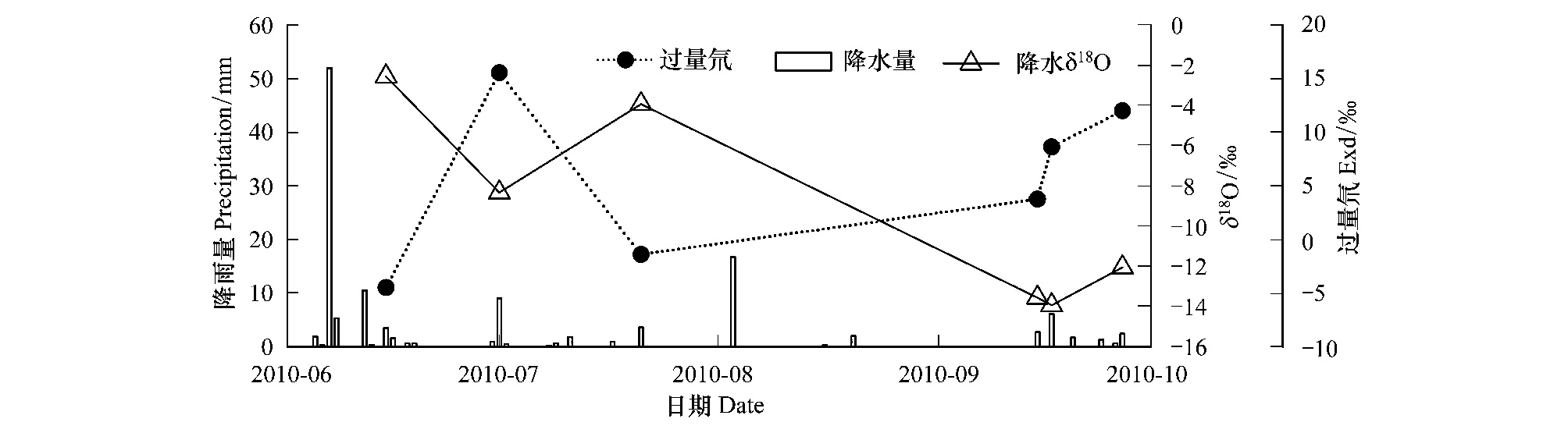
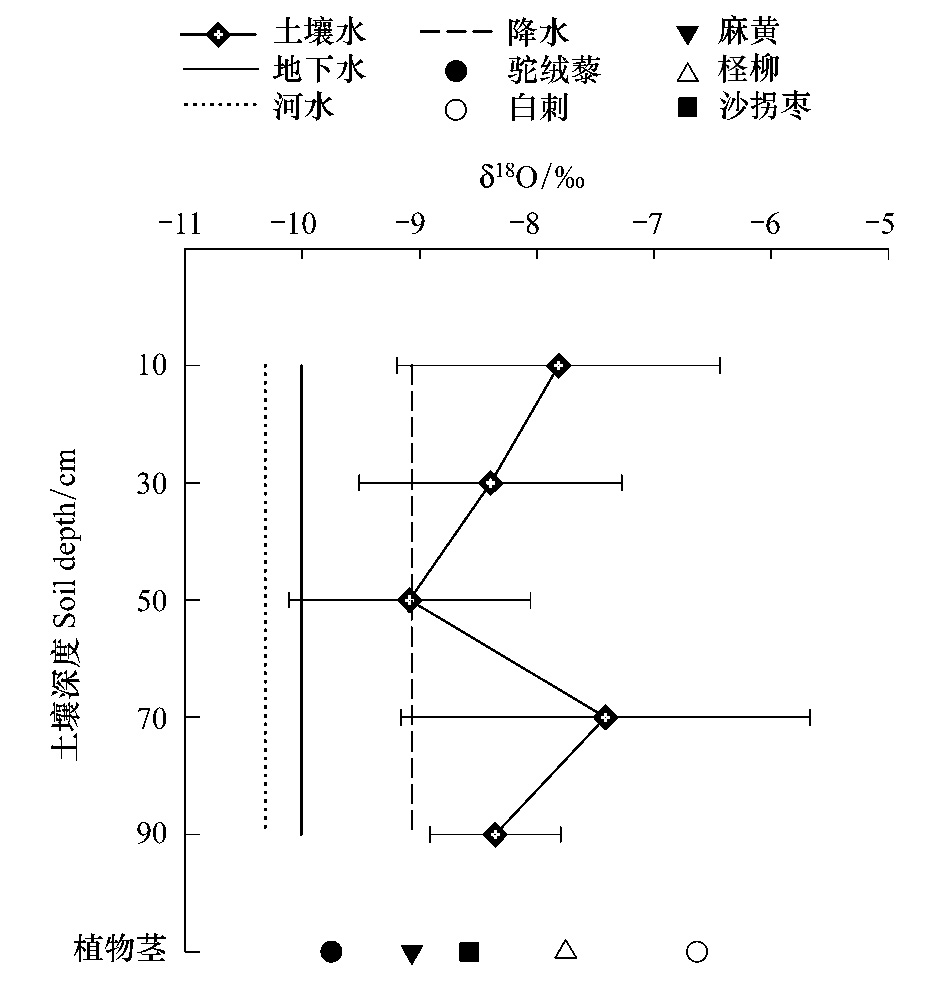
由图 3可知诺木洪在2010年生长季降雨事件较多,但是大于15 mm的降水只有两次:6月7日和8月3日,降水量分别为52 mm和16.7 mm。由于夏季水汽辐合能力较强,雨滴在降落过程中蒸发强烈,使得δ18O较高的局地水汽进入降水云团,致使降水中过量氘较低,而δ18O较高。降水量的变化对土壤、植被、水文等方面都会产生影响。降水可以直接补充土壤中的水分,降水量的大小对水分的补充有效程度却不同,有研究认为小于5 mm的降水不能对土壤水分起到有效的补充,而只能降温和缓解旱情[21]。杜建会[22]等人的研究认为甘肃民勤地区发生47.6 mm的强降雨事件后,发育中和活化阶段的沙堆补给深度可达50 cm,稳定阶段的白刺沙堆也可以达到30 cm。2010年诺木洪地区生长季的降雨总量达到132.0 mm,尤其是6月7日的降水,超过有历史记录以来的日降水极值,达到暴雨级别,对土壤水分进行了很好的补给。对比诺木洪地区土壤剖面δ18O与降水δ18O值(图 5),降水δ18O与50 cm土壤水δ18O值最接近,因此笔者认为诺木洪降水补给深度可以达到50 cm。
|
| 图 3 诺木洪2010年6—9月降水量、降水δ18O及过量氘 Fig. 3 Precipitation,δ18O values and deuterium excess from June to September,2010 in Nuomuhong area |
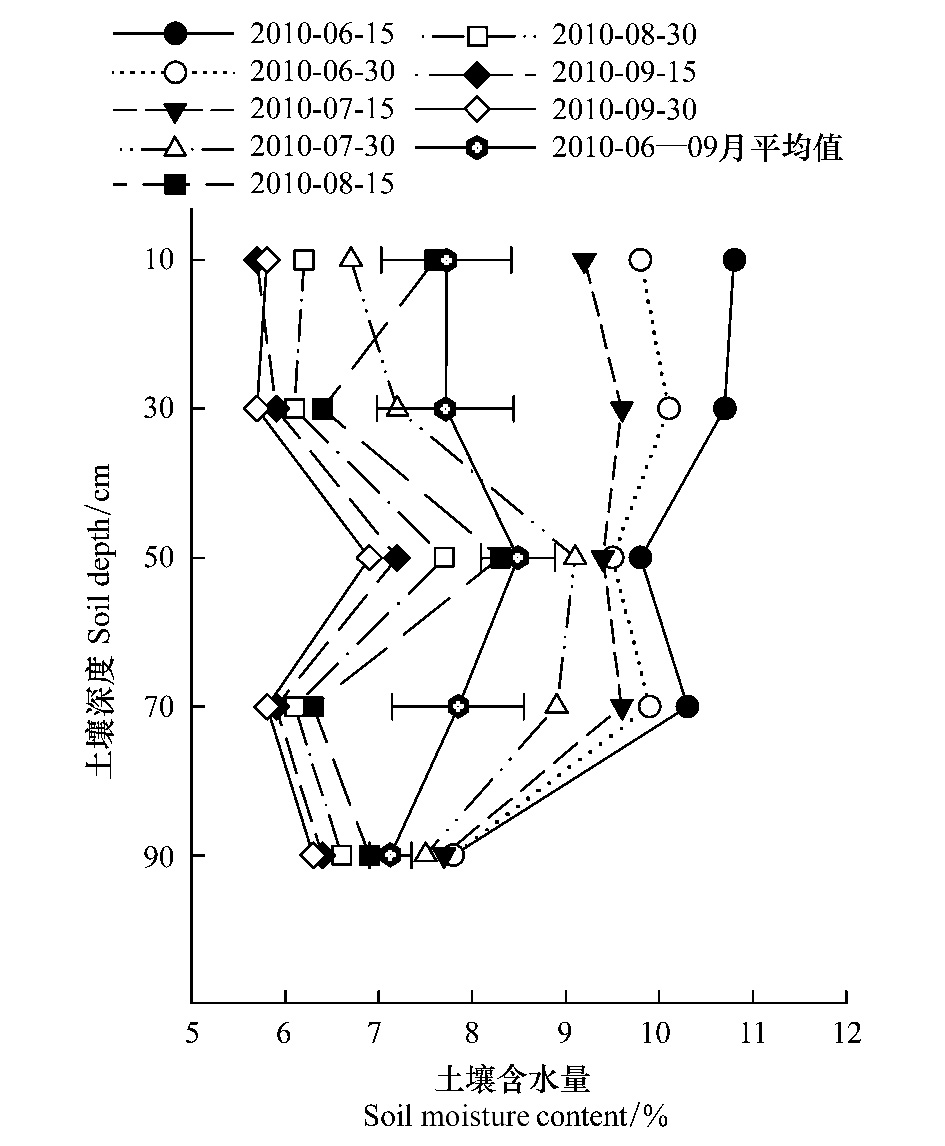
对比不同土层土壤含水量(图 4),50 cm土壤层含水量较高(8.5%),10 cm、30 cm以及70 cm层土壤含水量较为接近,90 cm含水量最少(7.1%)。诺木洪地区河水中δ18O的变化范围是:-11.823‰—-7.101‰,平均值为(-10.316±0.491)‰(Mean± SE);地下水样品中δ18O的变化范围是:-11.437‰— -5.752‰,平均值为(-10.009±0.671)‰(Mean±SE)。河水以及地下水δ18O波动范围较小。由于地下水较为稳定,并且循环周期慢,其中δ18O值较河水波动小。
|
| 图 4 诺木洪土壤剖面含水量变化 Fig. 4 Variations of soil water content along soil profiles in Nuomuhong area |
对诺木洪地区河水、地下水以及土壤水分析发现(图 5),河水中δ18O与地下水、土壤水相比偏负。造成这一现象的原因可能有两个:一是河水在入渗补给地下水和土壤水的过程中会有分馏作用导致重同位素的富集;二是当河水已经转化为土壤水之后,土壤剖面中的水分也会受到蒸发的影响,δ18O值因此升高[23]。诺木洪地区河水的补给主要来自于南部昆仑山冰雪融水[24],本次实验在玉珠峰采样的冰川水δ18O值为-11.2‰,与诺木洪河水δ18O值很接近。本研究区内分层土壤中的δ18O值在0—10 cm表层土壤中以及50—70 cm土壤层值偏高。0—10 cm层δ18O偏高的原因是干旱地区表层土壤水通过δ16O强烈蒸发而使重同位素δ18O在表层土壤剖面相对富集;50—70 cm土壤层δ18O偏高可能是由于该土层水被植物利用较多。30—50 cm层土壤水δ18O变小,结合土壤含水量进行分析,由于含水量的增多导致δ18O值下降,降水δ18O值同30—50 cm土壤层重合,说明雨水能补给到该土壤层30—50 cm深处。田立德[25]等在研究青藏高原那曲地区时发现,大约7d之前的降水δ18O值与土壤层20—30 cm处δ18O相对应。
|
| 图 5 诺木洪不同植物茎及各水源δ18O均值 Fig. 5 δ18O values profiles of different plant stem water and water sources in Nuomuhong area |
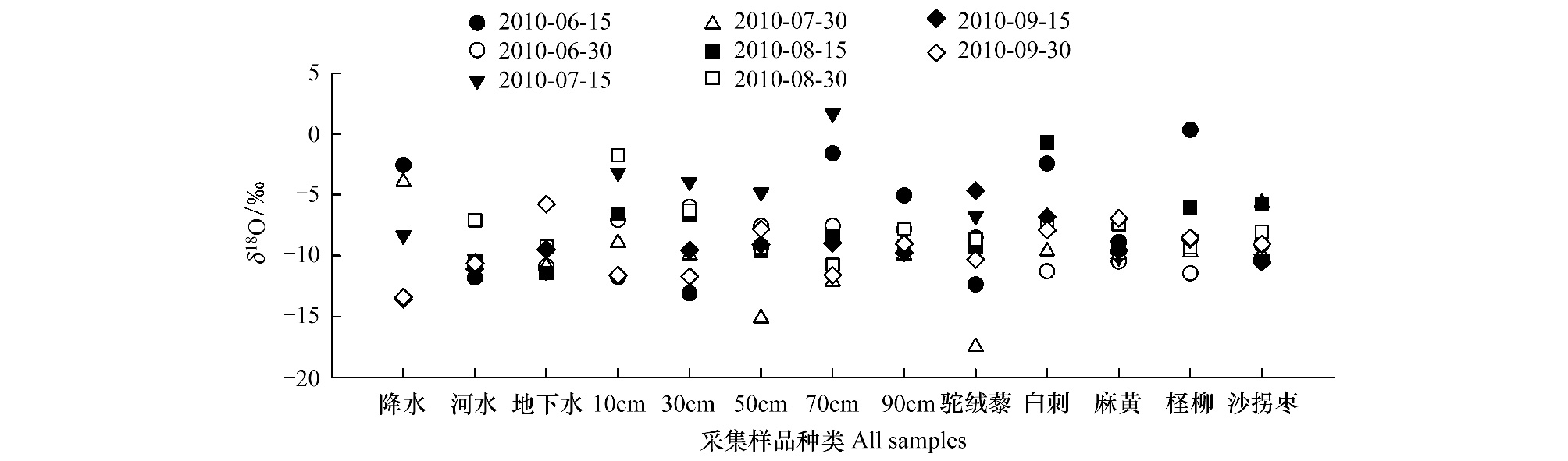
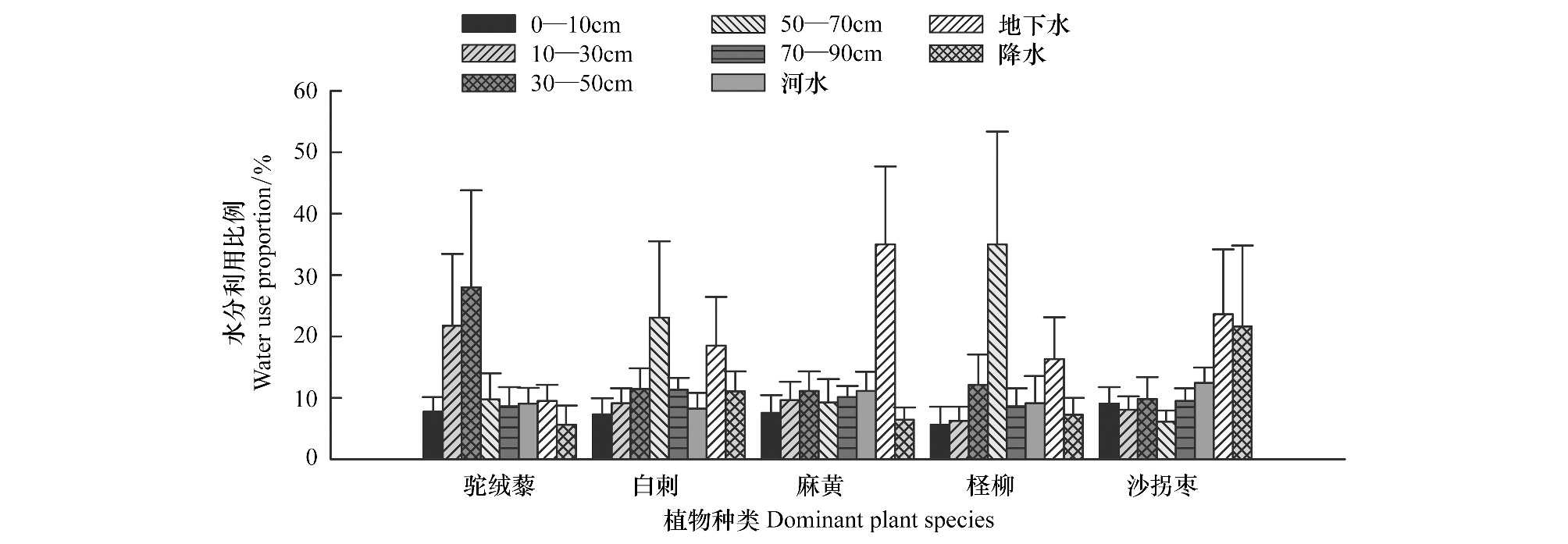
将采集到的所有水源样品加入分析,对比每个采样日期每种植物对水分的吸收利用情况(图 6)。所有植物对水分利用来源的选择显示(图 7),土壤水是植物水分利用的一个重要来源,其次是较为稳定的地下水。对于河水以及降水的分配比例出现了两种情况,驼绒藜、麻黄、柽柳使用河水大于降水,白刺、沙拐枣使用降水大于河水。
|
| 图 6 诺木洪所有样品δ18O值 Fig. 6 δ18O values of all samples |
|
| 图 7 诺木洪地区优势种生长季平均水分利用比例 Fig. 7 The water use proportion of dominant plant species in growth season in Nuomuhong area |
分析5种植物在不同季节水源利用变化(表 1)发现,在生长季初期和末期,驼绒藜对各种来源水分利用比例较为平均,6月15日对10—30cm土壤层水的利用达到67.6%,可能与6月7日强降雨的持续影响有关。生长旺季主要利用30—50 cm土壤水;白刺在生长季初期使用50—70 cm土壤层中的水分,生长旺季最多利用地下水,其次为表层土壤水,生长季末期则对地下水利用比例显著增大;麻黄在生长季初期对各来源水分利用比例较为平均,生长旺季开始对地下水利用比例逐渐升高,到生长季末期则对地下水利用比例升高至71.6%;柽柳在生长季初期对50—70 cm土壤层中的水分利用比例最多,生长旺季可同时利用50—70 cm土壤水以及地下水,到生长季末期则更倾向于使用地下水;沙拐枣在生长季初期对各种来源水分利用较为平均,生长旺季对降水(31%)以及地下水(25.7%)平均利用比例较大,生长季末期对地下水利用比例也达到24.6%。
| 种类 Species | 时间 Time | 0—10 cm | 10—30 cm | 30—50 cm | 50—70 cm | 70—90 cm | 河水 River water | 地下水 Groundwater | 降水 Precipitation |
| 驼绒藜 | 06-15 | 10.2 | 67.6 | 3 | 0.5 | 1 | 10.7 | 6.4 | 0.6 |
| Ceratoides | 06-30 | 12.5 | 10.2 | 13.8 | 13.8 | 14.7 | 17.9 | 17.1 | - |
| latens | 07-15 | 10.8 | 11.6 | 12.5 | 7.3 | 14.9 | 14.3 | 13.7 | 14.9 |
| 07-30 | 0.9 | 1.2 | 89.8 | 2.8 | 1.2 | 1.4 | 1.6 | 0.2 | |
| 08-15 | 9.6 | 9.7 | 17.4 | 14.1 | 17 | 16.9 | 15.4 | - | |
| 08-30 | 3.9 | 8.6 | 20.2 | 23.5 | 12.9 | 10.5 | 20.4 | - | |
| 09-15 | 3.2 | 15.3 | 22.8 | 24.6 | 12.5 | 4.4 | 16.1 | 1.2 | |
| 09-30 | 13.3 | 13.1 | 11.9 | 13.3 | 13.6 | 14.3 | 9.5 | 11.1 | |
| 白刺 | 06-15 | 1 | 0.8 | 1.5 | 71.7 | 4.4 | 1 | 1.1 | 18.4 |
| Nitraria | 06-30 | 0.2 | 0 | 0.2 | 0.2 | 0.3 | 8 | 91.1 | - |
| tangutorum | 07-15 | 9.7 | 10.5 | 11.5 | 6.3 | 15.4 | 15.7 | 15.4 | 15.6 |
| 07-30 | 16.1 | 13.7 | 7 | 9.9 | 13.7 | 12.4 | 11.8 | 15.4 | |
| 08-15 | 36.3 | 34.9 | 5 | 9.9 | 6 | 3.4 | 2.4 | - | |
| 08-30 | 14.2 | 18.3 | 12.3 | 10.2 | 15.4 | 17.2 | 12.3 | - | |
| 09-15 | 4.3 | 15.3 | 20.8 | 22.1 | 13.1 | 5.5 | 15.9 | 2.1 | |
| 09-30 | 5.2 | 5.1 | 16.4 | 5.2 | 10 | 6.4 | 48.1 | 3.7 | |
| 麻黄 | 06-15 | 13.8 | 13.1 | 14.5 | 9.1 | 11.7 | 13.8 | 14.1 | 9.8 |
| Ephedra | 06-30 | 1.5 | 1.1 | 2 | 1.9 | 2.3 | 28.4 | 62.9 | - |
| sinica | 07-15 | 1.8 | 2.1 | 2.5 | 0.9 | 6 | 20 | 60.2 | 6.5 |
| 07-30 | 15.5 | 14.4 | 7.6 | 10.6 | 14.4 | 13.2 | 12.6 | 11.7 | |
| 08-15 | 10 | 10.1 | 17.2 | 14.5 | 17 | 16.4 | 14.8 | - | |
| 08-30 | 11.8 | 17.2 | 13.1 | 11.1 | 16.1 | 17.3 | 13.4 | - | |
| 09-15 | 3.9 | 15.6 | 21.6 | 22.7 | 12.8 | 5.1 | 16.4 | 2 | |
| 09-30 | 2.7 | 2.7 | 9.4 | 2.7 | 5.6 | 3.4 | 71.6 | 1.9 | |
| 柽柳 | 06-15 | 0 | 0 | 0 | 96.3 | 0.3 | 0 | 0 | 3.3 |
| Tamarix | 06-30 | 5.6 | 4.2 | 6.5 | 6.5 | 7.2 | 31.8 | 38.3 | - |
| ramosissima | 07-15 | 4.9 | 5.5 | 6.3 | 2.8 | 12.9 | 24.1 | 29.7 | 13.9 |
| 07-30 | 16 | 14 | 7.2 | 10.2 | 14 | 12.7 | 12.1 | 13.8 | |
| 08-15 | 30.9 | 30.1 | 7.6 | 12.4 | 8.5 | 5.8 | 4.6 | - | |
| 08-30 | 2.1 | 5.1 | 18.3 | 42.4 | 8.2 | 6.6 | 17.3 | - | |
| 09-15 | 0.4 | 4.7 | 27 | 58.5 | 3.2 | 0.7 | 5.3 | 0.1 | |
| 09-30 | 6.7 | 6.6 | 19.8 | 6.7 | 12.7 | 8.2 | 34.5 | 4.9 | |
| 沙拐枣 | 06-15 | 14.4 | 13.9 | 14.5 | 8.3 | 10.9 | 14.4 | 14.6 | 9 |
| Calligonum | 06-30 | 2.8 | 2 | 3.3 | 3.3 | 3.7 | 32.9 | 51.9 | - |
| mongolicum | 07-15 | 1.6 | 1.9 | 2.2 | 0.8 | 5.4 | 18.4 | 63.7 | 5.9 |
| 07-30 | 5.3 | 4.3 | 1.9 | 2.9 | 4.3 | 3.8 | 3.6 | 74.1 | |
| 08-15 | 34.4 | 33.1 | 6.3 | 10.6 | 7.1 | 4.8 | 3.7 | - | |
| 08-30 | 6.9 | 13 | 16.8 | 15 | 16.5 | 15 | 16.7 | - | |
| 09-15 | 15.6 | 11.6 | 10.5 | 10.2 | 12.1 | 15.5 | 11.4 | 13 | |
| 09-30 | 8.2 | 8.1 | 19.9 | 8.2 | 14.8 | 10 | 24.6 | 6.1 |
植物对资源的竞争是一种普遍现象,多数生态系统的竞争主要发生在地下根系对水分和养分的竞争[26, 27],同一生境中吸水层位相似的植物间存在对水源的竞争现象[28]。因此,在生长季初期,白刺和柽柳对50—70 cm土壤层中的水分存在竞争,驼绒藜、麻黄和沙拐枣则对每层土壤水都有竞争现象;生长旺期,4种灌木白刺、麻黄、柽柳和沙拐枣开始对地下水竞争,到生长末期,对地下水源的竞争加剧。
2.3.2 植物利用土壤水分定量分析对诺木洪地区5种植物土壤水分利用比例进行深入分析。驼绒藜在整个生长季对表层0—10 cm土壤层利用比例最少,其次为50—70 cm土壤层,对30—50 cm土壤层中的水分利用比例最高,平均可以达到32.33%。白刺利用50—70 cm土壤层中的水分最多。麻黄对各层土壤水分利用比例较为平均。柽柳对于50—70 cm的土壤层利用比例最多,情况与白刺相似。沙拐枣对各土壤层中水分利用比例较为均匀,没有出现对某层水分的过于依赖。
植物生长于土壤之中,土壤水是植物水的直接来源。植物根系吸收土壤水分这一过程,控制着水分状态和光合作用等[29]。对于水分稀少的荒漠地区来说,荒漠灌木根系表现型或者空间结构特征是划分根系功能的重要依据[30]。驼绒藜在土壤水使用方面与其他植物不同。驼绒藜属于半灌木,而白刺、麻黄、柽柳、沙拐枣都属于灌木。白刺主根粗壮,入土较浅,根系以0—40 cm土层比例较大,但是平均根深80 cm,甚至1 m以上[31]。麻黄主根发达,毛根分布范围广[32],根系发达,呈网络状固结土壤[33]。深根系植物柽柳,在天山地区的挖掘发现其主要根系分布范围为50—160 cm,最深可达300 cm,0—60 cm根系分布较少[34]。柽柳对50—70 cm以及深层地下水利用比例较高,同徐贵青,朱林[35]等的研究结果一致。沙拐枣根系较深,侧根在10—20 cm层分布最多,吸水能力也更强[36]。前人对沙拐枣的研究中认为,其水平与垂直根系均发达,可以利用到深层土壤水。在本研究中发现该植被对地下水源的利用比例很大,这一现象同麻黄相似。因此,植物根系可能会存在于整个土壤剖面,但是根的存在却并不意味着对土壤水分吸收活跃。植物用来吸收水分的活根往往会因为外界条件的刺激而改变。4种灌木白刺、麻黄、柽柳、沙拐枣根系都比较深,在整个生长季对不同水源的利用比例却存在差异。生长季初期白刺、柽柳对50—70 cm土壤水利用比例最大,麻黄和沙拐枣则对各种水源利用比例较为平均,但是在生长季的末期,这4种植物都对地下水利用比例最高。这一结果表明,过去利用根系结构进行植物水分来源判断的方法存在一定的局限性。植物根系分布的位置,不一定是其吸收水分的位置。
地下水是多数荒漠植物重要的水分来源[37]。地下水位下降可以直接影响土壤水分和养分分布,引起植物对水资源竞争,从而影响荒漠植被分布、生长、种群演替等群落格局[38]。樊自立等认为西北干旱区生态地下水埋深深度可以在很大程度上影响非地带性中生和中旱生植被[39]。杨自辉[40]等通过对民勤地区地下水和降水监测研究白刺群落消长,发现地下水位的下降驱动绿洲外围环境的旱化。刘发民[41]等认为巴丹吉林沙漠西南缘柽柳可在0—200 cm范围内土壤含水量较低的条件下生存。梁少民[42]等对塔克拉玛干腹地灌水量分析认为,根系区土壤水分低于2.5%沙拐枣就会受到干旱胁迫。诺木洪地区系潜水,随着城市化建设进程加快,用水量逐渐加大。在本研究中发现,生长季末期,本研究区植物对地下水利用比例普遍较高,因此维持地下水水位将对本区植物的生长极为重要。
3 结论(1) 诺木洪地区大气降水线为y=7.019x-3.217 (R2=0.970,P<0.001),很好地反应了干旱区的气候特点。斜率小于8,截距为负,表明该地温度高湿度低。大气降水过量氘值较低,表明本地降水中来自局地蒸发的水分较多。诺木洪地区河水、地下水、土壤水都位于大气降水线附近,说明降水都对他们有补给作用。河水主要来源于山区冰雪融水,对地下水补给量大,所以δ18O值较小,位于大气降水线左上方;此地气候干旱蒸发强烈,造成土壤水中δ18O的富集,所以位于大气降水线下方。
(2) 诺木洪地区5种优势种植物都使用土壤水比例最大,其次为地下水。半灌木驼绒藜使用10—50 cm层土壤水分,灌木白刺、麻黄、柽柳、沙拐枣在土壤水分利用比例方面存在显著不同,白刺、柽柳吸水层位相同,都对50—70 cm土壤层水分吸收最大,存在对该层水分的竞争;麻黄和沙拐枣对每层土壤水分的利用比例较为平均,出现对土壤水分的竞争现象。
4 种灌木白刺、麻黄、柽柳、沙拐枣生长季的不同时期都存在对利用水源的转换现象,但是到生长季末期,都对地下水的需求较多。因此维持干旱半干旱地区地下水水位对荒漠植物的生长具有重要意义。
(3) 植物根系贯穿于整个土壤剖面,但是根的存在却并不意味着对土壤水分吸收活跃。植物用来吸收水分的活根往往会因为外界条件的刺激而发生改变。因此,植物根系分布的位置,不一定是其吸收水分的位置。过去利用根系结构进行植物水分来源判断的方法存在一定的局限性。
| [1] | Cao Y L, Lu Q,Lin G H. Review and perspective on hydrogen stable isotopes technique in tracing plant water sources researches. Acta Ecologica Sinica, 2002, 22(1): 111-117. |
| [2] | Dawson T E, Ehleringer J R. Streamside trees that do not use stream water. Nature, 1991, 350(6316): 335-337. |
| [3] | Phillips S L, Ehleringer J R. Limited uptake of summer precipitation by bigtooth maple(Acer grandidentatum Nutt) and Gambel's oak (Quercus gambelii Nutt). Tree, 1995, 9(4): 214-219. |
| [4] | Ehleringer J R, Dawson T E. Water uptake by plants:perspectives from stable isotope composition. Plant, Cell and Environment, 1992, 15(9), 1073-1082. |
| [5] | Ehlerringer J R, Hall A E, Farquhar G D, Saugier B. Stable Isotopes and Plant Carbon-Water Relations. New York:Academic Press, 1993. |
| [6] | Dawson T E. Hydraulic lift and water use by plants: Implications for water balance, performance and plant-plant interactions. Oecologia, 1993, 95(4): 565-574. |
| [7] | Gonfiantini R, Gratziu S, Tongiorgi E. Oxygen isotopic composition of water in leaves// Isotopes and Radiation in Soil-Plant Nutrition Studies. Vienna: International Atonatic. Energy Agency, 1965: 405-410. |
| [8] | Wershaw R L, Friedman I, Heller S J. Hydrogen isotope fractionation of water passing through trees // Hobson F, Speers M, eds. Advances in Organic Geochemistry. New York: Pergamon, 1966: 55-67. |
| [9] | Shi H, Liu S R, Zhao X G, Application of stable hydrogen and oxygen isotope in water circulationg. Jourunal of Soil and Water Conservation, 2003, 17(2): 163-166. |
| [10] | Duan D Y, Ouyang H. Application of stable hydrogen and oxygen isotope in analyzing plant water use sources. Ecology and Environment, 2007, 16(2): 655-660. |
| [11] | Li S G, Remero-Saltosh G, Tsujimura M, Sugimoto A, Sasaki L,Davaa G, Oyunbaatar D. Plant water sources in the cold semiarid ecosystem of the upper Kherlen River catchment in Mongolia: A stable isotope approach. Journal of Hydrology, 2007, 333(1): 109-117. |
| [12] | Zhu L, Xu X, Mao G L. Water sources of shrubs grown in the northern Ningxia Plain of China characterized by shallow groundwater table. Chinese Journal of Plant Ecology, 2012, 36(7): 618-628. |
| [13] | Zhou Y D, Chen S P, Song W M, Lu Q, Lin G H. Water-use strategies of two desert plants along a precipitation gradient in northwestern China. Chinese Journal of Plant Ecology, 2011, 35(8): 789-800. |
| [14] | Zhao L J, Xiao H L, Chen G D, Song Y X, Zhao L, Li C Z, Yang Q.A preliminary study of water sources of riparian plants in the Lower Reaches of the Heihe Basin. Acta Geoscientica Sinica, 2008, 29(6): 709-718. |
| [15] | Zhu Y J, Jia Z Q, Lu Q, Hao Y G, Zhang J B, Li L, Qi Y L. Water use strategy of five shrubs in Ulanbuh desert. Scientia Silvae Sinicae, 2010, 46(4): 15-21. |
| [16] | McCole A A, Stern L A. Seasonal water use patterns of Juniperus ashei on the Edwards Plateau, Texas, based on stable isotopes in water. Journal of Hydrology, 2007, 34(3/4): 238-248. |
| [17] | Yao T D, Zhu L P. The response of environmental changes on Tibetan Plateau to global changes and adaptation strategy.Advances in Earth Science, 2006, 21(5): 459-464. |
| [18] | Craig H. Isotopic variations in meteoric water. Science, 1961, 133(3465): 1702-1703. |
| [19] | Xu S G, Liu Y F, Sun W G. Research on the stable isotope for soil water vertical transporting in unsaturated zone of Zhaolong Wetland. Journal of China Hydrology, 2006, 26(5): 1-6. |
| [20] | Yin L, Zhao L J, Ruan Y F, Xiao H L, Cheng G D, Zhou M X, Wang F, Li C Z. Study of the replenishment sources of typical ecosystems water and dominant plant water in the lower reaches of the Heihe, China. Journal of Glaciology and Geocryology, 2012, 34(6): 1478-1486. |
| [21] | Wei Y F, Guo K, Chen J Q. Effect of precipitation pattern on recruitment of soil water in Kubuqi Desert, Northwestern China. Journal of Plant Ecology, 2008, 32(6): 1346-1355. |
| [22] | Du J H, Yan P, E Y H, Han F G. Influence of heavy rain event on soil water content of Nitraria tangutorum nebkhas in different succession periods. Bulletin of Soil and Water Conservation, 2007, 27(6): 20-24. |
| [23] | Zimmermann U, Ehhalt D, Muennich K O. Soil-water movement and evapotranspiration: Changes in the isotopic composition of the water. Isotopes in Hydrology, 1968, 31(10): 567-585. |
| [24] | Liu Z M, Wang G L, Yang Z J, Ma M Z. Exploitation and utilization of future water resources and its environment effects at Geermu-Nuomuhong region. Geography and Territorial Research, 2001, 17(3): 68-72. |
| [25] | Tian L D, Yao T D, Sun W Z, Tsujimura M. Stable isotope in soil water in the middle of Tibetan Plateau. Acta Pedologica Sinica, 2002, 39(3): 289-295. |
| [26] | Zhang Y D,Bai S B,Wang Z Q,Shen Y X. Effect of the mixed on root growth and distribution of Fraxinus mandshurica and Larix gmelinii. Scientia Silvae Sinicae, 2001, 37(5): 16-23. |
| [27] | Wang Z Q, Zhang Y D, Wang Q C. Study on the root interactions between Fraxinus mandshurica and Larix gmelinii. Acta Phytoecologica Sinica, 2000, 24(3): 346-350. |
| [28] | Zeng Q, Ma J Y. Plant water sources of different habitats and its environmental indication in Heihe River Basin. Journal of Glaciology and Geocryology, 2013, 35(1): 148-155. |
| [29] | Macfall J S, John G A, Kramer P J. Comparative water uptake by roots of different ages in seedlings of loblolly pine(Pinus taeda L.). New Phytologist, 1991, 119(4): 551-560. |
| [30] | Atkinson D. Plant Root Growth: An Ecological Perspective.UK: Blackwell Scientific Publications, 1991. |
| [31] | Sun X, Yu Z. A study on root system of Nitraria Tangutorum.Journal of Desert Research, 1992, 12(4): 50-54. |
| [32] | Huang M. Studies on relationship between sprinkle irrigation system or Ephedra in dry sandy area and distribution of root system. Journal of Ningxia Agricultural College, 2003, 24(3): 34-36. |
| [33] | Li G H. Ephedra distachya. Soil and Water Conservation in China, 1989, (10): 48-48. |
| [34] | Xu G Q, Li Y. Roots distribution of three desert shrubs and their response to precipitation under co-occurring conditions. Acta Ecologica Sinica, 2009, 29(1): 130-137. |
| [35] | Zhu L, Xu X, Tang J N. Study on the water sources of 4 bushes based on the 18O stable isotope grew in Yinchuan plain northern area in the beginning of summer. Journal of Fujian Forestry Science and Technology, 2012, 39(1): 28-34. |
| [36] | Li H T. The primary study on the relation between Calligonum leucocladum and its environment. Journal of Xinjiang Agricultural University, 1996, 19(1): 56-61, 72-72. |
| [37] | Synder K A, William D C. Water resources used by riparian trees varies among stream types on the Pedro River, Arizona.Agricultural and Forest Metrology, 2000, 105(1/3): 227-240. |
| [38] | Chen Y N, Li W H, Chen Y P, Xu C C, Zhang L H. Water conveyance in dried-up riverway and ecological restoration in the lower reaches of Tarim River, China. Acta Ecologica Sinica, 2007, 27(2): 538-545. |
| [39] | Fan Z L, Chen Y N, Li H P, Ma Y J, Alishir K,Abdimijit.Determ ination of suitable ecological groundwater depth in arid areas in northwest part of China. Journal of Arid Land Resources and Environment, 2008, 22(2): 1-4. |
| [40] | Yang Z H, Gao Z H. Impact of precipitation and underground water level in the edge of oases on growth and decline of Nitraria tangugtorum Community. Chinese Journal of Applied Ecology, 2000, 11(6): 923-926. |
| [41] | Liu F M, Jin Y, Zhang X J. Soil water regime of Tamarix ramosissima sandbreak in the desert region. Acta Botanica Boreali-Occidentalia, Sinica, 2001, 21(5): 937-943. |
| [42] | Liang S M, Zhang X M, Zeng F J, Zhang Z W, Qiu S K, Yan H L. Ecophysiological responses of Calligonum arborescens Litv.to irrigation volume in the hinterland of the Taklimakan desert. Journal of Desert Research, 2010, 30(6): 1348-1353. |
| [1] | 曹燕丽, 卢琦, 林光辉.氢稳定性同位素确定植物水源的应用与前景.生态学报, 2002, 22(1): 111-117. |
| [9] | 石辉, 刘世荣, 赵晓广. 稳定性氢氧同位素在水分循环中的应用.水土保持学报, 2003, 17(2): 163-166. |
| [10] | 段德玉, 欧阳华. 稳定氢氧同位素在定量区分植物水分利用来源中的应用. 生态环境, 2007, 16(2): 655-660. |
| [12] | 朱林, 徐兴, 毛桂莲. 宁夏平原北部地下水埋深浅地区不同灌木的水分来源. 植物生态学报, 2012, 36(7): 618-628. |
| [13] | 周雅聃, 陈世苹, 宋维民, 卢琦, 林光辉.不同降水条件下两种荒漠植物的水分利用策略. 植物生态学报, 2011, 35(8): 789-800. |
| [14] | 赵良菊, 肖洪浪, 程国栋, 宋耀选, 赵亮, 李彩芝, 杨秋. 黑河下游河岸林植物水分来源初步研究. 地球学报, 2008, 29(6): 709-718. |
| [15] | 朱雅娟, 贾志清, 卢琦, 郝玉光, 张景波, 李磊, 綦艳林. 乌兰布和沙漠5种灌木的水分利用策略. 林业科学, 2010, 46(4): 15-21. |
| [17] | 姚檀栋, 朱立平. 青藏高原环境变化对全球变化的响应及其适应对策. 地球科学进展, 2006, 21(5): 459-464. |
| [19] | 许士国, 刘盈斐, 孙万光. 扎龙湿地包气带土壤水分垂直运移的稳定同位素研究. 水文, 2006, 26(5): 1-6. |
| [20] | 尹力, 赵良菊, 阮云峰, 肖洪浪, 程国栋, 周茅先, 王芳, 李彩芝. 黑河下游典型生态系统水分补给源及优势植物水分来源研究. 冰川冻土, 2012, 34(6): 1478-1486. |
| [21] | 魏雅芬, 郭柯, 陈吉泉. 降雨格局对库布齐沙漠土壤水分的补充效应. 植物生态学报, 2008, 32(6): 1346-1355. |
| [22] | 杜建会, 严平, 俄有浩, 韩富贵. 强降雨事件对不同演化阶段白刺灌丛沙堆土壤水分的影响.水土保持通报, 2007, 27(6): 20-24. |
| [24] | 刘志明, 王贵玲, 杨振京, 马明珠. 格尔木至诺木洪地区水资源开发利用及其环境效应分析.地理学与国土研究, 2001, 17(3): 68-72. |
| [25] | 田立德, 姚檀栋, 孙维贞, Tsujimura M. 青藏高原中部土壤水中稳定同位素变化. 土壤学报, 2002, 39(3): 289-295. |
| [26] | 张彦东, 白尚斌, 王政权, 沈有信. 混交条件下水曲柳落叶松根系的生长与分布. 林业科学, 2001, 37(5): 16-23. |
| [27] | 王政权, 张彦东, 王庆成. 水曲柳落叶松根系之间的相互作用研究. 植物生态学报,2000, 24(3): 346-350. |
| [28] | 曾巧, 马剑英. 黑河流域不同生境植物水分来源及环境指示意义. 冰川冻土, 2013, 35(1):148-155. |
| [31] | 孙祥, 于卓. 白刺根系的研究. 中国沙漠, 1992, 12(4): 50-54. |
| [32] | 黄梅. 干旱多沙区麻黄喷灌灌溉制度和根系分布试验研究. 宁夏农学院学报, 2003, 24(3): 34-36. |
| [33] | 李焕广. 麻黄. 中国水土保持, 1989, (10): 48-48. |
| [34] | 徐贵青, 李彦. 共生条件下三种荒漠灌木的根系分布特征及其对降水的响应. 生态学报, 2009, 29(1): 130-137. |
| [35] | 朱林, 许兴, 唐建宁. 基于18O稳定同位素的银川平原北部4种灌木夏初水分来源的研究. 福建林业科技, 2012, 39(1): 28-34. |
| [36] | 李海涛. 白皮沙拐枣(Calligonum leucocladum)根系与环境关系的初步研究.新疆农业大学学报, 1996, 19(1): 56-61, 72-72. |
| [38] | 陈亚宁, 李卫红, 陈亚鹏, 徐长春, 张丽华. 新疆塔里木河下游断流河道输水与生态恢复.生态学报, 2007, 27(2): 538-545. |
| [39] | 樊自立, 陈亚宁, 李和平, 马英杰, 艾里西尔·库尔班, 阿布都米吉提. 中国西北干旱区生态地下水埋深适宜深度的确定. 干旱区资源与环境, 2008, 22(2): 1-4. |
| [40] | 杨自辉, 高志海. 荒漠绿洲边缘降水和地下水对白刺群落消长的影响. 应用生态学报, 2000, 11(6): 923-926. |
| [41] | 刘发民, 金燕, 张小军. 荒漠地区柽柳人工固沙林土壤水分动态研究. 西北植物学报, 2001, 21(5): 937-943. |
| [42] | 梁少民, 张希明, 曾凡江, 张仲伍, 邱士可, 闫海龙. 沙漠腹地乔木状沙拐枣对灌水量的生理生态响应. 中国沙漠, 2010, 30(6): 1348-1353. |
 2014, Vol. 34
2014, Vol. 34




