文章信息
- 马放, 苏蒙, 王立, 张雪, 李世阳
- MA Fang, SU Meng, WANG Li, ZHANG Xue, LI Shiyang
- 丛枝菌根真菌对小麦生长的影响
- Effects of Arbuscular mycorrhizal fungi (AMF) on the growth of wheat
- 生态学报, 2014, 34(21): 6107-6114
- Acta Ecologica Sinica, 2014, 34(21): 6107-6114
- http://dx.doi.org/10.5846/stxb201301280181
-
文章历史
- 收稿日期:2013-1-28
- 网络出版日期:2014-3-13
2. 哈尔滨工业大学, 城市水资源与水环境国家重点实验室, 哈尔滨 150090
2. Harbin Institute of Technology, State Key Laboratory of Urban Water Resource and Environment, Harbin 150090, China
丛枝菌根真菌(Arbuscula mycorrhizal fungi,AMF)广泛的分布在土壤中,对自然环境中植物营养的摄取有着十分重要的作用[1, 2]。其可以在植物根内皮层细胞形成泡囊和丛枝结构,从而与植物形成互惠互利共生体。在这种共生体系中,植物为菌根真菌提供需要的碳源和能量,菌根在根外土壤中形成根外菌丝网,扩大植物根系吸收范围,从而提高植物对氮、磷养分和水分的吸收[3],改善寄主植物的营养状况[4, 5, 6, 7, 8]。从而促进植株生长[9, 10]。
我国是农业生产大国,每年化肥施加造成的农业面源污染严重,利用丛枝菌根真菌对耕作土壤中营养元素的吸收利用来对农业面源污染进行控制是一条有效的途径[11]。现有各类研究表明,施加AMF菌剂后,菌根能提高植物对土壤或肥料中养分的利用效果,从而促进植物的生长[12, 13, 14]。但目前各类研究大多集中于实验研究阶段,对大田环境,特别是农业生产种植环境下AMF菌剂运用情况的考察十分缺少。因此,考察在大田环境下,丛枝菌根真菌对作物的生长状况以及土壤养分情况的影响以及其相关性具有积极意义。
因此,本研究选择南方主要经济作物——小麦为研究对象,比较两种土著优势丛枝菌根真菌摩西球囊霉(Glomus mosseae,GM)和根内球囊霉(Glomus intraradices,GI),考察在正常田间管理条件下其对小麦生长的影响以及土壤中氮、磷元素含量的影响。
1 材料和方法 1.1 材料采用大田实验的方法,实验地点在江苏省宜兴市和桥镇北新村城市水资源与水环境国家重点实验室“农业清洁生产示范基地(E:31°30′07.31,N:119°52′06.17)”。土壤中总氮含量185 g/kg,水解性氮含量44.38 mg/kg,总磷含量0.36 g/kg,有效磷含量17.42 mg/kg,pH 6.9。
施肥处理:播种前施加基肥(复合肥):每666.67 m2施加40 kg,折合每666.67 m2施加总氮6 kg,每666.67 m2施加有效磷8 kg,每666.67 m2施加有效钾4 kg;提苗肥施加尿素,每666.67 m2施加12.5 kg。折合666.67 m2施加N 5 kg;2月末—3月初施加返青肥尿素:每666.67 m2施加12.5 kg。折合666.67 m2施加N 5 kg。
供试菌剂:供试AMF为广适菌种——摩西球囊霉 (Glomus mosseae,GM),根内球囊霉(Glomus intraradices,GI),由本课题组独立自主培养。以白三叶草为宿主分别对其进行扩繁,产生的菌剂包括扩繁后产生的相应基质以及植物根段等,菌剂孢子密度为130/10 g。
宿主作物:小麦种子为扬麦(Triticum aestivum Linn)14号。
1.2 试验田设计试验田共九块,每块大小为3 m×3 m,分别接种摩西球囊霉(GM)、根内球囊霉(GI)以及不接菌(CK)处理,每种处理重复3次,小麦播种时,施加菌剂与小麦种子混合,其中每小区施加菌剂量为500 g/小区。每小区之间以0.5 m作为间隔,并用厚度为2 mm的防水材料围隔。
1.3 试验方法菌根侵染率检测方法 选取不同小麦生长周期的根系进行测定,随机选取各条件中1—2 cm长植物根系进行解离与染色,每个重复观察100个根段[15]。
株高 采用卷尺测量,每组处理,测量9株小麦的高度。
生物量 包括地上生物量及地下生物量。地下部分洗净泥土,吸干表面水分后和地上部分105 ℃杀青5 min 后60—80 ℃烘干至恒重,称量得地上、地下生物量,两部分之和为总生物量。
菌根依赖性指数(MD%)=接菌后植物生物量(M+)/未接菌植物生物量(M-)×100%
根据Nemec[16]的分类方法,可将植物的菌根的依赖程度被分为三级,当MD= 300%时,为高强度依赖,MD=200%时,为中等强度依赖,MD=100%时,为弱依赖或无依赖。
土壤有效磷 采用碳酸氢钠浸提-钼锑抗分光光度法测定Olsen-P[17]。
土壤总磷 消解-钼锑抗分光光度法[17]。
土壤水解性氮 碱解扩散法[18]。
土壤总氮 全自动凯氏定氮仪UDK159[19]。
1.4 采样方式按照小麦的生长周期,分别在生长过程中的30,60,120,150,180,210 d对土壤以及小麦地表植株以及地下根系进行采样。
1.5 数据分析试验数据采用Spss19.0进行差异显著性分析和相关性分析,运用Matlab,Origin软件进行曲线绘制及曲线拟合。
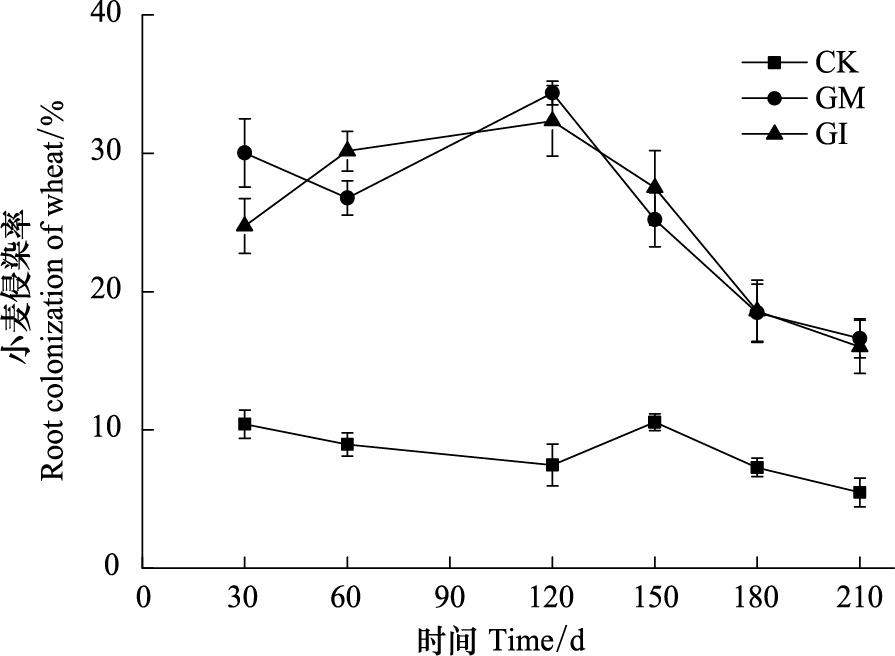
2 结果与分析 2.1 AMF对小麦侵染效果GM与GI是两种土著菌根真菌,在自然条件下可与小麦形成菌根,但自然侵染能力较弱,通过人工强化技术可有效促进二者互利共生关系的形成,进而提高植物生长能力(图 1)。
|
| 图 1 AMF对小麦生长周期侵染率的影响 Fig. 1 Effects of AMF on root colonization of wheat during the growth cycle CK:对照空白;GM:摩西球囊霉(Glomus mosseae);GI:根内球囊霉(Glomus mosseae) |
如图 1,人工强化施加菌剂可以显著提高麦田原生环境下AMF对小麦的侵染率(P<0.05)。接菌的小麦侵染率随着小麦的生长过程呈现先升高后降低的变化。在120 d时GM侵染率最高34.36%,GI的小麦侵染率为32.34%,与CK相比,分别显著提高小麦侵染率24.54%,21.93%。
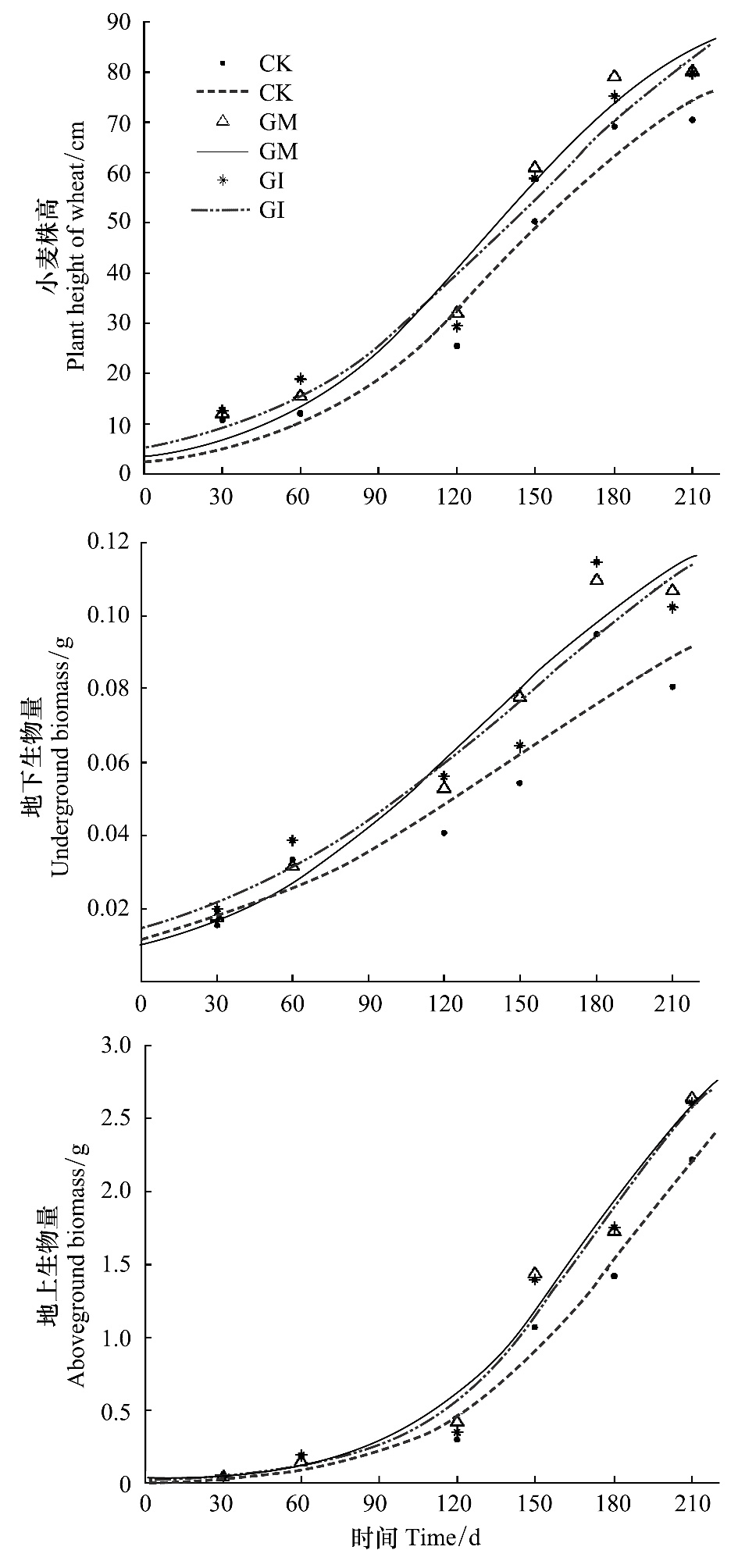
2.2 AMF对小麦株高以及生物量的影响以及菌根依赖性的研究小麦的株高和生物量是反应小麦生长状况的重要指标,考察菌剂强化对小麦生长的影响(图 2,图 3)。
|
| 图 2 不同AMF侵染对小麦株高,地下生物量和地上生物量的影响 Fig. 2 Effects of different AMFs on plant height underground biomass and aboveground biomass of wheat |

|
| 图 3 小麦菌根依赖性 Fig. 3 Mycorrhizal dependency of wheat |
对小麦生长过程中株高、地上生物量、地下生物量的随时间变化进行的曲线拟合,结果显示不同处理的小麦的株高以及生物量(图 2)均符合logistic曲线的变化规律(表 1)。
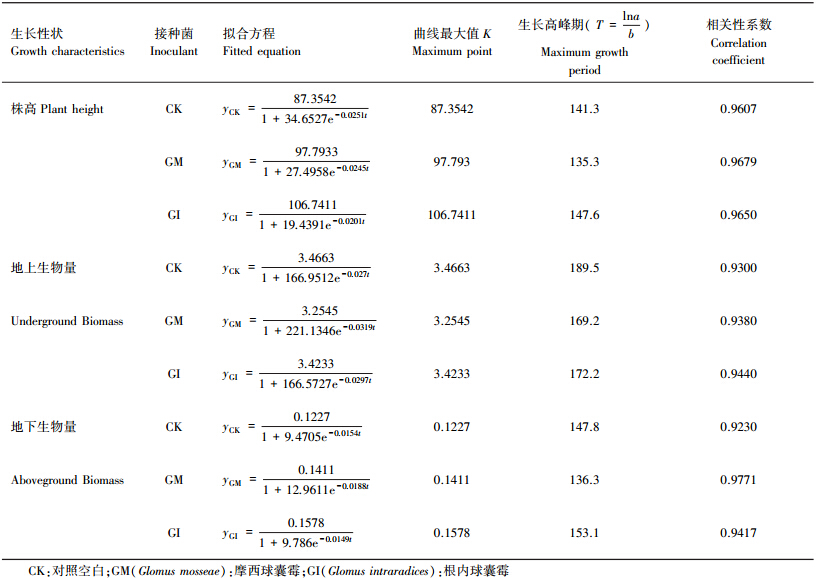 |
接菌小麦(GM、GI)相对于不接菌(CK),株高在60 d时显著开始提高,最终GM,GI接菌处理分别高于CK小麦14.08%和13.57%,但接种GM与GI之间无显著差异。接种AMF(GM、GI),150 d时地下生物量的提高幅度分别为43.3%和18.9%,180 d时地上生物量的提高幅度分别为23.5%和21.7%。根据对小麦株高及生物量周期变化的拟合方程发现(表 1),GM使小麦地上、地下生物量增长高峰期分别提前20 d、11 d;GI使小麦地上生物量增长高峰期提前17 d。根据拟合方程结果,小麦地上生物量的最高生长时期位于180 d前后,地下生物量最快生长时期位于150 d前后,小麦根系的快速生长期要先于地上部分。
考察180d时小麦的菌根依赖性指数(图 3),结果发现,小麦地上和地下对GM的菌根依赖指数分别为123%和143%,对GI的菌根依赖指数分别121%和128%。小麦地下部分对GM的依赖性指数更高,由此可以说明小麦根系对AMF的菌根依赖性更高。
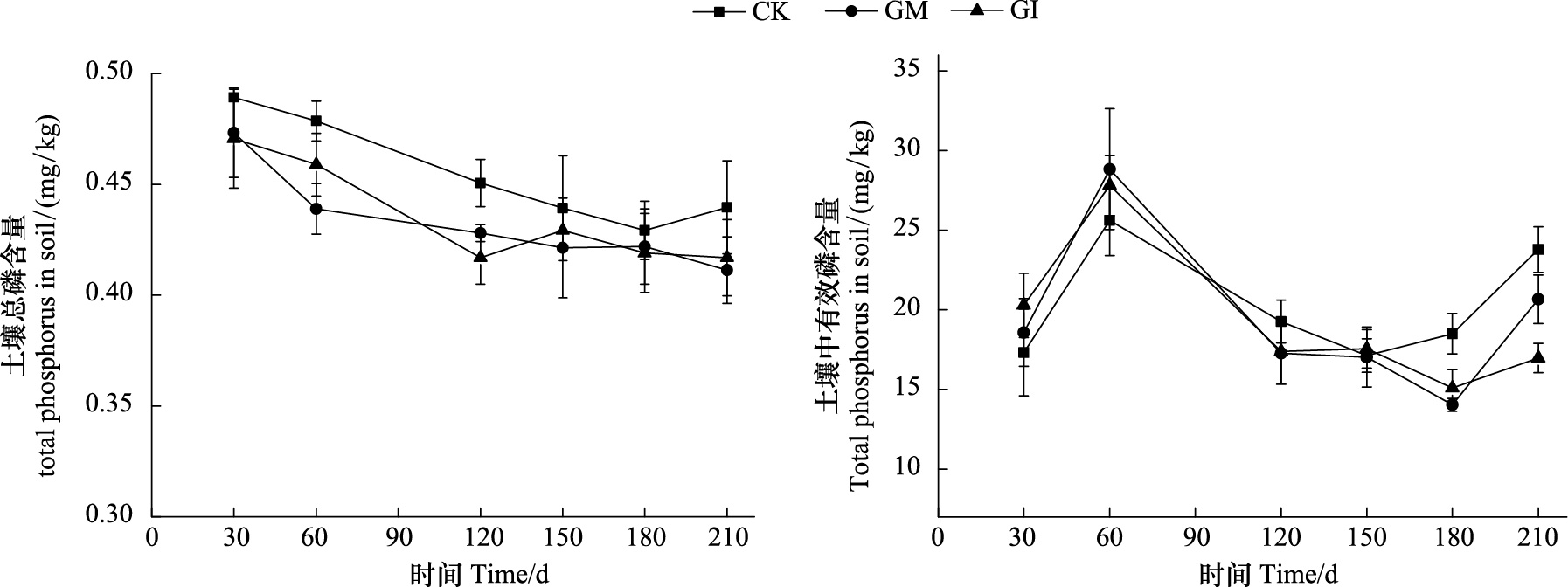
2.3 AMF对麦田土壤中P素变化的影响由图 4可以看出不同处理下,土壤中总磷含量均呈现总体下降的趋势。GM处理条件下,总磷含量最低为0.411 g/kg,有效磷含量最高18.50 mg/kg,60 d(分蘖期)、120 d(拔节期)、210 d(结实期)总磷含量与CK相比具有显著性差异(P<0.05)。有效磷含量在120 d(拔节期)、180 d(孕穗期)时与CK相比具有显著性差异(P<0.05)。GI处理土壤总磷最低含量为0.416 g/kg,有效磷最低为15.08 mg/kg,总磷在60 d(分蘖期)、120 d(拔节期)、210 d(结实期)与CK相比具有显著性差异(P<0.05),有效磷含量在120 d(拔节期)、180 d(孕穗期)时与CK相比具有显著性差异(P<0.05)。有效磷含量变化最大值发生在90—120 d,此时CK处理的土壤有效磷吸收量为6.35 mg/kg,GM、GI处理的土壤有效磷吸收量为11.55 mg/kg和10.41 mg/kg。
|
| 图 4 AMF对土壤中总磷和有效磷的影响 Fig. 4 Effect of different AMFs on total phosphorus (a) and available phosphorus (b) in soil |
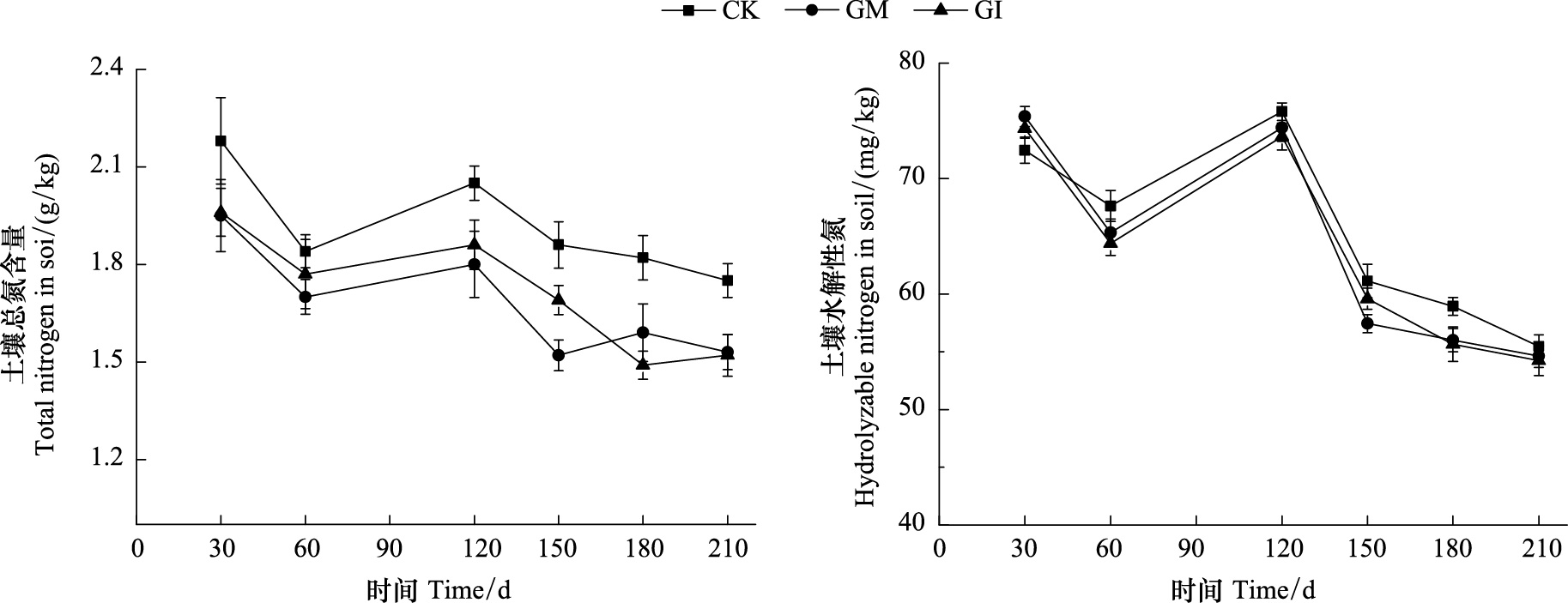
由图 5可以看出,不同处理土壤中总氮以及水解性氮含量总体呈现下降趋势,随着小麦的生长时期的不同呈现先升高,后降低,然后又逐渐降低的变化规律。其中GM、GI处理的小麦各发育阶段土壤的总氮含量均显著低于CK (P<0.05),最终总氮含量对比CK分别降低了13.1%和12.6%。在30d时,GM、GI处理的土壤有效氮含量显著高于CK(P<0.05),其中GM处理的为75.38 mg/kg,GI处理的为74.34 mg/kg;在180d时,施加GM、GI的土壤水解性氮含量显著低于CK处理(P<0.05)。在150 d时,GM与GI处理之间土壤总氮的含量呈现显著性差异 (P<0.05)。120—150 d时,土壤水解性氮的变化量最大,其中CK处理的土壤变化量为14.05 mg/kg,GM处理的土壤变化量为16.96 mg/kg,GI处理的土壤变化量为14.67 mg/kg。
|
| 图 5 AMF对土壤中总氮和水解性氮的影响 Fig. 5 Effect of different AMFs on total nitrogen and hydrolysable nitrogen in soil |
AMF可以改善土壤养分的有效性,促进作物生长,AMF的侵染率与土壤中营养元素,特别是土壤中氮素有密切相关性(表 2)。
| 参数 Parameters | 接种菌 Inoculant | 侵染率 Colonization rate | 地上生物量 Aboveground biomass | 地下生物量 Underground biomass | 土壤全氮 Total soil nitrogen | 土壤全磷 Soil total phosphorus | 土壤水解性氮 Hydrolysable nitrogen | 土壤有效磷 Soil available phosphorus |
| *显著相关(P<0.05); **极显著相关(P<0.01) | ||||||||
| 侵染率 | GM | 1 | -.879* | -0.799 | 0.805 | 0.589 | 0.819* | -0.122 |
| Colonization rate | GI | 1 | -8.11* | -0.707 | 0.735 | 0.528 | 0.699 | -0.498 |
| CK | 1 | -0.666 | -0.764 | 0.517 | 0.307 | 0.292 | -0.353 | |
| 地上生物量 | GM | 1 | 0.888* | -0.829* | -0.785 | -0.853* | -0.337 | |
| Aboveground biomass | GI | 1 | 0.941** | -0.906* | -0.705 | -0.878* | -0.606 | |
| CK | 1 | 0.972** | -0.761 | -0779 | -0.835* | -0.170 | ||
| 地下生物量 | GM | 1 | -0.768 | -0.817* | -0.898* | -0.443 | ||
| Underground biomass | GI | 1 | -0.941** | -0.840* | -0.881* | -0.702 | ||
| CK | 1 | -0.810 | -0.795 | -0.818* | -0.055 | |||
| 土壤全氮 | GM | 1 | 0.661 | 0.915* | 0.088 | |||
| Total soil nitrogen | GI | 1 | 0.509 | 0.969** | 0.445 | |||
| CK | 1 | 0.640 | 0.834* | -0.295 | ||||
| 土壤全磷 | GM | 1 | 0.756 | 0.167 | ||||
| Soil total phosphorus | GI | 1 | 0.554 | 0.734 | ||||
| CK | 1 | 0.674 | -0.269 | |||||
| 土壤水解性氮 | GM | 1 | 0. 082 | |||||
| Hydrolysable nitrogen | GI | 1) | 0. 236 | |||||
| CK | 1 | 0.321 | ||||||
由表 2可以发现,随着小麦生长周期的变化,小麦地上生物量、地下生物量与土壤中的总磷、有效磷呈现负相关性,与水解性氮、总氮呈现显著负相关性(P <0.05)。小麦丛枝菌根真菌侵染率与土壤中的全氮、全磷、具有正相关性,GM侵染率与水解性氮极显著正相关(P <0.05),并且施加菌剂的小麦,与土壤中全氮、全磷、水解性氮的相关性要高于CK处理的小麦。
3 讨论 3.1 AMF对小麦侵染效果施加菌剂的小麦侵染率要显著高于非施加菌剂的小麦(P<0.05),其中GM效果要优于GI。在小麦的全生长周期内,早期侵染效果较高,由于小麦前期生长活力旺盛,强化的AMF菌剂内孢子或孢子果、菌丝、菌根根段等繁殖体远远高于自然生境土壤,而形成强势侵染,从而可能加强植物根系与菌根真菌之间的共生结合,因此小麦侵染率较高[20, 21],最高点出现在120 d,后期略有下降。随着小麦的生长,小麦根系木质化程度加强,不利于AMF侵染,而且根系面积扩大,均可能导致侵染率降低。
3.2 AMF对小麦株高以及生物量的影响以及菌根依赖性接菌处理并没有影响小麦株高以及生物量变化整体规律,但是在其中几个生长阶段会对小麦的株高和生物量有显著提高的效果,说明丛枝菌根真菌具有促进植物生长的作用。通过对整个生长过程的曲线拟合,发现接菌AMF会促使小麦最快生长速率时期的提前,其中地下部分的快速生长期要提前与地上部分,而且小麦根系对AMF的菌根依赖性高与地上部分,说明了AMF通过有效的促进根系发育,进而提高营养吸收范围,以保证植物旺盛生长。同时经过比较发现GM菌剂处理要优于GI菌剂处理。
3.3 AMF对土壤中磷含量影响GM、GI处理后的土壤中总磷含量普遍低于CK处理的土壤,说明丛枝菌根真菌可以促进植物对土壤中磷素的吸收。土壤中有效磷素的含量随时间变化呈现先升后降的总体趋势。处理初期,由于小麦进入分蘖越冬期,磷能使促使小麦的早分蘖早生根增强小麦的抗寒能力[22],因此,在土壤中微生物的活化作用下,致使土壤中有效磷含量的增加[23]。施加菌剂GM、GI后,土壤中有效磷含量高于非施加菌剂(CK)的土壤,其原因是丛枝菌根真菌可以分泌有机酸和磷酸酶使总磷中一部分难溶性磷酸盐活化[13],施加菌剂后,这种活化作用被增强,导致土壤中有效磷含量更高。在小麦生长120 d后,土壤中有效磷含量明显降低,这是由于此时小麦处于拔节期,株高生长速率最大,小麦对土壤中有效磷具有较高的需求量。其中,GM、GI的土壤的有效磷含量低于CK的土壤,说明施加菌剂可以促进植物对土壤中有效磷的利用,这与刘进法[24]等人的研究结果一致。
3.4 AMF对土壤中氮含量的影响氮素是植物生长利用的重要元素,施加菌剂(GM、GI)的总氮含量普遍低于非施加菌剂(CK)的总氮含量,表明从枝菌根真菌会通过根外菌丝[24]促进植物对土壤中氮的吸收。土壤中的水解性氮主要包括无机氮和一部分可溶性有机氮,本实验结果发现GM、GI对可以促进植物对土壤中水解性氮的吸收利用,这一结果与前人的研究结果一致[12]。本实验中以小麦为宿主植物,接菌GM对土壤中氮素的利用明显优于接菌GI的土壤,这一结果与徐亚男[13]对白三叶草的研究结果一致,与李侠[25]对玉米研究结果不同,这要是由于宿主植物与菌根真菌的共生关系存在选择性,不同的宿主植物对不同菌根真菌的依赖性已经侵染率并不相同,且这种差异将直接影响到土壤中元素的活化和转化效率。
3.5 AMF侵染率与土壤营养、小麦生物量的相关性本实验土壤中侵染率与水解性氮之间表现出显著正相关,表明氮素有利于AMF的生长。被侵染的土壤中,可以被植物利用的水解性氮的增多会促进植物根系的发育[26],根系的发育又增强了从枝菌根真菌的侵染效果。小麦生物量与土壤中总氮以及水解性氮含量之间表现出显著负相关,说明氮素对植物的生长起着十分重要的作用。施加菌剂(GM、GI)的小麦生物量与土壤中总氮含量呈现显著负相关变化,但未施加菌剂(CK)的小麦生物量并未与土壤总氮呈现出显著相关性,这主要是由于丛枝菌根真菌加强了对植物对土壤中各类形态氮素的利用[27],进而加强小麦生物量与土壤中总氮的相关性。
4 结论(1)施加AMF菌剂可以显著提高小麦的菌根侵染率。
(2)接种AMF可以有效提高小麦的株高以及生物量。
(3)AMF可以改善小麦根际土壤养分,促进小麦对土壤氮素的吸收利用。
(4)GM接菌处理效果优于GI接菌处理,更为适合作为人工强化菌剂使用。
| [1] | Mohammad A, Mitra B, Khan A G. Effects of sheared-root inoculum of Glomus intraradices onwheat grown at different phosphorus levels in the field. Agriculture, Ecosystems and Environment, 2004, 103(1): 245-249. |
| [2] | Li H, Ye Z H, Chan W F, Chen X W, Wu F Y, Wu S C, Wong M H. Can arbuscular mycorrhizal fungi improve grain yield, as uptake and tolerance of rice grown under aerobic conditions? Environmental Pollution, 2011, 159(10): 2537-2545. |
| [3] | Zhang Y T, Zhu M, Xian Y X W, Shen H, Zhao J, Guo T. Influence of mycorrhizal inoculation on competition between plant species and inorganic phosphate forms. Acta Ecologica Sinica, 2012, 32(22): 7091-7101. |
| [4] | Jones M D, Durall1 D M, Tinker P B. A comparison of arbuscular and ectomycorrhizal Eucalyptus coccifera: growth response, phosphorus uptake efficiency and external hyphal production. New Phytologist, 1998, 140(1): 125-134. |
| [5] | Pairunan A, Robson A D, Abbott L K. The effectiveness of vesicular-arbuscular mycorrhizas in increasing growth and phosphorus uptake of subterranean clover from phosphorus sources of difference solubilities. New Phytologist, 1980, 84: 237-338. |
| [6] | Rai M, Acharya D, Singh A, Varma A. Positive growth responses of the medicinal plants Spilanthes calva and Withania somnifera to inoculation by Piriformospora indicia in a field trial. Mycorrhiza, 2001, 11(3): 123-128. |
| [7] | Gyuricza V, Dupre de Boulois H. Effect of potassium and phosphorus on the transport of radio cesium by arbuscular mycorrhizal fungi. Journal of Environmental Radioactivity, 2010, 101(6): 482-487. |
| [8] | Zakaria S M, Hirata H. Effects of indigenous arbuscular mycorrhizal fungi in paddy fields on rice growth and N, P, K nutrition under different water regimes. Soil Science and Plant Nutrition, 1995, 41(3): 505-514. |
| [9] | Shrestha Y H, Ishii T, Kadoya K. Effect of vesicular-arbuscular mycorrhizal fungi on the growth, photosynthesis, transpiration and the distribution of photosynthates of bearing satsuma mandarin [Citrus reticulate] trees. Journal of Japanese Society of Horticultural Science, 1995, 64(3): 517-525. |
| [10] | Chinnusamy M, Kaushik B D, Prasanna R. Growth nutritional and yield parameters of wetland rice as influenced by microbial consortia under controlled conditions. Journal of Plant Nutrition, 2006, 29(5): 857-871. |
| [11] | Wang L, Jia W Q, Ma F, Li S Y, Zhang S J. Perspective of mycorrhizal technology application for environmental remediation. Ecology and Environmental Sciences, 2010, 19(2): 487-493. |
| [12] | Zhang X, Wang L, Ma F, Zhang S J, Xu Y N, Li Z, Fu S J. Effects of nitrogen and biological fertilizer coupling on rice resource utilization. Journal of Harbin Institute of Technology, 2012, 44(8): 39-42. |
| [13] | Wang L, Xu Y N, Ma F, Zhang S J, Zhang X, Li Z. Effect of different AMF microbial inoculum on the growth of Trifolium repens lawn. Journal of Harbin Institute of Technology, 2012, 44(10): 43-47. |
| [14] | Wu T, Tan Z Y. Vesicular arbuscular Mycorrhiza and its function on Phosphorus in Soil. Hunan Agricultural Sciences, 2005, (2): 41-43. |
| [15] | Liu R J, Chen Y L. Mycorrhizology. Beijing: Science Press, 2007: 79-82. |
| [16] | Nemec S. Response of six citrus rootstocks to three species of Glomus, a mycorrhizal fungus. Proceedings of the Florida State Horticultural Society, 1978, 91: 10-14. |
| [17] | Du S, Gao X Z. Technical specification for soil analysis. Beijing: China Agriculture Press, 2006: 52-58. |
| [18] | Du S, Gao X Z. Technical specification for soil analysis. Beijing: China Agriculture Press, 2006: 42-44. |
| [19] | Bao S D. Analysis of Soil Agrochemical. Beijing: China Agriculture Press, 2005: 147-148. |
| [20] | Ding L, Bai K Z. Effect of atmospheric CO2 increase on root nodules and mycorrhizal activity. Journal of Hubei Institute for Nationalities, 1997, 15(3): 6-9. |
| [21] | Zhang S J, Wang L, Ma F, Li S Y, Zhang X, Wu J T. Application of arbuscular mycorrhiza on promoting the growth of rice and reducing the usage of chemical fertilizer. Journal of Harbin Institute of Technology, 2010, 42(6): 958-962. |
| [22] | Liang Y L, Kang S Z. Effect of irrigating-limited and phosphorus supplied on yield and water use of winter wheat. Journal of Soil Erosion and Soil and Water Conservation, 1997, 3(1): 60-67. |
| [23] | Li X Y, Zhao B Q, Li X H, Li Y T, Sun R L, Zhu L S, Xu J, Wang L X, Li X P, Zhang F D. Effects of different fertilization systems on soil microbe and its relation to soil fertility. Scientia Agriculutra Sinica, 2005, 38(8): 1591-1599. |
| [24] | Liu J, Xia R, Wang M Y, Wang P, Ran Q, Luo Y. Effects of inoculation with arbuscular mycorrhizal fungi on AlPO4 uptake by Poncirus trifoliata. Chinese Journal of Applied Ecology, 2008, 19(10): 2155-2160. |
| [25] | Li X, Zhang J L. Uptake of different forms of nitrogen by hyphae of arbuscular mycorrhizal fungi. Journal of Nuclear Agricultural Sciences, 2007, 21(2): 195-200. |
| [26] | Shi J W, Wang M B, Yu L Z, Zhang Y P, Zhang G M. Effects of soil available nitrogen and related factors on plant fine root. Chinese Journal of Ecology, 2007, 26(10): 1634-1639. |
| [27] | Deng Y, Shen H, Guo T. Review of researches on nitrogen utilized by arbuscular mycorrhizal. Acta Ecologica Sinica, 2009, 29(10): 5627-5635. |
| [3] | 张宇亭, 朱敏, 线岩相洼, 申鸿, 赵建, 郭涛. 接种AM真菌对玉米和油菜种间竞争及土壤无机磷组分的影响. 生态学报, 2012, 32(22): 7091-7101. |
| [11] | 王立, 贾文奇, 马放, 李世阳, 张淑娟. 菌根技术在环境修复领域中的应用及展望. 生态环境学报, 2010, 19(2): 487-493. |
| [12] | 张雪, 王立, 马放, 张淑娟, 徐亚男, 李哲, 傅生杰. 生物肥氮肥耦合对水稻资源利用的影响. 哈尔滨工业大学学报, 2012, 44(8): 39-42. |
| [13] | 王立, 徐亚男, 马放, 张淑娟, 张雪, 李哲. 不同AMF菌剂对白三叶草坪的扶壮作用. 哈尔滨工业大学学报, 2012, 44(10): 43-47. |
| [14] | 吴铁, 覃照宇. VA菌根及其对土壤中磷的作用. 湖南农业科学, 2005, (2): 41-43. |
| [15] | 刘润进, 陈应龙. 菌根学. 北京: 科学出版社, 2007: 79-82. |
| [17] | 杜森, 高祥照. 土壤分析技术规范. 北京: 中国农业出版社, 2006: 52-58. |
| [18] | 杜森, 高祥照. 土壤分析技术规范. 北京: 中国农业出版社, 2006: 42-44. |
| [19] | 鲍士旦. 土壤农化分析. 北京: 中国农业出版社, 2005: 147-148. |
| [20] | 丁莉, 白克智. 大气CO2浓度增加对根瘤和菌根活动的影响. 湖北民族学院学报: 自然科学版, 1997, 15(3): 6-9. |
| [21] | 张淑娟, 王立, 马放, 李世阳, 张雪, 吴洁婷. 丛枝菌根(AM)对水稻生长促进及化肥减量研究. 哈尔滨工业大学学报, 2010, 42(6): 958-962. |
| [22] | 梁银丽, 康绍忠. 限量灌水和磷营养对冬小麦产量及水分利用的影响. 土壤侵蚀与水土保持学报, 1997, 3(1): 60-67. |
| [23] | 李秀英, 赵秉强, 李絮花, 李燕婷, 孙瑞莲, 朱鲁生, 徐晶, 王丽霞, 李小平, 张夫道. 不同施肥制度对土壤微生物的影响及其与土壤肥力的关系. 中国农业科学, 2005, 38(8): 1591-1599. |
| [24] | 刘进法, 夏仁学, 王明元, 王鹏, 冉青青, 罗园. 接种丛枝菌根真菌对枳吸收利用磷酸铝的影响. 应用生态学报, 2008, 19(10): 2155-2160. |
| [25] | 李侠, 张俊伶. 丛枝菌根根外菌丝对不同形态氮素的吸收能力. 核农学报, 2007, 21(2): 195-200. |
| [26] | 史建伟, 王孟本, 于立忠, 张育平, 张国明. 土壤有效氮及其相关因素对植物细根的影响. 生态学杂志, 2007, 26(10): 1634-1639. |
| [27] | 邓胤, 申鸿, 郭涛. 丛枝菌根利用氮素研究进展. 生态学报, 2009,29(10): 5627-5635. |
 2014, Vol. 34
2014, Vol. 34




