文章信息
- 吴芳芳, 郑有飞, 吴荣军, 王锦旗, 李萍
- WU Fangfang, ZHENG Youfei, WU Rongjun, WANG Jinqi, LI Ping
- 麦田根际土壤反硝化作用对O3熏气和太阳辐射减弱的响应
- Soil denitrification responses of wheat rhizosphere against ozone fumigation and reduction of solar irradiance
- 生态学报, 2013, 34(20): 5840-5848
- Acta Ecologica Sinica, 2013, 34(20): 5840-5848
- http://dx.doi.org/10.5846/stxb201301240152
-
文章历史
- 收稿日期:2013-1-24
- 网络收稿日期:2014-3-11
近地层臭氧是非常重要的污染气体,是控制低层大气化学反应与循环的重要因子,占总氧化剂的90%以上[1]。地球对流层大气平均O3浓度已经从工业革命前的38 nL/L上升到目前的50 nL/L,这个浓度已经超过了敏感作物O3伤害阀值AOT40的25%[2],在过去的30a中,北半球O3浓度以每年0.5%—2%的速度递增[3],估计到2100年O3浓度将在现有基础上增加40%—60%[4]。工业化革命以来,人类活动造成的空气污染除了近地层臭氧浓度增加以外,其它大量有害粒子,比如SO2、NOx、黑碳、飞灰、土壤尘粒子等,引起大气气溶胶光学厚度逐年增加。IPCC第四次评估报告(AR4)指出,在含有大量气溶胶粒子的区域,抑制了较大尺度云滴和雨滴的形成,云量增多,云的反照率加强,导致地面变暗变冷[4]。2008年联合国环境规划署(UNEP)发布了亚洲大气棕色云的研究报告,在中国和印度仅亚洲大气棕色云的直接辐射强迫引起的年均地表变暗就达14—16 W/m2(大约6%)[5]。近地层大气太阳辐射减弱和O3浓度增加,目前已经成为全球科学家和公众密切关注的重要环境问题。 太阳辐射不仅密切地影响着地面O3浓度的变化,同时通过改变光合有效辐射(PAR),严重影响农业生产[6, 7, 8, 9]。土壤环境是农业生产的根本,其对大气环境变化的响应以根际微生物最为活跃[10, 11],由微生物介导的土壤氮素的转化作用受大气环境的扰动,土壤中矿质态氮含量、微生物区系、含氮气体排放量是受臭氧影响的首要因子[12, 13, 14]。土壤氮素在微生物驱动下的反硝化作用,能增加土壤N2O的排放,降低土壤氮肥的生物有效性,土壤反硝化作用及N2O排放的动态和定量研究日益受到重视[12, 15, 16]。研究近地层臭氧浓度增加和太阳辐射减弱对土壤氮素反硝化作用的影响,在维护农业生态平衡和保护环境等方面具有非常重要的意义。本文模拟O3浓度增加和太阳辐射减弱,4a定点试验,研究麦田根际土壤反硝细菌和反硝化强度与O3浓度增加以及太阳辐射减弱的相互关系。
1 材料与方法 1.1 大田试验概况于2008年至2011年在南京信息工程大学农业气象试验站(32.16°N,118.86°E)进行冬小麦生长季田间观测试验。当地多年平均温度为15.6 ℃,多年平均降水为每年1 100 mm。供试土壤为潴育型水稻土(灰马肝土属),土壤质地为壤质黏土,耕层土壤黏粒含量为26.1%,土壤pH(H2O) 值为6.2,有机碳和全氮的含量分别为19.4 g/kg、1.15 g/kg。
1.2 O3浓度增加试验设计试验采用直径3 m,高2.5 m 的开顶箱(OTC)作为臭氧布气的容纳装置,设置CK(正常空气)﹑T1(100 nL/L臭氧)、T2 (150 nL/L臭氧)共3个臭氧浓度处理,每一处理3个重复。通过气泵对臭氧发生器产生的臭氧进行预先稀释,之后吹入OTC 内的布气装置,最终使OTC内均匀布满气体,OTC内设置臭氧浓度传感器(精度可达1 nL/L),对臭氧浓度传感器进行预先设定浓度阈值,当OTC 内臭氧浓度未达到此阈值时,臭氧发生器持续工作并向OTC 内通入臭氧气体,当OTC 内浓度超过此阈值时,臭氧传感器则提示报警,其信号通过微型电子控制仪的指令控制与臭氧发生器相连的电磁阀断开,此时臭氧发生器停止工作. 这样可实现OTC 内臭氧浓度的自动调控. 每天臭氧处理时间段为08:00—16:00,遇有雨天则关闭整个装置。
1.3 辐射减弱试验设计通过在自然条件下搭建不同透光度(网孔密度不同)的黑色聚乙烯遮荫网实现。遮荫棚采用镀锌钢管为主要支柱,搭建成3 m×3 m×3 m的立方体,两两间隔3 m。遮荫棚顶部用铁丝搭建为可上下调节的网状结构,用以支撑遮荫网,采用TBQ-2型总辐射表对不同处理下达到冬小麦冠层的太阳总辐射强度进行了监测,监测时间为6:00—18:00,步长为1 min,每日实际监测到的太阳总辐射强度瞬 时值见图 1。通过计算确定各处理组实际接收的太阳辐射强度分别比对照减弱(20±5)% (S1)、(40±5)% (S2)、(60±5)% (S3),对照Field为完全自然环境,不增加OTC气室,不进行O3曝气和遮光处理,田间大气O3浓度和太阳辐射强度没有人为干扰。并随着作物生长高度,调节遮荫网与冬小麦冠层间的距离,根据情况适当更换遮荫网,保证网下空气流通,使到达植物冠层的太阳总辐射变化量控制在预设值±5%范围内。
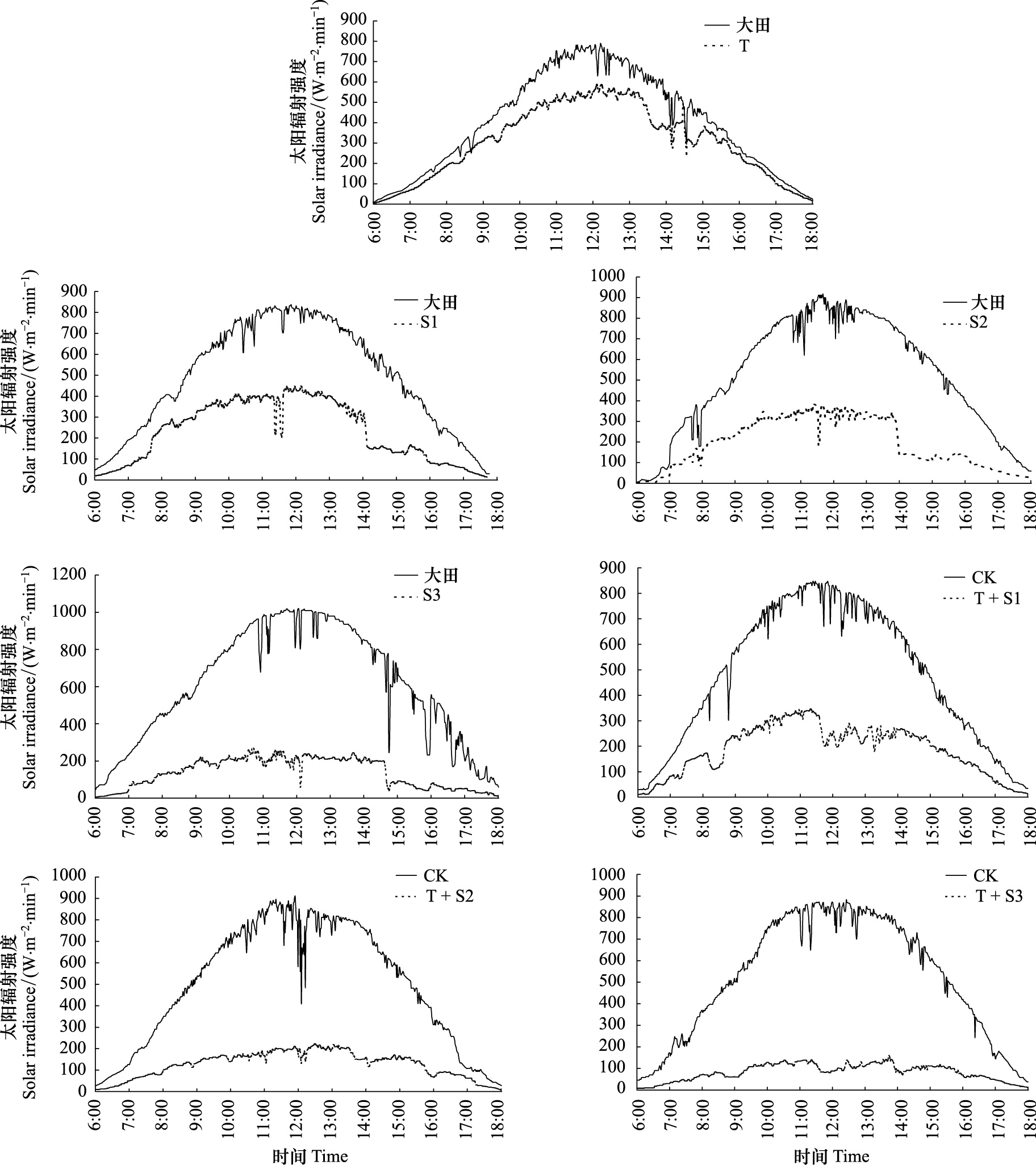
|
| 图 1 不同处理下冬小麦冠层太阳辐射强度 Fig. 1 Solar irradiance of winter wheat canopy under different treatments S1: 太阳辐射强度比对照减弱(20±5)%; S2:(40±5)%; S3:(60±5)%; T+S1: O3(浓度为)(100±8)nL/L+太阳辐射强度减弱20% |
通过在OTC上方搭建各透光度的黑色遮荫网实现,试验设置3个处理组:T+S1(O3浓度为(100±8) nL/L+太阳辐射强度减弱20%),T+S2(O3浓度为(100±8) nL/L +太阳辐射强度减弱40%),T+S3(O3浓度为(100±8) nL/L +太阳辐射强度减弱60%),以不通入O3不加遮荫网的OTC棚为对照。
1.5 田间管理和取样供试小麦品种为扬麦16号,水肥供应适量而充分,其他农田管理措施均相同,无病虫害及杂草的影响。播种日期、熏气起止日期、采样日期以及AOT40累积量如表 1所示。按五点取样法,定点分别选取5株小麦,将其0—20 cm耕层根系区土样挖出,抖掉根系外围土,取紧贴在根表附近的土样,混合后作为根际土,用四分法取适量装于无菌纸袋中,立即带回实验室,一部分土样用于土壤反硝化细菌数量的计数,另一部分土样经自然风干后,过1 mm孔径分样筛,4 ℃下冰箱保存。
| 试验年份 Test date | 播种日期(年-月-日) Sowing date (year-month-day) | 开始熏气日期 (年-月-日) Start fume date(year-month-day) | 停止熏气日期(月-日) Stop fumeing date (month-day) | 日小时O3 浓度大于4 0 nL/L(AOT40) | 取样时期Sampling period | |||||||
| 3—5月AOT40累积量/(nL L-1 h-1)cumulant | 累积天数cumulant day | 占试验期比例/%Percentage of trial period | 返青期(月-日) Reviving (month-day) | 拔节期(月-日) Jointing (month-day) | 孕穗期(月-日) booting(month-day) | 抽穗期(月-日) Heading (month-day) | 灌浆期(月-日) Filing(month-day) | 成熟期(月-日) Mature(month-day) | ||||
| 2008 | 2007-11-14 | 2008-03-07 | 05-20 | 8.208 | 63 | 68.48% | 03-10 | 03-24 | 04-02 | 04-17 | 04-29 | 05-8 |
| 2009 | 2008-11-20 | 2009-03-08 | 05-21 | 8.462 | 59 | 64.13% | 03-04 | 04-02 | 04-17 | 04-23 | 05-07 | 05-15 |
| 2010 | 2009-11-12 | 2010-03-07 | 05-26 | 8.638 | 62 | 67.39% | 03-19 | 04-01 | 04-14 | 04-26 | 05-06 | 05-20 |
| 2011 | 2010-11-12 | 2011-03-07 | 05-27 | 8.357 | 58 | 63.04% | 03-24 | 04-02 | 04-12 | 04-22 | 05-02 | 05-12 |
根据文献[17]分别制备反硝化细菌液体富集培养基与固体分离培养基。采用MPN(最大或然数) 法测定。接种土壤悬液于液体富集试管,各浓度梯度设置4个重复,在30 ℃恒温培养14 d,根据阳性管数查表得数量近似值,并经水分测定换算成1 g干土中反硝化细菌的数量。
1.7 土壤反硝化作用强度的测定以氧化亚氮计测定土壤反硝化强度,称取过1 mm筛的新鲜土样10 g于250 mL培养瓶中,向其中加入含硝酸钾和葡萄糖的混合溶液5 mL(含N 和C各3 mg),并用丁基橡胶塞将培养瓶密封,利用真空泵抽真空,然后再向培养瓶中充入体积分数为10% 的乙炔来抑制氧化亚氮转化为氮气,在28 ℃下培养48 h,培养结束后从培养瓶中抽取气体10 mL,装入气袋,室温下利用气相色谱进行分析。
1.8 数据统计分析采用DPS(Data processing system)[18]数据处理系统软件处理数据,进行相关分析。
2 结果与分析 2.1 臭氧浓度升高对反硝化细菌数量的影响4年间,对照组的反硝化细菌数量随小麦生长而变化的时序特征为拔节期、孕穗期、抽穗期和灌浆期没有显著差异,成熟期则增加了两个数量级;O3浓度增加处理组与对照组的时序变化规律相同,不同的是成熟期反硝化细菌数量增加了3个数量级。在试验生育期内,只有成熟期T1、T2与对照差异显著,且T1与T2之间没有显著差异,其它时期T1、T2与对照没有明显不同。如表 2所示。结果说明,小麦生长的前、中期,土壤反硝化细菌数量受小麦的生长调节不大,对O3浓度升高引起的环境变化因子不敏感,成熟期后,土壤反硝化细菌数量增加,O3在成熟期对土壤反硝化细菌的生长繁殖有明显的促进作用。
| 年份Year | 反硝化细菌数量 denitrifying bacteri (lg(n/g)) | |||||
| 拔节期 Reviving stage | 孕穗期 Jointing stage | 抽穗期 Booting stage | 灌浆期 Filing stage | 成熟期 Maturing stage | ||
| T1: 100 nL/L臭氧; T2: 150 nL/L臭氧; 相同生育期内不同字母表示处理间经Duncan氏多重极差检验差异显著(P<0.05) | ||||||
| 2008 | CK | 5.24±0.67 a | 5.30±0.35 a | 5.62±0.29a | 5.95±0.34 a | 7.54±0.76 a |
| T1 | 5.73±0.56 a | 5.50±0.5 a | 5.35±0.36 a | 5.63±0.43 a | 8.74±0.46 b | |
| T2 | 5.44±0.20 a | 5.06±0.41 a | 5.37±0.72 a | 5.55±0.52 a | 8.48±0.43 b | |
| 2009 | CK | 5.44±0.25 a | 5.35±0.23 a | 5.60±0.54 a | 5.36±0.50 a | 7.35±0.32 a |
| T1 | 5.67±0.35 a | 5.21±0.46a | 5.45±0.46a | 5.30±0.43 a | 8.83±0.36b | |
| T2 | 5.43±0.30 a | 5.18±0.57 a | 5.43±0.53 a | 5.16±0.37 a | 8.75±0.47 b | |
| 2010 | CK | 5.53±0.45 a | 5.46±0.27 a | 5.79±0.62 a | 5.74±0.42 a | 7.66±0.22 a |
| T1 | 5.35±0.53 a | 5.38±0.37 a | 5.66±0.75 a | 5.82±0.13 a | 8.48±0.26 b | |
| T2 | 5.47±0.38 a | 5.22±0.84 a | 5.47±0.43 a | 5.58±0.27 a | 8.58±0.62 b | |
| 2011 | CK | 5.44±0.30 a | 5.60±0.37 a | 5.62±0.67 a | 5.38±0.25 a | 7.74±0.36 a |
| T1 | 5.48±0.77 a | 5.32±0.44 a | 5.41±0.33 a | 5.51±0.29 a | 8.89±0.45b | |
| T2 | 5.45±0.67a | 5.12±0.43 a | 5.49±0.57 a | 5.78±0.34 a | 8.72±0.49 b | |
土壤反硝化作用强度随小麦生育进程的推进而变化,对照组呈现先降低后升高的趋势,抽穗期降到最低值,成熟期升到最高值,4a试验期间变化规律一致(表 3)。第1年(2008)和第2年(2009)试验,T1、T2与对照呈现相同的变化规律,即先降低后升高的趋势;第3年(2010)和第4年(2011)试验,T1和T2则表现为从拔节期到灌浆期无显著变化,成熟期迅速显著升高。在相同生育期内,第1年和第2年试验中,T1和T2与CK均没有显著差异;第3年和第4年试验中,T1和T2在孕穗期和抽穗期的反硝化强度比对照显著升高,另外T2在第四年的成熟期也显著促进了反硝化作用。反硝化作用是土壤中氮素转化的最主要过程之一,植物通过吸收同化NO-3而抑制反硝化作用[19],在孕穗期和抽穗期小麦由营养生长转入生殖生长,需吸取大量的NO-3,由于土壤反硝化作用受到NO-3限制,所以孕穗期和抽穗期反硝化 作用降低,在成熟期小麦减小了对NO-3的吸收,土壤NO-3供应充足,小麦根际分泌物的存在促进了反硝化作用,所以成熟期反硝化作用强度升高。O3对反硝化作用的影响具有一定的积累效应,O3剂量和作用时间的累积量达到一定阈值,在小麦生长需N敏感期,由于O3长时间的作用,土壤理化性质改变,小麦的生长受严重抑制[20],O3显著增加土壤反硝化强度。反硝化过程是N2O产生的主要生物过程,在一定的小麦生长期还会导致麦田土壤N2O排放的增加。
| 年份Year | 反硝化作用强度Intensity of denitrification/(μg g-1 d-1) | |||||
| 拔节期 Reviving stage | 孕穗期 Jointing stage | 抽穗期 Booting stage | 灌浆期filing stage | 成熟期 Maturing stage | ||
| 相同生育期内不同字母表示处理间经Duncan氏多重极差检验差异显著(P<0.05) | ||||||
| 2008 | CK | 20.04±0.37a | 19.34±0.23a | 16.65±0.09a | 22.05±0.63a | 26.54±0.76a |
| T1 | 21.72±0.41a | 20.32±0.32a | 17.45±0.36a | 23.13±0.33a | 26.74±0.36a | |
| T2 | 21.74±0.24a | 21.63±0.13a | 17.07±0.77a | 22.45±0.09a | 26.88±0.18a | |
| 2009 | CK | 22.41±0.15a | 20.37±0.23a | 16.70±0.29a | 22.34±0.20a | 27.34±0.09a |
| T1 | 23.60±0.55a | 21.21±0.56a | 17.85±0.44a | 23.70±0.43a | 28.82±0.52a | |
| T2 | 23.43±0.80a | 20.78±0.27a | 17.49±0.54a | 23.48±0.82a | 28.77±0.23a | |
| 2010 | CK | 23.53±0.45a | 21.46±0.27a | 18.79±0.62a | 23.74±0.52a | 27.66±0.28a |
| T1 | 25.35±0.53a | 26.18±0.37b | 25.66±0.85b | 25.02±0.19a | 30.48±0.57a | |
| T2 | 25.47±0.38a | 26.22±0.84b | 25.47±0.44b | 26.28±0.25a | 32.58±0.42a | |
| 2011 | CK | 22.44±0.30a | 20.60±0.37a | 17.62±0.64a | 23.38±0.27a | 27.74±0.37a |
| T1 | 25.48±0.77a | 25.02±0.44b | 25.41±0.38b | 24.71±0.69a | 31.89±0.35ab | |
| T2 | 26.45±0.67a | 25.72±0.43b | 25.49±0.54b | 25.78±0.14a | 33.72±0.45b | |
从拔节期至灌浆期,相同处理组反硝化细菌数量在相同数量级,成熟期则至少增加两个数量级,反硝化菌数量急剧增加。成熟期小麦根系呼吸会消耗O2,根际有机物的微生物降解也是消耗O2,成熟期土壤处于低氧微区,而且根分泌物及残屑等有机物质的分解使供碳充足,这样成熟期小麦促进了反硝化细菌数量增加。太阳辐射减弱在所有生育期中均显著增加了反硝化菌数量,成熟期增加的幅度更大,如表 4所示。因为成熟期土壤NO-2、C、O2等含量的变化更有利于反硝化菌的生长繁殖。反硝化细菌将NO-3还原为NO-2再还原为N2O,而能够还原N2O的微生物数量相对较少,因而在反硝化过程中常有N2O的释放。反硝化菌作为根际微生物群体的一部分,其活性受到小麦植株的影响,同时植物根分泌物及残屑是反硝化细菌的主要碳源供给者,一方面植物通过吸收同化NO-3而抑制反硝化作用,另一方面植物提供根分泌物及残屑等有机物质,经矿化和硝化作用而供给NO-3来促进反硝化作用。
| 年份Year | 反硝化细菌数量Number of denitrifying bacteria/(lg(n/g) | |||||
| 拔节期 Reviving stage | 孕穗期 Jointing stage | 抽穗期 Booting stage | 灌浆期filing stage | 成熟期 Maturing stage | ||
| 相同生育期内不同字母表示处理间经Duncan氏多重极差检验差异显著(P<0.05); S1: 太阳辐射强度比对照减弱(20±5)%; S2:(40±5)%; S3:(60±5)%; | ||||||
| 2010 | CK | 5.53±0.45 a | 5.46±0.27 a | 5.79±0.62 a | 5.74±0.42 a | 7.66±0.22 a |
| S1 | 7.57±1.17b | 7.73±1.26b | 7.27±1.13ab | 7.47±0.56b | 9.9±0.76b | |
| S2 | 7.37±1.21b | 7.67±1.46b | 7.84±1.00b | 7.96±0.86b | 10.76±0.65b | |
| S3 | 8.89±1.01b | 8.42±1.23b | 8.97±0.96b | 8.64±0.64c | 12.72±0.62c | |
| 2011 | CK | 5.44±0.30 a | 5.60±0.37 a | 5.62±0.67 a | 5.38±0.25 a | 7.74±0.36 a |
| S1 | 7.09±1.34ab | 7.84±1.06b | 7.37±0.86b | 7.63±0.63b | 9.63±0.56b | |
| S2 | 7.55±1.22b | 7.86±0.96b | 7.94±0.66b | 7.64±0.66b | 11.17±1.03bc | |
| S3 | 9.06±1.16b | 9.77±104b | 9.07±0.77b | 9.78±1.33b | 12.98±0.60c | |
土壤反硝化强度,对照组在抽穗期最低,因为此时植物高效率吸收同化NO-3,抑制了反硝化作用;太阳辐射减弱处理组,随小麦生育期的推进有逐渐增加的趋势,成熟期达最大。如表 5所示。土壤生物反硝化过程是N2O的主要来源,是土壤中氮素转化的最主要过程之一。一方面植物通过吸收同化NO-3而抑制反硝化作用,另一方面植物提供根分泌物及残屑等有机物质,经矿化和硝化作用而供给NO-3来促进反硝化作用。在孕穗期、抽穗期由于根系与微生物竞争NO-3 土壤反硝化作用减弱,灌浆、成熟期小麦吸氮量减少,对反硝化功能有促进作用。太阳辐射减弱对反硝化作用强度的促进作用从孕穗期开始呈显著水平。太阳辐射减弱后麦田光合有效辐射降低,小麦光合积累减少,吸收同化NO-3的能力减弱,反硝化作用增加。
| 年份Year | 反硝化细菌数量Number of denitrifying bacteria/(lg(n/g) | |||||
| 拔节期 Reviving stage | 孕穗期 Jointing stage | 抽穗期 Booting stage | 灌浆期filing stage | 成熟期 Maturing stage | ||
| 2010 | CK | 23.53±0.45 a | 21.46±0.27 a | 18.79±0.62 a | 23.74±0.52 a | 27.66±0.28 a |
| S1 | 24.73±0.67a | 25.63±0.63 b | 26.47±0.57b | 27.37±0.73b | 29.84±0.67b | |
| S2 | 25.36±0.63a | 26.28±0.66b | 26.82±0.85b | 28.84±0.79 b | 29.73±0.48b | |
| S3 | 25.55±0.74a | 27.35±0.83 b | 28.64±0.46b | 28.72±0.93 b | 30.64±0.73 b | |
| 2011 | CK | 22.44±0.30 a | 20.60±0.37 a | 17.62±0.64 a | 23.38±0.27 a | 27.74±0.37 a |
| S1 | 23.32±0.83a | 24.12±0.69 b | 25.36±0.38b | 27.02±0.61b | 31.38±0.68b | |
| S2 | 24.83±0.57a | 25.02±0.58 b | 28.22±0.83c | 29.78±0.65c | 32.43±0.62b | |
| S3 | 24.98±0.74a | 25.99±0.63 b | 30.38±0.82c | 30.11±0.77c | 32.94±0.34 b | |
反硝化菌数量随小麦生长发育而发生的时序波动不大,在灌浆期之前,相同的处理组反硝化菌数量均在相同的数量级,而成熟期比之前的生育期增加了2—3个数量级。这说明植物通过吸收同化NO-3而对反硝化作用的抑制程度约等于植物提供根分泌物及残屑等有机物质,经矿化和硝化作用而供给NO-3对反硝化作用的促进程度。成熟期反硝化菌急剧增加,因为成熟期小麦生长量很小,根系与微生物竞争NO-3的能力减弱,当NO-3供应有富余时,植物向根际提供了有机碳源以及根系呼吸耗O2,因而促进反硝化作用。从表 6可看出,增加O3浓度仅在成熟期促进反硝化细菌的增长,其余时期效果不显著;辐射减弱的处理组以及减弱辐射与增加O3复合作用的处理组,在每个试验生育期均显著增加了反硝化菌数量,它们作用的效应依次为:(T1+S3) >(T1+S2) >(T1+S1)>S1>CK。这也说明O3与太阳辐射减弱对反硝化菌生长繁殖的促进作用具有协同效应。
| 年份Year | 反硝化细菌数量Number of denitrifying bacteria/(lg(n/g) | |||||
| 拔节期 Reviving stage | 孕穗期 Jointing stage | 抽穗期 Booting stage | 灌浆期filing stage | 成熟期 Maturing stage | ||
| 2010 | CK | 5.53±0.45 a | 5.46±0.27a | 5.79±0.62 a | 5.74±0.42 a | 7.66±0.22 a |
| T1 | 5.35±0.53 a | 5.38±0.37 a | 5.66±0.75 a | 5.82±0.13 a | 8.48±0.26 b | |
| S1 | 7.57±1.17b | 7.73±1.26b | 7.27±1.13ab | 7.47±0.56b | 9.9±0.76c | |
| T1+S1 | 7.85±0.85b | 7.89±1.03b | 7.64±0.66b | 7.82±0.66bc | 10.41±0.95c | |
| T1+S2 | 8.86±0.75b | 8.58±1.11bc | 8.53±0.76bc | 8.82±0.73bc | 11.61±0.56cd | |
| T1+S3 | 9.16±0.75b | 9.37±1.22c | 9.32±0.89c | 9.21±0.56c | 12.43±0.56d | |
| 2011 | CK | 5.44±0.30 a | 5.60±0.37 a | 5.62±0.67 a | 5.38±0.25 a | 7.74±0.36 a |
| T1 | 5.48±0.77 a | 5.32±0.44 a | 5.41±0.33 a | 5.51±0.29 a | 8.89±0.45b | |
| S1 | 7.09±1.34ab | 7.84±1.06b | 7.37±0.86b | 7.63±0.63b | 9.63±0.56bc | |
| T1+S1 | 7.43±0.75ab | 7.58±0.93b | 7.78±0.72b | 7.95±0.66b | 10.73±0.66c | |
| T1+S2 | 8.37±0.75b | 8.73±0.67bc | 8.53±0.98b | 8.74±0.48c | 11.22±0.88cd | |
| T1+S3 | 9.26±0.75b | 9.68±0.64c | 9.24±1.06b | 9.45±0.85c | 12.46±0.94d | |
O3浓度增加与太阳辐射减弱复合作用下土壤反硝化强度增强,增强效应显著大于他们的各自的单独作用。O3浓度增加或太阳辐射减弱及它们的复合处理,土壤反硝化强度随小麦的生长发育逐渐升高,改变了对照在孕穗期和抽穗期反硝化强度降低的时序变化特征 (表 7)。对照在生长过程中植株的代谢对反硝化强度的调节占较大比重,孕穗期和抽穗期小麦吸N能力强,硝化活性高抑制了反硝化过程,而当地表O3浓度增加和太阳辐射减少时,小麦植株生长量减小,植株的代谢对反硝化强度的调节较弱,而O3导致土壤氧压变小,辐射减弱后有利于小麦对O3的吸收等因素促进了反硝化过程。农业生产中应加强小麦生长后期土壤环境管理减少土壤N素损失,减少农田N2O排放。
| 年份Year | 反硝化细菌数量Number of denitrifying bacteria/(lg(n/g) | |||||
| 拔节期 Reviving stage | 孕穗期 Jointing stage | 抽穗期 Booting stage | 灌浆期filing stage | 成熟期 Maturing stage | ||
| 2010 | CK | 23.53±0.45 a | 21.46±0.27 a | 18.79±0.62 a | 23.74±0.52 a | 27.66±0.28a |
| T1 | 25.35±0.53 b | 26.18±0.37 b | 25.66±0.85b | 25.02±0.19 b | 30.48±0.57b | |
| S1 | 24.73±0.67a | 25.63±0.63 b | 26.47±0.57b | 27.37±0.73c | 29.84±0.67b | |
| T1+S1 | 27.37±0.59c | 28.48±0.54c | 29.47±0.44c | 30.63±0.79d | 32.75±0.62c | |
| T1+S2 | 28.42±0.63c | 28.97±0.37c | 30.27±0.73c | 31.37±0.85d | 33.27±0.67c | |
| T1+S3 | 27.98±0.62c | 29.46±0.63c | 30.86±0.62c | 31.86±0.69d | 34.51±0.76c | |
| 2011 | CK | 22.44±0.30 a | 20.60±0.37 a | 17.62±0.64 a | 23.38±0.27 a | 27.74±0.37a |
| T1 | 25.48±0.77 b | 25.02±0.44b | 25.41±0.38b | 24.71±0.69 a | 31.89±0.35b | |
| S1 | 23.32±0.83a | 24.12±0.69 b | 25.36±0.38b | 27.02±0.61b | 31.38±0.68b | |
| T1+S1 | 26.76±0.49bc | 28.47±0.63c | 30.27±0.59c | 32.38±0.54c | 33.79±0.89c | |
| T1+S2 | 27.86±0.61c | 29.71±0.59c | 31.11±0.79c | 33.27±0.63c | 35.02±0.79c | |
| T1+S3 | 29.03±0.56c | 30.16±0.66c | 31.78±0.87c | 33.89±0.69c | 35.26±0.99c | |
土壤生物反硝化是土壤中氮素转化最重要的过程之一。N2O是反硝化作用的主要产物,反硝化速率和反硝化菌的数量是N2O释放量的决定因素[19]。降低土壤含水量或消耗NO-3则抑制反硝化过程,而根分泌物和残屑为反硝化菌提供有机碳并在降解过程中降低O2分压则促进反硝化作用。反硝化细菌作为根际微生物群体的一部分,其活性受到植物的显著影响,当土壤反硝化作用主要受到NO-3限制时,那么由于根系与微生物竞争NO-3,就会减弱反硝化作用,当 NO-3供应有富余时,植物的存在,向根际提供了有机碳源以及根系呼吸耗O2,因而促进反硝化作用。在小麦成熟期地上部分收割后,土壤N2O释放量增加特别显著,这是由于植物受伤后根系有效碳的释放造成的。植物根际在对反硝化作用产生影响的同时,对土壤N2O释放也起了重要的通道作用。近地层臭氧浓度日益升高,太阳辐射日趋减弱,O3引起的植物叶面伤害以及有效光合辐射减少引起光合积累的降低,已引起植物生物量和根系分泌物的变化[21],并将通过植物的介导影响土壤生态系统氮素循环过程以及相关功能微生物的活性[22]。研究发现,当受到环境胁迫时,作物会做出必要的生理调节,即通过吸收更多的营养来弥补外界胁迫对其自身的损伤[23],经过几个小麦生长季O3的累积作用,以及辐射减弱条件下,成熟期反硝化细菌数量和反硝化强度增强,影响土壤氮库的调节,影响土壤氮营养的供给和N2O的排放。
4 结论(1) O3对土壤反硝化细菌数量仅在小麦成熟期有明显促进作用,在较短时间里O3对土壤反硝化强度没有显著影响,而O3连续作用3个生长季后,土壤反硝化强度显著升高,特别是小麦生长旺盛、吸氮高峰期,反硝化强度增强辐度最大。长时间的O3胁迫条件下,O3对反硝化作用强度的影响超过了小麦生长活性对反硝化作用强度的调节,O3成为影响反硝化强度的主要因素。
(2)太阳辐射减弱在小麦各生育期促进反硝化细菌数量增加和反硝化强度增强,反硝化菌数量在成熟期有最显著响应,而反硝化强度则在小麦吸氮旺盛的孕穗期、抽穗期受太阳辐射减弱的促进效应最明显。反硝化菌增多和反硝化强度增加,则温室气体N2O排放的风险增加。
(3) O3浓度增加与太阳辐射减弱两因素复合作用对反硝化菌数量和反硝化强度的影响存在协作关系,减弱的太阳辐射与增加的O3复合作用,比较它们各自的单独作用,显著增加了小麦各生育期反硝化菌数量和反硝化强度。太阳辐射减弱小麦叶片的水汽压差变化,小麦气孔张开,有利O3的吸收,增加了O3伤害。O3浓度增加则土壤中O2分量减少促进了反硝化过程,加剧了土壤氮素营养的损失和温室气体N2O的排放。
| [1] | Tausz M, Grulke N E, Wieser G. Defense and avoidance of ozone under global change. Environmental Pollution, 2007, 147(3): 525-531. |
| [2] | Fuhrer J, Skärby L, Ashmore M. Critical levels for ozone effects on vegetation in Europe. Environmental Pollution, 1997, 97(1/2): 91-106. |
| [3] | Vingarzan R. A review of surface ozone background levels and treads. Atmospheric Environment, 2004, 38(21): 3441-3442. |
| [4] | Forster P, Ramaswamy V, Artaxo P, Berntsen T, Betts R, Fahey D W, Haywood J, Lean J, Lowe D C, Myhre G J, Nganga J, Prinn R, Raga G, Schulz M, Dorland R V. Changes in atmospheric constituents and in radiative forcing//Solomon S, Qin D, Manning M, Chen Z, Marquis M, Averyt K B, Tignor M, Miller H L, eds. Climate Change 2007: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge, United Kingdom and New York: Cambridge University Press, 2007. |
| [5] | Satheesh S K, Ramanathan V. Large differences in tropical aerosol forcing at the top of the atmosphere and earth's surface. Nature, 2000, 405(6782): 60-63. |
| [6] | Abraha M G Savage M J. Comparison of estimates of daily solar radiation from air temperature range for application in crop simulations. Agricultural and Forest Meteorology, 2008, 148(3): 401-416. |
| [7] | Greenwald R, Bergin M H, Jin X, Cohan D, Hoogenboom G, Chameidesc W L. The influence of aerosols on crop production: A study using the CERES crop model. Agricultural Systems, 2006, 89(2/3): 390-X113. |
| [8] | Zhai W. The Impacts of Radiative Effects of Atmospheric Aerosol on Primary Crops' Growth in the Yangtze Delta Region. Beijing: Chinese Academy of Meteorological Sciences, 2007. |
| [9] | Cai R G, Wang Z L, Zhang M, Wang X Y, Zhagn X Y, Zhou Y F, Wang W B, Li Y S. Effect of shading from flag leaf stage to anthesis on dry matter accumulation in strong-gluten wheat. Journal of Hebei Normal University of Science & Technology, 2009, 23(1): 12-16. |
| [10] | Zhang F S. Plant Nutrition Ecophysiology and Genetics. Beijing: Chinese Science and Technology Press, 1993. |
| [11] | Hu J L, Lin X G, Wang J H, Cui X C, Wu S, Zhang J, Zhu J G. Arbuscular mycorrhizal fungal effects on wheat growth in response to elevated tropospheric O3 concentration. Environmental Science, 2009, 30(11): 3393-3398. |
| [12] | Kanerva T, Palojarvi A, Rämö K, Ojanperä K, Esala M, Manninen S. A 3-year exposure to CO2 and O3 induced minor changes in soil N cycling in a meadow ecosystem. Plant and Soil, 2006, 286(1/2): 61-73. |
| [13] | Yoshida L C, Gamon J A Andersen C P. Differences in above-and below-ground responses to ozone between two populations of a perennial grass. Plant and Soil, 2001, 23, 3(2): 203-211. |
| [14] | Phillips R L, Zak D R, Holmes W E, White D C. Microbial community composition and function beneath temperate trees exposed to elevated atmospheric CO2 and O3. Oecologia, 2002, 131(2): 236-244. |
| [15] | Marinov D, Querner E, Roelsma J. Simulation of water flow and nitrogen transport for a Bulgarian experimental plot using SWAP and ANIMO models. Journal of Contaminant Hydrology, 2005, 77(3): 145-164. |
| [16] | Sun R L, Zhao B Q, Zhu L S, Xu J, Zhang F D. Effects of long-term fertilization on soil enzyme activities and its role in adjusting-controlling soil fertility. Plant Nutrition and Fertilizer Science, 2003, 9(4): 406-410. |
| [17] | Xu G H, Zhang H Y. Soil Microbial Analysis Method Manual. Beijing: China Agriculture Press, 1986. |
| [18] | Tang Q Y, Feng M G. DPS Data Processing System for Practical Statistics. Beijing: Science Press, 2002. |
| [19] | Zou G Y, Zhang F S. Denitrification in rhizosphere and N2O emission. Journal of China Agricultural University, 2002, 7(1): 77-82. |
| [20] | Huang H. Experimental Study on the Impacts of Increasing O3 and CO2 Concentrations on Crops[D]. Beijing: Chinese Academy of Meteorological Sciences, 2003. |
| [21] | Chen Z, Wang X K, Feng Z Z, Zheng Q W, Ouyan Z Y. Effects of elevated ambient ozone on ecosystem below-ground processes. Chinese Journal of Ecology, 2007, 26(1): 121-125. |
| [22] | Chen Z, Wang X K, Feng Z Z, Xiao Q, Duan X N. Impact of elevated O3 on soil microbial community function under wheat crop. Water, Air, & Soil Pollution, 2009, 198(1/4): 189-198. |
| [23] | Li Q S, Lin X G, Hu J L, Yu Y C, Shen B, Zhu J G. Effects of elevated O3 concentration in surface layer on activity of soil ammonia-oxidizing bacteria and denitrifying bacteria in wheat field. Journal of Ecology and Rural Environment, 2010, 26(6): 524-528. |
| [8] | 翟薇. 大气气溶胶辐射效应对长江三角洲地区主要作物生产的影响 [D]. 北京: 中国气象科学研究院, 2007. |
| [9] | 蔡瑞国, 王振林, 张敏, 王晓英, 张体彬, 周印富, 王文颇, 李彦生. 挑旗-开花期遮光对强筋小麦干物质积累的影响. 河北科技师范学院学报, 2009, 23(1): 12-16. |
| [10] | 张福锁. 植物营养生态生理学和遗传学. 北京: 中国科学技术出版社, 1993. |
| [11] | 胡君利, 林先贵, 王俊华, 崔向超, 武术, 张晶, 朱建国. 大气对流层臭氧浓度升高下AM真菌对小麦生长的影响. 环境科学, 2009, 30(11): 3393-3398. |
| [16] | 孙瑞莲, 赵秉强, 朱鲁生, 徐晶, 张夫道. 长期定位施肥对土壤酶活性的影响及其调控土壤肥力的作用. 植物营养与肥料学报, 2003, 9(4): 406-410. |
| [17] | 许光辉, 郑洪元. 土壤微生物分析方法手册. 北京: 农业出版社, 1986. |
| [18] | 唐启义, 冯明光. 实用统计分析及其DPS数据处理系统. 北京: 科学出版社, 2002. |
| [19] | 邹国元, 张福锁. 根际反硝化作用与N2O释放. 中国农业大学学报, 2002, 7(1): 77-82. |
| [20] | 黄辉. 近地层O3和C02浓度增加对作物影响的试验研究 [D]. 北京: 中国气象科学研究院, 2003. |
| [21] | 陈展, 王效科, 冯兆忠, 郑启伟, 欧阳志云. 臭氧对生态系统地下过程的影响. 生态学杂志, 2007, 26(1): 121-125. |
| [23] | 李全胜, 林先贵, 胡君利, 余永昌, 沈标, 朱建国. 近地层臭氧浓度升高对麦田土壤氨氧化与反硝化细菌活性的影响. 生态与农村环境学报, 2010, 26(6): 524-528. |
 2013, Vol. 34
2013, Vol. 34




