文章信息
- 史志明, 徐莉, 胡锋
- SHI Zhiming, XU Li, HU Feng
- 蚯蚓生物标记物在土壤生态风险评价中的应用
- Progress in earthworm biomarker studies and theirs applications in soil pollution risk assessment
- 生态学报, 2014, 34(19): 5369-5379
- Acta Ecologica Sinica, 2014, 34(19): 5369-5379
- http://dx.doi.org/10.5846/stxb201301090073
-
文章历史
- 收稿日期:2013-1-9
- 网络出版日期:2014-3-7
在土壤生态系统中,蚯蚓是最重要的栖息者之一[1]。一方面,蚯蚓在土壤的形成过程中,土壤结构和土壤肥力的保持等方面,具有独特的作用[2],另一方面,蚯蚓在陆地生态系统中具有特殊地位,很多动物如鼹鼠,獾和鸟类都可以取食蚯蚓,从某种意义上,它连接了土壤圈与大气圈,沟通了土壤生物同地上生物之间的联系[3, 4]。在生态毒理学上,还由于蚯蚓分布广泛,对土壤污染胁迫比较敏感,而被称为土壤质量的指示者,并在许多生态毒理国际标准中推荐受试物种之一[5, 6]。深入挖掘蚯蚓的“指示”功能,有利于更好地开发利用蚯蚓资源。
蚯蚓生物标记物试验蚯蚓生态毒理学研究的重要内容。自美国国家科学院生物标记物委员会于 1987年对生物标记物进行了系统论述后的20余年来,自2001年在丹麦举办第三次蚯蚓生态毒理学国际研讨会后的10余年来[7],尽管开展了很多研究,生物标记物的概念和研究方法也有了进一步发展,但在实际土壤污染风险评价中,蚯蚓生物标记物试验并没有像蚯蚓常规毒理试验那样可以形成标准并在实际中广泛应用。那么,着眼于科学研究服务现实问题的角度,令人困惑的问题就产生了,蚯蚓生物标记物研究是否有实际意义,当前对于蚯蚓生物标记物的研究工作是否可以应用于实际土壤污染风险管理和评价,但鲜有相关报道。因此本文拟就这个问题,从实际土壤污染风险评价的角度,首先探讨蚯蚓生物标记物的地位和意义,接着,对蚯蚓生物标记物研究现状进行归纳,总结和评述,最后提出推动蚯蚓生物标记物研究和实际应用的建议,包括尝试提出蚯蚓生物标记物研究方法的标准化的建议。
1 蚯蚓生物标记物土壤污染风险评价体系中的位置蚯蚓生物标记物是指在亚致死浓度条件下,通过检测蚯蚓在行为上,生理生化上等敏感指标的变化对土壤污染状况进行评价,从某种意义上讲,它是蚯蚓常规毒性试验方法的拓展[8]。由于蚯蚓生物标记物对土壤污染胁迫比较敏感,因此可以用作是土壤污染预警和诊断的一种工具。
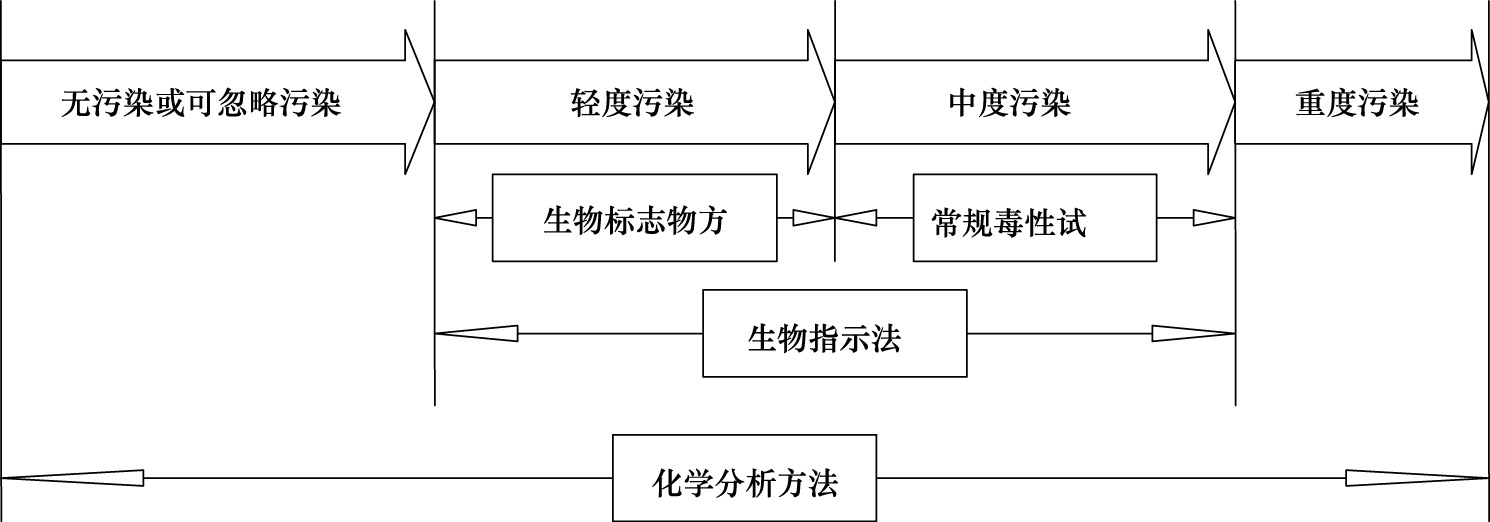
从实际应用的角度,可以将蚯蚓生物标记物融入到土壤风险评价框架中(图 1)。由图 1可以看出,在土壤污染风险评价中,1)广义上讲,蚯蚓生物标记物属于生物指示法的范畴,都是通过考察蚯蚓的相应水平的指标来指示环境污染状况,常规毒性试验检测致死率,繁殖率等个体水平的指标,而蚯蚓生物标记物试验通常检测细胞水平,生理生化水平,甚至基因水平上指标;2)从适用范围来讲,化学分析方法可以检测任何污染程度的土壤,而常规蚯蚓毒理试验(急性毒性试验和生殖毒性试验等),只对低于某种污染程度的土壤适用(中度污染土壤),但生物标记物方法只能对轻度污染土壤适用;3)同化学分析方法相比,面对一块未知风险的潜在污染土壤,生物指示法的缺点是,总体上,它无法确定土壤中存在污染物的类型和含量,但由于生物指示法能够客观反映出污染物在土壤真实的生物有效性和毒性,进而直观地指示潜在污染土壤是否存在现实风险,因此它可以对土壤污染的风险状况做出综合评估;4) 进一步地,由于土壤修复目标是无害化,而对无害化目标的确定,采用生物指示法就远远比化学分析法客观准确;这一点对于建立污染土壤的修复基准也尤其重要[9, 10, 11];综上,生物指示法在土壤污染风险评价中占据重要的位置,虽然它不能作为传统化学分析手段的替代,却是化学分析手段的有益不可或缺的补充,二者结合可以相得益彰。
|
| 图 1 生物标记物在土壤污染风险评价中的位置 Fig. 1 The role of biomarkers in soil pollutant risk assessment |
理解生物指示法在实际土壤污染风险评价和管理中的价值,有助于更好的认识和应用蚯蚓生物标记物。例如,在大规模土壤污染风险评价中,可以首先将土壤视作一个“黑箱”,通过生物测试方法(急性毒性试验,慢性毒性试验和生物标记物试验等),初步筛查出那些已经产生风险的污染地块,并粗略判断土壤污染程度,再通过化学分析手段对这些污染土壤做进一步分析。这样不但可以节约大量的化学分析成本,而且可以获得更为全面,准确和客观的土壤污染信息。
2 研究现状本小节通过对蚯蚓生物标记物研究中所涉及的试验要素进行梳理,并进行简要分析,从整体上为回答如果将蚯蚓生物标记物应用于实际土壤污染风险评价,那么试验中涉及到哪些类型的生物标记物,生物标记物响应的变异性怎么样,需要选用什么样的蚯蚓和污染物,用什么类型的土壤等问题提供依据。所参考的资料是1996年以来关于蚯蚓生物标记物研究的部分文献(表 1)。
| 蚯蚓种 Species | 生物标记物 Biomarkers | 受试物质 Test pollutant | 暴露时间/d Exposure time | 暴露介质 Exposure medium | 参考文献 References |
| E. fetida | 中性红试验 | Cu | 28 | 自然土壤 | [12] |
| E. fetida | 抗氧化酶 | 苯并芘 | 1,2,7,14 | 人工土壤,未老化 | [13] |
| E. fetida | 抗氧化酶,乙酰胆碱脂酶,谷光甘肽转移酶 | Pb | 2,7,14,28 | 人工土壤 | [14] |
| E. fetida | 形态学特征,乙酰胆碱脂酶 | 毒死蜱 | 1,2 | 滤纸 | [15] |
| E. fetida | 中性红试验 | Pb | 28 | 自然土壤,未稳定 | [16] |
| E. fetida | 中性红试验 | Pb | 28 | 自然土壤,未稳定 | [17] |
| E. fetida | 回避试验 | TNT,原油 | 2 | 长期污染土壤 | [18] |
| E. fetida | 中性红试验 | 氰氧化铜 | 28 | 人工土壤,稳定2d | [19] |
| E. fetida | 中性红试验彗星试验 | 乙草胺 | 5,15,30 | 人工土壤 未平衡 | [20] |
| E. fetida | 抗氧化酶 | 荧蒽 | 1,3,7,14 | 自然土壤,稳定3d | [21] |
| E. fetida | 抗氧化酶细胞色素P450 | 菲芘 | 2 | 滤纸 | [22] |
| E. fetida | 乙酰胆碱脂酶,组织病理响应 | 有机磷杀虫剂 | 2 | 滤纸 | [23] |
| E. fetida | 胆碱脂酶 | 双硫磷 | 2 | 滤纸 | [24] |
| E. fetida | 中性红试验 | As | 28 | 沙土 | [25] |
| E. fetida | 彗星试验抗氧化酶 | 阿特拉津 | 28 | 人工土壤,未老化 | [26] |
| E. fetida | 抗氧化酶 | 四溴双酚A | 7,14 | 人工土壤,未老化 | [27] |
| E. fetida | 抗氧化酶 细胞色素P450 | 苯并芘 | 1,3,7,14 | 自然土壤,未老化 | [28] |
| E. fetida | 中性红试验 | Cu | 21 | 长期污染土壤 | [29] |
| E. fetida | 中性红试验 | Zn | 42 | 自然土壤,稳定7d | [30] |
| E. fetida | 彗星试验抗氧化酶 | 三氯生 | 2,7,14 | 盐碱土,未老化 | [31] |
| E. fetida | 抗氧化酶热激蛋白 | 吐纳麝香加乐麝香 | 2 | 滤纸 | [32] |
| E. fetida | 抗氧化酶 | 菲 | 28 | 自然土壤,未老化 | [33] |
| E. fetida | 彗星试验中性红试验 | TNT | 1,2,3 | 滤纸 | [34] |
| E. fetida | 抗氧化酶 | HHCB | 3,7,14,28 | 自然土壤,稳定1d | [35] |
| E. fetida | 抗氧化酶 | 菲芘 | 14 | 自然土壤,平衡2d | [36] |
| E. fetida | 中性红试验 | Cu | 14 | 原位污染土壤 | [37] |
| E. fetida | 抗氧化酶 | 荧蒽 | 7 | 自然土壤,异老化时间 | [38] |
| E. fetida | 抗氧化酶 | 1,2,4-三氯苯 | 2,7,14 | 人工土壤,未老化 | [39] |
| E. fetida | 抗氧化酶 | 菲 芘 | 28 | 人工土壤,平衡15d | [40] |
| E. fetida | 抗氧化酶 | 抗生素类 | 7,14,28 | 森林公园,未老化 | [41] |
| E. fetida | 抗氧化酶 | 金霉素 | 28 | 盐碱土,未老化 | [42] |
| E. fetida | 抗氧化酶 | Cd芘 | 7,14,21,28,35,42,49,56 | 自然土壤,老化7d | [43] |
| E. fetida | 回避试验 | Pb Zn Cu | 2 | 铅矿区污染土壤 | [44] |
| E. fetida | 抗氧化酶 | 多溴联苯醚-Cd | 1,3,5,7,14,28 | 自然土壤,稳定1d | [45] |
| E. andrei | 回避试验 | 重金属 | 原位收集,长期暴露 | 原位污染矿区土壤 | [46] |
| E. andrei | 乙酰胆碱脂酶 | 西维因 | 1,3,5 | 自然土壤,稳定3d | [47] |
| E. andrei | 抗氧化酶,乙酰胆碱脂酶 | 溴氰菊酯 | 1,3,6,15,21,28 | 人工土壤,未老化 | [48] |
| E. andrei | 抗氧化酶,乙酰胆碱脂酶 | 乐果 | 1,3,6,15,21,8 | 人工土壤,未老化 | [49] |
| E. veneta | 中性红试验 | 重金属 | 14 | 黄铁矿区 | [50] |
| L. rubellus | 中性红试验 | Cu | 28 | 自然土壤,稳定3d | [51] |
| L. rubellus | 中性红试验 | Cu | 17,40,70,110 | 自然土壤 | [52] |
| L. rubellus | CAT,细胞色素P450 | 芘 | 42 | 人工土壤,稳定1d | [53] |
| L. terrestris | 伤口愈合 | Cd | 10,20,30 | 人工土壤,未平衡 | [54] |
| L. terrestris | 中性红试验总免疫活性 | 重金属PAHs | 12 | 长期污染田间土壤 | [55] |
| L. terrestris | 羧酸酯酶 | 毒死蜱 | 1 | 滤纸 | [56] |
| L. terrestris | 组织病理学上,抗氧化酶,谷光甘肽转移酶,粘液分泌 | 重金属 | 原位收集,长期暴露 | 原位污染土壤 | [57] |
| A. chlorotica | 胆碱脂酶 | 杀虫剂 | 原位收集,长期暴露 | 苹果园 | [58] |
| A. tuberculata | 金属硫蛋白,细胞色素P450,谷光甘肽转移酶 | Cu Zn | 2,7,14 | 工业原位污染土壤 | [59] |
| L. mauritii | 抗氧化酶,彗星试验,谷光甘肽转移酶 | Pb Zn | 28 | 自然土壤,稳定7d | [60] |
| L. castaneus | 中性红试验 | 重金属 | 原位收集,长期暴露 | 工业污染土壤 | [61] |
| A.caliginosa | 胆碱脂酶,谷光甘肽转移酶 | 毒死蜱 | 7,14,28 | 长期污染自然土壤 | [62] |
| A.caliginosa | 胆碱脂酶中性红试验 | 毒死蜱 | 28 | 长期污染果园土壤 | [63] |
| A.caliginosa | 胆碱脂酶,谷光甘肽转移酶,中性红试验 | 二嗪农毒死蜱 | 28 | 人工土壤,未老化 | [64] |
| D. octaedra | 糖元含量 | 重金属 | 28 | 长期污染森林土壤 | [65] |
| A.nocturnallolobophora icterica | 掘穴行为,乙酰胆碱脂酶 | 吡虫啉 | 7 | 污染废弃桃园 | [66] |
表 2将文献中出现的生物标记物类型进行了归类,可以看出,当前已经筛选出了多种多样的生物标记物,从微观分子水平上的变化到宏观个体行为形态上各个尺度变化的均有涉及。但研究者对这些生物标记物的关注程度是不同的,其中最多的有生理生化上的抗氧化酶系统,金属硫蛋白(MT),溶酶体膜稳定性,行为学上的回避反应和分子遗传学上的彗星试验。另外,研究者也特别关注对特定污染物响应的生物标记物,即特异性生物标记物,但综合文献可以发现除了金属硫蛋白(对重金属类污染物),乙酰胆碱脂酶(对有机磷、氨基甲酸酯类)等少量几类外,大多数生物标记物不具有特异性。如抗氧化酶既能为重金属污染胁迫所诱导[60],也可以为持久性有机污染物所诱导[21, 36],而回避反应[44, 67]和中性红试验则几乎对所有的污染胁迫均有应答[12, 16, 46, 52]。
| 分类依据Classification | 生物标记物种类Type of earthworm biomarkers |
| 生理生化学Physiological and biochemical | 抗氧化酶,细胞色素P450,谷胱甘肽转移酶,乙酰胆碱脂酶 羧酸酯酶,中性红试验,金属硫蛋白,热激蛋白,糖元含量 |
| 行为学Behavioral | 回避反应,掘穴行为,粘液分泌 |
| 组织病理学Histopathological | 表面形态完整性,伤口愈合 |
| 分子遗传学Molecular genetic | 彗星试验 |
| 免疫学Immunological | 总免疫活性 |
理论上,生物体在长期进化和自然选择过程中,其体内的各项生理生化指标应该是处于一个相对稳定的水平,因此,对于同一种蚯蚓来说,在理想生存条件下,其生物体内的各项指标包括生态毒理研究中所说的生物标记物,其基底或背景水平应该是在一定范围内变化,相对稳定的[8]。然而,不同文献报道中,同一种生物标记物的测定数据范围往往差异很大,即使考虑到有很多环境因子,如温度,湿度,污染物等对生物标记物应答的影响,这种巨大的差异值得思考的,如表 3中,赤子爱胜蚓体内超氧化物歧化酶(SOD)活性的变异性超过3个数量级。究其原因,蚯蚓生物标记物的测试方法不统一可能是一个重要的因素。这说明,不同的研究之间生物标记物响应,存在很大的不确定性,从而也限制蚯蚓生物标记物广泛应用,这同时也呼吁建立标准的生物标记物试验和结果表现方法(例如采用相对值的方法消除这种不确定性)。
| 蚯蚓大小E.fetida /(g/条) | SOD Superoxide dismutase /(U mg-1 pr-1) | CAT Catalase /(U mg-1 pr-1) | POD Peroxidase /(U mg-1 pr-1) | MDA Malondialdehyde /(nmol mg-1 pr-1) | 来源 References |
| SOD代表超氧化物歧化酶;CAT代表过氧化氢酶;POD代表过氧化物酶;MDA代表丙二醛 | |||||
| 0.3—0.6 | 40—60 | 10—12 | 5—7 | [40] | |
| 0.35—0.45 | 16—30 | 70—120 | 40—70 | 0.4—0.7 | [68] |
| 0.35—0.45 | 100—300 | 1—5 | 0.2—0.5 | [22] | |
| 0.25—0.35 | 40—60 | 6—10 | 3—6nmol/mg | [33] | |
| 0.3—0.4 | 0.4—0.8 | 3.4—9 | [41] | ||
| 0.3—0.4 | 0.3—0.7 | 15—40 | [26] | ||
| 0.3—0.6 | 0.84—1.41 | 3.65—6.99 | 0.035—0.081 | [31] | |
| 0.4—0.5 | — | — | — | 0.4—0.8 | [32] |
| 0.3—0.4 | 50—60 | 3—5 | [43] | ||
| 0.3—0.5 | 150—250 | 6—10 | [28] | ||
| 0.3—0.4 | 30—40 | 22—28 | 1.2—2.5 | [27] | |
| 0.3—0.4 | 3—6 | 1—4 | 40—100 | [45] | |
| 0.3—0.4 | 150—230 | 5—10 | 0.2—0.4 | [21] | |
蚯蚓生物标记物暴露介质大致说来有,OECD等国际组织推荐的人工模拟土壤,未受污染的自然土壤,从污染场地或矿区采集的长期污染土壤和滤纸。除了自然污染土壤外,试验介质中污染物主要是外源添加。采用人工添加污染物的生物标记物试验主要是着眼于评价评价污染物(单一污染和复合污染)释放到土壤环境中的毒理效应和相应的机理,也可以用作制定土壤环境质量标准的依据,是着眼于危险化学品的管理角度出发,而选用自然污染土壤作为介质,则是探讨生物标记物在实际土壤污染风险评价中的适用性。由于模拟污染土壤与实际长期的土壤污染存在本质上的不同(前者污染较为简单,且生物有效性往往较高),因此,很难通过实验室模拟特定污染的土壤类推到复杂的实际污染土壤。
暴露时间也会对蚯蚓生物标记物响应产生影响,因此暴露时间的不一致会为不同研究之间的比较带来困难[16, 43]。表 1显示,在暴露介质为滤纸时,蚯蚓暴露时间为48 h,通常不超过72 h;在土壤介质实验室条件,除了少量研究中,蚯蚓暴露时间基本一致,即28 d左右。这是由于28 d大致是蚯蚓从一个虫卵发育到成熟的一个周期。在实际操作中,研究者根据相关OECD蚯蚓毒性试验中规定的标准,并进行微小调整确定的[69],取样间隔时间和采样频度有所差异;而从污染场地采集的蚯蚓,其暴露时间可能更长。因此,总体上,在暴露时间的选择上,众多研究者的观点似乎是一致的,这其实也为将蚯蚓生物标记物应用于实际土壤污染风险评价提供了方便。
2.4 受试蚯蚓和受试污染物从表 1可以看出,蚯蚓生物标记物的研究中最常选用的蚯蚓是赤子爱胜蚓(E. fetida)和安德爱胜蚓(E. Andrei)[5],也包括了其它种类的蚯蚓,如陆正蚓 (L. terrestris)等。所选用的蚯蚓绝大多数是成年蚯蚓,少量研究也涉及幼年蚓[64]。这些蚯蚓涵盖了各种生态型,包括表层种如D. octaedra,E. veneta,L. rubellus,L. castaneus等,内层种如A. tuberculata,A. caliginosa,A. icterica,A. chlorotica等和深层种如L. terrestris,A. longata等。选择赤子爱胜蚓考虑到它是几个国际标准堆积中推荐的受试种,其生物学依据是活性较强,易于大规模饲养,繁殖率高,生活周期短而且对化学品反应敏感,但这种蚯蚓的缺点是它不是土著蚯蚓,只栖居在富含有机质的环境中[70]。选择其它蚯蚓大多是由于它们是土著蚯蚓,更能代表实际土壤风险的基本情况,主要缺点是这些蚯蚓难以饲养,若实地采集,虽然可以满足实验室研究需要,却无法大规模应用于实际土壤污染风险评价。
较早用于研究蚯蚓生物标记物响应的受试污染物是重金属,最近几年越来越多地涉及到了持久性有机污染物,例如农药,PAHs等,而新引起人们关注的环境激素类污染物也有涉及(表 1)。因此大体可以说,几乎所有的污染物类别都已经包括,其中代表性的污染物及复合污染对蚯蚓生物标记物的响应都有所研究。污染物之间的复合效应研究,既有重金属与重金属之内的复合,又有持久性有机污染物之内的联合,还有重金属与持久性有机污染物之间的交叉联合。同样地,这些研究或是评估单一污染物或复合污染的毒理效应,服务于危险化学品的管理,或者是模拟典型的现实污染状况,从更广泛的意义上讲,这些研究还远远不能类推到实际土壤污染风险评价。
2.5 其它实际上,很多过程可以影响蚯蚓生物标记物响应。例如,蚯蚓生物标记物测定前蚯蚓通常需要一个清肠过程,以排空肠道中残留的内容物,消除这些内容物对生物标记物测定的影响[70]。在所有的研究中,几乎都有这个过程,但清肠时间却并不一致,有的是12 h,有的是24 h,而清肠时间是否对蚯蚓生物标记物存在影响,鲜有人注意。再有,蚯蚓培养和暴露条件,有的是将蚯蚓处在20或22 ℃,完全黑暗条件下培养,有的则是明暗交替进行;还有,模拟土壤污染采用人工染毒的方式,所需平衡或老化的时间,不同的研究中也差别很大(表 1)。这些都可能是降低不同研究之间可比性的重要因素,理论上,这些问题应该都是可忽略的影响因素,只要在不同的研究中将这些因素统一,那么这些因素可以作为系统误差,而不会影响蚯蚓生物标记物的实际应用。
3 蚯蚓生物标记物研究现状评述及建议通过以上归纳和分析可以看出,目前关于蚯蚓生物标记物的研究,就研究尺度来说,多是停留在实验室基础研究阶段,即使有少量的应用于实际土壤污染预警的研究,也是零星的,分散的,探索性的,未能形成一整套体系;就研究内容来说,这些研究大致有两个方面,一个是研究污染物(单一污染物或复合污染物)对各种蚯蚓生物标记物的响应,探讨其中可能存在的剂量-效应关系,揭示响应机理;另一个是筛选新的生物标记物包括新的特异性生物标记物;就研究方法和结果的展示来说,这些研究从蚯蚓种的选择,到试验设计,到最后的测定方法和结果,都具有多样性和变异性,彼此之间的可比较性较低。因此,考虑到实际土壤污染的复杂性,总的来说,难以通过这些研究获得较为可靠的可指导实际的土壤污染风险评价的结论。
因此,从将生物标记物应用于实际土壤污染评价的角度,当前的研究并不成熟。但这些研究提供了大量有关蚯蚓生物标记物的第一手资料,一定程度上阐明了生物标记物应答的机制及其同土壤污染的关系,从而为将蚯蚓生物标记物用于实际土壤污染风险评价奠定了基础:1)筛选出了大量的,在实验室条件下较为有效和可靠的生物标记物(包括少量的特异性生物标记性物),如回避试验和中性红试验[61, 67];2)揭示了典型污染物的代表及其典型组合对蚯蚓生物标记物的影响及其机制[43, 59, 60]。
这些研究的重要性不言而喻,但着眼于实际污染风险评价的角度,目前关于蚯蚓生物标记物研究的两个内容似乎可以适可而止,当然为了评估新的化学品风险和研究化学品对蚯蚓的毒理学机制的基础研究除外。首先,穷尽研究所有污染物及其组合对各种蚯蚓,各类生物标记物在各种暴露介质中的响应是不可能的,也是没有必要的;其次,筛选新的蚯蚓生物标记物包括新的特异性生物标记物似乎变得很困难,可能也没有必要,因为一方面对蚯蚓生物标记物的筛选从分子水平到机体水平,已经从各个层次上筛选出了大量的生物标记物,而且这些生物标记物响应的生物学机制也一定程度的阐明了,即使存在新的生物标记物,可能也不便于推广应用;此外,虽然某些特异的生物标记物可以指示特定的污染物,但总体上,生物标记物是不具有指示特定污染物功能。任何污染胁迫都可能会对蚯蚓造成毒害,从而会通过蚯蚓的各项生理生化过程包括蚯蚓生物标记物反映出来,而且土壤的实际污染状况往往包括多种污染物,是复杂的,难以预测的,即使有更多的特异性生物标记物,也很难全面反映土壤实际污染状况,因此从实际风险评价和管理的角度来讲,筛选特异性生物标记物的意义可能值得重新认识。
而未来的研究重点,应该尝试通过系统研究和标准化方法推动和评估生物标记物应用于实际的价值,具体来说,1)将蚯蚓生物标记物研究方法标准化(4节),积累可供参照的实际土壤污染对生物标记物响应的数据资料,探索实际应用的可行性;2)在标准化的基础上,对现有的生物标记物进行再筛选和再评估,目标是筛选出那些在实际土壤污染条件下,反应敏感,操作简便,具有较好重现性的生物标记物;3)进一步地,结合我国各地土壤类型划分,建立赤子爱胜蚓生物标记物在各类洁净土壤中背景水平的数据库,实际上这也有利于建立环境质量基准[71];4)结合全国土壤污染普查数据和化学分析方法,建立生物标记物同污染水平的对应关系,最终建立通过生物标记物响应对土壤污染风险评价的模型。通过这些研究,应该能在很大程度上推动蚯蚓生物标记物的研究和在实际土壤污染风险评价中的应用。
4 蚯蚓生物标记物研究方法的标准化探讨3节提出了推动蚯蚓生物标记物研究的一些建议,其中,建立一种标准化的蚯蚓生物标记物试验方法是重要的,据此,尝试提出了一个蚯蚓生物标记物研究的推荐性方法(表 4)。需要说明的是,表中所列的只是主要需要标准化的条目,具体细节,尚需进一步探讨。
| 项目Items | 推荐 Recommendations | 评论 Comments |
| 受试蚯蚓 Earthworm species | 成年赤子爱胜蚓 大小为0.3—0.4g | 1)OECD常规毒理试验推荐的参考蚯蚓;2)对该蚯蚓的研究资料远远多于其它蚯蚓,有比较完备的资料;3)易于获取;4)最好也同时规定蚯蚓的饲养方式 |
| 暴露介质 Exposure medium | 实地污染土壤 | 1)OECD参考土壤和滤纸不能直接反应污染场地现实;2)该推荐标准直接用于土壤污染风险评价 |
| 暴露时间 Exposure time | 28d(回避反应2d) | 现在资料中,除个别报道,绝大多数都暴露28d(回避反应2d),方便参考以前资料 |
| 生物标记物 biomarkers | 抗氧化酶 溶酶体稳定性 回避反应 乙酰胆碱脂酶 金属硫蛋白等 | 1)这些生物标记物受到研究者的广泛关注,研究资料丰富;2)相关测定方法成熟;3)着眼于实际应用的角度,需要对各种生物标记物进行再评估和筛选。 |
| 生物标记物测定方法 Bioassay methods of biomarker | 严格规范 | 现有报道中关于酶生物标记物结果差异很大,尤其是对酶生物标记物的测定做详细的规范,从缓冲液的配制,到最后结果的计算和表达 |
在土壤污染风险评价中,蚯蚓生物标记物在理论上具有独特的应用价值,虽然它无法替代传统的化学分析方法,但它是化学分析手段的一种不可或缺的有益补充。虽然蚯蚓生物标记物的研究资料已经很多,但目前依然不可能将其应用于实际的土壤污染风险评价或预警。显然,需要开展更多的工作,其中重要的一项就是建立蚯蚓生物标记物研究的标准化规程,结合中国实际,积累可供参考的数据,最终可以将生物标记物理论融入到实际的土壤污染风险评价和管理体系。
| [1] | Bartlett M D, Briones M J I, Neilson R, Schmidt O, Spurgeon D, Creamer R E. A critical review of current methods in earthworm ecology: From individuals to populations. European Journal of Soil Biology, 2010, 46(2): 67-73. |
| [2] | Edwards C A. Earthworm Ecology. Boca Raton: CRC Press, 2004. |
| [3] | Jager T. Mechanistic approach for estimating bioconcentration of organic chemicals in earthworms (Oligochaeta). Environmental Toxicology and Chemistry, 1998, 17(10): 2080-2090. |
| [4] | Matscheko N, Lundstedt S, Svensson L, Harju J, Tysklind M. Accumulation and elimination of 16 polycyclic aromatic compounds in the earthworm (Eisenia fetida). Environmental Toxicology and Chemistry, 2002, 21(8): 1724-1729. |
| [5] | OECD. OECD guidelines for testing of chemicals No. 207: earthworm acute toxicity tests. OECD, 1984. |
| [6] | Zheng S L, Song Y F, Qiu X Y, Sun T H, Ackland M L, Zhang W. Annetocin and TCTP expressions in the earthworm Eisenia fetida exposed to PAHs in artificial soil. Ecotoxicology and Environmental Safety, 2008, 71(2): 566-573. |
| [7] | Spurgeon D J, Weeks J M, van Gestel C A. A summary of eleven years progress in earthworm ecotoxicology: The 7th international symposium on earthworm ecology· Cardiff· Wales· 2002. Pedobiologia, 2003, 47(5/6): 588-606. |
| [8] | Scott-Fordsmand J J, Weeks J M. Biomarkers in earthworms. Review of Environmental Contamination and Toxicology, 2000, 165: 117-159. |
| [9] | Zhou Q X, Wang M E. Researching advancement and arospect of aoil ecotoxicology. Asian Journal of Ecotoxicology, 2006, 1(1): 1-11. |
| [10] | Li P J, Xiong X Z, Yang G F, Liu W, Xu H X, Tai P D. Application of terrestrial invertebrates biomarkers in soil pollution ecology study. Chinese Journal of Applied Ecology, 2003, 14(12): 2347-2350. |
| [11] | Market B, Wang M E, Wünschmann S, Chen W P. Bioindicators and biomonitors in environmental quality assessment. Acta Ecologia Sinica, 2013, 33(1): 0033-0044. |
| [12] | Svendsen C, Weeks J M. Relevance and applicability of a simple earthworm biomarker of copper exposure. I. Links to ecological effects in a laboratory study with Eisenia andre. Ecotoxicology and Environmental Safety, 1997, 36(1): 72-79. |
| [13] | Saint-Denis M, Narbonne J, Arnaud C, Thybaud E, Ribera D. Biochemical responses of the earthworm Eisenia fetida andrei exposed to contaminated artificial soil: effects of benzo (a) pyrene. Soil Biology and Biochemistry, 1999, 31(13): 1837-1846. |
| [14] | Saint-Denis M, Narbonne J, Arnaud C, Ribera D. Biochemical responses of the earthworm Eisenia fetida andrei exposed to contaminated artificial soil: effects of lead acetate. Soil Biology and Biochemistry, 2001, 33(3): 395-404. |
| [15] | Venkateswara Rao J, Surya Pavan Y, Madhavendra S S. Toxic effects of chlorpyrifos on morphology and acetylcholinesterase activity in the earthworm, Eisenia foetida. Ecotoxicology and Environmental Safety, 2003, 54(3): 296-301. |
| [16] | Reinecke A, Reinecke S. The influence of exposure history to lead on the lysosomal response in Eisenia fetida (Oligochaeta). Ecotoxicology and Environmental Safety, 2003, 55(1): 30-37. |
| [17] | Booth L, Palasz F, Darling C, Lanno R, Wickstrom M. The effect of lead-contaminated soil from canadian prairie skeet ranges on the neutral red retention assay and fecundity in the earthworm Eisenia fetida. Environmental Toxicology and Chemistry, 2003, 22(10): 2446-2453. |
| [18] | Schaefer M. Behavioural endpoints in earthworm ecotoxicology. Journal of Soils and Sediments, 2003, 3(2): 79-84. |
| [19] | Maboeta M S, Reinecke S A, Reinecke A J. The relationship between lysosomal biomarker and organismal responses in an acute toxicity test with Eisenia fetida (Oligochaeta) exposed to the fungicide copper oxychloride. Environmental Research, 2004, 96(1): 95-101. |
| [20] | Xiao N W, Song Y, Ge F, Liu X H, Ouyang Z Y. Biomarkers responses of the earthworm Eisenia fetida to acetochlor exposure in OECD soil. Chemosphere, 2006, 65(6): 907-912. |
| [21] | Zhang W, Song Y F, Sun T X, Liu M. Effects of low dosage pyrene pollution on biochemical characters of earthworms Eisenia fetida in soil. Chinese Journal of Applied ecology, 2007, 18(9): 2097-2103. |
| [22] | Zhang W, Song Y F, Sun T X, Song X Y, Zhou Q X, Zhen S L. Influence of phenanthrene and pyrene on cytochrome p450 and antioxidant enzymes in earthworms Eisenia fetida. Environmental Chemistry, 2007, 26(002): 202-206. |
| [23] | Chakra Reddy N, Venkateswara Rao J. Biological response of earthworm, Eisenia foetida (Savigny) to an organophosphorous pesticide, profenofos. Ecotoxicology and Environmental Safety, 2008, 71(2): 574-582. |
| [24] | Hackenberger B K, Jaric-Perkusic D, Stepic S. Effect of temephos on cholinesterase activity in the earthworm Eisenia fetida (Oligochaeta, Lumbricidae). Ecotoxicology and Environmetnal Safety, 2008, 71(2): 583-589. |
| [25] | Lee B T, Kim K W. Lysosomal membrane response of earthworm, Eisenia fetida, to arsenic contamination in soils. Environmetnal Toxicology, 2009, 24(4): 369-376. |
| [26] | Song Y, Zhu L S, Wang J, Wang J H, Liu W, Xie H. DNA damage and effects on antioxidative enzymes in earthworm (Eisenia foetida) induced by atrazine. Soil Biology and Biochemistry, 2009, 41(5): 905-909. |
| [27] | Xue Y G, Wang X R, Gu X Y, Sun C. Acute toxicity of tetrabromobisphenol A to earthworms Eisenia fetida and its effects on antioxidant defense system enzymes. Asian Journal of Ecotoxicology, 2009, 4(1): 93-100. |
| [28] | Wang L, Song Y F, Zhang W, Chen L. Influence of benzo(a) pyrene on cytochrome P450 and antioxidant enzymes in earthworms Eisenia fetida. Jouranl of Agro-Environment Science, 2009, 28(2): 337-342. |
| [29] | Scott-Fordsmand J J, Weeks J M, Hopkin S P. Importance of contamination history for understanding toxicity of copper to earthworm Eisenia fetica (Oligochaeta: Annelida), using neutral-red retention assay. Environmental Toxicology and Chemistry, 2009, 19(7): 1774-1780. |
| [30] | Spurgeon D J, Svendsen C, Rimmer V R, Hopkin S P, Weeks J M. Relative sensitivity of life-cycle and biomarker responses in four earthworm species exposed to zinc. Environmental Toxicology and Chemistry, 2009, 19(7): 1800-1808. |
| [31] | Lin D S, Zhou Q X, Xie X J, Liu Y. Potential biochemical and genetic toxicity of triclosan as an emerging pollutant on earthworms (Eisenia fetida). Chemosphere, 2010, 81(10): 1328-1333. |
| [32] | Chen C, Zhou Q X, Liu S, Xiu Z M. Acute toxicity, biochemical and gene expression responses of the earthworm (Eisenia fetida) exposed to polycyclic musks. Chemosphere, 2011, 83(8): 1147-1154. |
| [33] | Wu S J, Wu E M, Qiu L Q, Zhong W L, Chen J. Effects of phenanthrene on the mortality, growth, and anti-oxidant system of earthworms (Eisenia fetida) under laboratory conditions. Chemosphere, 2011, 83(4): 429-434. |
| [34] | Fuchs J, Piola L, Gonzalez E P, Oneto M L, Basack S, Kesten E, Casabe N. Coelomocyte biomarkers in the earthworm Eisenia fetida exposed to 2, 4, 6-trinitrotoluene (TNT). Environ Monit Assess, 2011, 175(1/4): 127-137. |
| [35] | Liu S, Zhou Q X, Wang Y Y. Ecotoxicological responses of the earthworm Eisenia fetida exposed to soil contaminated with HHCB. Chemosphere, 2011, 83(8): 1080-1086. |
| [36] | Wu E M, Wang J L, Zhao S L, Li H L, Wu S J. Effects of single and combined pollution of phe, pyr on SOD, CAT activities and MDA content of Eisenia foteda in soils. Acta Scientiae Circumstantiae, 2011, 31(5): 1077-1085. |
| [37] | Rocco A, Scott-Fordsmand J J, Maisto G, Manzo S, Salluzzo A, Jensen J. Suitability of lysosomal membrane stability in Eisenia fetida as biomarker of soil copper contamination. Ecotoxicology and Environmental Safety, 2011, 74(4): 984-988. |
| [38] | Ma L L, Ma C, Shi Z M, Li W M, Xu L, Hu F, Li H X. Effects of fluoranthene on the growth, bioavailability and anti-oxidant system of Eisenia fetida during the ageing process. European Journal of Soil Biology, 2012, 50: 21-27. |
| [39] | Wu S J, Zhang H, Hu Y, Li H L, Chen J M. Effects of 1, 2, 4-trichlorobenzene on the enzyme activities and ultrastructure of earthworm Eisenia fetida. Ecotoxicology and Environmental Safety, 2012, 76(2): 175-181. |
| [40] | Wu S J, Zhang H X, Zhao S L, Wang J L, Li H L, Chen J M. Biomarker responses of earthworms (Eisenia fetida) exposured to phenanthrene and pyrene both singly and combined in microcosms. Chemosphere, 2012, 87(4): 285-293. |
| [41] | Dong L X, Gao J, Xie X J, Zhou Q X. DNA damage and biochemical toxicity of antibiotics in soil on the earthworm Eisenia fetida. Chemosphere, 2012, 89(1): 44-51. |
| [42] | Lin D S, Zhou Q X, Xu Y M, Chen C, Li Y. Physiological and molecular responses of the earthworm (Eisenia fetida) to soil chlortetracycline contamination. Environmental Pollution, 2012, 171: 46-51. |
| [43] | Yang X, Song Y, Kai J, Cao X. Enzymatic biomarkers of earthworms Eisenia fetida in response to individual and combined cadmium and pyrene. Ecotoxicology and Environmetal Safety, 2012, 86: 162-167. |
| [44] | Udovic M, Lestan D. Eisenia fetida avoidance behavior as a tool for assessing the efficiency of remediation of Pb, Zn and Cd polluted soil. Environmental Pollution, 2010, 158(8): 2766-2772. |
| [45] | Zhu S Z, Zhu L Y, Liu M, Chang C. Toxicity of Commercial Penta-BDE and Cd in soil on anti-oxidant Defensive Responses of earthworms. Environmental Science and Technology, 2010, (33)11: 10-16. |
| [46] | Da Luz T N, Ribeiro R, Sousa J P. Avoidance tests with collembola and earthworms as early screening tools for site-specific assessment of polluted soils. Environmental Toxicology and Chemistry, 2009, 23(9): 2188-2193. |
| [47] | Gambi N, Pasteris A, Fabbri E. Acetylcholinesterase activity in the earthworm Eisenia andrei at different conditions of carbaryl exposure. Comparative Biochemistry and Physiology Part C: Toxicology & Pharmacology, 2007, 145(4): 678-685. |
| [48] | Velki M, Hackenberger B K. Biomarker responses in earthworm Eisenia andrei exposed to pirimiphos-methyl and deltamethrin using different toxicity tests. Chemosphere, 2013, 90(3): 1216-1226. |
| [49] | Velki M, Hackenberger B K. Inhibition and recovery of molecular biomarkers of earthworm Eisenia andrei after exposure to organophosphate dimethoate. Soil Biology & Biochemistry, 2013, 57: 100-108. |
| [50] | Høensi T G, Stubberud H E, Andersen S, Stenersen J. Lysosomal fragility in earthworms (Eisenia veneta) exposed to heavy metal contaminated soils from two abandoned pyrite ore mines in Southern Norway. Water, Air, & Soil Pollution, 2003, 142(1/4): 27-37. |
| [51] | Weeks J M, Svendsen C. Neutral red retention by lysosomes from earthworm (Lumbricus rubellus) coelomocytes: a simple biomarker of exposure to soil copper. Environmental Toxicology and Chemistry, 1996, 15(10): 1801-1805. |
| [52] | Svendsen C, Weeks J M. Relevance and applicability of a simple earthworm biomarker of copper exposure. II. Validation and applicability under field conditions in a mesocosm experiment with Lumbricus rubellus. Ecotoxicology and Environmental Safety, 1997, 36(1): 80-88. |
| [53] | Brown P J, Long S M, Spurgeon D J, Svendsen C, Hankard P K. Toxicological and biochemical responses of the earthworm Lumbricus rubellus to pyrene, a non-carcinogenic polycyclic aromatic hydrocarbon. Chemosphere, 2004, 57(11): 1675-1681. |
| [54] | Cikutovic M, Fitzpatrick L, Goven A, Venables B, Giggleman M, Cooper E. Wound healing in earthworms Lumbricus terrestris: a cellular-based biomarker for assessing sublethal chemical toxicity. Bulletin of Environmental Contamination and Toxicology, 1999, 62(4): 508-514. |
| [55] | Hankard P K, Svendsen C, Wright J, Wienberg C, Fishwick S K, Spurgeon D J, Weeks J M. Biological assessment of contaminated land using earthworm biomarkers in support of chemical analysis. Science of The Total Environment, 2004, 330(1/3): 9-20. |
| [56] | Sanchez-Hernandez J C, Mazzia C, Capowiez Y, Rault M. Carboxylesterase activity in earthworm gut contents: Potential (eco) toxicological implications. Comparative Biochemistry and Physiology Part C: Toxicology & Pharmacology, 2009, 150(4): 503-511. |
| [57] | Kılıç G A. Histopathological and biochemical alterations of the earthworm (Lumbricus Terrestris) as biomarker of soil pollution along Porsuk River Basin (Turkey). Chemosphere, 2011, 83(8): 1175-1180. |
| [58] | Denoyelle R, Rault M, Mazzia C, Mascle O, Capowiez Y. Cholinesterase activity as a biomarker of pesticide exposure in Allolobophora chlorotica earthworms living in apple orchards under different management strategies. Environmental Toxicology and Chemistry, 2009, 26(12): 2644-2649. |
| [59] | Lukkari T, Taavitsainen M, Soimasuo M, Oikari A, Haimi J. Biomarker responses of the earthworm (Aporrectodea tuberculata) to copper and zinc exposure: differences between populations with and without earlier metal exposure. Environmental Pollution, 2004, 129(3): 377-386. |
| [60] | Maity S, Roy S, Chaudhury S, Bhattacharya S. Antioxidant responses of the earthworm Lampito mauritii exposed to Pb and Zn contaminated soil. Environmental Pollution, 2008, 151(1): 1-7. |
| [61] | Svendsen C, Meharg A A, Freestone P, Weeks J M. Use of an earthworm lysosomal biomarker for the ecological assessment of pollution from an industrial plastics fire. Applied Soil Ecology, 1996, 3(2): 99-107. |
| [62] | Booth L H, Hodge S, O'Halloran K. Use of biomarkers in earthworms to detect use and abuse of field applications of a model organophosphate pesticide. Bulletin of Environmental Contamination and Toxicology, 2001, 67(5): 633-640. |
| [63] | Reinecke S A, Reinecke A J. Biomarker response and biomass change of earthworms exposed to chlorpyrifos in microcosms. Ecotoxicology and Environmental Safety, 2007, 66(1): 92-101. |
| [64] | Booth L H, O'Halloran K. A comparison of biomarker responses in the earthworm Aporrectodea caliginosa to the organophosphorus insecticides diazinon and chlorpyrifos. Environmental Toxicology and Chemistry, 2009, 20(11): 2494-2502. |
| [65] | Holmstrup M, Sorensen J G, Overgaard J, Bayley M, Bindesbol A M, Slotsbo S, Fisker K V, Maraldo K, Waagner D, Labouriau R, Asmund G. Body metal concentrations and glycogen reserves in earthworms (Dendrobaena octaedra) from contaminated and uncontaminated forest soil. Environmental Pollution, 2011, 159(1): 190-197. |
| [66] | Capowiez Y, Rault M, Mazzia C, Belzunces L. Earthworm behaviour as a biomarker-a case study using imidacloprid. Pedobiologia, 2003, 47(5/6): 542-547. |
| [67] | Hund-Rinke K, Wiechering H. Earthworm avoidance test for soil assessments. Journal of Soils and Sediments, 2001, 1(1): 15-20. |
| [68] | Liu S, Zhou Q, Chen C. Antioxidant enzyme activities and lipid peroxidation in earthworm Eisenia fetida exposed to 1, 3, 4, 6, 7, 8-hexahydro-4, 6, 6, 7, 8, 8-hexamethyl-cyclopenta-γ-2-benzopyran. Environmental Toxicology, 2010: 472-279. |
| [69] | Davies N A, Hodson M E, Black S. The influence of time on lead toxicity and bioaccumulation determined by the OECD earthworm toxicity test. Environmental Pollution, 2003, 121(1): 55-61. |
| [70] | Nahmani J, Hodson M E, Black S. A review of studies performed to assess metal uptake by earthworms. Environmental Polluttion, 2007, 145(2): 402-424. |
| [71] | Ferreira N G C, Santos M J G, Domingues I, Calhôa C F, Monteiro M, Amorim M J B, Soares A M V M, Loureiro S. Basal levels of enzymatic biomarkers and energy reserves in Porcellionides pruinosus. Soil Biology and Biochemistry, 2010, 42(12): 2128-2136. |
| [9] | 周启星, 王美娥. 土壤生态毒理学研究进展与展望. 生态毒理学报, 2006, 1(1): 1-11. |
| [10] | 李培军, 熊先哲, 杨桂芬, 刘宛, 许华夏, 台培东. 动物生物标志物在土壤污染生态学研究中的应用. 应用生态学报, 2003, 14(12): 2347-2350. |
| [11] | Markert B, 王美娥, Wünschmann S, 陈卫平. 环境质量评价中的生物指示与生物监测. 生态学报, 2013, 33(1): 33-44. |
| [21] | 张薇, 宋玉芳, 孙铁珩, 刘淼, Ackland M L, Galina B. 土壤低剂量芘污染对蚯蚓若干生化指标的影响. 应用生态学报, 2007, 18(9): 2097-2103. |
| [22] | 张薇, 宋玉芳, 孙铁珩, 宋雪英, 周启星, 郑森林. 菲和芘对蚯蚓 (Eisenia fetida) 细胞色素 P450 和抗氧化酶系的影响. 环境化学, 2007, 26(2): 202-206. |
| [27] | 薛银刚, 王晓蓉, 顾雪元, 孙成. 四溴双酚 A 对赤子爱胜蚓的急性毒性及抗氧化防御系统酶的影响. 生态毒理学报, 2009, 4(1): 93-100. |
| [28] | 王磊, 宋玉芳, 张薇, 陈朗, Freestone D, Ackland M L. 蚯蚓 (Eiseniafetida) 细胞色素 P450 及抗氧化酶系对环境浓度苯并 (a) 芘的响应. 农业环境科学学报, 2009, 28(2): 337-342. |
| [36] | 吴尔苗, 王军良, 赵士良, 李辉龙, 吴石金. 菲和芘单一及复合污染对蚯蚓抗氧化酶活性和丙二醛含量的影响. 环境科学学报, 2011, 31(5): 1077-1085. |
| [45] | 朱淑贞, 祝凌燕, 刘慢, 常春. 五溴联苯醚-镉胁迫下蚯蚓抗氧化防御反应. 环境科学与技术, 2010, 33(11): 10-16. |
 2014, Vol. 34
2014, Vol. 34




