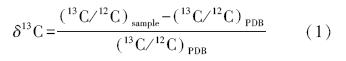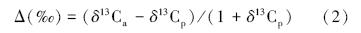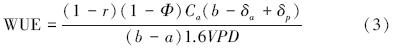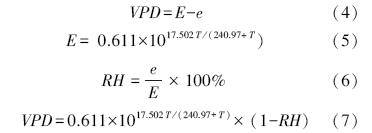文章信息
- 陈平, 张劲松, 孟平, 何春霞, 贾长荣, 李建中
- CHEN Ping, ZHANG Jinsong, MENG Ping, HE Chunxia, JIA Changrong, LI Jianzhong
- 稳定碳同位素测定水分利用效率——以决明子为例
- Feasibility analysis on the determination of WUE by stable carbon isotope:Cassia obtusifolia L. as an example
- 生态学报, 2014, 34(19): 5453-5459
- Acta Ecologica Sinica, 2014, 34(19): 5453-5459
- http://dx.doi.org/10.5846/stxb201301080064
-
文章历史
- 收稿日期:2013-1-8
- 网络出版日期:2014-3-13
2. 济源市国有大沟河林场, 济源 454650
2. Dagou-he National Forest Farm, Jiyuan 454650, China
复合农林业是华北低丘山区退耕还林工程建设的重要内容之一[1],林药复合系统作为农林复合系统的类型之一,在当地农业产业调整发展的过程中,得到了广泛的应用。由于该地区气候干旱、土层瘠薄、灌溉条件较差,水资源短缺制约了林业及农业的持续发展。因此,基于种间水分关系理论,研究林药复合系统水分生态问题,对当地林业生态建设、提高农民收入,促进生态与经济可持续发展,具有重要的指导意义[2]。
水分利用效率(WUE)是植物生理活动过程中消耗水形成有机物质的基本效率,是确定植物体生长发育所需要的最佳水分供应的重要指标之一[3],在一定程度上反映了植物的耗水性和干旱适应性[4]。水分利用效率越高,表明植株节水能力越强,耐旱生产力越高。高水分利用效率是植物适应水分亏缺的一种响应机制[5]或响应干旱环境的一种重要特征[6]。
目前WUE的测算方法有收获法、光合仪法、微气象法和稳定碳同位素法等。由于破坏性太大[7],传统的收获法不能用于复合系统内对植物WUE进行测算;而大多数复合模式位于石质丘陵、山区,下垫面不均一,使得水分平衡法、彭曼法以及随着微气象学理论发展起来的涡度相关法等估算田间耗水量和WUE也变得不现实。而常规的光合仪法只能进行短期及瞬时的蒸腾量和WUE研究、很难与植物的最终生产力和田间实际值联系起来[8, 9]。并且最近很多研究也表明光合仪法测出的瞬时水分利用效率不是估算植物实际WUE的一个可靠指标[10, 11]。由于上述方法在测算作物水分利用效率上的局限性,大田中复合系统各组分耗水量的估算也受到很多限制。最主要的是上述方法无法区分出林木和作物的耗水量差异。由于植物组织的碳是在一段时期(如整个生长期)内累积起来的,由其稳定碳同位素组成测算的WUE可以指示植物长期生活过程的平均WUE,且该方法采样破坏性小,不受时间、地点和下垫面情况等条件的限制,方便保存和测定[12]。
决明子(Cassia obtusifolia L.)是一种1年生豆科药用植物,含有丰富的氨基酸和多种维生素,具有很好的保健功能[13],并具有固氮、提高土壤肥力作用,发展前景较好。本文以决明子为例,采用称重法和稳定碳同位素法对盆栽决明子的WUE进行分析比较,以判定稳定碳同位素方法测定决明子WUE的可行性,为复合系统种间关系作物水分利用效率评价方法的应用提供一定的理论依据。
1 材料与方法 1.1 试验材料及处理试验材料为决明子(Cassia obtusifolia L.),试验地点为黄河小浪底森林生态系统定位研究站内的济源市大沟河林场,于2011年7月18日将决明子种子分别播入30盆开口直径为21cm的塑料盆中,每一盆中土的重量均为8.5kg,为了尽量使生长条件更接近大田条件,用当地土作为填充材料并将盆栽设在室外环境下。决明子出苗后进行间苗,每盆留3株大小一致的壮苗,用塑料膜覆盆减少土壤蒸发。隔天早晚对盆栽决明子称重,每次降雨前后将盆和塑料膜外的水倒出晾干后加测,并根据两次称重的重量变化算出耗水量。
在距离试验地约100m处的大沟河林场内设置小气候自动观测系统,于整个决明子生育期连续观测空气温度(Ta)和相对湿度(RH)(HMP45C,Vaisala,Finland)、降雨量(P)(RM Young,Inc)等气象数据,数据采集器为CR23X(Campbell公司,美国)。每2 min采集1次,每10 min输出1组平均值,将每天144组数据平均获得1个日平均值。
1.2 测定项目及方法 1.2.1 生物量测定分别在苗期(出苗后19d,记为S1)、快速生长期(出苗后46d,记为S2)、开花期(出苗后69d,记为S3)和成熟期(出苗后91d,记为S4)4个时期随机选出3盆决明子进行取样,每盆中3株同一部分的混合物作为一个样品。将每盆的地上部分取样后,对根进行分离取样。用水将土冲干净,获得全部根系。在80°C烘箱中烘干48h,用万分之一天平称重获得各部分的干重和总生物量。
1.2.2 稳定碳同位素比率和碳含量测定用研钵和粉碎机将决明子各部分的干物质进行研磨,过80目筛子,制备成供试样品。在中国林科院稳定同位素比率质谱实验室用稳定同位素质谱仪 (DELTA V Advantage Isotope Ratio Mass Spectrometer) 测定碳同位素比率(δ13C)值和碳含量。同时用小气泵把空气样品装入气体采样袋中用于分析空气的CO2浓度和δ13C值,每样品3个重复。空气CO2浓度采用气相色谱仪(Agilent6820)、火焰离子化检测器(FID)测定,分析精度为5‰;空气δ13C值在中科院地质与地球物理研究所稳定同位素地球化学实验室用质谱仪(MAT253)采用高温燃烧法测定。植物和空气δ13C值的测定以PDB(Pee Dee Belemnite)为标准,根据下面公式计算[14]:
式中,δ13C 表示样品13C/12C与标准样品偏离的千分率,(13C/12C)PDB表示标准物质PDB的13C/12C。稳定碳同位素分辨率Δ的计算方法为:
式中,δ13Cp和δ13Ca分别为植物组织及大气CO2的碳同位素比率。用叶片、茎和根计算出的稳定碳同位素比率和分辨率分别记为δ13CL、δ13CS、δ13CR和ΔL、ΔS、ΔR。
1.2.3 水分利用效率的计算稳定碳同位素方法估算决明子的水分利用效率是根据相关方面学者的研究进行计算[14, 15, 16, 17, 18]:
式中,WUE水分利用效率(mmol C·mol-1 H2O); r为根部含碳量占植物总含碳量的比例;Φ为植物整个生长期叶片夜间呼吸和其它器官呼吸消耗掉的碳的比率,取Φ=0.3[17];δa和δp分别为空气和植物的δ13C值;Ca为大气CO2浓度,其数值为取样日前一段时间的平均值,通过小浪底森林生态定位站的CO2同位素在线分析系统(Los Gatos Research,USA)获得;a、b分别为CO2扩散和羧化过程中的同位素分馏系数,其中a=4.4%,b=30 ‰;数值1.6为水蒸汽和CO2在空气中的扩散比率;VPD为叶片内外蒸汽压差(kPa),由植物生长过程中取样日期前一段的平均白日(7:00—17:30)气象数据(Ta、RH等)计算得出[10, 19]:
式中,E为同温度下的饱和水汽压;e为实际水汽压;T为叶片温度;RH为大气相对湿度;0.611为t=0℃时纯水平面上的饱和水汽压。
称重法计算WUE的方法为:分别用根、茎、叶、种子的干重乘以各自的碳含量得出总碳生物量,除以各时期的耗水量既得到取样前一段决明子的WUE。
1.3 数据统计与分析试验数据采用Excel 和SPSS 统计软件进行分析。
2 结果与分析 2.1 决明子不同生长时期生物量和耗水量的变化表 1和图 1所示,决明子地上部分和地下部分生物量均随着生长时期的增加而不断地增加,在生长前期(S1—S2阶段)增长速率较快,呈明显的上升趋势,生长中期(S2—S3阶段)增长速率缓慢上升,到生长后期(S3—S4阶段),增长速率呈现下降的趋势;干物质根冠比随着生长时期的增加而逐渐减小,但各个生长时期之间的差异不明显;用盆栽称重法得出的决明子耗水量随着生长时期的增加而不断的增加,其各个时期的差异都较明显。
| 生长时期 Growth stage | 生物量Biomass/g | 根冠比 Root shoot ratio RSR | 耗水量 Water use/kg | |
| 地上Above-ground | 地下Below-ground | |||
| 同列中相同小写字母表示差异不显著,不同的小写字母表示差异显著( P<0.05);*,**分别表示P<0.05、P<0.01水平下差异显著,NS表示在P<0.05的水平下差异不显著 | ||||
| S1 | 0.24±0.05a | 0.18 ±0.09a | 0.63±0.24a | 0.26±0.05a |
| S2 | 2.76±0.71b | 1.47 ±0.30b | 0.55±0.03a | 0.73±0.04b |
| S3 | 4.35±0.63bc | 1.74 ±0.18b | 0.41±0.03a | 1.10±0.11c |
| S4 | 5.48±0.55c | 1.83 ±0.35b | 0.33±0.03a | 1.53±0.11d |
| Sig | ** | ** | NS | ** |
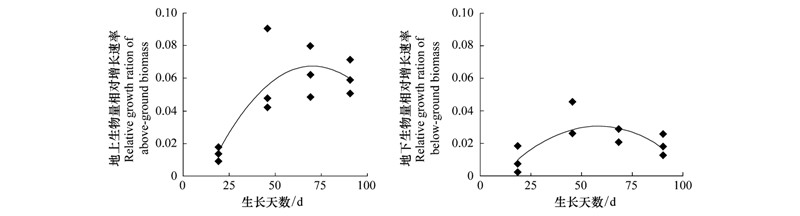
|
| 图 1 生物量相对增长速率 Fig. 1 Relative growth rate of biomass |
从表 2可以看出,决明子碳同位素比值在-29.48—-28.03‰之间变化,总的均值为-28.89‰。就不同部位均值来看,δ13CR>δ13CS>δ13CL。不同时期中,根δ13C值S2>S4>S1>S3,茎和叶δ13C值均表现为S4>S2>S3>S1。方差分析显示,只有根部碳同位素值在不同时期间差异达到极显著水平(P<0.01),茎和叶的碳同位素值在不同时期差异不明显;根、茎、叶的碳含量在25.42%—40.81%之间,均表现在苗期和成熟期较高,不同生长期间差异显著,根部碳含量明显低于茎、叶的碳含量;碳同位素分辨率的值在18.92—20.48‰之间,不同部位碳同位素分辨率值变化表现为ΔR<ΔS<ΔL。不同时期方差分析结果与碳同位素值一致,只有根部的差异达到显著水平,而茎和叶的差异不明显。
| 生长时期 Growth stage | 碳同位素比值(δ13C) Carbon isotope ratio/‰ | 碳含量 Carbon content/% | 碳同位素分辨率(Δ) Carbon isotope discrimination/‰ | ||||||
| δ13CR | δ13CS | δ13CL | 根 Root | 茎 Stem | 叶 Leaf | ΔR | ΔS | ΔL | |
| S1 | -28.52±0.04b | -29.23±0.28a | -29.48±0.12a | 32.14±0.85a | 40.81±0.66b | 40.63±1.47b | 19.48±0.04a | 20.22±0.29b | 20.48±0.13b |
| S2 | -28.36±0.12b | -28.82±0.14ab | -29.09±0.13a | 29.98±4.05a | 25.42±0.05a | 30.67±2.82a | 19.39±0.12a | 19.87±0.15ab | 20.15±0.14ab |
| S3 | -29.25±0.20a | -29.21±0.17a | -29.12±0.12a | 27.80±0.35a | 29.77±0.33a | 28.07±0.78a | 20.23±0.21b | 20.19±0.18b | 20.10±0.13ab |
| S4 | -28.51±0.07b | -28.03±0.47b | -29.02±0.20a | 38.83±0.53b | 39.76±4.36b | 40.03±0.42b | 19.43±0.07a | 18.92±0.49a | 19.96±0.22a |
| 均值Mean | -28.66 | -28.82 | -29.18 | 32.19 | 33.94 | 34.85 | 19.63 | 19.80 | 20.17 |
| Sig | ** | NS | NS | ** | ** | ** | ** | NS | NS |
不同生长时期决明子不同部位(根、茎、叶)稳定碳同位素值计算得出的WUE(分别记为WUER、WUES、WUEL)和盆栽称重法得出的WUE分析结果见表 3。就均值来看,随着生长时期的增加,WUER、WUES、WUEL和WUE均呈现逐渐增加的规律;方差分析显示,在不同生长时期,各水分利用效率差异均达极显著水平,而在同一时期不同部位和方法得出的WUE只有在苗期达到显著水平,其它时期各WUE之间差异均不显著。
| 生长时期Growth stage | WUEL | WUES | WUER | WUE | Sig |
| 同行的相同大写字母表示差异不显著,不同的大写字母表示差异显著(P=0. 05),其它标注同表 1; WUER、WUES、WUEL分别表示利用稳定碳同位素方法测定的决明子根、茎、叶的水分利用效率;WUE表示利用称重法测定的决明子水分利用效率;
WUER、WUES、WUEL indicate respectively water use efficiency of root、steam and leaf of Cassia obtusifolia L. by stable carbon isotope method;WUE indicate the measurement of water use efficiency of Cassia obtusifolia L. by weight method |
|||||
| S1 | 1.83±0.03aA | 1.91±0.08aA | 2.12±0.01aA | 0.95±0.23aB | ** |
| S2 | 2.26±0.05bA | 2.36±0.05bA | 2.51±0.04bA | 2.25±0.15bA | NS |
| S3 | 2.61±0.05cA | 2.57±0.07bA | 2.56±0.08bA | 2.33±0.22bA | NS |
| S4 | 2.86±0.09dAB | 3.29±0.20cA | 3.08±0.03cAB | 2.69±0.15bB | NS |
| Sig | ** | ** | ** | ** | — |
决明子不同器官(根、茎、叶)的稳定碳同位素值、分辨率、水分利用效率和盆栽称重法得出的WUE相关分析结果(表 4和图 2)表明:δ13CL、δ13CS、δ13CR与ΔL、ΔS、ΔR分别呈极显著负相关(相关系数均达到0.99);δ13CL、δ13CS分别与WUEL、WUES及WUE呈显著正相关;ΔL、ΔS分别与WUEL、WUES及WUE呈显著负相关;δ13CR和ΔR则与各个WUE相关性均无达到显著水平。WUE与WUEL、WUES、WUER均达到极显著正相关水平(P<0.01),其中与WUEL相关系数最大为0.86,其次是WUER为0.82,与WUES的相关系数为0.80。
| 指标Index | ΔL | ΔS | ΔR | WUEL | WUES | WUER | WUE |
| δ13CL | -0.99* * | 0.72* * | 0.84* * | ||||
| δ13CS | -0.99* * | 0.83* * | 0.63* | ||||
| δ13CR | -0.99* * | 0.09 | -0.01 | ||||
| ΔL | -0.78* * | -0.82* * | |||||
| ΔS | -0.84* | -0.61* | |||||
| ΔR | -0.14 | 0.01 | |||||
| WUEL | 0.86* * | ||||||
| WUES | 0.80* * | ||||||
| WUER | 0.82* * |
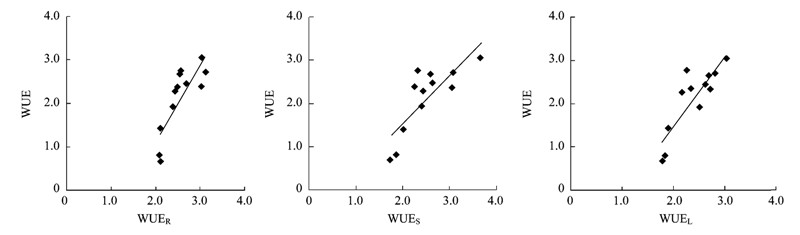
|
|
图 2
两种方法WUE回归分析
Fig. 2
Regression analysis for WUE of the two methods
WUER、WUES、WUL分别表示利用稳定碳同位素方法测定的决明子根、茎、叶的水分利用效率;WUE表示利用称重法测定的决明子水分利用效率 WUER、WUES、WUEL indicate respectively water use efficiency of root、steam and leaf of Cassia obtusifolia L. by stable carbon isotope method;WUE indicate the measurement of water use efficiency of Cassia obtusifolia L. by weight method |
随着生长时期的增加,决明子地上和地下生物量都不断地增加,生长速率呈现出生长前期快速增长,中期增长缓慢,后期降低的趋势;根冠比随着生长时期的增加而不断地减小;根、茎、叶的碳含量在25.42%—40.81%之间,在苗期和成熟期较高,生长中期较少,不同生长期间差异显著,地下根部碳含量明显低于地上茎、叶的碳含量;耗水量与生物量同步,随着生长时期的增加而不断的增加,各个时期的差异都较明显,这是由于植物光合作用同化的有机物质越多需要参与反应和消耗的水分也越多,与Abbate等大多数学者得出的结论一致[10]。
3.2 决明子碳同位素组成特点及其与WUE关系决明子碳同位素比值在-29.48‰—-28.03‰之间变化,平均值为-28.89‰,这与全球范围调查的植物δ13C 平均值(-28.74‰)相接近[20]。不同部位碳同位素比值变化表现为根>茎>叶,这与多数学者的研究结果相同,如冯虎云等[21]对大豆(Glycine max Merr.)10个品种的δ13C值研究表明,δ13C根>δ13C茎>δ13C种子>δ13C叶;Carol和Winner报道小麦(Triticum aestivum Linn.)根中δ13C值高于叶片[22];方晓娟等[23]研究毛白杨(Populus tomentosa)不同部位碳同位素比值,结果显示叶片<小枝<根。造成这种差异可能是由于植物不同器官生物化学成分不同,生理生态特性差异较大[24]。因为合成这些物质的途径不同会出现不同的碳同位素二次分馏,从而使各种化学成分具有不一样的碳同位素比率。碳同位素分辨率的值在18.92—20.48‰之间,不同部位碳同位素分辨率值变化同碳同位素比值相反,表现为根<茎<叶,不同时期方差分析结果与碳同位素值一致,都是只有根部差异达到显著水平,而茎和叶差异不明显。与以往的大多数研究结果一致[8, 14, 15, 16, 19],决明子叶片、茎的稳定碳同位素比值与分辨率呈负相关、两者与水分利用效率分别呈正相关和显著负相关。
3.3 称重法与稳定碳同位素法测定决明子WUE的关系称重法和稳定碳同位素法测定决明子水分利用效率相关分析表明,WUE与WUEL、WUES、WUER均呈显著的正线性相关,其中与WUEL相关系数最大。说明用稳定碳同位素方法估算决明子的长期水分利用效率是可靠的,相比决明子其他器官,用叶片的稳定碳同位素比率来估算更为可靠,由于植物叶片δ13C包含了各种各样的环境信息,它的优点是易于进行横向及纵向的验证和对比[25, 26],并且叶片取样较为简单、对植物破坏性也小,因此可以作为测定决明子长期水分利用效率的可靠指标。
| [1] | Zhang J S, Meng P. Simulation on water ecological characteristics of agroforestry in the hilly area of Taihang Mountain. Acta Ecologica Sinica, 2004, 24(6): 1172-1178. |
| [2] | Sun S J, Meng P, Zhang J S, Huang H, Wan X C. Deuterium isotope variation and water use in an agroforestry system in the rocky mountainous area of North China. Acta Ecologica Sinica, 2010, 30(14): 3717-3726. |
| [3] | Bohn B A, Kershner J L. Establishing aquatic restoration priorities using a watershed approach. Journal of Environmental Management, 2002, 64(4): 355-363. |
| [4] | Munns R. Genes and salt tolerance: Bringing them together. New Phytologist, 2005, 167(3): 645-663. |
| [5] | Sun X K, Fan Z P, Wang H, Bai J, Zhang Y, Deng D Z. Photosynthetic characteristics and water use efficiency of three broad-leaved tree species in the horqin sandland. Journal of Arid Land Resources and Environment, 2008, 22(10): 188-194. |
| [6] | Jaleel C A, Gopi R, Sankar B, Gomathinayagam M, Panneerselvam R. Differential responses in water use efficiency in two varieties of Catharanthus roseus under drought stress. Comptes Rendus Biologies, 2008, 331(1): 42-47. |
| [7] | Pieters A J, Núñez M. Photosynthesis, water use efficiency, and δ13C in two rice genotypes with contrasting response to water deficit. Photosynthetica, 2008, 46(4): 574-580. |
| [8] | Farquhar G D, Ehleringer J R, Hubick K T. Carbon isotope discrimination and photosynthesis. Annual Review of Plant Physiology and Plant Molecular Biology, 1989, 40(1): 503-537. |
| [9] | Wang J L, Yang X M, Fang Q X. The expatiation on mensurating method of field water use efficiency in different scale. Chinese Agricultural Science Bulletin, 2010, 26(6): 77-80. |
| [10] | Abbate P E, Dardanelli J L, Cantarero M G, Maturano M, Melchiori R J M, Suero E E. Climatic and water availability effects on water-use efficiency in Wheat. Crop Science, 2004, 44(2): 474-484. |
| [11] | Tomás M, Medrano H, Pou A, Escalona J M, Martorell S, Ribas-Carbó M. Water-use efficiency in grapevine cultivars grown under controlled conditions: effects of water stress at the leaf and whole-plant level. Australian Journal of Grape and Wine Research, 2012, 18(2): 164-172. |
| [12] | Joshua L A, Ann S E. Physiological variation among Populus fremontii populations: short-and long-term relationships between δ13C and water availability. Tree Physiology, 2001, 21(15): 1149-1155. |
| [13] | Zhu X, Hu Y, Wang X L, Chen S. Effects of several plant growth regulators on seed germinating and seedling growth of Cassia seed. Crops, 2010, (1): 46-48. |
| [14] | Farquhar G D, O'Leary M H, Berry J A. On the relationship between carbon isotope discrimination and the intercellular carbon dioxide concentration in leaves. Australian Journal of Plant Physiology, 1982, 9(2): 121-137. |
| [15] | Anyia A O, Slaski J J, Nyachiro J M, Archambault D J, Juskiw P. Relationship of carbon isotope discrimination to water use efficiency and productivity of barley under field and greenhouse conditions. Journal of Agronomy and Crop Science, 2007, 193(5): 313-323. |
| [16] | Chen J, Chang S X, Anyia A O. The physiology and stability of leaf carbon isotope discrimination as a measure of water-use efficiency in barley on the Canadian prairies. Journal of Agronomy and Crop Science, 2011, 197(1): 1-11. |
| [17] | Evans J R. Nitrogen and photosynthesis in the flag leaf of wheat (Triticum aestivum L.). Plant Physiology, 1983, 72(2): 297-302. |
| [18] | Lu P, Urban L, Zhao P. Granier's thermal dissipation probe (TDP) method for measuring sap flow in trees: theory and practice. Acta Botanica Sinica, 2004, 46(6): 631-646. |
| [19] | Hu J, Moore D J P, Riveros-Iregui D A, Burns S P, Monson R K. Modeling whole-tree carbon assimilation rate using observed transpiration rates and needle sugar carbon isotope ratios. New Phytologist, 2010, 185(4): 1000-1015. |
| [20] | Sun H L, Wang S M, Ma J Y, Zhang X. Study on stable carbon isotope composition in ephemeral plants in the Junggar basin. Arid Zone Research, 2007, 24(5): 652-656. |
| [21] | Feng H Y, Chen T, Xu S J, An L Z, Qiang W Y, Zhang M X, Wang X L. Effect of enhanced UV-B radiation on growth, yield and stable carbon isotope composition in glycine max cultivars. Acta Botanica Sinica, 2001, 43(7): 709-713. |
| [22] | Greitner C S, Winner W E. Increased in δ13C values of radish and soybean plants caused by ozone. New Phytologist, 1988, 108(4): 489-494. |
| [23] | Fang X J, Li J Y, Nie L S, Shen Y B, Zhang Z Y. The characteristics of stable carbon isotope and water use efficiency for Populus tomentosa hybrid clones. Ecology and Environmental Sciences, 2009, 18(6): 2267-2271. |
| [24] | Yan C R, Han X G, Chen L Z. Water use efficiency of six woody species in relation to micro-environmental factors of different habitats. Acta Ecologica Sinica, 2001, 21(11): 1952-1956. |
| [25] | Su B, Han X G, Li L H, Huang J H, Bai Y F, Qu C M. Responses of δ13 C value and water use effieicency of plant species to environmental gradients along the grassland zone of northeast China transect. Acta Phytoecologica Sinica, 2000, 24(6): 648-655. |
| [26] | Chen T, Feng H Y, Xu S J, Qiang W Y, An Z L. Stable carbon isotope composition of desert plant leaves and water-use efficiency. Journal of Desert Research, 2002, 22(3): 288-291. |
| [1] | 张劲松, 孟平. 农林复合系统水分生态特征的模拟研究. 生态学报, 2004, 24(6): 1172-1178. |
| [2] | 孙守家, 孟平, 张劲松, 黄辉, 万贤崇. 华北石质山区核桃-绿豆复合系统氘同位素变化及其水分利用. 生态学报, 2010, 30(14): 3717-3726. |
| [5] | 孙学凯, 范志平, 王红, 白洁, 张营, 邓东周. 科尔沁沙地复叶槭等3个阔叶树种的光合特性及其水分利用效率. 干旱区资源与环境, 2008, 22(10): 188-194. |
| [9] | 王建林, 杨新民, 房全孝. 不同尺度农田水分利用效率测定方法评述. 中国农学通报, 2010, 26(6): 77-80. |
| [13] | 朱霞, 胡勇, 王晓丽, 陈诗. 几种植物生长调节剂对决明种子萌发及幼苗生长的影响. 作物杂志, 2010, (1): 46-48. |
| [20] | 孙惠玲, 王绍明, 马剑英, 张霞. 准噶尔盆地早春短命植物碳同位素组成研究. 干旱区研究, 2007, 24(5): 652-656. |
| [21] | 冯虎元, 陈拓, 徐世健, 安黎哲, 强维亚, 张满效, 王勋陵. UV-B辐射对大豆生长、产量和稳定碳同位素组成的影响. 植物学报, 2001, 43(7): 709-713. |
| [23] | 方晓娟, 李吉跃, 聂立水, 沈应柏, 张志毅. 毛白杨杂种无性系稳定碳同位素值的特征及其水分利用效率. 生态环境学报, 2009, 18(6): 2267-2271. |
| [24] | 严昌荣, 韩兴国, 陈灵芝. 六种木本植物水分利用效率和其小生境关系研究. 生态学报, 2001, 21(11): 1952-1956. |
| [25] | 苏波, 韩兴国, 李凌浩, 黄建辉, 白永飞, 渠春梅. 中国东北样带草原区植物δ13C值及水分利用效率对环境梯度的影响. 植物生态学报, 2000, 24(6): 648-655. |
| [26] | 陈拓, 冯虎元, 徐世建, 强维亚, 安黎哲. 荒漠植物叶片碳同位素组成及其水分利用效率. 中国沙漠, 2002, 22(3): 288-291. |
 2014, Vol. 34
2014, Vol. 34