文章信息
- 高梅香, 孙新, 吴东辉, 张雪萍
- GAO Meixiang, SUN Xin, WU Donghui, ZHANG Xueping
- 三江平原农田土壤跳虫多尺度空间自相关性
- Spatial autocorrelation at multi-scale of soil collembolan community in farmland of the Sanjiang Plain, Northeast China
- 生态学报, 2014, 34(17): 4980-4990
- Acta Ecologica Sinica, 2014, 34(17): 4980-4990
- http://dx.doi.org/10.5846/stxb201301060040
-
文章历史
- 收稿日期:2013-1-6
- 网络出版日期:2014-3-5
2. 中国科学院东北地理与农业生态研究所, 长春市 130012
2. Northeast Institute of Geography and Agroecology, Chinese Academy of Sciences, Changchun 130012, China
土壤动物作为重要的生态因子存在显著的空间分布格局,研究土壤有机体的空间分布格局及其驱动因子是近些年来科学研究的重要领域[1]。然而物种在一定范围内的空间分布常常表现出空间自相关性,即彼此接近的样点比相互远离的样点具有更大的相似性[2]。当存在正的空间自相关性的时候,若使用传统标准方法(如ANOVA,相关分析和回归分析)来检验统计假设,标准误差常常会被低估,结果会引起统计分析中Type I errors的产生[3]。因此,识别土壤动物的空间自相关性特征,是准确揭示土壤动物空间异质性和空间共存格局的重要前提。
许多研究表明土壤动物存在显著的空间自相关性,如研究发现土壤有机体在<100 m的野外尺度内很少空间独立[4]。土壤动物的空间自相关性依赖于空间尺度,不同尺度条件下的空间自相关性特征可能是不同的。空间尺度是指研究某一事物或现象时所采用的空间单位,同时又可指某一现象或过程在空间上所涉及的范围和发生的频率。目前有很多研究致力于揭示不同尺度条件下土壤动物的空间特征,如Jiménez J J等[5]在1个50 m×50 m的样方内,对不同尺度条件下蚯蚓的空间特征进行了分析,结果表明蚯蚓群落存在明显的多尺度空间自相关性。但对于多尺度条件下土壤跳虫空间特征的研究相对少见。
我国土壤动物空间生态学研究开展已久,研究者对土壤动物的生态地理分布进行了广泛的调查研究[6],但有关土壤动物空间自相关性的研究仍然十分缺乏。本文以三江平原农田生态系统土壤跳虫为研究对象,使用规则采样点的方法设置50 m×50 m的空间样方,通过全局空间自相关性和局部空间自相关性相结合的方法,来研究土壤跳虫的多尺度空间自相关性特征,为土壤动物空间异质性和空间共存机制的研究打下基础。
1 研究地区与研究方法 1.1 研究区概况三江平原位于黑龙江省东部,包括完达山以北的松花江、黑龙江和乌苏里江冲积形成的低平原和完达山以南乌苏里江支流与兴凯湖形成的冲-湖积平原。是中国最大的淡水沼泽湿地集中分布区,现在已经成为重要的粮食生产基地。试验在中国科学院三江平原沼泽湿地生态实验站内进行 (133°31 ′ E,47°35′ N),研究区属温带大陆性季风气候区,年平均气温1.9 ℃,年均降水量约600 mm,降水集中在7—9月,地貌类型为三江平原沼泽发育最为普遍的碟形洼地;土壤为草甸沼泽土、腐殖质沼泽土、泥炭沼泽土、潜育白浆土和草甸白浆土。
1.2 样地设置与野外调查方法实验样地设置在沼泽湿地开垦的大豆地内,土壤类型为白浆土,具30 a以上的开发历史。在远离排水沟的中心区域,选择一块50 m×50 m的样地,将样地以5 m为间隔等间距划分为100个5 m×5 m的小样方,以此来揭示土壤跳虫空间自相关性特征。样方设置完毕,在每个网格样方内,以左下角网格线交叉点为中心,以15 cm为半径,用内径为7 cm的土钻随机采集4个10 cm深的土柱作为一个空间采样点采集土壤跳虫样品。野外样品于2011年8月和10月进行采集。回到室内采用Tullgren干漏斗法进行分离,分离结束后显微镜下鉴定种类并计数。
1.3 数据处理分析方法 1.3.1 土壤跳虫种类数量和平均密度差异性检验单因素方差分析比较8月和10月跳虫种类数量和平均密度的差异显著性,软件平台选择SPSS 19.0。
1.3.2 空间自相关分析空间自相关所统计的内容包括空间变量的空间位置及其属性,即每个变量与其相邻统计分析变量之间的空间位置关系以及属性取值特征。表示空间自相关的指标和方法很多,其中最常用的是Moran′s I指数。Moran′s I值一般可分为全局空间自相关(Global spatial autocorrelation)和局部空间自相关(Local spatial autocorrelation)两种[7]。
(1) 全局Moran′s I分析
应用全局Morans′ I统计判断一个区域是否存在空间聚集的结果比较可靠,并且可以通过属性值的相对大小直接判断是高值聚集还是低值聚集。其表达式如下:
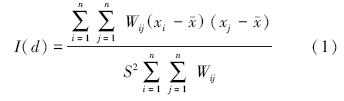
其中:
式中,n为参与分析的土壤跳虫样品的数目,xi和xj分别为样品i和样品j的观测值; 为所有样品观测值的平均值,Wij空间权重矩阵值,表示空间单元i和j的空间关系,当空间单元i和j为邻近的空间单元时,Wij =1,反之Wij=0。
在空间随机分布零假设下,I的预期值E(I)=-1/(n-1)。当被检验样本足够多时,E(I)接近于0。Moran′s I的值域为[-1, 1],Moran′s I值为0时,代表种群不存在空间自相关;Moran′s I值大于0,说明全局自相关性是正相关,小于0为负相关关系,其绝对值越大,说明自相关程度越大。正空间自相关代表相邻空间具有相似的特征或属性,负空间自相关则表示相邻空间具有不同的属性或特征。Moran′s I偏离预期值的显著程度采用标准正态偏差法检验。
(2) 局部Moran′s I分析
全局Moran′s I值从总体上反映了研究种群的空间自相关性,它不能反映局部区域是正相关还是负相关以及相关程度,而局部空间自相关提供了每个空间单元自相关性的判断。局部Moran′s I指标的计算公式如下:
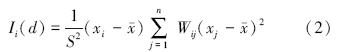
其中: 
在完全随机的假定下,Ii的理论平均值为E(Ii)=-Wi/(n-1) 。局部Moran′s I值可以对土壤动物密度的空间格局进行可视化,便于进一步研究其空间分布规律。本研究利用局部空间自相关指标结合Lisa聚类图将土壤跳虫空间分布划分为5种类型:“高—高”、“低—低”为空间聚集 (Spatial clusters),表示高高相邻或低低相邻,即某观测点自身和该观测点周围其它观测点的跳虫密度都较高或较低,同一聚集类型中土壤跳虫密度的空间差异程度显著较小;“高—低”、“低—高”为空间孤立 (Spatial outliers),表示高低相邻,即某观测点自身土壤跳虫密度较高 (或较低),而该观测点周围其它观测点的土壤跳虫密度较低 (或较高),同一聚集类型中土壤跳虫密度的空间差异程度显著较大;“不显著”表示某观测点与其周围观测点的土壤跳虫密度空间差异不显著。
全局Moran′s I指数和局部Moran′s I指数在Geoda 1.0.0软件平台上实现(http://geodacenter.asu.edu/software/downloads)。
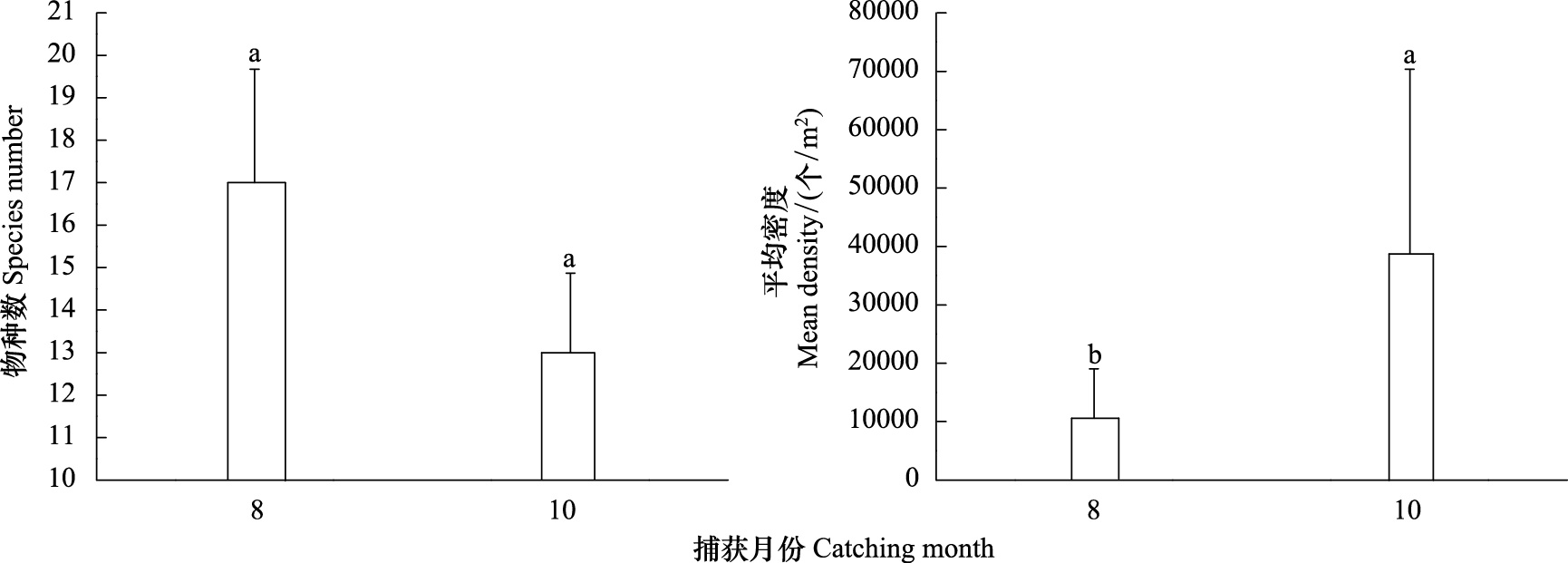
2 结果与分析 2.1 土壤跳虫群落统计特征8 月和10月分别捕获土壤跳虫17和13种,差异不显著;平均密度分别为10603.62和38698个/m2,差异显著(P<0.001) (图 1)。捕获的跳虫隶属于11属6科。其中小角棘跳属 (Oligaphorura ursi Fjellberg,1984) 和土跳属 (Tullbergia sp.1) 在8月和10月均为优势类群 (密度占总密度的10%以上)。8月份,Protaphorura sp.1、异棘跳属 (Allonychiurus songi Sun & Wu,2012)、小圆跳属 (Sminthurinus sp.1)、符跳属 (Folsomia sp.1)、德跳属 (Desoria sp.1)、长跳属 (Entomobrya sp.2)和鳞长跳属 (Hypogastrura sp.1)为常见类群 (密度占总密度的比例介于1%—10%之间);至10月份,除了小圆跳属 (Sminthurinus sp.1)、符跳属 (Folsomia sp.1)、长跳属 (Entomobrya sp.2)和鳞长跳属 (Hypogastrura sp.1)外,其他常见类群仍保持数量上的优势,另外,紫球角跳属 (Hypogastrura sp.1)在10月份成为常见类群。其余类群为稀有类群 (密度占总密度的比例<1%)。变异系数 (CV)表明,所有的土壤跳虫均表现出很强的空间变异性 (表 1)。
|
| 图 1 土壤跳虫群落种类数量和平均密度 (图中误差棒为标准误) Fig. 1 Species number and mean density of soil collembolan community (The bars are standard errors) |
| 物种 Species | 科 Family | 8月 August | 10月 October | ||||||
| 均值/(个/m2) Mean | 标准差 Standard Deviation | 密度百分比 Percentage of density/% | 变异系数 Coefficient of variation/% | 均值/(个/m2) Mean | 标准差 Standard Deviation | 密度百分比 Percentage of density/% | 变异系数 Coefficient of variation/% | ||
| J1: Protaphorura sp.1; J2: 异棘跳属 (Allonychiurus songi); J3: 小角棘跳属 (Oligaphorura ursi); Y1: 小圆跳属 (Sminthurinus sp.1); Y2: 齿棘圆跳属(Arrhopalites sp.1); Y3: 小圆跳属 (Sminthurinus sp.2); Y4: Sphyrotheca sp.1; Tu: 土跳属 (Tullbergia sp.1) D1: 符跳属 (Folsomia sp.2); D2: 符跳属 (Folsomia sp.1); D3: 德跳属 (Desoria sp.1); C1: 长跳属 (Entomobrya sp.2); C2: 长跳属 (Entomobrya sp.1); C4: 长跳属 (Entomobrya sp.3); C6: 长跳属 (Entomobrya koreana); C8: 紫球角跳属 (Hypogastrura sp.1); Z: 鳞长跳属 (Lepidocyrtus felipei) | |||||||||
| J1 | 棘跳科Onychiuridae | 281.28 | 431.70 | 2.65 | 153 | 611.93 | 1167.70 | 1.58 | 191 |
| J2 | 棘跳科Onychiuridae | 628.82 | 885.90 | 5.93 | 141 | 1367.43 | 1972.30 | 3.53 | 144 |
| J3 | 棘跳科Onychiuridae | 6603.96 | 6500.50 | 62.28 | 98 | 30075.09 | 27706.97 | 77.72 | 92 |
| Y1 | 圆跳科Sminthuridae | 381.32 | 334.40 | 3.60 | 88 | 31.18 | 129.09 | 0.08 | 414 |
| Y2 | 圆跳科Sminthuridae | 26.63 | 53.12 | 0.25 | 199 | 85.75 | 155.02 | 0.22 | 181 |
| Y3 | 圆跳科Sminthuridae | 20.14 | 85.47 | 0.19 | 424 | ||||
| Y4 | 圆跳科Sminthuridae | 12.34 | 39.92 | 0.12 | 323 | ||||
| Tu | 土跳科Tullbergiidae | 1606.49 | 1629.31 | 15.15 | 101 | 3891.18 | 3969.26 | 10.06 | 102 |
| D1 | 等跳科Isotomidae | 38.98 | 131.88 | 0.37 | 338 | ||||
| D2 | 等跳科Isotomidae | 147.46 | 436.78 | 1.39 | 296 | 248.80 | 347.08 | 0.64 | 140 |
| D3 | 等跳科Isotomidae | 345.59 | 730.47 | 3.26 | 211 | 1157.61 | 2229.26 | 2.99 | 193 |
| C1 | 长角跳科Entomobryidae | 289.08 | 252.08 | 2.73 | 87 | 137.07 | 175.89 | 0.35 | 128 |
| C2 | 长角跳科Entomobryidae | 5.20 | 23.86 | 0.05 | 459 | 5.20 | 19.97 | 0.01 | 384 |
| C4 | 长角跳科Entomobryidae | 17.54 | 44.14 | 0.17 | 252 | 207.23 | 293.68 | 0.54 | 142 |
| C6 | 长角跳科Entomobryidae | 0.65 | 6.50 | 0.01 | 1000 | ||||
| C8 | 长角跳科Entomobryidae | 18.19 | 65.34 | 0.17 | 359 | 558.67 | 1592.18 | 1.44 | 285 |
| Z | 紫球角跳科Hypogasturidae | 179.94 | 199.93 | 1.70 | 111 | 321.56 | 451.14 | 0.83 | 140 |
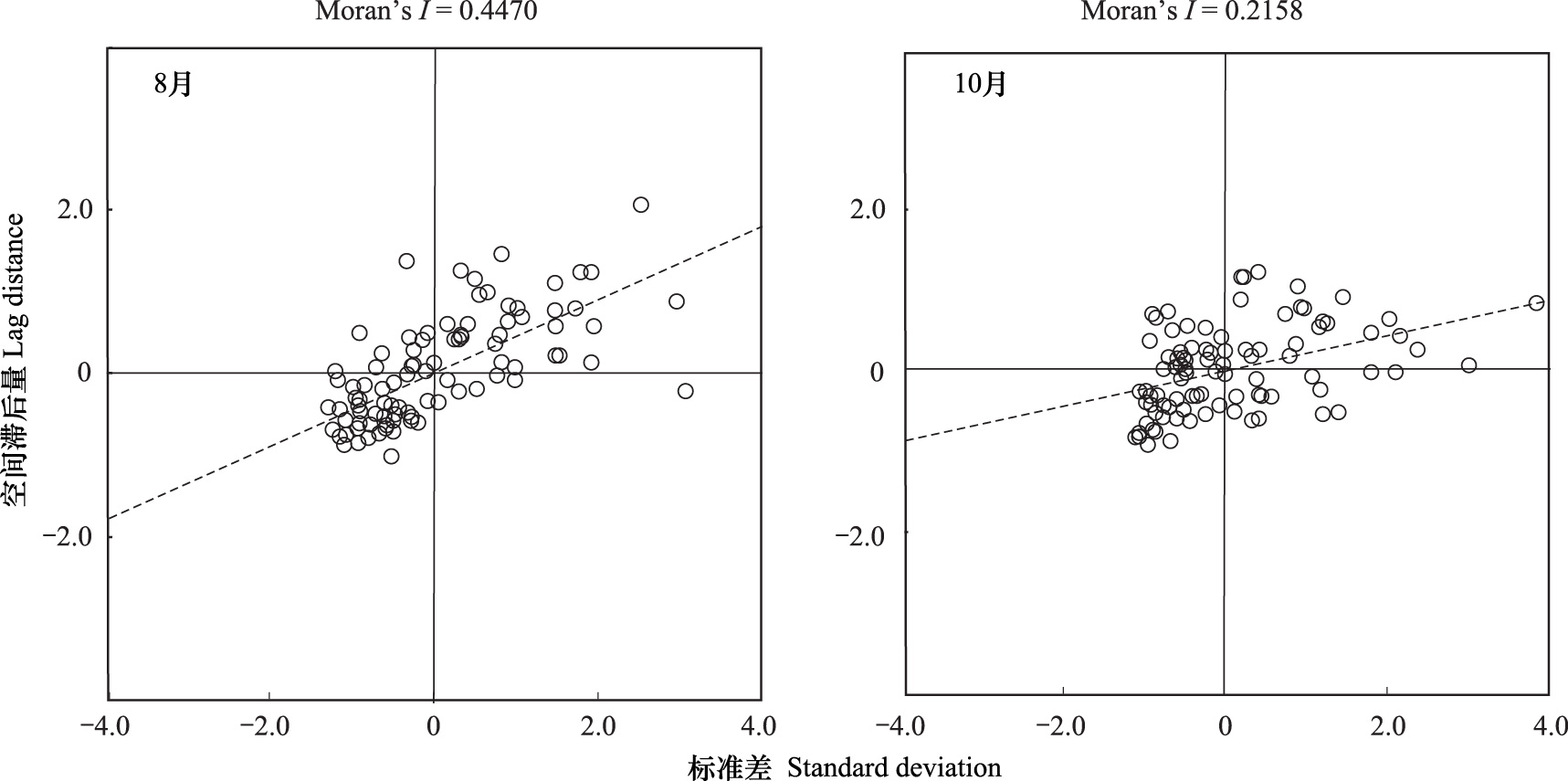
图 2为土壤跳虫群落总密度的Moran I散点图。第一、三象限代表土壤跳虫密度正的空间相关联系,第二、四象限代表负的空间相关联系。其中第一象限代表了土壤跳虫密度高值采样点为其他高值采样点所包围 (高—高);第二象限代表了土壤跳虫密度低值采样点为其它高值采样点所包围 (低—高);第三象限代表了土壤跳虫密度低值采样点为其它低值采样点所包围 (低—低);第四象限代表了跳虫密度高值采样点为其它低值采样点所包围 (高—低)。在研究样地,8月份分别有32个和52个采样点落在第一和第三象限内,二者合计占总样点数的84%;分别有9个和7个采样点落在第二和第四象限内,二者合计占总样点数的16%;说明多数采样点表现出“高—高”集聚和“低—低”集聚的类型。10月份分别有 23个和42个采样点落在第一和第三象限内,二者合计占总样点数的65%;分别有21个和14个采样点落在第二和第四象限内,二者合计占总样点数的35%;说明多数采样点表现出“高—高”和“低—低”集聚的类型。
|
| 图 2 土壤跳虫总密度的Moran′s I散点图 Fig. 2 Moran′ I scatter plot of soil collembolan community mean density |
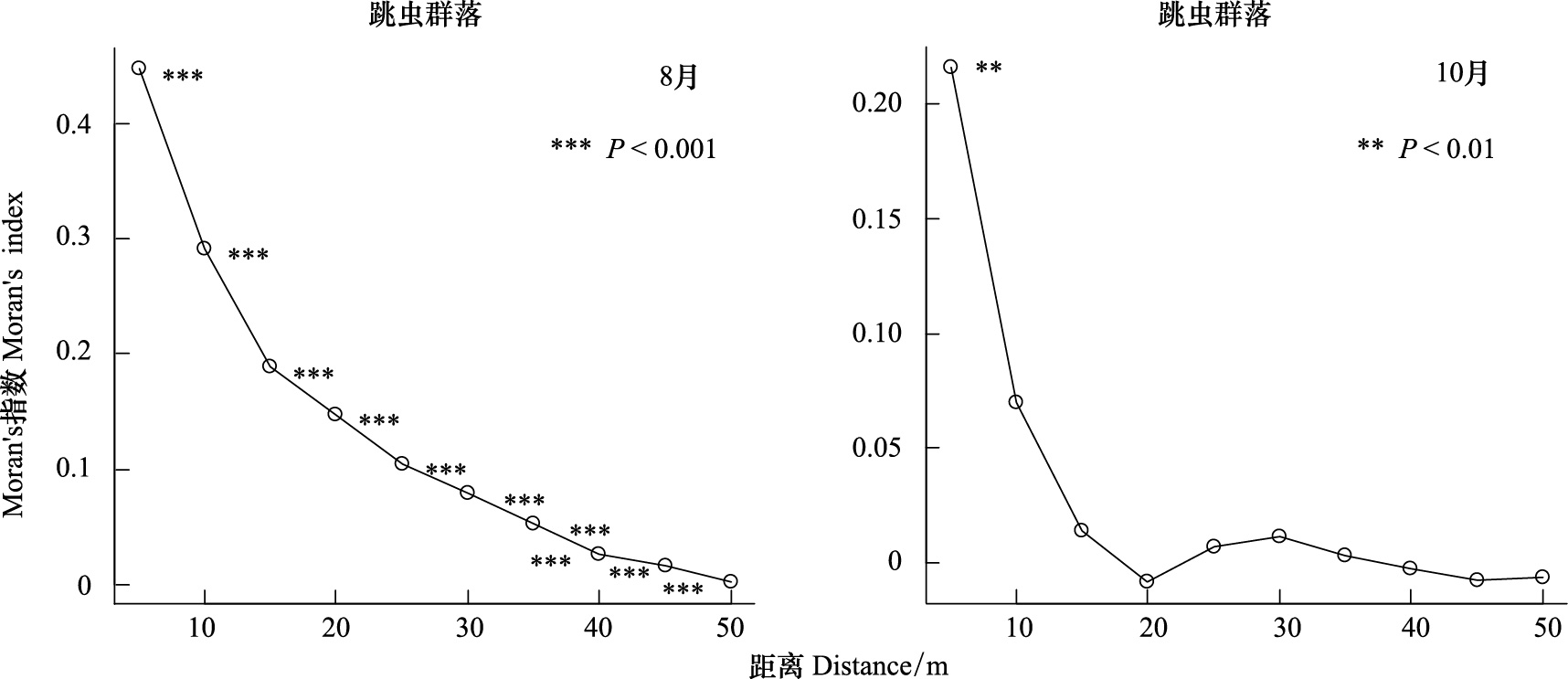
将Moran′s I指数与步长相结合,便可得到跳虫群落总密度的多尺度空间自相关变化。8月份,跳虫群落总密度的Moran′s I系数在5—50 m尺度内均表现出极显著的正的空间自相关性(P<0.001),形成特定的空间集群。10月份,跳虫群落总密度的Moran′s I系数在5 m尺度表现为显著的正的空间自相关(P<0.01),其他尺度均没有显著的空间自相关 (图 3)。
|
| 图 3 不同尺度土壤跳虫总密度的空间自相关性 Fig. 3 Spatial correlograms of soil collembolan community mean density at different scale |
表 2列举出不同土壤跳虫种类多尺度全局Moran′s I指数。小角棘跳属(Oligaphorura ursi),8月份在5—50 m的尺度内均为明显的正空间自相关性,10月份仅在5 m、35 m和40 m尺度上具有显著的正空间自相关性;Protaphorura sp.1、异棘跳属 (Allonychiurus songi)、小圆跳属 (Sminthurinus sp.1)、土跳属 (Tullbergia sp.1)、德跳属 (Desoria sp.1)、长跳属 (Entomobrya sp.3)、 紫球角跳属 (Hypogastrura sp.1)和鳞长跳属 (Lepidocyrtus felipei)于8月和10月分别在不同的尺度上具有显著的空间自相关性,多数为显著的正空间自相关性;符跳属 (Folsomia sp.2)和符跳属 (Folsomia sp.1)仅8月份在个别尺度上具显著的空间自相关性;其余6种跳虫在8月和10月均没有显著的多尺度空间自相关性,占捕获种数的35.29%。
| 尺度/m Scale | 月份 Month | J1 | J2 | J3 | Y1 | Y2 | Y3 | Y4 | Tu | D1 | D2 | D3 | C1 | C2 | C4 | C6 | C8 | Z |
| *P<0.05,**P<0.01,***P<0.001,E(I)=-0.0101; 序列数量(Permutations)=9999; J1: Protaphorura sp.1; J2: 异棘跳属 (Allonychiurus songi); J3: 小角棘跳属 (Oligaphorura ursi); Y1: 小圆跳属 (Sminthurinus sp.1); Y2: 齿棘圆跳属(Arrhopalites sp.1); Y3: 小圆跳属 (Sminthurinus sp.2); Y4: Sphyrotheca sp.1; Tu: 土跳属 (Tullbergia sp.1) D1: 符跳属 (Folsomia sp.2); D2: 符跳属 (Folsomia sp.1); D3: 德跳属 (Desoria sp.1); C1: 长跳属 (Entomobrya sp.2); C2: 长跳属 (Entomobrya sp.1); C4: 长跳属 (Entomobrya sp.3); C6: 长跳属 (Entomobrya koreana); C8: 紫球角跳属 (Hypogastrura sp.1); Z: 鳞长跳属 (Lepidocyrtus felipei) | ||||||||||||||||||
| 5 | 8 | 0.25* * * | 0.25* * * | 0.43* * * | 0.14* | -0.1 | -0.01 | -0.01 | 0.38* * * | 0.13* | 0.12* | 0.45* * * | 0.05 | 0.04 | 0.16* | -0.01 | 0.14* | 0.18* |
| 10 | 0.24* * | 0.30* * * | 0.22* * | 0.09* | 0.06 | 0.19* * | 0.10 | 0.42* * * | 0.03 | -0.01 | 0.01 | 0.44* * * | 0.15* | |||||
| 10 | 8 | 0.15* * | 0.15* * | 0.30* * * | 0.11* * | -0.03 | -0.03 | -0.05 | 0.22* * * | 0.03 | 0.05 | 0.26* * * | 0.03 | -0.02 | 0.08* | -0.01 | 0.06 | 0.09* |
| 10 | 0.21* * * | 0.24* * * | 0.06 | 0.01 | 0.02 | 0.14* * | 0.06 | 0.26* * * | 0.05 | -0.05 | 0.07* | 0.32* * * | 0.07 | |||||
| 15 | 8 | 0.10* * | 0.06* | 0.21* * * | 0.03 | -0.04 | -0.03 | -0.02 | 0.11* * * | 0.01 | 0.01 | 0.09* * | 0.01 | 0.00 | 0.06* | -0.01 | 0.01 | 0.05* |
| 10 | 0.16* * * | 0.15* * * | 0.01 | -0.02 | 0.02 | 0.12* * | 0.03 | 0.10* * | 0.02 | -0.01 | 0.01 | 0.17* * * | 0.06* | |||||
| 20 | 8 | 0.07* * | 0.03* | 0.16* * * | 0.02 | -0.02 | -0.03 | -0.01 | 0.05* | -0.01 | 0.0123 | 0.01 | 0.01 | 0.99 | 0.03* | -0.01 | -0.01 | 0.03* |
| 10 | 0.08* * | 0.07* * | -0.01 | -0.02 | 0.01 | 0.06* * | 0.02 | 0.03* | 0.01 | -0.01 | -0.01 | 0.10* * * | 0.06* * | |||||
| 25 | 8 | 0.01 | 0.05* * | 0.11* * * | -0.02 | -0.03 | -0.01 | -0.01 | -0.01 | -0.01 | 0.00 | -0.02 | -0.01 | -0.02 | 0.01 | -0.01 | 0.00 | 0.04* * |
| 10 | 0.02* | 0.00 | 0.01 | -0.02 | 0.01 | 0.01 | -0.01 | -0.01 | 0.00 | 0.00 | -0.01 | 0.05* * | 0.02 | |||||
| 30 | 8 | -0.01 | 0.05* * * | 0.09* * * | -0.02 | -0.03 | -0.01 | -0.01 | -0.03 | -0.02 | -0.01 | -0.03 | -0.01 | -0.02 | -0.01 | -0.01 | 0.00 | 0.02* * |
| 10 | -0.01 | -0.03 | 0.02* | -0.02 | 0.00 | -0.01 | -0.02 | -0.02 | -0.01 | -0.01 | -0.01 | 0.02* * | 0.01 | |||||
| 35 | 8 | -0.02 | 0.04* * * | 0.06* * * | -0.01 | -0.02 | -0.01 | -0.01 | -0.03* * | -0.03* * | 0.00 | -0.02 | -0.01 | -0.02 | -0.01 | -0.01 | 0.99 | 0.01* * |
| 10 | -0.03* * | -0.03* * * | 0.01* | -0.01 | -0.01 | -0.02 | -0.02 | -0.02 | -0.01 | -0.01 | -0.01 | 0.01* | 0.00 | |||||
| 40 | 8 | -0.03* * | 0.02* * * | 0.04* * * | -0.01 | -0.02 | -0.01 | -0.01 | -0.02 | -0.03* * * | 0.00 | -0.02* * | -0.02 | -0.02 | 0.00 | -0.01 | -0.01 | 0.00 |
| 10 | -0.03* * * | -0.03* * * | 0.01* | -0.01 | -0.01 | -0.02* | -0.01 | -0.02 | -0.02 | -0.01 | -0.02 | 0.00 | 0.01* | |||||
| 45 | 8 | -0.02* * | -0.01 | 0.02* * * | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | 0.00 | -0.01 | -0.01 | -0.01 |
| 10 | -0.02* * | -0.02* * | -0.01 | -0.01 | -0.01 | -0.02* | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | 0.00 | 0.00 | |||||
| 50 | 8 | -0.01* | -0.01 | 0.01* * * | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | 0.00 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 |
| 10 | -0.01* | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | -0.01 | 0.00 | 0.00 | -0.01 | -0.01 | 0.01* * * | -0.01 | |||||
全局空间自相关能够判断跳虫密度空间分布上是否存在空间聚集区和空间孤立区,可以描述跳虫密度的自相关系数随步长的变化,而局部空间自相关指标能够揭示跳虫密度的空间分布规律,指出跳虫密度空间聚集区和空间孤立区在研究区内的具体位置。
2.3.1 土壤跳虫群落总密度的局部空间自相关以土壤跳虫群落总密度为观测值,对样方内土壤跳虫的空间分布进行局部Moran′s I分析,结果见图 4。从8月份到10月份,土壤跳虫群落总密度均存在显著的局部空间自相关性。8月份,跳虫群落总密度存在两个明显的“高—高”空间聚集区斑块,其中一个较小的空间聚集区斑块位于样方的近中心区域,10月份仍能发现该斑块的痕迹,但斑块面积有所扩大;另一个较大的连续的空间聚集区斑块位于样方的右侧区域,至10月份仍稳定的占据样方的右侧区域,但空间分布区向右下角退缩。

|
| 图 4 跳虫群落总密度的空间聚类图 Fig. 4 Spatial cluster maps of soil collembolan community mean density |
8 月份,跳虫群落总密度存在两个明显的“低—低”空间聚集区斑块,分别位于样方的左上部偏中间和近中心区域。至10月份,这两个“低—低”空间聚集区斑块仍保留在原有区域附近,左上部斑块向右移动,近中心的斑块向右上方移动且斑块面积扩大。
8月份仅有“低—高”空间孤立区1个,伴随着“高—高”空间聚集区出现在样方的右下角;没有“高—低”空间孤立区的分布。10月份没有显著的“低—高”和“高—低”空间孤立区。
2.3.2 不同跳虫种类的局部空间自相关优势类群的小角棘跳属 (Oligaphorura ursi),8月份于样方右侧形成一个连续的面积较大的“高—高”空间聚集区,另外在样方的近中心区域存在一个面积较小的“高—高”空间聚集区;至10月份,样方右侧“高—高”空间聚集区明显变小,退缩到样方右侧中部区域。8月份于样方左上角形成一个面积很大的“低—低”空间聚集区,另外在样方的左下部近中心区域存在一个较小的“低—低”空间聚集区;至10月份,左上角“低—低”空间聚集区残存于原来的空间位置,但面积明显缩小,而左下部“低—低”空间聚集区向左侧偏移,但面积明显扩大。8月份的“低—高”空间孤立区伴随着显著的“高—高”空间聚集区出现在样方的右下角,至10月份消失 (图 5)。

|
| 图 5 3种跳虫的空间聚类图 Fig. 5 Spatial cluster maps of three collembolan species |
常见类群的Protaphorura sp.1,8月份存在明显的“高—高”空间聚集区,主要分布在样方的中下部区域;至10月份,该“高—高”空间聚集区面积缩小,退缩到样方的下部偏中间区域。8月份“低—低”空间聚集区存在两个斑块,分别位于样方的左上角和右上角区域;至10月份,这两个“低—低”空间聚集区仍残留于原来的位置,另外在样方的左侧和右侧偏中部区域新形成两个较小的“低—低”空间聚集区。8月和10月均存在“高—低”和“低—高”空间孤立区,面积较小,且空间分布范围略有变化 (图 5)。
稀有类群的齿棘圆跳属 (Arrhopalites sp.1),8月份“高—高”空间聚集区位于样方的上部近中心区域,且斑块面积较小;至10月份该斑块面积扩大,并向东侧移动。8月至10月均不存在显著的“低—低”空间聚集区。8月份存在显著的“低—高”空间孤立区,分别位于样方的上侧近中心区域和右下角区域;至10月份,“低—高”空间孤立区明显的分布于样方的右侧近中心区域,且斑块面积增大。8月份存在明显的“高—低”空间孤立区,从样方的左上角至右下角广泛分布,这些孤立区至10月份消失不见 (图 5)。
其他跳虫种类均存在显著的局部空间自相关性 (P<0.05),在局部地区形成“高—高”和/或“低—低”的空间聚集区以及“低—高”和/或“高—低”的空间孤立区。总体看来,从8月份至10月份,这些空间聚集区和空间孤立区的空间分布表现为一定的时间变动性,斑块大小和分布范围略有变化。
3 讨论本次调查共捕获土壤跳虫17种,隶属于5科11属。从水热条件较好的夏季(8月份)到土壤温度较低的秋季 (10月份),土壤跳虫种类数减少、捕获密度显著增加;优势类群的组成保持稳定,常见类群的组成略有变化;所有的跳虫种类都具有明显的空间变异性。
土壤跳虫总密度和大多数跳虫种类具有明显的多尺度空间自相关性特征,即存在明显的尺度效应。全局Moran′s I指数表明,夏季土壤跳虫群落总密度在5—50 m尺度内均表现出极显著的多尺度正空间自相关性;至土温较低的秋季,这种显著的正空间自相关性仅出现在5 m尺度上。其中,64.71%的跳虫种类在夏季和/或秋季具显著的多尺度空间自相关特征,基本为优势和常见类群;其余跳虫种类未发现显著的多尺度空间自相关性,且主要为稀有类群。许多研究证明土壤动物群落具多尺度的空间自相关性特征。Jiménez J J等[8]在以5 m×5 m为最小单元的50 m×50 m的空间尺度内,发现蚯蚓具明显的多尺度空间自相关性特征;Gutiérrez-López M等[9]在以16 m×14 m为最小单元的112 m×84 m的空间尺度内,发现蚯蚓、跳虫和螨类在多种距离水平具明显的空间自相关性。
空间集群是土壤跳虫的常见空间分布格局,并在局部地区呈现“斑块”和“孔隙”相间分布的镶嵌格局。本次调查发现春季和秋季,土壤跳虫群落总密度和多数跳虫种类具显著的正空间自相关性,在全局形成显著的空间集群。同时,土壤跳虫群落总密度和所有跳虫种类具明显的局部空间自相关特征,在局部地区形成显著的“高—高”和/或“低—低”的空间集群斑块,这些集群斑块往往与“高—低”和/或“低—低” 的“孔隙”相伴发生。Decans T和Rossi J P[10]在哥伦比亚的热带牧草生境发现空间集群是蚯蚓群落的常见特征,Rossi J P[11]也在蚯蚓群落发现了相似的特征,分别证明了“斑块”和“孔隙”这种水平镶嵌格局的存在。
土壤跳虫群落总密度和多数跳虫种类在局部地区形成的“斑块”和“孔隙”相间分布镶嵌格局具有一定的时间变异性。夏季,土壤跳虫在局部地区形成显著的“高—高”和/或“低—低”空间集群区;至秋季,仍能发现夏季空间集群斑块的痕迹,但斑块大小会略有变化,相应的空间分布范围略有移动。与此相伴发生的“高—低”和/或“低—高”空间孤立区也表现一定的时间动态性,“孔隙”的大小和范围略有变化。Decans T和Rossi J P[10]发现年内蚯蚓的“斑块”和“孔隙”分布格局具时间波动性,Pauli N[12]在短时间内发现蚯蚓排泄物空间斑块的时间变异性,Hernández P等[13]证实蚯蚓群落和一些蚯蚓种类的水平斑块格局表现出明显的年内变异性。
根据地理学第一定律,空间邻近的地理变量常常具空间自相关性[14],尺度是地理学研究的基本问题,不同尺度条件下的空间格局及形成机制可能会有不同[15]。因而,多尺度空间自相关性特征是土壤动物空间生态学研究的首要前提,更是土壤动物群落空间格局和生物多样性维持机制研究的重要基础。总体看来,土壤动物多尺度空间自相关性特征的研究主要集中于蚯蚓种群,少有研究对跳虫群落的多尺度空间自相关性研究开展系统的对比研究。本研究证明,土壤跳虫总密度和多数跳虫种类具明显的多尺度空间自相关性,为土壤动物空间格局及生物多样性维持机制的研究奠定基础。
4 结论本次调查发现,(1)土壤跳虫具有明显的多尺度空间自相关性特征,即存在明显的尺度效应。(2)空间集群是土壤跳虫的常见空间分布格局,并形成“斑块”和“孔隙”相间分布的水平镶嵌格局。(3)土壤跳虫的“斑块”和“孔隙”水平镶嵌格局具有年内时间变异性。
本研究仅能说明50 m×50 m的空间尺度内,年内土壤跳虫的多尺度空间自相关特征,大于或小于该时空尺度的自相关特征还有待于深入开展。
致谢: 感谢常亮、张兵、宋理洪对野外调查和样品分离的帮助。| [1] | Huston M A. Biological Diversity: The Coexistence of Species on Changing Landscapes. New York: Cambridge University Press, 1994. |
| [2] | Dormann C F, McPherson J M, Araújo M B, Bivand R, Bolliger J, Carl G, Davies R G, Hirzel A, Jetz W, Kissling W D, Kühn I, Ohlemüller R, Peres-Neto P R, Reineking B, Schröder B, Schurr F M, Wilson R. Methods to account for spatial autocorrelation in the analysis of species distributional data: a review. Ecography, 2007, 30(5): 609-628. |
| [3] | Legendre P. Spatial autocorrelation: trouble or new paradigm?. Ecology, 1993, 74(6): 1659-1673. |
| [4] | Robertson G P. Geostatistics in ecology: interpolating with known variance. Ecology, 1987, 68(3): 744-748. |
| [5] | Jiménez J J, Decaéns T, Amézquita E, Rao I, Thomas R J, Lavelle P. Short-range spatial variability of soil physico-chemical variables related to earthworm clustering in a neotropical gallery forest. Soil Biology and Biochemistry, 2011, 43(5): 1071-1080. |
| [6] | Yin X Q, Song B, Dong W H, Xin W D, Wang Y Q. A review on the eco-geography of soil fauna in China. Journal of Geographical Sciences, 2010, 20(3): 333-346. |
| [7] | Fortin M J, Dale M R T. Spatial Analysis: A Guide for Ecologists. New York: Cambridge University Press, 2005. |
| [8] | Jiménez J J, Decaéns T, Rossi J P. Soil environmental heterogeneity allows spatial co-occurrence of competitor earthworm species in a gallery forest of the Colombian ‘Llanos'. Oikos, 2012, 121(6): 915-926. |
| [9] | Gutiérrez-López M, Jesús J B, Trigo D, Fernández R, Novo M, Díaz-Cosín D J. Relationships among spatial distribution of soil microarthropods, earthworm species and soil properties. Pedobiologia, 2010, 53(6): 381-389. |
| [10] | Decaéns T, Rossi J P. Spatio-temporal structure of earthworm community and soil heterogeneity in a tropical pasture. Ecography, 2001, 24(6): 671-682. |
| [11] | Rossi J P. Short-range structures in earthworm spatial distribution. Pedobiologia, 2003, 47(5/6): 582-587. |
| [12] | Pauli N, Oberthür T, Barrios E, Conacher A J. Fine-scale spatial and temporal variation in earthworm surface casting activity in agroforestry fields, western Honduras. Pedobiologia, 2010, 53(2): 127-139. |
| [13] | Hernández P, Fernández R, Novo M, Trigo D, Díaz-Cosín D J. Geostatistical and multivariate analysis of the horizontal distribution of an earthworm community in El Molar (Madrid, Spain). Pedobiologia, 2007, 51(1): 13-21. |
| [14] | Keitt T H, Bjørnstad O N, Dixon P M, Citron-Pousty S. Accounting for spatial pattern when modeling organism-environment interactions. Ecography, 2002, 25(5): 616-625. |
| [15] | Gongalsky K B, Cividanes F J. Distribution of carabid beetles in agroecosystems across spatial scales-a review. Baltic Journal of Coleopterology, 2008, 8(1): 15-30. |
 2014, Vol. 34
2014, Vol. 34




