文章信息
- 卢群, 曾小康, 石俊慧, 陈里娥, 周凯, 雷安平, 昝启杰
- LU Qun, ZENG Xiaokang, SHI Junhui, CHEN Li'e, ZHOU Kai, LEI Anping, ZAN Qijie
- 深圳湾福田红树林群落演替
- Succession of a mangrove forest in Futian, Shenzhen Bay
- 生态学报, 2014, 34(16): 4662-4671
- Acta Ecologica Sinica, 2014, 34(16): 4662-4671
- http://dx.doi.org/10.5846/stxb201212271885
-
文章历史
- 收稿日期:2012-12-27
- 网络出版日期:2014-3-4
2. 广东内伶仃福田国家级自然保护区管理局, 深圳518040;
3. 深圳市海洋与渔业环境监测站, 深圳518067;
4. 深圳市东华园林绿化有限公司, 深圳518003
2. Neilingding-Futian National Nature Reserve of Guangdong, Shenzhen 518040, China;
3. Oceanic and Fishering Environment Monitoring Station of Shenzhen, Shenzhen 518067, China;
4. Shenzhen Donghua Landscaping Co., Ltd., Shenzhen 518003, China
红树林是分布于热带、亚热带海岸潮间带特有的湿地生态系统,由于其具有一些不同于陆地森林群落的特征而被世界各国所关注[1]。但是,由于城市的快速发展及人类干扰强度和频度的加大,红树林生态系统的结构遭到较大的破坏[2]。因此,如何将已被破坏的红树林生态系统较快地进行重建,在理论研究和生产实践中都有重要意义,而对红树林群落进行演替研究则有着极其重要的参考价值。目前,国内外已有不少关于红树林群落演替方面的研究成果[3, 4, 5, 6, 7, 8],然而,从伐迹地开始的演替研究则还未见报道。
1994年,广东深圳福田区下沙村当地村民非法修建避风塘,将广东深圳湾福田凤塘河河口东侧红树林非法砍伐,后经制止,被砍伐的红树林区域部分没有进行建设,砍伐迹地红树林林地得以自我恢复,为研究红树林的演替提供了一个理想样地。本文在已有调查数据的基础上,对福田凤塘河红树林被砍伐地的群落演替过程进行研究,旨在更好地揭示红树林群落自身恢复的过程及演替动态,为更好地恢复、保护及管理红树林提供科学的理论依据。
1 研究地自然条件广东内伶仃福田国家自然保护区位于深圳湾东北方向,东经114°02′,北纬22°52′,与香港米埔自然保护区隔河相望。保护区成立于1984年,1998年正式批准为国家级自然保护区,区内共有红树植物18种,若包括其它半红树植物或伴生植物及堤岸植物则有68种,另有鸟类16目36科119种[9]。
本区属于南亚热带季风气候区,气候温和,雨量充沛,日照时间长,年均温约22℃,极端最高温为38.7℃,极端最低温为0.2℃,年均降雨量1926.7 mm,干湿季节明显,5—9月为雨季。保护区土壤基质为花岗岩及砂页岩,地带性土壤为砖红壤。林地内滩涂淤泥深厚,潮汐属于不规则半日潮,平均潮差约1.9 m[10, 11]。
2 研究方法采用定位研究和时空替代相结合的方法[7, 12],定位样地设置在次生林和原生林演替的不同阶段群落。其中次生林为皆伐地自我恢复群落,紧邻次生林东侧的为原生林。
2.1 植被调查方法分别于1994、2011年在凤塘河红树林原生林由岸→滩涂方向设置10 m×60 m样条,再把样条划分成10 m×10 m小样方;1998、2011年在次生林处设置由岸→滩涂方向30 m×60 m样条,将每样条划分成相邻10 m×10 m的小样方,对小样方内植物进行每木调查,记录每木的名称、树高、胸径和冠幅等指标。
2.2 演替系列林龄的确定据前人皆伐处理样地的时间和皆伐后各期调查恢复植被的时间确定次生林各阶段的林龄。结合前人的研究成果来推断原生林各阶段的林龄。用空间代替时间法[7],把以下4个林龄群落作为一个演替系列过程进行研究。
(1)4年龄群落
前人皆伐时间为1994年,皆伐后首次调查时间为1998年11月,确定群落林龄为4 a。
(2)17年龄群落
2 011年11月,皆伐后第二次调查,确定群落林龄为17 a。
(3) 56年龄群落
1994年首次对原生林进行调查,林鹏等[13]于1994年通过径杆解析确定紧邻研究区原生林的白骨壤林林龄为56 a。
(4) 73年龄群落
2011年第二次对原生林进行调查,结合林鹏[13]研究结果,确定林龄为73 a。
2.3 数据处理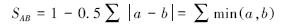
式中,SAB为群落相似性系数;a和b分别为群落A和B中某一共有物种相应的重要值。
(2) 采用Shannon-Wiener多样性指数(H)测定物种多样性;采用Simpson指数(D)测度生态优势度;采用Pielou指数(JH)测定群落均匀度;其公式为[15, 16]:
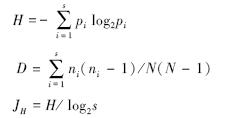
式中,s为群落中物种数; N为所有物种的个体总数; ni为第i个种的个体数; pi为第i个种的个体总数的百分数。
(3) 立木级的划分 立木级划分为5级[14],Ⅰ级为幼苗,高度在33 cm以下者;Ⅱ级苗木,高度级在33 cm以上,胸径不足2.5 cm者;Ⅲ级幼树,胸径在2.5—7.5 cm者;Ⅳ级立木,胸径在7.5—22.5 cm者;Ⅴ级大树,胸径在22.5 cm以上者。
(4) 重要值 根据相对多度(RA%)、相对频度(RF%)、相对显著度(RD%)或相对盖度(RC%)3项指数的综合[17],即:
IV(重要值)=(RA%+RF%+RD%或RC%)/300
(5)本文采用超球面模型趋势对演替主要阶段的群落演替趋势进行分析。
超球面模型的思想是:样方除以向量长度,向单位超球面投影,便保留了所有维上的信息。投影到超球面的植被向量保留了方向和角度,而失掉了距离和方差,因为向量方向承载着植被组成的全部信息。从植被组成角度来说,植被在物种空间的射线和射线在单位超球面上的投影点是一一对应的,映射是全映射。植被在空间的每一个微小的组成变化、方向的变化都将反映在超球面上代表植被的点的位移[17, 18]。
超球面模型对植被演替趋势分析的步骤:
JP4]①列出第i年植被中各种的重要值向量,然后在超球面上聚类,中心化数据,求出代表整个植被的向量长度:
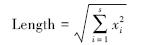
式中,xi为物种i的重要值,s为物种数。
②各种的重要值向量除以向量长度,进行数据标准化,求出植被状态向量的各分量:

③用相同的方法求出第i+k年的STDi+k。
④求出各物种的趋势向量

趋势向量大于1,该物种重要值在增加;趋势向量小于1,该物种重要值下降。
⑤求出伪趋势指数
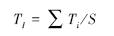
式中,TI表示整个植被的一般演替趋势。
根据研究地的滩涂高程情况,在由岸→滩涂方向60 m的样条内,以每隔20 m依次划分为内滩、中滩、外滩3种生境,内滩基本属于高潮位区域,中滩基本属于中潮位区域,外滩则基本上处在低潮位区域,以此来研究演替过程中各红树植物在潮滩的水平空间分布情况。虽然本研究调查时间横跨近20年,但2011与1994年调查样带的海陆格局没有变化,因此其滩涂分布是一致的。
3 研究结果与分析 3.1 群落的物种组成及其滩涂分布演替过程中群落物种组成见表 1,从4 a至73 a各群落基本都由秋茄(Kandelia candel)、木榄 (Bruguiera gymnorrhiza)、桐花树(Aegiceras corniculatum)、 白骨壤(Avicennia marina)及老鼠簕(Acanthus ilicifolius) 5个种类组成。
| 种名 Species | 林龄Age/a | |||||||||||
| 乔木层Tree layer | 幼树灌木层Shrub layer | 幼苗层 Seeding layer | ||||||||||
| 4 | 17 | 56 | 73 | 4 | 17 | 56 | 73 | 4 | 17 | 56 | 73 | |
| 秋茄Kandelia candel | + | + | + | + | + | + | + | + | + | + | + | |
| 木榄Bruguiera gymnorrhiza | + | + | + | + | + | + | + | |||||
| 桐花树Aegiceras corniculatum | + | + | + | + | + | + | + | + | + | + | + | |
| 白骨壤Avicennia marina | + | + | + | + | + | + | + | + | + | |||
| 老鼠簕Acanthus ilicifolius | + | + | + | + | + | + | ||||||
由于各个潮位或滩位上的生境条件(土壤基质、养分状况、环境盐度、波浪和潮汐等)不同,各种红树植物对这些生境条件的要求和适应性存在差异[19],使得各红树植物在不同潮滩上的数量不同,其水平空间分布亦不同。
从图 1可看出,次生林的4 a和17 a群落,各潮滩基本都由秋茄、桐花树、白骨壤和老鼠簕(木榄数量极少未列在图中)组成。其中秋茄和桐花树在每一潮滩均有分布,种群呈连续分布,但秋茄的数量较桐花树的多;白骨壤的数量在中滩较内滩及外滩明显要多,17 a群落中这种分布尤其明显,种群呈现非连续分布;老鼠簕则在内滩有较多的分布,17 a时在中滩和外滩带几乎没有分布,种群呈非连续分布。

|
| 图 1 各红树植物在不同滩涂的数量分布 Fig. 1 The amount distribution of different mangrove species in different tidal flats |
原生林的56 a和73 a群落,各潮滩群落物种组成基本相同(除73 a时外滩无秋茄),桐花树在内滩有较多的分布,而白骨壤则在中滩和外滩有较多分布。秋茄在中滩和外滩的数量较少且波动较大,在外滩的数量波动尤为明显:由56 a的较多分布到73 a的几乎零分布;而在内滩不仅数量较多,且有着较稳定分布,种群呈现非连续分布。
综合演替系列的4个林龄群落,内滩的种类和数量较外滩多,中滩处于两者之间。其中桐花树在各个潮滩均有分布,呈连续分布;秋茄基本也呈连续分布;白骨壤在17 a时呈现非连续分布,其它林龄群落均呈现连续分布;老鼠簕只在4 a、17 a群落中有分布,呈现非连续分布。
图 2表明,演替过程中不同潮滩上的红树植物数量变化不同,其优势种(从数量上看)变化亦不同。在内滩和中滩,秋茄的单一强优势地位在下降,桐花树和白骨壤则有一定程度上升;至外滩,秋茄的优势地位降至极低,白骨壤的优势地位则明显上升。总的看来,内滩由秋茄单一强优势林向着秋茄、桐花树双优势林演替,中滩由秋茄单一强优势林向着白骨壤单一强优势林演替,外滩则由秋茄、桐花树双优势林向着白骨壤单优势林演替。

|
| 图 2 演替过程中不同潮滩上各红树植物数量的变化 Fig. 2 Amount change of different mangrove species in different tidal zones during the succession process |
演替过程中群落的高度级和立木级分布的变化列于表 2、表 3。
| 高度级 Height | ﹤1m | 1—2.5m | 2.5—5m | 5—10m | |
| 高度级处于分级线的个体归于较高的一级 | |||||
| 4a群落 | 多度/(个体数/100m2) | 4.67 | 59.28 | 24.56 | |
| 4 age community | 百分数 /% | 5.27 | 66.98 | 27.75 | |
| 17a群落 | 多度/(个体数/100m2) | 2.03 | 16.51 | 28.13 | |
| 17 age community | 百分数/% | 4.35 | 35.37 | 60.27 | |
| 56a群落 | 多度/(个体数/100m2) | 2.17 | 5.50 | 20.50 | |
| 56 age community | 百分数/% | 7.69 | 19.53 | 72.78 | |
| 73a群落 | 多度/(个体数/100m2) | 0.33 | 5.67 | 9.33 | |
| 73 age community | 百分数/% | 2.17 | 36.96 | 60.87 | |
| 立木级 Tree class | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | |
| 4a群落 | 多度/(个体数/100m2) | 33.78 | 54.00 | 0.72 | 0 | |
| 4 age community | 百分数/% | 38.17 | 61.02 | 0.82 | 0 | |
| 17a群落 | 多度/(个体数/100m2) | 1.33 | 30.10 | 15.24 | 0 | |
| 17 age community | 百分数/% | 2.86 | 64.49 | 32.65 | 0 | |
| 56a群落 | 多度/(个体数/100m2) | 0.67 | 10.67 | 15.50 | 1.33 | |
| 56 age community | 百分数/% | 2.37 | 37.87 | 55.03 | 4.73 | |
| 73a群落 | 多度/(个体数/100m2) | 0.33 | 3.83 | 10.67 | 0.50 | |
| 73 age community | 百分数/% | 2.17 | 25.00 | 69.57 | 3.26 | |
表 2显示,4 a时群落以1—2.5 m幼树个体占优势,为群落个体数的 66.98%,2.5—5 m个体次之,幼苗(<1 m)在群落中所占比例最小,仅5.27%,说明群落已由幼苗阶段进入幼龄林阶段。至17 a时几乎看不到幼苗,1—2.5m幼树个体数量明显减少,由4 a时的 66.98%减少到17 a时的4.35%;17 a时高度级再上一级,60.27% 的个体进入5—10 m高度级。至56 a、73 a,群落没有再进入更高的高度级,但两群落均以5—10 m个体占绝对优势,分别占各自群落个体数的72.78%、60.87%。可见,演替早期(4 a)群落高度增长较快,之后群落高度继续保持较快增长率,至17 a时群落高度慢慢趋于稳定,17 a后群落高度增长速度缓慢。
从4 a→73 a群落,除4 a时有少数﹤1 m(同时高于33 cm)的幼苗外,其它演替系列群落则几乎未能看到,说明次生裸地恢复的早期(4 a前)时幼苗大量生长,之后由于苗木长大,群落郁闭度增大,林下幼苗较少能长成幼树。而在整个演替系列中,所有群落的立木高度均没有达10 m以上的数量级。世界上红树植物群落发育良好的地区,如马来亚和东苏门答腊的阿罗湾等地的红树植物群落高达35—40 m[20, 21],我国地处南亚热带的北端,红树林群落虽没有达35—40 m的高度,但也有部分能达20 m的高度[18],而南亚热/热带陆地森林群落几乎都有20 m以上的群落[12, 22, 23],说明深圳福田凤塘河红树林的层次结构较简单,群落缺乏高大的乔木。
从表 3群落立木级分布可知,4 a 时群落形成 Ⅱ、Ⅲ、Ⅳ 级苗木,其中 Ⅲ 级立木数量比例最大,占总数量的61.02%;其次为 Ⅱ 级苗木,少数的个体进入到 Ⅳ 级立木,此时群落为苗木和幼树阶段。至 17 a 时,群落 Ⅳ 级立木大幅度增加,Ⅱ 级苗木则大幅度降低,此时群落为成林阶段。从 17 a 至 56 a 时,群落 Ⅳ 级立木数量比例大大增多,部分个体进入 Ⅴ 级立木,群落为老年林前期阶段。从 56 a 演替至 73 a 时,群落 Ⅳ 级立木继续增加,Ⅳ 级立木的比例在演替系列中出现最高峰,部分个体进入 Ⅴ 级立木,此时群落为老年林阶段,整个群落的立木级近似稳定的金字塔型结构,群落年龄趋向稳定或趋向衰退[24]。
从 4 a 至 73 a 群落,演替早期群落中无 Ⅴ 级立木出现,但随着演替向前进展,56 a群落开始有 Ⅴ 级立木出现。而演替系列群落中均无 Ⅰ 级幼苗,据立木级的划分[14],Ⅰ 级幼苗为高度在 33 cm 以下者,因本研究所调查的立木为 33 cm 以上者,故无 Ⅰ 级幼苗。但在其它森林群落的研究中,Ⅰ 级苗木也仅在早期群落中出现,如黑石顶森林群落的 Ⅰ 级幼苗在 1—4 a 群落中出现[12],红树植物海桑群落也仅在 1 a 时出现[18]。
3.2.2 群落水平结构动态群落演替过程中群落的盖度、密度及胸高断面积(显著度)变化如表 4。
| 群落年龄 Community age | 4 a | 17 a | 56 a | 73 a |
| 盖度Coverage/(m2/100m2) | 103.31 | 147.47 | 177.38 | 123.60 |
| 密度 Density/(株/100m2) | 88.50 | 46.67 | 28.17 | 15.33 |
| 胸高断面Area of breast height/(cm2/100m2) | 1531.87 | 2149.43 | 2583.50 | 1969.49 |
表 4显示,在演替过程中,随着群落林龄的增加,群落盖度逐渐增加,其中4 a的幼树时期进入17 a的成林阶段,17 a的成林阶段到56 a的老年林前期阶段,这2个演替阶段群落的盖度增加比较显著,分别增加约37.17%、36.9%。而73 a群落盖度较56 a及17 a的低,这可能与73 a群落内一些老龄高大立木的枯死有关。
随着演替的进展,群落林龄的增加,群落的个体密度逐渐降低,其中由4 a至17 a过程中个体密度大幅度下降,这是由于早期苗木死亡和自疏作用的结果,期间群落高度级及立木级分布动态大幅度变化可证实这一推论。由17 a至56 a,个体密度继续下降,胸高断面积大幅度增加,这是由于Ⅳ级立木大幅度增长的结果。从56 a至73 a,个体密度仍继续下降,实地调查发现:这与近岸边的一些高大立木枯死有关,而此时还未形成倒木,故林下仍无幼苗或幼树大量生长。
随着演替向前发展,群落胸高断面积在演替早期阶段快速增长,至56 a时,达到了胸高断面积的最高峰。其中4 a至17 a期间,胸高断面积增加最快,增幅为40.3%,这主要是由于群落立木快速长大,胸径也随着增大的结果;73 a时,群落的胸断面积有所下降,这主要与群落个体密度降低有关。
相比红树植物海桑种群[18]和广东黑石顶森林群落[12]的盖度、密度及胸高断面积,凤塘河红树林群落的盖度在演替过程中变化极小,且在演替早期就已达到较大值100%,而海桑种群和黑石顶森林群落的早期群落盖度均较小。但凤塘河红树林的个体密度及胸高断面积均较海桑种群和黑石顶森林群落小,这可能与凤塘河红树林群落种类较少,群落层次较简单有关。
3.3 群落物种结构动态 3.3.1 演替过程群落的相似性表 5显示,17 a和73 a群落的相似性系数最小,为0.67;56 a和73 a群落的相似系数最大0.96。其中4 a与56 a、73 a的群落相似性系数较17 a大,表明皆伐地早期群落主要以伐桩萌生植株为主,故其与原生林群落的相似性较大。与其它森林群落的群落相似性相比,可知凤塘河红树林属于较大值,如红树植物海桑群落的相似性系数为0.31—0.95[18],贵州常绿阔叶林群落为0.11—0.64[25],广东黑石顶森林群落次生演替群落为0.12—0.73[12],较高的群落相似性系数表明演替过程中各群落物种变化不明显。值得一提的是,本研究中群落物种种类相对较少,这也是造成整个演替过程中各群落相似性系数较大的原因之一。
| 演替时间 Time/a | 4 | 17 | 56 |
| 17 a | 0.68 | ||
| 56 a | 0.83 | 0.70 | |
| 73 a | 0.83 | 0.67 | 0.96 |
物种多样性、生态优势度和群落均匀度是反映群落中物种数目、个体数量、优势种的组成及其均匀性的综合指标。
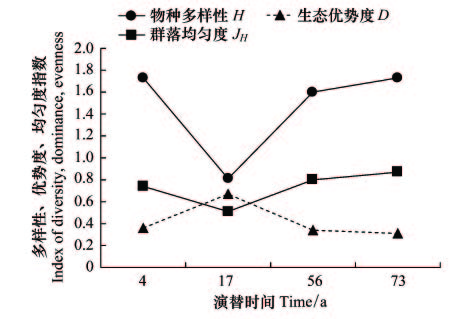
从图 3可知,演替过程中物种多样性与群落均匀度的变化表现为:由4 a时的最大值降至17 a的最低值,之后又大幅度上升,至73 a慢慢趋于稳定。这表明在次生裸地恢复阶段中,随着群落垂直结构的逐渐形成和群落盖度的逐渐增加,群落的密度迅速下降,桐花树由丛生状的幼树向单株的立木生长,引起了物种多样性和群落均匀度的下降,之后随着演替向前发展,群落内各物种数量和分布不断得到优化,使得群落的物种多样性和均匀度升高。
|
| 图 3 演替过程中群落的物种多样性、生态优势度和均匀度 Fig. 3 Species diversity,ecological dominance and community evenness during succession process |
与其它红树林群落相比,凤塘河红树林植物群落的多样性处于中等大小0.81—1.73,比海南岛清澜港红树林群落0.53—4.3[7]稍小,较广西英罗湾红树植物0.3—1.5[20]稍大。而与我国热带及南亚热带陆生森林植物Shannon多样性指数对比,凤塘河红树林植物群落多样性指数较小。如西双版纳热带季节雨林物种多样性约为5.4—5.7[26],广东亚热带常绿阔叶林的约为4.0—5.0[27],海南山地雨林的约为5.0—6.0[27];均匀度指数除了较西双版纳热带季节雨林[26]小外,凤塘河红树林群落均匀度与南亚热带森林群落(无论是同为海岸滩涂的红树林[20]还是陆地森林群落[27])的大小相当。说明凤塘河红树林群落物种多样性虽较小,但其群落物种均匀度较好。
生态优势度的变化表现为:17 a>4 a>56 a>73 a群落(图 3)。表明随着演替的进展,群落优势种由4 a时的较多优势种发展为17 a的稍少优势种,之后每个演替阶段较多的优势种。凤塘河红树林的生态优势度较保护区内红树林植物群落0.56[28]略小,较同是南亚热带的黑石顶森林群落0.48—0.74[12]亦小,但比广东亚热带常绿阔叶林群落0.08—0.12[27]大。表明凤塘河红树林群落的优势度处于中等水平,群落优势种种类数相对较少。
3.4 群落种群的重要值动态图 4显示,随着演替向前进展,秋茄的重要值在17 a群落中达最高值,亦是所有物种中的最高值,其它阶段则相当,其优势地位先表现为占优势、再到占绝对优势、之后为占优势。桐花树的重要值在整个演替过程中均较秋茄小且无明显变化,占次优势地位。白骨壤和木榄的重要值在整个演替过程中表现为上升的趋势,尤其是白骨壤,由不是优势地位到占优势地位,明显表现出重要值上升的趋势。老鼠簕在演替早期群落(4 a)中的作用非常明显,其重要值仅次于秋茄,而17 a之后,老鼠簕在群落中所起作用慢慢减小直至极小。

|
| 图 4 演替过程中群落物种重要值的变化 Fig. 4 Changes of species important value during succession process |
由群落中各种群重要值的变化可知,从4 a至73 a群落演变过程为:秋茄+桐花树群落→秋茄群落→白骨壤+秋茄群落→白骨壤群落。对比广西[19]、海南及福建[1]红树林群落的原生演替来看,凤塘河红树林群落演替模式较广西和海南的原生演替模式简单、演替过程中出现的群落类型较少;而与福建红树林群落的原生演替模式较相似:两红树林演替过程各阶段群落均以秋茄、桐花树及白骨壤3种红树的单一群落或混交群落组成。而与同为南亚热带森 林的演替[12]对比来看,凤塘河红树林演替过程中群 落类型较单一。
3.5 群落的演替趋势分析本研究选用演替过程中 4 a→17 a、17 a→56 a、56 a→73 a 群落样地调查资料,对不同群落的演替趋势进行分析。分析结果列于表 6。
| 物种 Species | 重要值向量 IV Important value | 重要值标准化 STD/S Important value standardization | 趋势向量Ti Trend vector | 伪趋势向量TI Pseudo trend vetor | ||||||||||
| IV4 | IV17 | IV56 | IV73 | S4 | S17 | S56 | S73 | Ti(4→17) | Ti(17→56) | Ti(56→73) | TI(4→17) | TI(17→56) | TI(56→73) | |
| 秋茄Kandelia candel | 20.11 | 50.00 | 19.17 | 22.00 | 0.37 | 0.85 | 0.29 | 0.36 | 2.27 | 0.34 | 1.24 | 0.57 | 0.07 | 0.31 |
| 桐花树 Aegiceras corniculatum | 34.72 | 19.00 | 19.33 | 25.17 | 0.65 | 0.32 | 0.29 | 0.41 | 0.50 | 0.90 | 1.41 | 0.12 | 0.18 | 0.35 |
| 白骨壤Avicennia marina | 11.39 | 8.00 | 60.67 | 51.67 | 0.21 | 0.14 | 0.91 | 0.84 | 0.64 | 6.70 | 0.92 | 0.16 | 1.34 | 0.23 |
| 木榄Bruguiera gymnorrhiza | — | — | 1.17 | 0.83 | — | — | 0.02 | 0.01 | — | — | 0.77 | — | — | 0.19 |
| 老鼠簕 Acanthus ilicifolius | 33.39 | 23.00 | — | — | 0.62 | 0.39 | — | — | 0.63 | — | — | 0.16 | — | — |
| 向量长度 Vector length | 53.67 | 58.77 | 66.51 | 61.55 | ||||||||||
| 演替趋势TI Succeesion trend | 1.01 | 1.59 | 1.08 | |||||||||||
在演替初期(4 a→17 a),群落的一般演替趋势呈上升趋势,上升率为1.01(表 6)。从各种的趋势向量Ti来看,秋茄的趋势向量大于1,在群落演替中呈上升趋势;其它种的趋势向量均小于1,在群落中呈下降趋势。而从各物种趋势向量对群落一般演替趋势的影响大小的伪趋势TI来看,对群落一般演替趋势影响最大的种是秋茄的上升趋势,其它种的变化对整个群落的一般演替影响均较小。
17 a至56 a,群落的一般演替趋势呈上升趋势,上升率为1.59(表 6)。从各种的趋势向量Ti来看,白骨壤的趋势向量Ti大于1,在群落演替中呈上升趋势。秋茄和桐花树的趋势向量Ti均小于1,在群落演替中呈下降趋势。而从各物种趋势向量对群落一般演替趋势的影响大小的伪趋势TI来看,对群落一般演替趋势影响最大的是白骨壤的上升趋势,其次是桐花树。
56 a至73 a,群落的一般演替趋势呈上升趋势,上升率为1.08(表 6)。从各种的趋势向量Ti来看,秋茄和桐花树两个种的趋势向量大于1,这两个种在群落演替中呈上升趋势。白骨壤和木榄的趋势向量Ti小于1,在群落演替中呈下降趋势。但从各物种趋势向量对群落一般演替趋势的影响大小的伪趋势TI来看,以上4个种对群落一般演替趋势的影响较小且相当。
由此可见,在自然条件下,凤塘河红树林演替各阶段群落均表现为上升演替趋势,表明像凤塘河这样的南亚热带红树林在皆伐裸地上的演替,在自然条件下可以由较矮小的灌木——乔木林演替至较高大的乔木林。
4 结论 4.1 演替过程中群落物种组成及结构动态从皆伐裸地开始至73 a群落,演替过程各阶段群落均由秋茄、桐花树、白骨壤、老鼠簕及木榄5个种类组成。演替早期(4 a)群落高度增长较快,之后继续保持较快增长率,至17 a时趋于稳定,之后增长速度缓慢。
随着演替的进展,群落高度级、立木级、盖度、密度、胸高断面积、物种多样性、均匀度、优势度、群落相似性系数及优势种群重要值均发生明显的变化,表明这些指标均能很好地指示演替过程中群落的动态变化。
4.2 凤塘河红树林群落演替的特点4 a→73 a群落演替为:秋茄+桐花树群落→秋茄群落→白骨壤+秋茄群落→白骨壤群落。凤塘河红树植物最大的演替特点是不同滩涂有不同的变化:内滩由秋茄单一强优势林向着秋茄、桐花树双优势林演替,中滩由秋茄单一强优势林向着白骨壤单一强优势林演替,外滩则由秋茄、桐花树双优势林向着白骨壤单优势林演替。
致谢: 深圳大学生命科学学院李西妮、郝文龙、杨俊达、刘丹霞等研究生及香港城市大学深圳研究院韦萍萍等博士研究生参与野外考察,特此致谢。
| [1] | Lin P. A review on the mangrove research in China. Journal of Xiamen University: Natural Science, 2001, 40(2): 592-603. |
| [2] | Lin P. The characteristics of mangrove wetlands and some ecological engineering questions in China. Engineering Science, 2003, 5(6): 33-38. |
| [3] | Xu H M, Ye C, Zhang B, Xu H L, Xin G R, Liao W B. Structure and dynamic succession on mangrove communities from Techeng Island, Zhanjiang, Guangdong, China. Ecology and Environmental Sciences, 2010, 19(4): 864-869. |
| [4] | Li Z Q, Lin Z D, Xue C Q. The succession and distribution of mangrove community in Gungdong. Guangdong Forestry Science and Technology, 2002, 18(2): 52-55. |
| [5] | Liang S C, Liu J F, Liang M Z. Ecological study on the mangrove communities in Beilunhekou National Nature reserve. Journal of Guangxi University, 2004, 22(2): 70-76. |
| [6] | Chen Y J, Liao B W, Zheng S F, Li M, Song X Y. Dynamics and species-diversity of artificial Sonneratia apetata, Sonneratia caseolaris and Kandelia candel communities. Chinese Journal of Applied Ecology, 2004, 15(6): 924-928. |
| [7] | Liao B W, Zheng D Z, Zheng S F, Chen Y J, Song X Y. The characteristics of species diversity for the successional series of mangrove community in Qinglan harbor of Hainan Island. Ecologic Science, 2000, 19(3): 17-22. |
| [8] | Ball M C. Patterns of secondary succession in a mangrove forest of Southern Florida. Oecoligia, 1980, 44(2): 226-235. |
| [9] | Wang B S, Liao B W, Wang Y J, Zan Q J. The Ecosystem and Sustainable Development of Mangrove Forest in Shenzhen Bay. Beijing: Science Press, 2002. |
| [10] | Zan Q J, Wang Y J, Liao B W, Zheng D Z, Chen Y J. The structure of sonneratia apetala+S. caseolaris-Kandelia candel mangrove plantations of Futian, Shenzhen. Forest Research, 2001, 14(6): 610-615. |
| [11] | Li M S, Lan C Y, Chen G Z, Li S H, Huang Y S, Tan F Y, Chen X R. Mangrove community in Futian, Shenzhen. Ecologic Science, 1992, (1): 40-43. |
| [12] | Zhou X Y, Wang B S, Li M G, Zan Q J. The community dynamics of the forest secondary succession in Heishiding natural reserve of Guangdong province. Acta Botanica Sinica, 1999, 41(8): 877-886. |
| [13] | Lin P, Hu H Y, Zheng W J, Li Z J, Lin Y M. A study on the biomass and energy of mangrove community in Shenzhen bay. Scientia Silvae Sinicae, 1998, 34(1): 18-24. |
| [14] | Wang B S. Phytocoenology. Beijing: Higher Education Press, 1987: 14-184. |
| [15] | Peng S L, Wang B S. Analysis on the forest commnities of Dinghushan, I Species diversity. Ecologic Science, 1983, (1): 11-17. |
| [16] | Pielou E C. Mathematical Ecology Introduction. Lu Z Y, translation. Beijing: Science Press, 1978. |
| [17] | Wang B S, Yu S X, Shi S H, Wang T, Liao W B, Jing J H. The Biological Diversity and Species Evolution of Tropical Forest in Hainan. Beijing: Science Press, 2005: 161-195. |
| [18] | Bai·T G J Z B. Trend Analysis and Its Application in Ecological Stock Market. Beijing: Ethnic Publishing House, 2006: 46-55. |
| [19] | Liang S C. Characteristics of mangrove communities in Guangxi. Guangxi Sciences, 2000, 7(3): 210-216. |
| [20] | Liang S C. Studies on the mangrove communities in Yingluo bay of Guangxi. Acta Phytoecologica Sinica, 1996, 20(3): 310-321. |
| [21] | Lin P. A Collection of Research Papers on the Mangrove Forest. Xiamen: Xiamen University Press, 1990: 23-30. |
| [22] | Ye W H, Cao H L, Huang Z L, Lian J Y, Wang Z G, Lin L, Wei S G, Wang Z M. Community structure of a 20 hm2 lower subtropical evergreen broadleaved Forest plot in Dinghushan. Journal of Plant Ecology: Chinese Version, 2008, 32(2): 274-286. |
| [23] | Lin Y M. The structure characteristics of mountain rain forest in Bawangling, Hainan Island. Ecologic Science, 1992, (1): 29-38. |
| [24] | Wang B S, Yu S X, Peng S L, Li M G. Phytocoenology Laboratory Manual. Guangzhou: Guangdong Higher Education Press, 1996. |
| [25] | Zhang L, Xie S X, Wu Z W, Wang Y F. The similarity and cluster analysis of forest communities in Xishui national nature reserve of Guizhou province. Guizhou Agriculture Science, 2011, 39(6): 170-172. |
| [26] | Guo L, Xu Z F. A research method for species diversity of plant in seasonal tropical rainforsts in Xishuangbanna. Journal of Ecology, 1990, 9(5): 61-62, 60-60. |
| [27] | Peng S L, Zhou H C, Chen T X, Guo S C. The quantitative characters of organization of forest communities in Guangdong. Acta Phytoecologica Et Geobotanica Sinica, 1989, 13(1): 10-17. |
| [28] | Chen G Z, Wang Y J, Huang Q L. A study on the biodiversity and protection in Futian national nature reserve of mangrove and birds, Shenzhen. Chinese Biodiversity, 1997, 5(2): 104-111. |
| [1] | 林鹏. 中国红树林研究进展. 厦门大学学报: 自然科学版, 2001, 40(2): 592-603. |
| [2] | 林鹏. 中国红树林湿地与生态工程的几个问题. 中国工程科学, 2003, 5(6): 33-38. |
| [3] | 许会敏, 叶蝉, 张冰, 徐华林, 辛国荣, 廖文波. 湛江特呈岛红树林植物群落的结构和动态特征. 生态环境学报, 2010, 19(4): 864-869. |
| [4] | 黎植权, 林中大, 薛春泉. 广东省红树林植物群落分布与演替分析. 广东林业科技, 2002, 18(2): 52-55. |
| [5] | 梁士楚, 刘镜法, 梁铭忠. 北仑河口国家级自然保护区红树植物群落研究. 广西师范大学学报: 自然科学版, 2004, 22(2): 70-76. |
| [6] | 陈玉军, 廖宝文, 郑松发, 李玫, 宋湘豫. 无瓣海桑、海桑、秋茄红树人工林群落动态及物种多样性研究. 应用生态学报, 2004, 15(6): 924-928. |
| [7] | 廖宝文, 郑德璋, 郑松发, 陈玉军, 宋湘豫. 海南岛清澜港红树林群落演替系列的物种多样性特征. 生态科学, 2000, 19(3): 17-22. |
| [9] | 王伯荪, 廖宝文, 王勇军, 昝启杰. 深圳湾红树林生态系统及其可持续发展. 北京: 科学出版社, 2002. |
| [10] | 昝启杰, 王勇军, 廖宝文, 郑德璋, 陈玉军. 深圳福田无瓣海桑+海桑-秋茄人工林结构的研究. 林业科学, 2001, 14(6): 610-615. |
| [11] | 李明顺, 蓝崇钰, 陈桂珠, 李世华, 黄玉山, 谭凤仪, 陈相如. 深圳福田的红树林群落. 生态科学, 1992, (1): 40-43. |
| [12] | 周先叶, 王伯荪, 李鸣光, 昝启杰. 广东黑石顶自然保护区森林次生演替过程中的群落动态. 植物学报, 1999, 41(8): 877-886. |
| [13] | 林鹏, 胡宏友, 郑文教, 李振基, 林益明. 深圳福田白骨壤红树林生物量和能量研究. 林业科学, 1998, 34(1): 18-24. |
| [14] | 王伯荪. 植物群落学. 北京: 高等教育出版社, 1987: 14-184. |
| [15] | 彭少麟, 王伯荪. 鼎湖山森林群落分析, I物种多样性. 生态科学, 1983, (1): 11-17. |
| [16] | Pielou E C. 数学生态学引论//卢泽愚, 译. 北京: 科学出版社, 1978. |
| [17] | 王伯荪, 余世孝, 施苏华, 王艇, 廖文波, 金建华. 海南岛热带林生物多样性及其物种进化. 北京: 科学出版社, 2005: 161-195. |
| [18] | 白·图格吉扎布. 趋势分析及其在生态股市中的应用. 北京: 民族出版社, 2006: 46-55. |
| [19] | 梁士楚. 广西红树植物群落特征的初步研究. 广西科学, 2000, 7(3): 210-216. |
| [20] | 梁士楚. 广西英罗湾红树植物群落的研究. 植物生态学报, 1996, 20(4): 310-321. |
| [21] | 林鹏. 红树林研究论文集. 厦门: 厦门大学出版社, 1990: 23-30. |
| [22] | 叶万辉, 曹洪麟, 黄忠良, 练琚愉, 王志高, 李林, 魏识广, 王章明. 鼎湖山南亚热带常绿阔叶林20公顷样地群落特征研究. 植物生态学报, 2008, 32(2): 274-286. |
| [23] | 林益民. 海南岛霸王岭山地雨林群落的结构特征. 生态科学, 1992, (1): 29-39. |
| [24] | 王伯荪, 余世孝, 彭少麟, 李鸣光. 植物群落学实验手册. 广州: 广东高等教育出版社, 1996. |
| [25] | 张磊, 谢双喜, 吴志文, 王艳芳. 贵州习水国家级自然保护区森林群落相似性与聚类分析. 贵州农业科学, 2011, 39(6): 170-172. |
| [26] | 郭玲, 许再富. 西双版纳热带季节雨林植物种类多样性的一种研究方法. 生态学杂志, 1990, 9(5): 61-62, 60-60. |
| [27] | 彭少麟, 周厚城, 陈天杏, 郭少聪. 广东森林群落的组成结构数量特征. 植物生态学与植物学报, 1989, 13(1): 10-17. |
| [28] | 陈桂珠, 王勇军, 黄乔兰. 深圳福田红树林鸟类自然保护区生物多样性及其保护研究. 生物多样性, 1997, 5(2): 104-111. |
 2014, Vol. 34
2014, Vol. 34




