文章信息
- 王爱民, 席贻龙, 牛翔翔, 李瑶, 温新利
- WANG Aiming, XI Yilong, NIU Xiangxiang, LI Yao, WEN Xinlin
- 汀棠湖冬季出现的萼花臂尾轮虫对水温的适应
- Adaptation of Brachionus calyciflorus (Rotifera) occurred in winter in Lake Tingtang to water temperature:a life table demography study
- 生态学报, 2014, 34(16): 4588-4595
- Acta Ecologica Sinica, 2014, 34(16): 4588-4595
- http://dx.doi.org/10.5846/stxb201212221842
-
文章历史
- 收稿日期:2012-12-22
- 修订日期:2012-6-20
轮虫是各类水体中广泛分布的一类浮游动物,在水生态系统的结构组成、物质循环和能量流动过程中具有重要的作用。由于水环境中物理﹑化学和生物因子等普遍具有随着时间的流逝或季节的更替而发生变化的特点,栖息于其中的轮虫种群密度也随之发生变化。为探明自然水体中轮虫种群数量的时空变动及其调节机制,众多学者作出了不懈的努力。温新利[1]曾以芜湖市汀棠湖中的萼花臂尾轮虫等为对象,研究了其种群数量的周年变动,探讨了水温、chl-a浓度、捕食者密度等外源性因素对种群数量周年变动的影响;但尚未涉及轮虫种群对特定环境的适应性等内源性因素。同一水体中的轮虫种群遗传结构[2, 3, 4, 5]和生态特征[4, 5, 6, 7]均存在着显著的季节变化,使人们相信内源性调节机制的存在。因此,研究特定时期内存在于自然水体中的轮虫种群在存活、发育、生殖和种群增长等方面对水温变化的响应有助于我们正确理解轮虫种群数量的周年变动机制。
汀棠湖是一亚热带浅水湖泊,平均水深2m,面积13.47hm2。该湖位于芜湖市中心,市区年平均温度约16℃,最高温度为41℃,最低温度为-15℃。湖泊内,萼花臂尾轮虫种群密度的周年变动表现为:11月中旬,萼花臂尾轮虫开始在水体中出现;12月初至次年1月初,种群密度维持在较低水平;之后,种群密度持续上升,至2月初达全年最高值;之后快速下降,但在3月初开始增长,至中旬时形成全年次高峰;4月初,种群密度急剧下降,至4月中旬几近消失。在此期间,水温的波动范围在6—23℃之间[1]。为了解汀棠湖冬季出现的萼花臂尾轮虫对水温的适应性,探讨其在春季的种群消长机制,特别是在3月中旬形成全年次高峰的内源性调节机制,参照春季自然水温的波动范围,本研究选择了12℃、16℃、20℃和24℃等4个温度。同时,考虑到与水温变化密切相关的藻类等食物所产生的上行效应也可能是影响轮虫种群密度季节变动的重要因素,而处于轻度富营养状态的汀棠湖水体中藻类和有机碎屑等轮虫食物较为丰富[8],本研究选择了1.0×106、3.0×106和5.0×106 个/mL等3个较高的斜生栅藻密度。
生命表统计学方法是一种研究在不断变化的环境条件下生物生活史策略和种群动态的重要方法,可以提供包括存活率和繁殖率等在内的信息。对于浮游生物来说,一些统计学参数例如存活率、繁殖率、平均寿命、世代时间和种群增长率可以作为衡量环境条件适宜性的重要参数[9]。因此,本研究应用生命表统计学方法研究了温度和食物密度对汀棠湖冬季出现的萼花臂尾轮虫生命表统计学参数的影响。
1 材料与方法 1.1实验所用萼花臂尾轮虫于2011年12月、2012年1月和2月上旬采自芜湖市汀棠湖。在此期间,水温的变动范围为6—9℃。采样后,随机挑取轮虫非混交雌体,于(25±1)℃、自然光照(光照强度约1300 lx)条件下进行克隆培养。轮虫培养液采用Gilbert配方[10],所用的饵料为HB-4培养基[11]培养的、处于指数增长期的斜生栅藻。从最终建立的轮虫克隆中随机选取12个克隆用于本实验研究。
1.2 生命表实验实验前,将12个轮虫克隆分别置于温度为12、16、20℃和24℃,斜生栅藻密度为1.0×106、3.0×106和5.0×106 个/mL的条件下进行为期1周的预培养。预培养过程中,每12 h悬浮沉积于试管底部的藻类食物;每24 h更换轮虫培养液并投喂饵料1次,同时通过去除一部分个体使得轮虫种群始终处于指数增长期。
实验开始时,从各温度和食物密度组合条件下预培养一周后的各轮虫克隆中随机吸取若干个带卵的非混交雌体,分别置于和预培养条件相同的玻璃杯中进行培养;期间,每隔4 h观察1次,并把孵化出的幼体取出用于生命表实验。实验在容积为8mL的玻璃杯中进行,培养液体积为5 mL。实验也设12、16、20℃和24℃等4个温度,1.0×106、3.0×106和5.0×106 个/mL等3个斜生栅藻密度。实验时,各温度和食物密度组合条件下所使用的轮虫幼体数为12个,分别取自各相应组合条件下的12个轮虫克隆中;各温度和食物密度组合条件下设置4个重复。实验过程中,每间隔12 h观察并计数1次各玻璃杯中轮虫母体的存活数和孵化出的幼体数,移去死亡母体;观察的同时用微吸管悬浮沉于杯底的藻细胞;每隔24 h更换培养器皿和培养液,并投喂食物1次。
1.3 生活史参数的定义和计算方法特定年龄存活率(lx):X年龄组开始时存活个体百分数;
特定年龄繁殖率(mx):X年龄组平均每个个体所产的雌性后代数;
出生时的生命期望:每个个体出生时能活多久的估计值;
平均寿命:所有个体平均存活时间的观察值;
总生殖率:每个个体一生所产的雌性后代数,
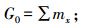
净生殖率:种群经过一个世代后的净增长率,
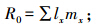
世代时间:完成一个世代所需要的时间,
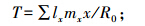
种群内禀增长率:种群在特定实验条件下的最大增长率;
根据方程r=lnR0/T在粗略计算的基础上,再根据方程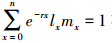 在Excel中试算求得种群内禀增长率的精确值。
在Excel中试算求得种群内禀增长率的精确值。
采用SPSS 16.0统计分析软件对上述数据进行统计分析。对所得的各生命表统计学参数进行正态分布检验后,对符合正态分布的数据进行方差分析以揭示温度、食物密度以及两者间的交互作用对轮虫各生命表统计学参数的影响,采用多重比较(SNK-q检验法)对同一温度下各食物密度间、同一食物密度下各温度间轮虫各生命表统计学参数的差异显著性进行分析;运用生存分析中的Kaplan-Meier分析同一温度下各食物密度间、同一食物密度下各温度间轮虫的生存时间的差异显著性。
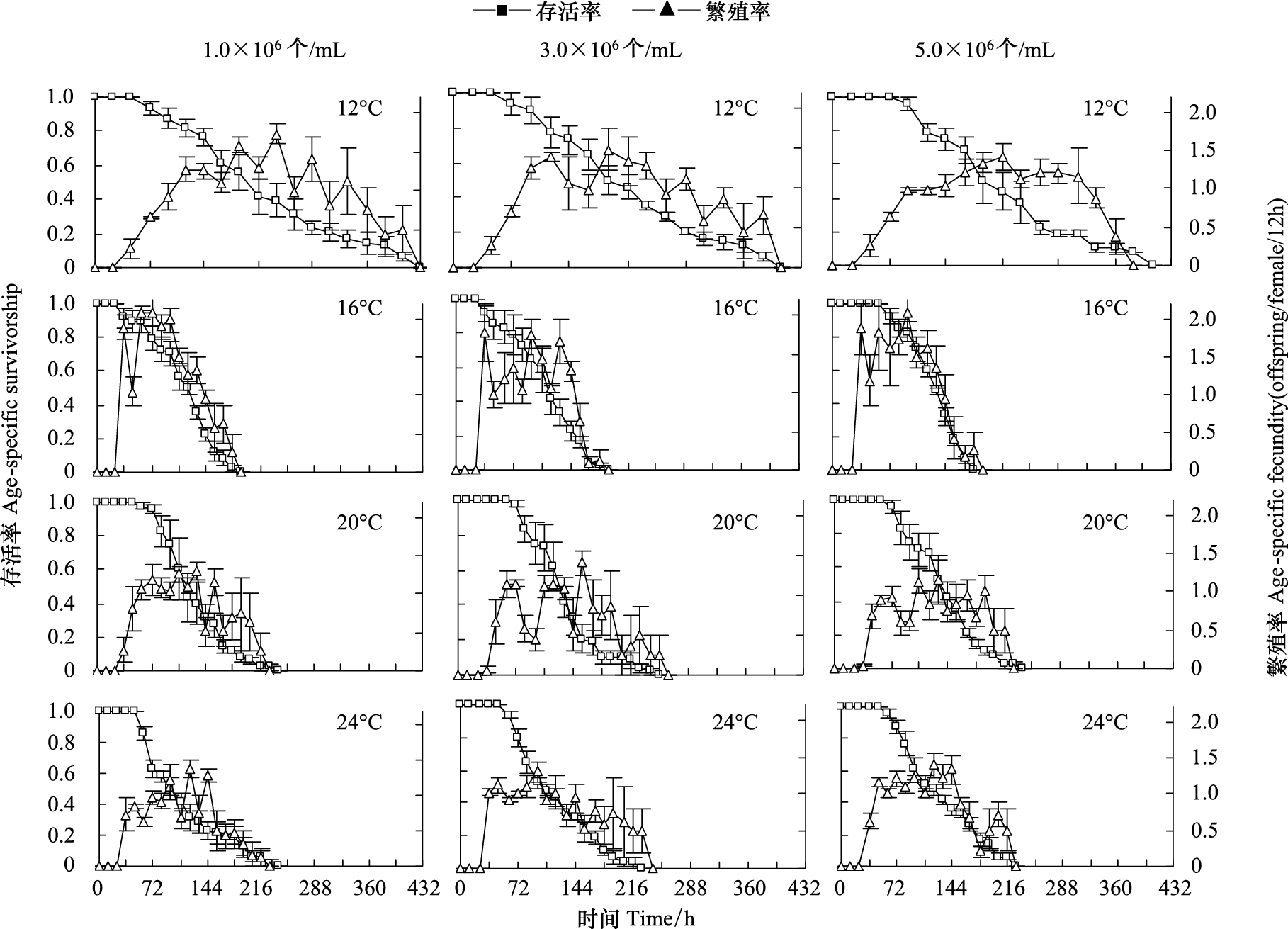
2 结果与分析 2.1 轮虫的存活率和繁殖率各温度下,食物密度对轮虫的存活时间均无显著性影响(P>0.05);但各食物密度下,温度对轮虫的存活时间均有极显著性影响(P<0.01)。除了24℃、1.0×106 个/mL食物密度下轮虫的存活时间最短外,各食物密度下,轮虫的存活时间均在12℃下最长,16℃下最短(图 1)。
|
| 图 1 不同温度和食物密度下汀棠湖冬季出现的萼花臂尾轮虫的存活率和繁殖率 Fig. 1 Survivorship and fecundity of B. calyciflorous occurred in winter in Lake Tingtang and cultured at four temperatures and three food levels |
各温度下,食物密度对轮虫的繁殖率均无显著性影响(P>0.05);食物密度以及食物密度和温度之间的交互作用对轮虫繁殖率均无显著性影响(P>0.05)。除3.0×106 个/mL食物密度外,其它各食物密度下温度对轮虫的繁殖率均有极显著性影响(P<0.01)。在1.0×106 个/mL食物密度下,轮虫的繁殖率在24℃与20、20℃与12、12℃与16℃间均无显著性差异;在5.0×106 个/m食物密度下,轮虫的繁殖率在12、20℃和24℃之间均无显著性差异,但它们均显著低于16℃下(图 1)。
2.2 轮虫的生命表统计学参数1.0×106 个/mL食物密度下,轮虫出生时的生命期望、世代时间和平均寿命均在12℃下较长,其它3个温度下较短且无显著性差异;食物密度的升高总体上并不改变它们对升高的温度的反应格局,但5.0×106 个/mL食物密度下轮虫的世代时间在20℃下显著长于16℃下除外。各温度下,食物密度对轮虫出生时的生命期望、世代时间和平均寿命均无显著性影响(P>0.05)(表 1)。
| 参数 Parameters | 食物密度 Food level /(×106个/mL) | 12℃ | 16℃ | 20℃ | 24℃ |
| * 多重比较(SNK-q检验法):同行具有相同大写字母表示在同一食物密度下各温度间轮虫的生命表参数无显著性差异,同列具有相同小写字母表示在同一温度下各食物密度间轮虫的生命表参数无显著性差异 | |||||
| 生命期望/h | 1.0 | 219.0±17.3aB* | 111.8±6.4aA | 126.0±10.7aA | 110.0±7.2aA |
| Life expectancy at hatching | 3.0 | 211.0±12.4aB | 108.8±11.6aA | 132.3±10.5aA | 115.8±2.3aA |
| 5.0 | 213.5±16.3aB | 126.0±3.6aA | 135.8±9.0aA | 126.3±5.3aA | |
| 世代时间/h | 1.0 | 173.5±10.2aB | 77.5±2.6aA | 89.6±3.9aA | 85.6±6.8aA |
| Generation time | 3.0 | 159.0±4.6aB | 79.1±2.2aA | 97.9±4.2aA | 82.9±1.4aA |
| 5.0 | 161.6±5.5aC | 80.3±1.6aA | 99.0±3.2aB | 89.4±1.5aAB | |
| 平均寿命/h | 1.0 | 195.0±17.3aB | 99.8±6.4aA | 114.0±10.7aA | 98.0±7.2aA |
| Average lifespan | 3.0 | 187.0±12.4aB | 96.8±11.6aA | 120.3±10.5aA | 103.8±2.3aA |
| 5.0 | 189.5±16.3aB | 114.0±3.6aA | 123.8±9.0aA | 114.325±5.3aA | |
| 总生殖率/个体 | 1.0 | 16.0±1.1aAB | 17.6±1.2aB | 13.7±1.6aAB | 11.5±1.5aA |
| Gross reproductive rate | 3.0 | 14.4±1.2aA | 14.3±0.2aA | 13.4±1.5aA | 14.3±0.9aA |
| 5.0 | 13.8±0.5aA | 16.6±3.1aA | 12.1±1.0aA | 14.8±0.7aA | |
| 净生殖率/个体 | 1.0 | 7.7±0.7aA | 11.5±1.4aB | 7.7±0.7aA | 5.8±0.7aA |
| Net reproductive rate | 3.0 | 7.0±0.2aA | 8.5±1.1aA | 7.0±0.5aA | 7.1±0.3abA |
| 5.0 | 6.8±0.6aA | 12.8±2.5aB | 6.6±0.5aA | 8.2±0.5bA | |
| 内禀增长率/h | 1.0 | 0.0145±0.0004aA | 0.0381±0.0023aC | 0.0262±0.0014aB | 0.0245±0.0007aB |
| Intrinsic rate of population | 3.0 | 0.0152±0.0001aA | 0.0333±0.0027aC | 0.0233±0.0015aB | 0.0296±0.0008bC |
| increase | 5.0 | 0.0144±0.0006aA | 0.0385±0.0043aC | 0.0220±0.0005aB | 0.0289±0.0012bB |
1. 0×106 个/mL食物密度下,轮虫的总生殖率在16℃下显著高于24℃下,但两者均与12℃和20℃下的总生殖率无显著性差异。当食物密度升高至3.0×106和5.0×106 个/mL时,轮虫的总生殖率在4个温度间无显著性差异。各温度下,食物密度对轮虫的总生殖率均无显著性影响(P>0.05)(表 1)。
1.0×106和5.0×106 个/mL食物密度下,轮虫的净生殖率在16℃下较高,在其它3个温度下较低且无显著性差异;3.0×106 个/mL食物密度下,温度对轮虫的净生殖率无显著性影响(P>0.05)。12、16℃和20℃下,食物密度对轮虫的净生殖率均无显著性影响(P>0.05);24℃下,轮虫的净生殖率在5.0×106 个/mL食物密度下显著高于1.0×106 个/mL食物密度下,但两者均与3.0×106 个/mL食物密度间无显著性差异(表 1)。
1. 0×106和5.0×106 个/mL食物密度下,轮虫的种群内禀增长率在16℃下最高,20℃和24℃下次之,12℃下最低;3.0×106 个/mL食物密度下,轮虫的种群内禀增长率在16℃和24℃下最高,12℃下最低。12、16℃和20℃下,食物密度对轮虫的种群内禀增长率均无显著性影响(P>0.05);24℃下,轮虫的种群内禀增长率在1.0×106 个/mL食物密度下较低,3.0×106和5.0×106 个/mL食物密度下较高且两者间无显著性差异(表 1)。
双因素方差分析结果表明,温度对轮虫出生时的生命期望、世代时间、平均寿命、净生殖率和种群内禀增长率均有显著性影响(P<0.05),但对总生殖率无显著性影响(P>0.05);食物密度以及食物密度与温度之间的交互作用对轮虫所有生命表统计学参数均无显著性影响(P>0.05)(表 2)。轮虫出生时的生命期望和平均寿命在12℃下较长,16、20℃和24℃下较短且三者间无显著性差异;轮虫的世代时间在12℃下最长,16℃和24℃下最短且两者间无显著性差异;轮虫的净生殖率在16℃下较高,12、20℃和24℃下较低且三者间无显著性差异;轮虫的种群内禀增长率在12℃下最低,16℃下最高,20℃和24℃间无显著性差异。
| 变异源Source | SS | df | F | P |
| 生命期望Life expectancy at hatching | ||||
| 温度Temperature | 79827.333 | 3 | 61.526 | 0.000 |
| 食物密度Food level | 782.542 | 2 | 0.905 | 0.414 |
| 温度×食物密度Temperature×Food level | 769.292 | 6 | 0.296 | 0.935 |
| Error | 15569.500 | 36 | ||
| 世代时间Generation time | ||||
| 温度Temperature | 56208.648 | 3 | 145.718 | 0.000 |
| 食物密度Food level | 65.971 | 2 | 0.257 | 0.775 |
| 温度×食物密度Temperature×Food level | 728.253 | 6 | 0.944 | 0.476 |
| Error | 4628.839 | 36 | ||
| 平均寿命Average lifespan | ||||
| 温度Temperature | 61011.333 | 3 | 47.024 | 0.000 |
| 食物密度Food level | 782.542 | 2 | 0.905 | 0.414 |
| 温度×食物密度Temperature×Food level | 769.292 | 6 | 0.296 | 0.935 |
| Error | 15569.500 | 36 | ||
| 总生殖率Gross reproductive rate | ||||
| 温度Temperature | 67.858 | 3 | 2.901 | 0.048 |
| 食物密度Food level | 2.629 | 2 | .169 | 0.846 |
| 温度×食物密度Temperature×Food level | 61.088 | 6 | 1.306 | 0.280 |
| Error | 280.694 | 36 | ||
| 净生殖率Net reproductive rate | ||||
| 温度Temperature | 133.767 | 3 | 10.948 | 0.000 |
| 食物密度Food level | 11.452 | 2 | 1.406 | 0.258 |
| 温度×食物密度Temperature×Food level | 42.125 | 6 | 1.724 | 0.144 |
| Error | 146.624 | 36 | ||
| 种群内禀增长率Intrinsic rate of population increase | ||||
| 温度Temperature | 0.003 | 3 | 76.018 | 0.000 |
| 食物密度Food level | 3.164×10-6 | 2 | 0.121 | 0.886 |
| 温度×食物密度Temperature×Food level | 0.000 | 6 | 2.111 | 0.076 |
| Error | 0.000 | 36 | ||
自然水体中,水温是季节性变化特征最明显的生态因子之一。因此,在对轮虫种群数量季节变动机制进行研究时,人们自然会想到水温变化对轮虫种群动态的影响。通常,研究温度的选择大多包括了轮虫实验种群能够耐受的亚致死高温。与常规做法不同,为了揭示冬季出现于汀棠湖水体中的萼花臂尾轮虫对春季升高的水温的适应,本研究参考轮虫野外种群能够耐受的春季自然水温的上限,选择了12、16、20℃和24℃等4个温度。由于特定研究对象(萼花臂尾轮虫冬季种群)、温度范围和较高的食物密度的选择,由此得出了汀棠湖冬季出现的萼花臂尾轮虫种群在存活、发育、生殖和种群增长等方面对升高的水温和食物密度的独特响应方式。
已有研究结果表明,轮虫的存活和发育时间对升高的温度的反应因轮虫种类和食物密度的不同而异。在所有测试的食物密度下,十指臂尾轮虫(B. patulus)和哈瓦那臂尾轮虫(B. havanaensis)出生时的生命期望和世代时间均随着温度的升高而逐渐显著的缩短[12, 13]。在1.0×106和10.0×106 个/mL的微绿球藻(Nannochloris oculata)密度下,月形腔轮虫(Lecane luna)和四齿腔轮虫(L. quadridentata)的平均寿命和世代时间均随着温度的升高而逐渐显著地缩短;但在5.0×106 个/mL的微绿球藻密度下,两种轮虫的平均寿命和世代时间均在20℃和25℃之间无显著的差异[14]。在3.0×106 个/mL的斜生栅藻密度下裂足臂尾轮虫(B. diversicornis)出生时的生命期望以及1.0×106、3.0×106和5.0×106 个/mL的斜生栅藻密度下裂足臂尾轮虫的世代时间均随着温度的升高而逐渐显著地缩短;但在1.0×106和5.0×106 个/mL的斜生栅藻密度下,其出生时的生命期望均在15℃下最长,30℃下最短,而20℃和25℃间无显著的差异[15]。本研究中,1.0×106 个/mL食物密度下,汀棠湖冬季出现的萼花臂尾轮虫出生时的生命期望、世代时间和平均寿命均在12℃下较长,其它3个温度下较短且无显著性差异;食物密度的升高总体上并不改变它们对升高的温度的反应格局,仅5.0×106 个/mL食物密度下轮虫的世代时间在20℃下显著长于16℃下。
Fanestil和Barrows[16]、Meadow和Barrows[17]认为,理论上,变温动物的净生殖率应该不随着温度的变化而发生显著的变化。但事实上,十指臂尾轮虫、哈瓦那臂尾轮虫、月形腔轮虫、四齿腔轮虫、壶状臂尾轮虫(B. urceolaris)、红臂尾轮虫(B. rubens)、剪形臂尾轮虫(B. forcatus)、尾突臂尾轮虫(B. caudatus)以及萼花臂尾轮虫的3个姐妹种等的净生殖率均受温度的显著影响[12, 13, 14, 18, 19, 20]。1.0×106、3.0×106和5.0×106 个/mL等3个斜生栅藻密度下,温度对裂足臂尾轮虫的净生殖率均有显著的影响;但裂足臂尾轮虫的净生殖率对升高的温度的响应因食物密度的不同而存在着差异。在1.0×106和3.0×106 个/mL的斜生栅藻密度下,裂足臂尾轮虫在20℃下的净生殖率分别与25℃和30℃下的净生殖率无显著性差异,其它3个温度下的净生殖率随温度的升高而显著地增大;但在5.0×106 个/mL的斜生栅藻密度下,裂足臂尾轮虫在20、25℃和30℃下的净生殖率无显著性差异[15]。与上述研究结果不同,本研究中,1.0×106和5.0×106 个/mL食物密度下,汀棠湖冬季出现的萼花臂尾轮虫的净生殖率在16℃下较高,在其它3个温度下较低且无显著性差异;3.0×106 个/mL食物密度下,萼花臂尾轮虫的净生殖率在4个温度间无显著性差异。
种群内禀增长率对升高的温度的反应也因轮虫种类和食物密度的不同而异。哈瓦那臂尾轮虫、壶状臂尾轮虫、红臂尾轮虫、剪形臂尾轮虫和尾突臂尾轮虫的种群内禀增长率均随着温度的升高而显著升高[13, 18, 19];但萼花臂尾轮虫种复合体内姐妹种LE9的种群内禀增长率在28℃下最高,13℃和18℃最低且两者间无显著的差异;姐妹种HE1的种群内禀增长率在13、18℃和28℃间无显著的差异;姐妹种HE3的种群内禀增长率在23℃和28℃下最高且两者间无显著的差异[20]。1.0×106、3.0×106和5.0×106 个/mL等3个斜生栅藻密度下,温度对裂足臂尾轮虫的种群内禀增长率均无显著的影响[15]。本研究中,1.0×106和5.0×106 个/mL食物密度下,汀棠湖冬季出现的萼花臂尾轮虫的种群内禀增长率在16℃下最高,12℃下最低;3.0×106 个/mL食物密度下,轮虫的种群内禀增长率在16℃和24℃下最高,12℃下最低。
温度、食物密度以及两者间的交互作用对十指臂尾轮虫的平均寿命、出生时的生命期望、世代时间、总生殖率、净生殖率和种群内禀增长率均有显著的影响[12]。温度和食物密度对哈瓦那臂尾轮虫的所有生命表统计学参数均有显著的影响,但温度和食物密度间的交互作用对其却无显著的影响[13]。温度仅对裂足臂尾轮虫出生时的生命期望、世代时间、净生殖率和总生殖率有显著的影响,食物密度仅对轮虫的净生殖率和总生殖率有显著的影响,而食物密度与温度之间的交互作用对轮虫所有的生命表统计学参数均无显著的影响[15]。本研究中,温度对汀棠湖冬季萼花臂尾轮虫出生时的生命期望、世代时间、平均寿命、净生殖率和种群内禀增长率均有显著性影响,但对总生殖率无显著性影响;食物密度以及食物密度与温度之间的交互作用对轮虫所有生命表统计学参数均无显著性影响。可见,温度、食物密度以及两者间的交互作用对轮虫生命表统计学参数的影响因轮虫种类、温度和食物密度的设置范围不同而异。
3.2 汀棠湖冬季出现的萼花臂尾轮虫对水温的适应平均寿命、净生殖率和种群内禀增长率常被用作轮虫的适合度特征[7, 21]。本研究发现,汀棠湖冬季出现的萼花臂尾轮虫的平均寿命在12℃下较长,16、20℃和24℃下较短且三者间无显著性差异;净生殖率在16℃下较高,12、20℃和24℃下较低且三者间无显著性差异;种群内禀增长率在12℃下最低,16℃下最高,20℃和24℃间无显著性差异。可见,汀棠湖冬季出现的萼花臂尾轮虫在16℃下的适合度最高;这或许是汀棠湖水体中萼花臂尾轮虫种群密度在3月中旬(此时水温为17℃)达到春季最高峰的重要原因之一。至于4月初(此时水温为18℃)该种轮虫的种群密度降至较低水平的原因,则与在此之前水温等环境因子的剧烈波动导致此时轮虫种群中的混交雌体百分率较高(37%)有关[1]。
在有关轮虫种群遗传结构的时空变化格局的研究中,取自不同地理区域的轮虫种群常被称为地理种群;与此相似,取自不同季节的同一水体中的轮虫种群常被称为季节种群。无论是地理种群或季节种群,种群遗传结构(遗传因素)是决定其生态特征的重要内源性因素[2, 4, 6, 7, 21]。本研究中,虽然冬季出现于汀棠湖中的萼花臂尾轮虫在实验室内已被驯化;驯化不仅诱发了轮虫的生理补偿机制,还避免了由同一温度(25℃)突然将轮虫转入不同温度下可能因对轮虫影响幅度的不同而产生的误差;但实验室驯化并没有消除该种群在不同温度间的适合度差异。轮虫种群在平均寿命、净生殖率和种群内禀增长率等方面的差异应该是由遗传决定的,对其进行研究应有助于人们正确理解轮虫种群数量动态及其调节机制。
| [1] |
Wen X L. Population Dynamics and Regulation Mechanisms of |
| [2] | King C E, Serra M. Seasonal variation as a determinant of population structure in rotifers reproducing by cyclical parthenogenesis. Hydrobiologia, 1998, 387-388: 361-372. |
| [3] |
Xiang X L, Xi Y L, Hu H Y. Seasonal changes in the genetic diversity of |
| [4] |
Jiang D H, Xi Y L, Liu S G, Zhang L, Dong L L. Allozyme analysis on |
| [5] |
Cheng X F, Xi Y L, Li H B. Seasonal changes in the genetic structure of a |
| [6] | King C E. Adaptation of rotifers to seasonal variation. Ecology, 1972, 53(3): 408-418. |
| [7] |
Zhao Y Q, King C E. Ecological genetics of the rotifer |
| [8] | Wen X L, Xi Y L, Qian F P, Zhang G, Xiang X L. Comparative analysis of rotifer community structure in ve subtropical shallow lakes in east China: role of physical and chemical conditions. Hydrobiologia, 2011, 661(1): 303-316. |
| [9] | Stearns S C. Life history tactics: a review of the ideas. The Quarterly Review of Biology, 1976, 51(1): 3-47. |
| [10] |
Gilbert J J. Mictic female production in the rotifer |
| [11] | Zhang Z S, Huang X F. Method for Study on Freshwater Plankton. Beijing: Science Press, 1991: 410-411. |
| [12] |
Sarma S S S, Rao T R. The combined effects of food and temperature on the life history parameters of |
| [13] |
Pavón-Meza E L, Sarma S S S, Nandini S. Combined effects of algal ( |
| [14] | Pérez-Legaspi I A, Rico-Martínez R. Effect of temperature and food concentration in two species of littoral rotifers. Hydrobiologia, 1998, 387-388: 341-348. |
| [15] |
Ning L F, Xi Y L, Sun Q, Zhou A. Combined effects of temperature and algal food density on life table demography of |
| [16] | Fanestil D D, Barrows C H. Aging in the rotifer. Journal of Gerontology, 1965, 20(4): 462-469. |
| [17] | Maedow N D, Barrows C H. Studies on aging in a bdelloid rotifer. II. The effects of various environmental conditions and maternal age on longevity and fecundity. Journal of Gerontology, 1971, 26(3): 302-309. |
| [18] |
Hu C B, Xi Y L, Tao L X. Comparative on the life history characteristics of |
| [19] |
Tao L X, Xi Y L, Hu C B. Characteristics in life history of |
| [20] |
Li H B, Xi Y L, Cheng X F. Comparative studies on life history characteristics of three sibling species in |
| [21] |
Li L, Niu C, Ma R. Rapid temporal succession identied by COI of the rotifer |
| [1] | 温新利. 浅水富营养湖泊中两种臂尾轮虫的种群变动和机制研究 [D]. 安徽: 安徽师范大学, 2011. |
| [3] |
项贤领, 席贻龙, 胡好远. 镜湖萼花臂尾轮虫( |
| [4] | 江东海, 席贻龙, 刘胜国, 张雷, 董丽丽. 镜湖萼花臂尾轮虫种群等位酶分析和生殖参数的季节变化. 水生生物学报, 2008, 32(6): 908-915. |
| [5] | 程新峰, 席贻龙, 李化炳. 基于r DNA ITS序列分析莲塘湖萼花臂尾轮虫种群遗传结构的季节变化. 动物学报, 2008, 54(2): 245-255. |
| [11] | 章宗涉, 黄祥飞. 淡水浮游生物研究方法. 北京: 科学出版社, 1991: 410-411. |
| [15] |
宁乐锋, 席贻龙, 孙强, 周澳. 温度和食物密度对裂足臂尾轮虫( |
| [18] | 胡存兵, 席贻龙, 陶李祥. 红臂尾轮虫和壶状臂尾轮虫生活史特征比较. 生态学报, 2008, 28(12): 5957-5963. |
| [19] | 陶李祥, 席贻龙, 胡存兵. 镰形臂尾轮虫和尾突臂尾轮虫的生活史特征比较. 应用生态学报, 2008, 19(5): 1104-1109. |
| [20] |
李化炳, 席贻龙, 程新峰. 萼花臂尾轮虫( |
 2014, Vol. 34
2014, Vol. 34




