文章信息
- 冯志华, 方涛, 李玉, 阎斌伦, 徐加涛
- FENG Zhihua, FANG Tao, LI Yu, YAN Binlun, XU Jiatao
- 苏北沿海滩涂养殖湿地磷化氢的释放及其影响因素
- Emission of phosphine in intertidal zone for aquaculture along the northern Jiangsu coast and its influencing factors
- 生态学报, 2014, 34(15): 4167-4174
- Acta Ecologica Sinica, 2014, 34(15): 4167-4174
- http://dx.doi.org/10.5846/stxb201301060039
-
文章历史
- 收稿日期:2013-1-6
- 修订日期:2014-5-10
2. 淮海工学院江苏省海洋生物技术重点建设实验室, 连云港 222005
2. Jiangsu Key Laboratory of Marine Biotechnology, Huaihai Institue of Technology, Lianyungang 222005, China
生态系统生源气体排放是全球C、N、P、S和Cl循环研究的重要内容,是当前全球变化生态学和生物地球化学循环的研究热点和焦点[1, 2]。通常,广为关注的生源气体主要是温室气体(二氧化碳、甲烷和一氧化二氮等)、卤代烷烃和还原性硫气体[3],而关于磷生源气体的研究相对较少。作为还原态磷的气态存在形式,磷化氢是一种活泼的还原性气体,可与其它温室气体,如甲烷,竞争消耗羟基自由基,具有间接温室效应,已被确认为自然环境中普遍存在的痕量气体[4, 5, 6, 7]。因此,开展地球典型生态系统磷化氢的释放研究对查明自然界中磷的地球化学循环具有重要意义[8]。目前,关于磷化氢释放通量的研究主要涉及稻田湿地、淡水湖泊湿地、潮间带沼泽、垃圾填埋场,甚至极地地区等[9, 10, 11, 12],但相关报道较少。Hou等人[13]详细研究了长江口潮间带滩涂磷化氢的释放。
滨海湿地处于海陆交界地带,是地球上重要的生态系统之一,其对全球变化和人类活动的响应也极为敏感。江苏海岸湿地资源丰富,总面积约45.6万 hm2,是目前亚洲最大的淤泥质海岸湿地。水产养殖是滨海湿地主要的开发利用方式,存在自身污染,能够造成养殖底泥富营养化,对滨海湿地生态系统的自然属性产生剧烈的影响[14]。滩涂养殖湿地,作为典型的受人类活动影响的滨海湿地类型,是否存在显著的磷化氢释放?其释放的水平和规律如何?受哪些因素的影响?为探索这些科学问题,本研究以苏北沿海滩涂养殖湿地为研究对象,调查了磷化氢的释放通量特征,比较了其与其它湿地环境中磷化氢释放的差异,探讨了影响磷化氢释放的主要环境因素,分析了磷化氢产生的潜在机制,以期为进一步深入研究人为活动影响下滨海湿地磷的循环过程提供依据。
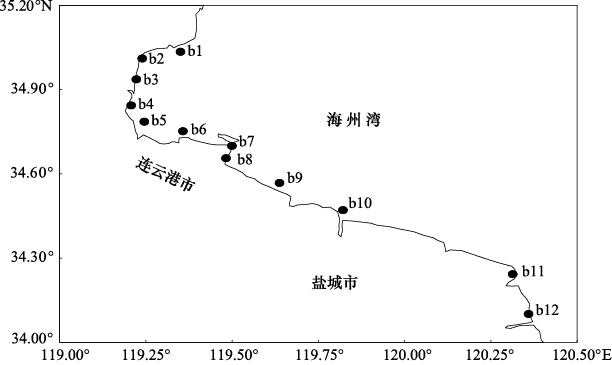
1 材料与方法 1.1 样品采集本研究沿江苏北部海岸,在滩涂养殖区布设了12个采样站位,分别位于柘汪(b1)、石桥(b2)、海头(b3)、青口(b4)、新浦(b5)、连云(b6)、高公岛(b7)、板桥(b8)、埒子口(b9)、灌河口(b10)、废黄河口(b11)和扁担港(b12)(图 1)。12个站点的养殖方式均为底播养殖,养殖生物,b1和b2为四角蛤蜊,b3和b4为毛蚶,b5、b6和b7为光滑河蓝蛤,b8、b9和b10为杂色蛤,b11和b12为泥螺。于2010年8月(夏季)、11月(秋季)和2011年2月(冬季)、5月(春季)进行现场调查。四个季度的采样,选择同一个养殖场埕地的固定位置,确保采样站位一致,采样时间在8:00—16:00。释放通量的测定采用静态箱法,静态采样箱为顶部密闭的圆柱形箱体,直径31 cm,高65 cm,材料为有机玻璃,外覆铝箔避光。在退潮后水深10 cm以下的养殖滩涂采样点,在开启风扇将箱内空气混匀后,将采样箱缓慢插入沉积物 中,以避免对沉积物产生扰动,同时保证水面以上采样箱的有效使用高度为50 cm。用针管在0,15,30,45 min时间点从顶部采样口分别抽取100 mL气样,注入外覆铝箔避光的Tedlar气袋保存,并置于低温保温箱内,及时送实验室分析。在每个采样点均利用两个相同的静态箱进行释放通量的平行测定。同时,采集表层(0—5 cm)沉积物放入聚乙烯塑料袋中,然后立即密封、避光并置于-20℃冷冻保存。
|
| 图 1 采样点位置示意 Fig. 1 Map showing sampling sites |
利用柱前二次冷阱富集和气相色谱-氮磷检测器(GC-NPD)联用技术分析磷化氢气体。色谱条件同文献[15, 16],每个样品重复测定3次,该仪器的检测限约为0.1 ng/m3。释放通量根据箱内磷化氢浓度随时间的变化进行估算,计算公式如下[17]:

式中,F为气体的释放通量(ng m-2 h-1),Q为箱内目标气体质量,S为箱体有效底面积,H为气室有效高度,T为箱内平均气温,P为采样时大气压力,P0为标准状况的大气压力,ρ为目标气体密度,c为目标气体浓度,t为采样时间,Δc/Δt为箱内目标气体的浓度变化速率。
1.3 沉积物理化因子的分析沉积物总磷(TP)的测定:称取约1.0 g沉积物,在550℃高温灼烧1.5 h,用50 mL 1 mol/L的HCl在25℃室温下振荡提取16 h,然后离心5 min(2000 r/min),取上清液稀释后用磷钼蓝法测定其含量[18]。沉积物无机磷(IP)的测定无需高温灼烧,其它步骤与总磷测定基本一致。有机磷(OP)的含量为TP与IP之差。沉积物中有机碳(OC)和总氮(TN)利用PE2400Ⅱ型CHNS/O元素分析仪测定,参照《海洋调查规范》(GB/T 12763.8—2007)规定方法进行。硫化物(SC)采用碘量法测定,氧化还原电位(Eh)利用铂丝电极和饱和甘汞电极,采用电位计法现场测定,同时现场测定泥温(T),均参照《海洋监测规范》(GB 17378.5—2007)。含水率的测定:称取一定量的样品于105℃烘干至恒重,利用失重差计算其含水率。所有生源要素组分含量均以单位沉积物干重计。
1.4 数据分析文中数据的方差分析、相关性分析和回归分析等统计分析均利用SPSS 13.0进行。
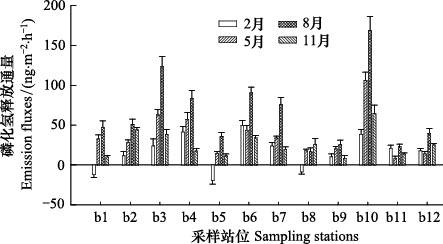
2 结果与分析 2.1 磷化氢的释放通量苏北沿海滩涂养殖湿地磷化氢释放通量介于-19.5—168.9 ng m-2 h-1之间,均值为36.0 ng m-2 h-1,除2月b1,b5,b8三个站位的释放通量为负值,表现为滩涂沉积物对磷化氢的弱吸收外,其它45个监测样次均为正值,监测站位表现出显著的磷化氢释放特征,最小和最大释放通量分别监测于2月的b5站位和8月的b10站位。磷化氢释放通量的时空变化如图 2所示,不同站位的磷化氢释放通量存在明显的空间变化特征,从季节平均值看,b10站位最高,b3次之,b5和b8站位相对较低。四个季节之间的单因素方差分析结果显示,磷化氢的释放通量具有显著的季节性变化(ANOVA,N=48,F=5.89,P=0.002<0.05)。并进行了各季节磷化氢释放通量的多重比较,8月与2、5、11月之间均存在显著的差异(P值分别为0.000,0.025和0.003,均<0.05),而2月与5月、2月与11月、5月与11月之间的差异则不显著(P值分别为0.108,0.442和0.391,均>0.05),说明夏季磷化氢释放通量显著高于其它三个季节,而春、秋、冬季之间的释放通量不存在显著差异。 2、5、8、11月磷化氢释放通量的变化范围分别为-19.5—49.6,8.3—105.9,16.5—168.9和8.2—64.5 ng m-2 h-1,平均值分别为16.4,36.5,65.0和25.9 ng m-2 h-1,各季节磷化氢释放通量的高低排序为:8月份>5月份>11月份>2月份,夏季最高,冬季最低,春秋两季介于两者之间。
|
| 图 2 苏北沿海滩涂养殖湿地磷化氢的释放通量 Fig. 2 The emission fluxes of phosphine in intertidal zone for aquaculture along Jiangsu coast |
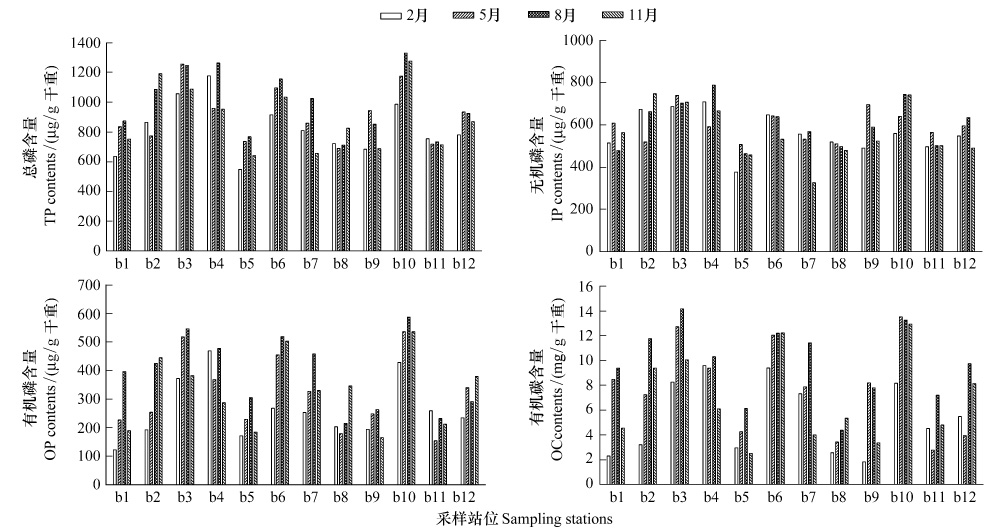
苏北沿海滩涂养殖湿地表层沉积物中TP、IP、OP和OC的含量分布特征如图 3所示。TP的含量介于547—1331 μg/g之间,平均值为908 μg/g,最高值和最低值分别位于b10站位(8月)和b5站位(2月);IP的含量介于326—788 μg/g之间,平均值为582 μg/g,占TP含量的49.7%—80.8%,平均值为TP含量的65.0%,其最高值和最低值分别出现在b4站位(8月)和b7站位(11月);OP的含量要低于IP的含量,范围为122—587 μg/g,平均值为327 μg/g,占TP的19.2%—50.3%,平均值为35.0%,8月份的b10站位含量最高,2月份的b1站位含量最低;沉积物中OC含量最高值为14.16 mg/g,出现在8月份的b3站位,最低值为1.82 mg/g,出现在2月份的b9站位,平均值为7.51 mg/g。
|
| 图 3 苏北沿海滩涂养殖湿地表层沉积物TP、IP、OP、OC含量分布 Fig. 3 TP,IP,OP and OC of surface sediments in intertidal zone for aquaculture along Jiangsu coast |
沉积物中TN和SC在4个季节各站位的含量分布见表 1。沉积物TN含量变化范围为113—1381 μg/g,平均值为634 μg/g,最高值和最低值分别位于b10站位(8月)和b1站位(11月),不同季节的含量分布为8月最高,2月最低,5月和11月差别不大;沉积物SC含量介于47.3—282.4 μg/g之间,平均值为141.5 μg/g,最高值和最低值分别出现在b3站位(8月)和b9站位(2月),不同季节的含量分布为8月最高,5月次之,2月和11月相对较低。
| 站位 Stations | 总氮 TN/(μg/g) | 硫化物 SC/(μg/g) | ||||||
| 2月Feb. | 5月May. | 8月Aug. | 11月Nov. | 2月Feb. | 5月May. | 8月Aug. | 11月Nov. | |
| b1 | 462 | 732 | 577 | 113 | 61.6 | 234.3 | 184.3 | 73.1 |
| b2 | 908 | 584 | 851 | 1035 | 101.9 | 76.2 | 217.7 | 51.3 |
| b3 | 653 | 439 | 1064 | 828 | 130.1 | 126.2 | 282.4 | 155.0 |
| b4 | 1032 | 651 | 433 | 1090 | 184.3 | 184.9 | 239.1 | 81.3 |
| b5 | 614 | 137 | 882 | 432 | 82.6 | 85.5 | 147.5 | 181.4 |
| b6 | 469 | 1140 | 1022 | 1021 | 229.1 | 136.3 | 82.6 | 145.5 |
| b7 | 912 | 588 | 1247 | 204 | 88.4 | 170.4 | 127.8 | 75.5 |
| b8 | 283 | 219 | 619 | 647 | 167.1 | 111.7 | 211.7 | 203.2 |
| b9 | 128 | 910 | 353 | 542 | 47.3 | 148.8 | 69.1 | 112.9 |
| b10 | 336 | 423 | 1381 | 345 | 197.2 | 263.6 | 243.8 | 228.7 |
| b11 | 411 | 586 | 504 | 526 | 147.3 | 73.1 | 110.2 | 81.4 |
| b12 | 303 | 623 | 798 | 380 | 94.0 | 69.5 | 136.1 | 138.4 |
| 站位 Stations | 氧化还原电位 Eh/mv | 泥温 T/℃ | ||||||
| 2月Feb. | 5月May. | 8月Aug. | 11月Nov. | 2月Feb. | 5月May. | 8月Aug. | 11月Nov. | |
| b1 | -51 | -124 | -138 | -50 | 3.6 | 16.8 | 29.4 | 17.1 |
| b2 | -46 | -88 | -155 | -194 | 4.3 | 17.4 | 30.1 | 19.8 |
| b3 | -177 | -198 | -236 | -215 | 3.9 | 18.5 | 31.3 | 20.4 |
| b4 | -191 | -181 | -167 | -158 | 4.2 | 19.9 | 31.9 | 18.2 |
| b5 | -59 | -56 | -209 | -71 | 4.1 | 18.1 | 29.6 | 16.7 |
| b6 | -169 | -161 | -239 | -77 | 4.7 | 18.8 | 30.7 | 18.5 |
| b7 | -122 | -89 | -226 | -98 | 3.9 | 20.5 | 29.9 | 17.8 |
| b8 | -68 | -76 | -79 | -157 | 3.5 | 17.3 | 28.1 | 19.5 |
| b9 | -94 | -69 | -166 | -133 | 2.8 | 16.6 | 27.6 | 16.7 |
| b10 | -147 | -207 | -265 | -184 | 4.9 | 17.2 | 31.5 | 20.2 |
| b11 | -135 | -58 | -180 | -48 | 5.2 | 18.9 | 28.3 | 17.3 |
| b12 | -157 | -61 | -151 | -70 | 4.1 | 15.8 | 28.8 | 18.6 |
表 1也给出了各站位沉积物Eh和T的分布情况。所有调查站位沉积物Eh的变化范围为-265 mv到-48 mv,平均值为-134 mv,沉积物处于显著的还原环境,最高和最低值分别位于b11站位(11月)和b10站位(8月);沉积物T的变化范围为2.8—31.9℃,2、5、8、11月份,各调查站位泥温的平均值分别为4.1、18.0、29.8℃和18.4℃。
3 讨论 3.1 不同湿地环境中磷化氢释放通量的比较本研究首次调查了苏北沿海滩涂养殖湿地磷化氢的释放通量。为确定该调查区域磷化氢释放通量的水平,并与其它湿地生态系统中的磷化氢释放通量进行比较,现对相关的研究成果进行汇总,如表 2所示。目前,关于湿地生态系统磷化氢释放通量的研究,调查数据极为有限。与淡水湖泊湿地生态系统相比,本研究结果显著高于太湖水体的报道结果;与水稻田湿地生态系统相比,本研究结果也显著高于中国北方水稻田和南方水稻田的相关报道。
| 释放源 Release sources | 释放通量Emission fluxes/(ng m-2 h-1) | 参考文献 References | |
| 平均值 Mean values | 范围 Ranges | ||
| 路易斯安那州微碱湿地 Louisiana brackish marsh | 无 | 0.42—3.03 | [11] |
| 路易斯安那州含盐湿地 Louisiana salt marsh | 无 | 0.91—6.52 | [11] |
| 长江口潮间带泥沼 Intertidal marsh of the Yangtze Estuary,China | 8.04 | 0.21—36.5 | [10] |
| 盐城滩涂(泥滩) Yancheng marsh (mudflat) | 20.1 | -49.6—179 | [10] |
| 盐城滩涂(互花米草) Yancheng marsh (Spartina alterniflora) | 60.3 | -70.4—276 | [10] |
| 盐城滩涂(碱蓬) Yancheng marsh (Suaeda glauca) | -28.3 | -225—116 | [10] |
| 盐城滩涂(芦苇) Yancheng marsh (Phragmites communis) | -45.9 | -227—38.4 | [10] |
| 苏北养殖滩涂 Intertidal marsh for aquaculture,the Northern Jiangsu Coast,China | 36.0 | -19.5—168.9 | 本研究 |
| 太湖水体 Lake Taihu | 14.4 | -69.9—121 | [10] |
| 中国北方水稻田 Paddy fields,Northern China | 1.78 | -4—15 | [10] |
| 中国南方水稻田 Paddy fields,Southern China | 6.67 | -1.49—41.7 | [19] |
与同类型的滨海湿地相比,本研究中苏北沿海滩涂养殖湿地磷化氢的释放通量要显著高于路易斯安那州湿地和长江口潮间带泥沼,也高于盐城滩涂湿地保护区天然泥滩,说明人为的底播养殖活动可能加剧了磷化氢的释放。而有耐盐植物生长的滩涂,则随植物种类的不同,磷化氢释放通量变化较大,本研究结果低于互花米草滩涂,高于碱蓬和芦苇滩涂。另外,本研究12个站位,按5种不同底播养殖生物种类进行划分,四角蛤蜊、毛蚶、光滑河蓝蛤、杂色蛤和泥螺养殖区的磷化氢释放通量平均值分别为26.5、56.0、34.3、41.1和20.2 ng m-2 h-1,毛蚶养殖区最高,四角蛤蜊和泥螺养殖区较低。5种养殖品种从习性上来说是相同的,均为非选择性滤食的贝类,其对磷化氢释放通量的影响,更多来自于放养密度和养殖技术等的不同带来的沉积环境因子的差别。
3.2 磷化氢释放的机制与影响因子探讨沉积物磷化氢的释放,是一个动态平衡过程,受控于沉积物中磷化氢的产生和消耗,并被沉积环境因子影响[20]。本文调查区域磷化氢释放的空间和季节变化可能与沉积环境特征密切相关。苏北沿海滩涂养殖湿地磷化氢的释放通量与沉积理化因子的相关性分析结果如表 3所示。首先进行了一元线性回归分析,结果显示沉积物TP、IP、OP、OC、TN、SC、Eh和T与磷化氢释放通量相关性分析的P值都小于0.01,均存在显著线性相关关系,表明各沉积环境因子对磷化氢的释放具有显著的影响;其次进行了多元线性逐步回归分析,从8个变量中,先后引入OP、Eh、SC和T建立模型,复相关系数为0.880,P值小于0.01,说明在这些因子中,按贡献率高低,影响磷化氢释放的主要沉积环境因子依次为OP、Eh、SC和T。
| 线性回归分析方法 Linear regression method | 沉积理化因子 (x) Environmental factors | 磷化氢释放通量 Emission fluxes/(y,ng m-2 h-1) | |||
| 直线回归方程 Linear regression equation | 相关系数 R | 样本数 N | 显著性检验P值 P | ||
| 一元线性回归分析 Unitary linearity regression | TP/(μg/g) | y=0.136x-87.554 | 0.807 | 48 | < 0.00001 |
| IP/(μg/g) | y=0.194x-77.060 | 0.579 | 48 | 0.00002 | |
| OP/(μg/g) | y=0.224x-37.055 | 0.828 | 48 | < 0.00001 | |
| OC/(mg/g) | y=7.956x-23.773 | 0.825 | 48 | < 0.00001 | |
| TN/(μg/g) | y=0.051x+3.435 | 0.467 | 48 | 0.00082 | |
| SC/(μg/g) | y=0.333x-11.099 | 0.605 | 48 | 0.00001 | |
| Eh/mv | y=-0.435x-22.464 | -0.774 | 48 | < 0.00001 | |
| T/℃ | y=2.047x+0.015 | 0.551 | 48 | 0.00005 | |
| 多元线性逐步回归 Multiple linear stepwise regression | OP(x1)、Eh(x2)、SC(x3)、T(x4) | y=-52.439+0.116 x1-0.167 x2+0.114 x3+0.681 x4 | 0.880 | 48 | < 0.00001 |
磷化氢释放通量与磷组分含量均存在显著的线性正相关关系,与TP、IP和OP的相关系数分别为0.807,0.579和0.828,释放通量与有机磷的线性相关要强于与无机磷的线性相关关系。释放通量与碳、氮、硫组分含量也都存在显著的线性正相关关系,与OC、TN、SC的相关系数分别为0.825、0.467和0.605,与有机碳的相关性最强,硫化物次之。由此揭示了磷化氢的释放与沉积物中磷等生源要素组分密切相关,这与以往的研究结果相类似[21, 22, 23]。尽管目前有关自然环境中磷化氢的来源及其形成机制仍存在诸多争议,但是很多研究表明磷化氢可能是由无机磷和有机磷等作为前体物在微生物的作用下还原降解和转化产生的[24, 25, 26]。与无机磷相比,本研究中磷化氢释放通量与有机磷组分的相关性更为显著,并且有研究证实添加易降解的小分子有机物有利于磷化氢的产生[27],由此可推断在富营养化养殖滩涂沉积环境下有机磷作为磷化氢前体物的可能性更大。而碳、氮、硫组分含量与磷化氢释放通量的显著线性正相关关系进一步说明OC、TN和SC组分在磷化氢的产生过程中可能起重要的作用,支持了微生物降解有机磷产生磷化氢的论断。
磷化氢的释放过程不仅与生源要素组分含量有关,还会受到沉积物其它理化性质的影响,如氧化还原电位、温度等都可能是影响磷化氢释放的重要因子,对磷化氢在沉积环境中的迁移和转化起着一定的作用[28, 29]。本研究中,相关性分析结果显示,磷化氢释放通量与Eh存在显著的线性负相关关系,相关系数为-0.774,说明在还原环境区域内,磷化氢的释放通量普遍较高。磷化氢易被氧化,还原环境更利于沉积物中磷化氢的产生和存留已被很多研究者证实[23, 30],本研究结果进一步验证了较低氧化还原电位下更可能存在较高的磷化氢释放通量。另外,温度通常也是影响沉积物磷化氢产生和释放过程的重要因素,温度较低时,微生物的活动减弱,生物降解产生磷化氢的速率也随之降低,当水温达到20—30℃时,微生物活动加强,磷化氢生成速率加快[31]。本研究在四个季节分别采集样品,温度变化范围较大,沉积物温度与磷化氢释放通量也存在显著的线性正相关关系(R=0.551,P=0.00005),证实较高的温度更利于磷化氢的产生和释放。
4 结论苏北沿海滩涂养殖湿地磷化氢的释放通量介于-19.5—168.9 ng m-2 h-1之间,均值为36.0 ng m-2 h-1,并且具有明显的季节性变化特征,各季节磷化氢释放通量的高低排序为:8月份>5月份>11月份>2月份,空间变化上,b10站位最高,b3次之,b5和b8站位相对较低。磷化氢释放通量与沉积物TP、IP、OP、OC、TN、SC和T存在显著线性正相关关系,与Eh存在显著线性负相关关系。较高的磷、碳、氮、硫生源要素组分含量,较高的温度以及较低的氧化还原电位与磷化氢的产生和释放过程密切相关,富营养化养殖滩涂沉积环境中磷化氢的释放来源可能为有机磷的微生物还原降解。本研究对滩涂养殖湿地磷化氢释放通量的调查结果显著高于相关淡水湖泊、水稻田和滨海湿地天然泥沼的报道。
| [1] | Jenkinson D S. Soil organic matter and its dynamics// Wild A, ed. Russell′s Soil Conditions and Plant Growth. 11th ed. New York: Longman, 1988, 564-607. |
| [2] | Post W M, Peng T H, Emanuel W R, King A W, Dale V H, DeAngelis D L. The global carbon cycle. American Scientist, 1990, 78: 310-326. |
| [3] | Wang Y, Zhang Z K, Zhu D K, Yang J H, Mao L J, Li S H. River-sea interaction and the north Jiangsu plain formation. Quaternary Sciences, 2006, 26(3): 301-320. |
| [4] | Chen Z Y, Wang G X, Liu J E, Xuan Y, Xu W W, Qiu L, Wang G. Relative competitive ability of Spartina alterniflora patches to native species in tidal zone ecotone of north Jiangsu. Ecology and Environment, 2011, 20(10):1436-1442. |
| [5] | Zhang Y H, Zhang F C, Zhou X D, Xie X J, Wang X W, Li Q, Lei J. Effects of plant invasion along a Spartina alterniflora chronosequence on organic carbon dynamics in coastal wetland in north Jiangsu. China Environmental Science, 2011, 31(2): 271-276 |
| [6] | Qin P, Li S Y. Positive and negative effects of the non-native plant, Spartina alterniflora and its ecological control. Journal of Biosafety, 2012, 21(3): 167-176. |
| [7] | Ren L J, Wang G X, He D, Mao Z G, Liu J E. Spatial distributions of soil organic matter in different vegetation zones of the Yancheng tidal flat. Advances in Marine Science, 2011, 29(1): 54-62. |
| [8] | Zhang Y H, Wang Y L, Li R Y, Zhu H X, Zhang F C, Huang B B, Peng X D. Effects of Spartina alterniflora invasion on active soil organic carbon in the coastal marshes. Chinese Journal of Soil Science, 2012, 43(1): 102-106. |
| [9] | Wang G, Wang G X, Yang W B, Liu J E, Hang Z Q. The effects of Spartina alterniflora seaward invasion on soil organic carbon fractions,sources and distribution. Acta Ecologica Sinica, 2013. |
| [10] | Chen C R, Xu Z H, Mathers N J. Soil carbon pools in adjacent natural and plantation forests of subtropical Australia. Soil Science Society of America Journal, 2004, 68(1): 282-291. |
| [11] | Huang Z Q, Xu Z H, Chen C R, Boyd S. Changes in soil carbon during the establishment of a hardwood plantation in subtropical Australia. Forest Ecology and Management, 2008, 254(1): 46-55. |
| [12] | Vance E D, Brookes P C, Jenkinson D S. An extraction method for measuring soil microbial biomass C. Soil Biology and Biochemistry, 1987, 19(6): 703-707. |
| [13] | Schnitzer M, Schuppli P. Method for the sequential extraction of organic matter from soils and soil fractions. Soil Science Society of America Journal, 1989, 53(5): 1418-1424. |
| [14] | Senesi N. Molecular and quantitative aspects of the chemistry of fulvic acid and its interactions with metal ions and organic chemicals: Part II. The fluorescence spectroscopy approach. Analytica Chimica Acta, 1990, 232: 77-106. |
| [15] | Chen M J, Wang M K, Chia C Y. Determination of low molecular weight dicarboxylic acids and organic functional groups in Tsuga and Yushania rhizosphere and bulk soils in the Saddle of Ta-Ta-Chia. Soil and Environment, 1999, 2(2):159-170. |
| [16] | Jones D L, Willett V B. Experimental evaluation of methods to quantify dissolved organic nitrogen (DON) and dissolved organic carbon (DOC) in soil. Soil Biology and Biochemistry, 2006, 38(5): 991-999. |
| [17] | Mathers N J, Xu Z H, Berners-Price S J, Senake Perera M C, Saffigna P G. Hydrofluoric acid pre-treatment for improving13C CPMAS NMR spectral quality of forest soils in south-east Queensland, Australia. Australian Journal of Soil Research, 2002, 40(4): 665-674. |
| [18] | Ros G H, Tschudy C, Chardon W J, Temminghoff E J M, van der Salm C, Koopmans G F. Speciation of water-extractable organic nutrients in grassland soils. Soil Science, 2010, 175(1): 15-26. |
| [19] | Xue J F, Gao Y M, Wang J K, Fu S F, Zhu F C. Microbial biomass carbon and nitrogen as an indicator for evaluation of soil fertility. Chinese Journal of Soil Science, 2007, 38(2): 247-250. |
| [20] | Jiang P K, Xu Q F, Xu Z H, Cao Z H. Seasonal changes in soil labile organic carbon pools within a phyllostachys praecox stand under high rate fertilization and winter mulch in subtropical China. Forest Ecology and Management, 2006, 236(1): 30-36. |
| [21] | Biederbeck V O, Janzen H H, Campbell C A, Zentner R P. Labile soil organic-matter as influenced by cropping practices in an arid environment. Soil Biology and Biochemistry, 1994, 26(12): 1647-1656. |
| [22] | Mao Z G, Wang G X, Liu J E, Ren L J. Influence of salt marsh vegetation on spatial distribution of soil carbon and nitrogen in Yancheng coastal wetland. Chinese Journal of Applied Ecology, 2009, 20(2): 293-297. |
| [23] | Wan Z M, Song C C, Yang G S, Huang J Y, Wang L L, Li Y C. The active soil organic carbon fraction and its relationship with soil enzyme activity in different types of marshes in the San jiang Plain. Acta Scientiae Circumstantiae, 2009, 29(2):406-412. |
| [24] | Zhou J, Xiao W, Qin P. Effect of an alien species(Spartina alterniflora) on soil microbial biomass and functional groups in salt marshes.Journal of Nanjing University: Natural Sciences, 2007, 43(5): 494-500. |
| [25] | Guggenberger G, Christensen B T, Zech W. Land-use effects on the composition of organic matter in particle-size separates of soil: Ⅰ. Lignin and carbohydrate signature. European Journal of Soil Science, 1994, 45(4): 449-458. |
| [26] | Martens D A, Reedy T E, Lewis D T. Soil organic carbon content and composition of 130-year crop, pasture and forest land-use managements. Global Change Biology, 2004, 10(1): 65-78. |
| [27] | Mathers N J, Xu Z H. Solid-state13C NMR Spectroscopy characterization of soil organic matter under two contrasting residue management regimes in a 2-year-old pine plantation of subtropical Australia. Geoderma, 2003,114(1/2):19-31. |
| [28] | Shang S Y, Li Y F, Jiang P K, Zhou G M, Liu J, Wu J S, Lin L. Effects of the conversion from native shrub forest to Chinese chestnut plantation on soil carbon and nitrogen pools. Chinese Journal of Applied Ecology, 2012, 23(3): 659-665. |
| [29] | Dou S, Zhang J J, Li K. Effect of organic matter applications on13C-NMR spectra of humic acids of soil. European Journal of Soil Science, 2008, 59(3): 532-539. |
| [30] | Ussiri D A N, Johnson C E. Characterization of organic matter in a northern hardwood forest soil by13C NMR Spectroscopy and chemical methods. Geoderma, 2003(1/2), 111: 123-149. |
| [3] | 王颖, 张振克, 朱大奎, 杨競红, 毛龙江, 李书恒. 河海交互作用与苏北平原成因. 第四纪研究, 2006, 26(3): 301-320. |
| [4] | 陈正勇, 王国祥, 刘金娥, 宣勇, 徐伟伟, 仇乐, 王刚. 苏北潮滩群落交错带互花米草斑块与土著种竞争关系研究. 生态环境学报, 2011, 20(10):1436-1442. |
| [5] | 张耀鸿, 张富存, 周晓冬, 谢晓金, 王小巍, 李强, 雷俊. 互花米草对苏北滨海湿地表土有机碳更新的影响. 中国环境科学, 2011, 31(2): 271-276. |
| [6] | 钦佩, 李思宇. 互花米草的两面性及其生态控制. 生物安全学报, 2012, 21(3): 167-176. |
| [7] | 任丽娟, 王国祥, 何聃, 毛志刚, 刘金娥. 盐城潮滩湿地不同植被带土壤有机质空间分布特征. 海洋科学进展, 2011, 29(1): 54-62. |
| [8] | 张耀鸿, 王艳玲, 李仁英, 朱红霞, 张富存, 黄宾宾, 彭晓丹.互花米草入侵对潮滩土壤活性有机碳组分的影响. 土壤通报, 2012, 43(1): 102-106. |
| [9] | 王刚, 王国祥, 杨文斌, 刘金娥, 杭子清. 互花米草海向入侵对土壤有机碳组分、来源和分布影响. 生态学报, 2013, 33(8): 2474-2783. |
| [15] | 陈孟君, 王明光, 邱志郁. 塔塔加鞍部铁杉林及玉山箭竹之根圈与本体土壤低分子量有机酸含量和有机碳官能基之测定. 土壤与环境, 1999, 2(2):159-170. |
| [22] | 毛志刚, 王国祥, 刘金娥, 任丽娟. 盐城海滨湿地盐沼植被对土壤碳氮分布特征的影响. 应用生态学报, 2009, 20(2): 293-297. |
| [23] | 万忠梅, 宋长春, 杨桂生, 黄靖宇, 王丽丽, 李英臣. 三江平原湿地土壤活性有机碳组分特征及其与土壤酶活性的关系. 环境科学学报, 2009, 29(2): 406-412. |
| [24] | 周军, 肖炜, 钦佩. 互花米草入侵对盐沼土壤微生物生物量和功能群的影响.南京大学学报: 自然科学版, 2007, 43(5): 494-500. |
| [28] | 商素云, 李永夫, 姜培坤, 周国模, 刘娟, 吴家森, 林琳. 天然灌木林改造成板栗林对土壤碳库和氮库的影响. 应用生态学报, 2012, 23(3): 659-665. |
 2014, Vol. 34
2014, Vol. 34




