文章信息
- 马彦霞, 郁继华, 张晶, 曹刚, 李杰, 张帆
- MA Yanxia, YU Jihua, ZHANG Jing, CAO Gang, LI Jie, ZHANG Fan
- 设施蔬菜栽培茬口对生态型无土栽培基质性状变化的影响
- Effect of different rotation systems on the characteristic change of ecotype soilless culture media for vegetables in greenhouse environments
- 生态学报, 2014, 34(14): 4071-4079
- Acta Ecologica Sinica, 2014, 34(14): 4071-4079
- http://dx.doi.org/10.5846/stxb201211301717
-
文章历史
- 收稿日期:2012-11-30
- 修订日期:2014-2-27
2. 定西市农业科学研究院, 定西 743000
2. Dingxi Academy of Agricultural Sciences, Dingxi 743000, China
随着生态农业和可持续循环农业的发展,设施番茄生态型无土栽培发展很快,栽培面积不断扩大。但是,由于种植习惯和降低基质成本的需要,设施番茄栽培中基质的重复利用较为普遍,导致的连作障碍问题也日益突出[1],成为制约番茄生态型无土栽培可持续发展的重要因素。大量研究表明,发生连作障碍的根本原因是由于连续单一种植同一作物引起了土壤酶活性下降,作物根圈微生态平衡失调,土壤理化性质变劣[2, 3, 4]等。据报道,辣椒连作对土壤微生态环境产生显著影响,导致生态平衡破坏,这可能是导致辣椒连作障碍的主要原因之一[5];大豆连作障碍的原因可能更主要的归结于大豆根圈土壤微生态环境的改变[6],那么,设施番茄连作障碍的原因是否也是由于根圈基质微生态环境的改变造成的?目前还没有相关报道。
根圈土壤酶活性是土壤根圈微生态环境中生理活性最强的部分,是评价土壤微生态环境质量和土壤生产力的重要指标[7]。樊军等[8]认为不同栽培方式和作物茬口对土壤酶活性有不同的影响;杨丽娟[9]报道,菜园土壤的转化酶活性与黄瓜产量呈显著或极显著正相关;张新慧[10]等的研究表明,不同茬口对当归根圈土壤酶活性及其产量和品质的影响差异很大,多酚氧化酶活性在整个生育期均是连茬显著高于正茬;大豆轮作与连作不同年限土壤酶活性有较大变化,与正茬相比,迎茬、连作土壤酶活性均降低[11]。此外,土壤酶活性与土壤理化性状密切相关[12],研究表明,作物连作可导致土壤理化性状变差、土壤酶活性降低,产量下降[13]。
实践证明,轮作和间套作是克服作物连作障碍的有效途径[14]。迄今关于连作和轮作与土壤酶活性及理化性状的关系已有大量研究[9, 12],但认识尚不一致。本文系统研究了不同茬口对基质酶活性和理化性状的影响,以期为设施番茄生态型无土栽培的可持续发展和减轻连作障碍提供参考依据。
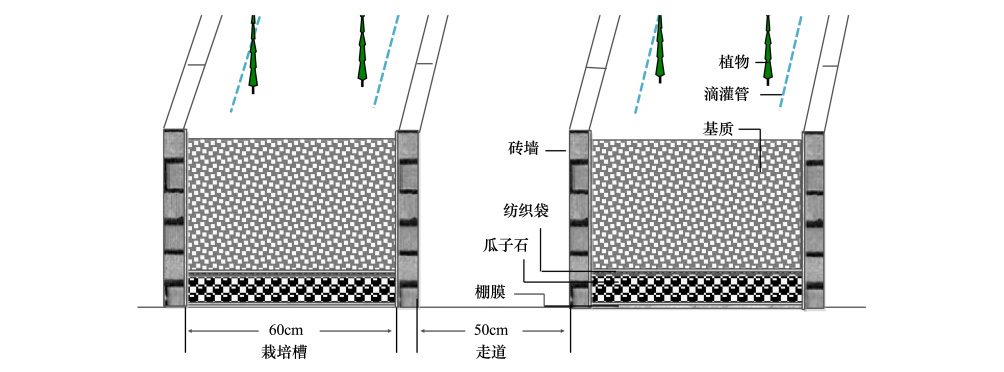
1 材料与方法 1.1 试验材料地概况试验基质采自酒泉市戈壁绿丰农业专业合作社非耕地设施蔬菜标准园温室,标准园主要产品为温室一大茬番茄,番茄品种为粉红果。该园区是2009年国家非耕地有机生态无土栽培关键技术研究和产业示范重点园区,也是肃州区 “一特四化”设施农业示范基地之一。标准园由合作社统一品种、统一技术指导、统一标准管理。园内统一采用基质槽培,栽培槽为下挖式砂石栽培槽,槽内径60 cm,槽深30 cm,槽长7 m,呈“U”型,槽两边码1层砖,槽间走道80 cm,走道内径50 cm,槽内壁铺一层棚膜,底部填5 cm厚的瓜子石,上铺一层编织袋,再填充25 cm深的栽培料。
试验番茄品种为“欧盾”,粉果、无限生长型,株行距25 cm×40 cm,每1个栽培槽为1个小区,每小区28株。番茄9月上中旬播种育苗,10月下旬定植,6月中下旬采收结束。一个生长季共追肥2次,第1次在第1花序坐果后,果实似核桃大时追肥,第2次在盛果期追肥,每次追施大三元复合肥300 kg/hm2和有机肥22.5 m3/hm2(鸡粪 ∶ 牛粪=1 ∶ 3),在栽培槽中间施肥。灌水方式为膜下滴灌,每槽铺设两根双上孔型薄壁软管(Φ=0.25 cm),滴水孔间距25 cm。
1.2 试验设计试验选用基质为不同茬口的生态型无土栽培基质,基质成分为:炉渣、菌渣、牛粪、鸡粪、玉米秸秆按体积比13 ∶ 5 ∶ 5 ∶ 2 ∶ 14组成。基质茬口为 ① 正茬:豇豆-黄瓜-番茄;② 迎茬:番茄-黄瓜-番茄;③ 连茬:黄瓜-番茄-番茄。
试验共设4个处理,分别为正茬、迎茬、连茬,以新基质为对照(CK),每1个温室(温室管理条件一致)为1个处理,每3个小区为1个重复,每处理3次重复,分别取温室东西两边和中间的小区,为防止边际效应影响,减小误差,每小区均设2—3行保护行。所有处理均同时进行。
|
| 图 1 栽培槽结构示意图 Fig.1 Schematic diagram of cultivation bed used in the experiment |
各处理均在结果末期取样,取样时在栽培槽中采用五点法呈S型取根系周围0—15 cm基质层,每小区取样1 kg,然后将各小区基质混合,剔除基质鲜样中可见的动植物残体,过1 mm筛,将过筛基质储于4 ℃冰箱中待测。
试验的前期种植在非耕地设施蔬菜标准园日光温室中进行的,试验温室为半地下式无立柱砖混结构,坐北向南偏西10°,长度50 m、跨度8 m、脊高3.9 m、前屋面合理采光角度 43°。种植结束后,将采样基质带回甘肃农业大学农学院实验室进行生物、理化性质的测定。
1.3 测定项目与方法 1.3.1 基质酶活性的测定基质蔗糖酶活性用3,5-二硝基水杨酸比色法测定[15];纤维素酶活性采用蒽酮比色法[15];多酚氧化酶活性测定采用邻苯三酚比色法[15];脱氢酶参照文献[16]方法测定。酶活性测试均重复3次。
1.3.2 基质理化性状的测定基质容重、总孔隙度、通气孔隙度等特性的测定参照郭世荣[17]的方法;酸碱度(pH值)和电导率(EC)测定参照程斐等的方法[18];用烘干称重法测基质绝对含水量:绝对含水量(%)=(基质湿重-基质干重)/基质干重×100%。
1.3.3 生理生态指标的可塑性根据Valladares等[19]的方法计算:可塑性指标(PI)=(最大值-最小值)/最大值×100%,式中PI为可塑性指标,最大值为测定指标的最大值,最小值为所测定指标最小值。
1.4 数据处理数据采用SPSS 16. 0软件进行ANOVA方差分析和Duncan′s新复极差法多重比较,并进行相关性分析。其他统计分析采用Excel 2003处理。
2 结果与分析 2.1 不同茬口对设施番茄根圈基质酶活性的影响 2.1.1 蔗糖酶土壤蔗糖酶是评价土壤中物质转化强度的酶类,它的活性不仅可以表征土壤生物学活性强度,也可作为评价土壤熟化程度和肥力水平的指标[20]。从表 1可以看出,不同茬口对设施番茄根圈基质蔗糖酶活性的影响较显著,其中正茬的蔗糖酶活性最高,且与其他处理差异显著或极显著;连茬的基质蔗糖酶活性最低,仅为6.13 mg/g,比对照降低了69.2%,说明连茬降低了基质的熟化程度和肥力水平。
2.1.2 纤维素酶土壤纤维素酶有助于腐殖质的形成和碳素养分的释放,纤维素的分解利用不仅对提高土壤肥力和增加作物产量具有十分重要的意义,而且也是自然界碳素循环的重要环节,它能水解纤维素中的β-1,4-糖苷键[21]。由表 1可知,种植番茄后基质的纤维素酶活性均显著(P<0.05)高于对照,其中以连茬的纤维素酶活性最高,其次为迎茬、正茬。连茬的酶活性高,原因可能与连茬番茄残体积累和根系分泌物的产生、积累有关;而正茬酶活性低,可能是由于正茬的环境和营养条件都不利于纤维分解菌的繁殖和活动。
2.1.3 脱氢酶脱氢酶是典型的胞内酶,其活性的大小既反映土壤的物质代谢能力,也可间接反映土壤微生物的数量和活性。不同茬口基质的脱氢酶活性差异显著(表 1),正茬的酶活性最高,比对照提高了68.3%,且与其他处理达差异显著或极显著水平;迎茬的酶活性次之,比正茬的降低了26.5%;连茬的酶活性与对照差异不显著,与正茬、迎茬差异显著。说明种植番茄可提高基质的脱氢酶活性,可提高基质的物质代谢能力。
|
处理
Treatment | 蔗糖酶
Invertase/(mg/g) | 纤维素酶
Cellulase/(mg/g) | 脱氢酶
Dehydrogenase/(μg/g) | 多酚氧化酶
Polyphenol oxidase/(mg/g) |
| 不同的小写字母表示处理间在5%水平上的差异显著(P<0.05);不同的大写字母表示处理间在1%水平上的差异显著(P<0. 01) | ||||
| 正茬Normal cropping | 29.54±0.443aA | 46.34±0.813cB | 13.15±0.512aA | 1.97±0.069cC |
| 迎茬 Alternate cropping | 17.17±0.318cC | 66.55±0.703bA | 9.66±0.325bB | 3.31±0.066bB |
| 连茬 Continuous cropping | 6.12±0.108dD | 68.41±0.564aA | 8.21±0.251cC | 5.18±0.084aA |
| 新基质(CK) New matrix | 20.19±0.512bB | 35.68±0.958dC | 7.82±0.316cC | 2.07±0.038cC |
土壤多酚氧化酶主要来源于根圈微生物、植物根系分泌物及动植物残体分解释放的酶,是一种复合性酶。从表 1可以看出,不同茬口间基质的多酚氧化酶活性差异显著,其活性大小为连茬>迎茬>正茬,但正茬的酶活性与对照间差异不显著,由此可见,连茬和迎茬有助于基质多酚氧化酶的积累,正茬对多酚氧化酶活性的抑制作用显著大于迎茬和连茬。
2.2 不同茬口对设施番茄根圈基质主要理化性状的影响不同茬口基质的理化性状差异显著,由表 2可知,连茬基质的容重最大,为0.695 g/cm3;对照容重最小,为0.329 g/cm3,各种茬口的基质容重差异显著,但所有茬口基质的容重都在理想基质[22] (0.1—0.8g/cm3)的范围之内。除连茬基质的酸碱度(pH值)略高于理想基质外,其他处理的都能满足理想基质的要求(6.0—7.5)。电导率(EC)是基质化学性质的指标,它反映基质中原来带有的可溶性盐分的多少。EC值过高,容易发生盐害,烧苗;EC值过低,作物生长不良,表 2中对照和不同茬口基质的电导率都在理想EC值范围内。3种茬口中,连茬基质的绝对含水量最小,为9.206%;正茬的绝对含水量最高,为9.71%,与连茬差异显著,与迎茬差异不显著。从表 3可以看出,对照的总孔隙度略大于理想基质的最低要求,种植番茄后基质的总孔隙度均显著低于理想基质的要求(总孔隙度大于75%);而通气孔隙度除连茬外,正茬和迎茬均能满足理想基质的要求(通气孔隙度大于15%);3种茬口的持水孔隙度均在理想基质(40%—75%)要求的范围内;3个茬口基质的大小孔隙比正茬最大,连茬最小,除连茬的大小孔隙比略低于理想基质外,正茬和迎茬的均在理想基质要求的范围内。
|
处理
Treatment | 容重
Bulk density/(g/cm3) | pH | 电导率(EC)
/(ms/cm) | 绝对含水量
Absolute water content/% |
| 正茬Normal cropping | 0.405±0.014cC | 6.477±0.075dD | 1.737±0.038bB | 9.71±0.249aA |
| 迎茬Alternate cropping | 0.575±0.007bB | 6.88±0.075cB | 1.303±0.153cC | 9.402±0.263abA |
| 连茬Continuous cropping | 0.695±0.010aA | 7.60±0.140aA | 1.127±0.015dD | 9.206±0.218bA |
| 新基质(CK) New matrix | 0.329±0.005dD | 7.18±0.148bB | 1.923±0.057aA | 8.202±0.187cB |
| 理想基质Ideal matrix | 0.1—0.8 | 6.0—7.5 | <2.5 |
|
处理
Treatment | 总孔隙度
Total porosity/% | 通气孔隙度
Aeration porosity/% | 持水孔隙度
Water retaining porosity/% | 大小孔隙比
Void ratio |
| 正茬Normal cropping | 72.94±0.715bB | 17.77±1.172bB | 55.17±0.717aA | 0.322±0.025bB |
| 迎茬Alternate cropping | 70.80±0.383cC | 15.93±0.996cB | 54.88±0.868aA | 0.290±0.022bB |
| 连茬Continuous cropping | 64.86±0.196Dd | 12.45±0.597dC | 52.40±0.788bB | 0.238±0.015cC |
| 新基质(CK)New matrix | 75.29±0.513aA | 21.55±1.404aA | 53.75±1.314abAB | 0.401±0.036aA |
| 理想基质Ideal matrix | >75 | >15 | 40—75 | 0.25—0.67 |
从表 4可以看出,基质酶活性与主要理化性质有着密切的关系,但不同理化性质表现出的相关性存在差异。多酚氧化酶、蔗糖酶和纤维素酶活性与基质理化性质的相关性显著,而脱氢酶活性与理化性质的相关性较小。其中脱氢酶活性与pH值呈极显著负相关(P<0.01),与绝对含水量呈极显著正相关,与持水孔隙度呈显著正相关;多酚氧化酶活性与
| pH | 电导率(EC)
Electrical conductivity | 绝对含水量
Absolute water content | 容重
Bulk density | 总孔隙度
Total porosity | 通气孔隙度
Aeration porosity | 持水孔隙度
Holding water porosity | 大小孔隙比
Void ratio | |
| n=12,*P<0. 05,**P<0. 01 | ||||||||
| 脱氢酶 Dehydrogenase | -0.838* * | 0.213 | 0.719* * | -0.244 | 0.235 | 0.036 | 0.591* | -0.035 |
| 多酚氧化酶 Polyphenol oxidase | 0.746* * | -0.910* * | 0.175 | 0.947* * | -0.963* * | -0.867* * | -0.602* | -0.810* * |
| 蔗糖酶Invertase | -0.901* * | 0.766* * | 0.172 | -0.803* * | 0.807* * | 0.650* | 0.696* | 0.578* |
| 纤维素酶 Cellulase | 0.339 | -0.983* * | 0.512 | 0.963* * | -0.858* * | -0.894* * | -0.226 | -0.879* * |
基质pH值和容重呈极显著正相关(相关系数为0.746* *、0.947* *),与EC值、总孔隙度、通气孔隙度、持水孔隙度、大小孔隙比呈极显著负相关;蔗糖酶活性与pH值、容重呈极显著负相关关系,与EC值、总孔隙度呈极显著正相关,与通气孔隙度、持水孔隙度、大小孔隙比呈显著正相关;纤维素酶活性与EC值、总孔隙度、通气孔隙度、大小孔隙比呈极显著负相关,与容重呈极显著正相关。
2.4 不同茬口对设施番茄根圈基质酶活性和理化性状可塑性的影响表型可塑性是生物适应变化的环境的重要方式[23]。由表 5可知,对照的可塑性指数除绝对含水量、总孔隙度、通气孔隙度、持水孔隙度外,其他指标的可塑性指数均为最大;连茬基质的可塑性指数均较低,其中脱氢酶、多酚氧化酶、纤维素酶、绝对含水量、总孔隙度、通气孔隙度、大小孔隙比的可塑性指数均最小;与对照相比,正茬基质各指标的可塑性指数除容重、总孔隙度和通气孔隙度最大外,其他指标的可塑性指数均低于对照。由此可见,新基质的适应性较好,连茬基质的适应性较差。不同茬口基质各指标的可塑性指数大小分别为正茬(大小孔隙比>通气孔隙度>脱氢酶>容重>绝对含水量>EC值>多酚氧化酶>纤维素酶>蔗糖酶>持水孔隙度>pH值>总孔隙度)、迎茬(大小孔隙比>通气孔隙度>脱氢酶>绝对含水量>多酚氧化酶>蔗糖酶>持水孔隙度>EC>容重>pH值>纤维素酶>总孔隙度)、连茬(大小孔隙比>通气孔隙度>脱氢酶>绝对含水量> pH值>蔗糖酶>多酚氧化酶>持水孔隙度> EC值 >容重>纤维素酶>总孔隙度)。
|
生理生态参数
Eco-physiological parameter | 正茬
Normal cropping | 迎茬
Alternate cropping | 连茬
Continuous cropping | 新基质(CK)
New matrix |
| 脱氢酶 Dehydrogenase | 7.455 | 6.232 | 5.588 | 7.665 |
| 多酚氧化酶 Polyphenol oxidase | 3.153 | 3.937 | 3.145 | 6.494 |
| 蔗糖酶Invertase | 2.918 | 3.363 | 3.148 | 4.412 |
| 纤维素酶 Cellulase | 3.042 | 2.048 | 1.589 | 4.846 |
| 酸碱度(pH值) | 2.290 | 2.158 | 3.351 | 3.673 |
| 电导率(EC) Electrical conductivity | 3.933 | 2.273 | 2.632 | 5.584 |
| 绝对含水量Absolute water content | 4.949 | 4.993 | 4.166 | 4.466 |
| 容重 Bulk density | 6.018 | 2.223 | 2.581 | 3.158 |
| 总孔隙度 Total porosity | 1.715 | 1.066 | 0.597 | 1.244 |
| 通气孔隙度 Aeration porosity | 12.381 | 11.723 | 9.103 | 11.788 |
| 持水孔隙度 Holding water porosity | 2.376 | 3.025 | 2.953 | 4.726 |
| 大小孔隙比Void ratio | 14.147 | 14.393 | 11.787 | 15.957 |
根圈是一个很特别的微区域,由于植物根系的影响,使其周围的微域在物理、化学和生物特性方面与土体主体不同[24]。土壤酶是表征土壤中物质、能量代谢旺盛程度和土壤质量水平的一个重要生物指标[2]。本研究中,不同茬口对设施番茄根圈基质蔗糖酶、纤维素酶、多酚氧化酶和脱氢酶活性的影响较显著。蔗糖酶活性的强弱反应了土壤熟化程度和肥力水平,对增加土壤中易溶性营养物质起重要作用[2]。张淑香等[25]发现大豆连作土壤蔗糖酶活性降低;大棚冬闲季节在连作番茄的有机基质中轮作蒜苗、白菜和莴苣,能显著提高基质中蔗糖酶活水平[7]。本研究结果表明,基质蔗糖酶活性以正茬最高、连茬最低,说明连茬使基质的生物学活性、熟化程度和肥力水平变差,这可能是由于连茬栽培产生了某些对基质生物化学过程有抑制作用的物质。纤维素酶是表征土壤碳素循环速率的重要指标,在降解有机碳复合物(植物残茬、人畜粪便等)的过程中发挥重要作用,其水解产物(糖类)是土壤微生物的主要能量来源[26]。有研究认为,与正茬相比,大豆连作2a的成熟期土壤中纤维素酶活性最低[27],这与本研究结果相悖,可能是由于土壤与基质的理化性质不同造成的,因为基质较土壤疏松、富含维生素、蛋白质等营养物质,有利于微生物活动,可促进酶的分泌。多酚氧化酶在土壤有机质形成中起重要作用,它参与土壤有机组分中芳香族化合物的转化,对增加土壤有机质含量,提高土壤肥力具有重要意义。本研究中,连茬基质的多酚氧化酶活性最高、正茬最小,这与张新慧[10]等在当归上的研究结果一致,这可能是由于番茄根系分泌物质经过诱导作用而使基质中多酚氧化酶的活性增强。多酚氧化酶专一性很强,它的活性高会阻碍有机质矿化过程中产生的酚类中间产物进一步合成腐殖质,导致酚类化合物的积累[28],从而引起中毒。脱氢酶是一种典型的胞内酶,它存在于所有微生物体内,与土壤呼吸具有极显著的相关关系,可以作为土壤微生物活性的指示指标[29, 30]。研究表明,莓-稻轮作能提高草莓连作土壤的脱氢酶活性[31],稻麦轮作土壤中脱氢酶活性非常高,连作露地蔬菜土壤中脱氢酶活性显著下降[32],本研究也得出了类似的结果,正茬基质的脱氢酶活性最高,迎茬酶活性次之,连茬最低,但3个茬口的脱氢酶活性均高于新基质,可能是种植番茄后引起了基质中微生物区系发生改变进而引起脱氢酶活性的显著增加,提高了基质的物质代谢能力。
土壤的物理性质是影响土壤酶活性的重要因素之一,而土壤容重是土壤重要的物理性质之一,它不仅直接影响到土壤孔隙度与孔隙大小分配、土壤的穿透阻力及土壤水肥气热变化[33],也影响着土壤酶活性的变化。土壤容重和酶活性之间关系十分密切,容重过大,土壤通气差,养分转化和供应慢。研究表明,连作后,土壤结构破坏严重,表现为容重增大,大小孔隙比相对降低,土壤含盐量逐渐增加,有次生盐渍化倾向[34, 35],烟田连作导致土壤的酸化、酶活性显著下降[36]。本研究发现,不同茬口对基质的理化性质影响差异显著,连茬基质的容重和pH值最大,而EC值、绝对含水量、总孔隙度、通气孔隙度、持水孔隙度与大小孔隙比均最小,连茬基质的pH值、总孔隙度、通气孔隙度和持水孔隙度均不在理想基质的范围之内,这与柴仲平[37]等的研究结果相似,说明连茬改变了基质的理化性质,破坏了基质的结构,不利于维持质地和持续利用。
土壤理化性状是影响作物生长发育的重要因素,是反映土壤肥力的重要指标,与土壤酶活性有着密切关系。土壤酶活性与理化性状有一定的相关性,本研究结果表明,多酚氧化酶活性与基质pH值和容重呈极显著正相关,与EC、总孔隙度、通气孔隙度、持水孔隙度、大小孔隙比呈极显著负相关;蔗糖酶活性与pH值、容重呈极显著负相关关系,与EC、总孔隙度呈极显著正相关,与通气孔隙度、持水孔隙度、大小孔隙比呈显著正相关;纤维素酶活性与EC、总孔隙度、通气孔隙度、大小孔隙比呈极显著负相关,与容重呈极显著正相关;脱氢酶活性与pH值呈极显著负相关,与绝对含水量呈极显著正相关,与持水孔隙度呈显著正相关。说明脱氢酶活性的大小对基质理化性状的影响不显著;多酚氧化酶和纤维素酶活性与基质理化性状的相关性趋势基本一致,当基质容重增大时,多酚氧化酶和纤维素酶活性均显著增强,腐殖质合成增多,酚类化合物积累,引起毒害;蔗糖酶活性对总孔隙度和持水孔隙度具有正效应,当基质的总孔隙度和持水孔隙度增大时,蔗糖酶的活性也显著增强,这将有利于营养物质的水解,为植物提供营养,促进植物生长。
可塑性是表型进化的一个基本特点,是植物种群适应环境异质性的重要途径,是生物界中普遍存在的现象[38]。本研究中,连茬基质的可塑性指数均较低,其中脱氢酶、多酚氧化酶、纤维素酶、绝对含水量、总孔隙度、通气孔隙度、大小孔隙比的可塑性指数均最小;与对照相比,正茬基质各指标的可塑性指数除绝对含水量、容重、总孔隙度和通气孔隙度最大外,其他指标的可塑性指数均低于对照。说明基质种植番茄后其适应环境的能力减弱,不同的作物茬口对基质酶活性和理化性质的影响很大,其中连茬的影响力最大,适应环境的能力最差。
4 结论综上所述,蔗糖酶、多酚氧化酶和纤维素酶活性是影响基质pH值、EC和理化性质的重要因素;大小孔隙比、通气孔隙度、脱氢酶活性和绝对含水量能较其他指标更好地反映不同茬口基质的优越性;不同茬口基质生物、理化性状的优越性表现为:正茬>迎茬>连茬;设施生态型无土栽培番茄连茬严重破坏了基质的生物和理化性质,正茬栽培对基质生物和理化性质的影响较小。
| [1] | Abla W, Yushan A. The barrier under succession cropping and prevention measures in greenhouse. Xinjiang Agricultural Science and Technology, 2008, (3): 47. |
| [2] | Sun Y Y, Jiang G Y, Liu J G, Zhang W, Tang Z M. Effects of continuous cropping tomato for processing on soil enzyme activities and microbial flora. Acta Ecologica Sinica, 2010, 30(13): 3599-3607. |
| [3] | Liu S H, Liu S Q, Zhang Z K, Wei H, Qi J J, Duan J F. Influence of garlic continuous cropping on rhizosphere soil microorganisms and enzyme activities. Scientia Agricultura Sinica, 2010, 43(5): 1000-1006. |
| [4] | Liu J G, Zhang W, Li Y B, Sun Y Y, Bian X M. Effects of long-term continuous cropping system of cotton on soil physical-chemical properties and activities of soil enzyme in oasis in Xinjiang. Scientia Agricultura Sinica, 2009, 42(2): 725-733. |
| [5] | He Z G, Wang X J, Dong H, Lou C R, Niu S W, Yu T. Study on microbial and enzyme activity of capsicum soil different ages in sunlight greenhouse. Soil and Fertilizer Sciences in China, 2013, (1): 42-46. |
| [6] | Wang G H, Jin J, Pan X W, Zhou K Q, Liu X B. Effect of different rotation systems on soil pH and N nutrition distribution across soybean rhizosphere. Chinese Journal of Oil Crop Sciences, 2004, 26(1): 55-59. |
| [7] | Li W, Cheng Z H, Meng H W, Zhou J, Liang J, Liu X J. Effect of rotating different vegetables on microbiomass and enzyme in tomato continuous cropped substrate and afterculture tomato under plastic tunnel cultivation. Acta Horticulturae Sinica, 2012, 39(1): 73-80. |
| [8] | Fan J, Hao M D. Study on long-term experiment of crop rotation and fertilization in the Loess Plateau I. Effect of crop rotation and continuous planting on soil enzyme activities. Nutrition and Fertilizer Science, 2003, 9(1): 9-13. |
| [9] | Yang L J, Xu H, Qiu Z X, Liu Y Q. Relationship between activities of enzyme and cucumber yield in vegetable soil. Plant Nutrition and Fertilizer Science, 2000, 6(1): 113-116. |
| [10] | Zhang X H, Zhang E H, Lang D Y, Zhao Y S, Wang H Z. Effect of different cropping rotations on enzyme activities in rhizosphere soil and production quality of Angelica sinensis. Chinese Traditional and Herbal Drugs, 2011, 42(11): 2322-2325. |
| [11] | Wang S Q, Han X Z, Qiao Y F, Wang S Y, Li X H, Xu Y L. Variation of soil enzymes activity and relevant nutrients at different years of soybean (Glycine max L.) rotation, alternate and continuous cropping. Soybean Science, 2009, 28(4): 611-615. |
| [12] | Zheng L L, Ren M B, Chen X, Shi Y, Ma X H, Tian L, Zhang J G, Wang W J, Wu Y H, Yuan J, Zhang Z F. Effects of different tobacco planting systems on soil enzyme activities. Chinese Tobacco Science, 2010, 31(3): 23-28. |
| [13] | Liu J G, Bian X M, Li Y B, Zhang W, Li S. Effects of long-term continuous cropping of cotton and returning cotton stalk into field on soil biological activities. Chinese Journal of Applied Ecology, 2008, 19(5): 1027-1032. |
| [14] | Hao L X, Cheng Z H, Meng H W, Sun J L, Han L. Biological and ecological effect of interplanting tomato/garlic in the facility: influence of interplanting dates on growth, development and yield of different Garlic Cultivars. Acta Ecologica Sinica, 2010, 30(19): 5316-5326. |
| [15] | Guan S Y. Soil Enzyme Activity and Research Methods. Beijing: Agricultural Press, 1986: 274-276, 291-293, 323-325. |
| [16] | Carbonell G, Pablos M V, García P, Ramos C, Sánchez P, Fernández C, Tarazona J V. Rapid and cost-effective multiparameter toxicity tests for soil microorganisms. The Science of the Total Environment, 2000, 247(2/3): 143-150. |
| [17] | Guo S R. Soilless Culture. Beijing: China Agriculture Press, 2003: 423-424. |
| [18] | Cheng F, Sun Z H, Zhao Y G, Li S J. Analysis of physical and chemical properties of reed residue substrate. Journal of Nanjing Agricultural University, 2001, 24(3): 19-22. |
| [19] | Valladares F, Wright S J, Lasso E, Kitajima K, Pearcy R W. Plastic phenotypic response to light of 16 congeneric shrubs from a panamanian rainforest. Ecology, 2000, 81(7): 1925-1936. |
| [20] | Alef K, Nannipieri P. Methods in Applied Soil Microbiology and Biochemistry. London: Academic Press, 1995: 229-355. |
| [21] | Thauer R K. Biochemistry of methanogenesis: A tribute to Marjory Stephenson: 1998 marjory stephenson prize lecture. Microbiology, 1998, 144(9): 2377-2406. |
| [22] | Li J, Zhao X L, Wei S Q, Zheng J F, Hu Y Z. Study on the physico-chemical properties of soil-less cultural substrates of pollution-free vegetable. Journal of Southwest Agricultural University: Natural Science, 2000, 22(2): 112-115. |
| [23] | Ma Y X, Yu J H, Zhang G B, Cao G. Protective Effects of exogenous chitosan on oxidative damage in pepper seedling leaves under water stress. Scientia Agricultura Sinica, 2012, 45(10): 1964-1971. |
| [24] | Ma D Y, Guo T C, Song X, Wang C Y, Zhu Y J, Wang Y H, Yue Y J, Zha F N. Effects of urea application rate on the quantity of microorganisms and activity of enzymes in wheat rhizosphere. Acta Ecologica Sinica, 2007, 27(12): 5222-5228. |
| [25] | Zhang S X, Gao Z Q, Liu H L. Continuous cropping obstacle and rhizospheric microecology Ⅱ. Root exudates and phenolic acids. Chinese Journal of Applied Ecology, 2000, 11(1): 152-156. |
| [26] | Keeler B L, Hobbie S E, Kellogg L E. Effects of long-term nitrogen addition on microbial enzyme activity in eight forested and grassland sites: implications for litter and soil organic matter decomposition. Ecosystems, 2009, 12(1): 1-15. |
| [27] | Fu H L, Zhan J R, Zhou Y Z, Yang Z M. The effect of soybean continuous cropping on soil cellulolytic enzyme activity. Soybean Science, 1999, 18(1): 81-84. |
| [28] | Zhang X H, Zhang E H. Effect of various rotation systems on yield of Angelica sinensis and microbial populations in its rhizosphere. Chinese Traditional and Herbal Drugs, 2008, 39(2): 267-269. |
| [29] | Bolton H, Elliott L F, Papendick R I, Bezdicek D F. Soil microbial biomass and selected soil enzyme activities: effect of fertilization and cropping practices. Soil Biology and Biochemistry, 1985, 17(3): 297-302. |
| [30] | Nannipieri P, Grego S, Ceccanti B Ecological Significance of the Biological Activity in Soil. Soil biochemistry, 1990, 6:293-355. |
| [31] | Chen Y Q, Dong Y H, Wang H, Huang G Y, Huo H Z. Effects of different agricultural managements on characteristics of soil microbial community under continuous cropped strawberry (Fragaria ananassa Duchesne). Agricultural Science & Technology, 2011, 12(6): 870-875. |
| [32] | Zhang H Y, Yin R, Huang J F, Lin X G, Cao Z H, Wang J H. Changes in soil biochemical properties caused by cropping system alteration from rice-wheat rotation to vegetable cultivation. Soils, 2005, 37(2): 182-186. |
| [33] | Xie K Z, Xu P Z, Yan C, Zhang F B, Chen J S, Tang S H, Huang X, Gu W J. Study the effects of soil improvement on acid soil in the south of China. Chinese Agricultural Science Bulletin, 2009, 25(20): 160-165. |
| [34] | Elliott G C. Urea hydrolysis in potting media. Journal of the American Society for Horticultural Science, 1986, 11(6): 862-866. |
| [35] | Carlile W R, Wilson D P. Microbial activity in growing media: a brief review. Acta Horticulturae, 1991, 294: 197-206. |
| [36] | Yu N, Guan L Z, Lou Y L, Ma Y, Yan L. Lime application regulates soil acidity and restores enzyme activities in the fields cultivated continuously with tobacco, Northern China. Chinese Journal of Soil Science, 2008, 39(4): 849-851. |
| [37] | Chai Z P, Liang Z, Wang X M, Jia H T. The Influence of the continuous cropping to the physicochemical characters of cotton soil. Chinese Agricultural Science Bulletin, 2008, 24(8): 192-195. |
| [38] | Ma Y X, Yu J H, Zhang G B, Cao G, Li W L. Effects of glutathione on photosynthetic characteristics of pepper leaves under autotoxicity. Journal of Nuclear Agricultural Sciences, 2012, 26(2): 396-402. |
| [1] | 温切木·阿不拉, 艾尼瓦尔·玉山. 温室蔬菜连作障碍及其防止措施. 新疆农业科技, 2008, (3): 47. |
| [2] | 孙艳艳, 蒋桂英, 刘建国, 张伟, 唐志敏. 加工番茄连作对农田土壤酶活性及微生物区系的影响. 生态学报, 2010, 30(13): 3599-3607. |
| [3] | 刘素慧, 刘世琦, 张自坤, 尉辉, 齐建建, 段吉锋. 大蒜连作对其根际土壤微生物和酶活性的影响. 中国农业科学, 2010, 43(5): 1000-1006. |
| [4] | 刘建国, 张伟, 李彦斌, 孙艳艳, 卞新民. 新疆绿洲棉花长期连作对土壤理化性状与土壤酶活性的影响. 中国农业科学, 2009, 42(2): 725-733. |
| [5] | 何志刚, 王秀娟, 董环, 娄春荣, 牛世伟, 于涛. 日光温室辣椒连作不同年限土壤微生物种群变化及酶活性研究. 中国土壤与肥料, 2013, (1): 42-46. |
| [6] | 王光华, 金剑, 潘相文, 周克琴, 刘晓冰. 不同茬口大豆根圈土壤pH值和氮营养分布的变化. 中国油料作物学报, 2004, 26(1): 55-59. |
| [7] | 李威, 程智慧, 孟焕文, 周静, 梁静, 刘雪娇. 轮作不同蔬菜对大棚番茄连作基质中微生物与酶及后茬番茄的影响. 园艺学报, 2012, 39(1): 73-80. |
| [8] | 樊军, 郝明德. 黄土高原旱地轮作与施肥长期定位试验研究Ⅰ. 长期轮作与施肥对土壤酶活性的影响. 植物营养与肥料学报, 2003, 9(1): 9-13. |
| [9] | 杨丽娟, 须晖, 丘忠祥, 刘永青. 菜田土壤酶活性与黄瓜产量的关系. 植物营养与肥料学报, 2000, 6(1): 113-116. |
| [10] | 张新慧, 张恩和, 郎多勇, 赵云生, 王惠珍. 不同茬口对当归根际土壤酶活性及其产量和品质的影响. 中草药, 2011, 42(11): 2322-2325. |
| [11] | 王树起, 韩晓增, 乔云发, 王守宇, 李晓慧, 许艳丽. 寒地黑土大豆轮作与连作不同年限土壤酶活性及相关肥力因子的变化. 大豆科学, 2009, 28(4): 611-615. |
| [12] | 郑林林, 任明波, 陈旭, 石屹, 马兴华, 田磊, 张继光, 王文杰, 吴元华, 元建, 张忠锋. 不同种植方式下烤烟烟田土壤酶活性研究. 中国烟草科学, 2010, 31(3): 23-28. |
| [13] | 刘建国, 卞新民, 李彦斌, 张伟, 李崧. 长期连作和秸秆还田对棉田土壤生物活性的影响. 应用生态学报, 2008, 19(5): 1027-1032. |
| [14] | 郝丽霞, 程智慧, 孟焕文, 孙金利, 韩玲. 设施番茄套作大蒜的生物和生态效应——套播时期对不同品种大蒜生长发育和产量的影响. 生态学报, 2010, 30(19): 5316-5326. |
| [15] | 关松荫. 土壤酶及其研究法. 北京: 农业出版社, 1986: 274-276, 291-293, 323-325. |
| [17] | 郭世荣. 无土栽培学. 北京: 中国农业出版社, 2003: 423-424. |
| [18] | 程斐, 孙朝晖, 赵玉国, 李式军. 芦苇末有机栽培基质的基本理化性能分析. 南京农业大学学报, 2001, 24(3): 19-22. |
| [22] | 李静, 赵秀兰, 魏世强, 郑建锋, 胡勇智. 无公害蔬菜无土栽培基质理化特性研究. 西南农业大学学报: 自然科学版, 2000, 22(2): 112-115. |
| [23] | 马彦霞, 郁继华, 张国斌, 曹刚. 壳聚糖对水分胁迫下辣椒幼苗氧化损伤的保护作用. 中国农业科学, 2012, 45(10): 1964-1971. |
| [24] | 马冬云, 郭天财, 宋晓, 王晨阳, 朱云集, 王永华, 岳艳军, 查菲娜. 尿素施用量对小麦根际土壤微生物数量及土壤酶活性的影响. 生态学报, 2007, 27(12): 5222-5228. |
| [25] | 张淑香, 高子勤, 刘海玲. 连作障碍与根际微生态研究Ⅱ. 根系分泌物与酚酸物质. 应用生态学报, 2000, 11(1): 152-156. |
| [27] | 傅慧兰, 战景仁, 周曰哲, 杨振明. 大豆连作对土壤纤维素酶活性的影响. 大豆科学, 1999, 18(1): 81-84. |
| [28] | 张新慧, 张恩和. 不同茬口对当归根际微生物数量和产量的影响. 中草药, 2008, 39(2): 267-269. |
| [32] | 张华勇, 尹睿, 黄锦法, 林先贵, 曹志洪, 王俊华. 稻麦轮作田改为菜地后生化指标的变化. 土壤, 2005, 37(2): 182-186. |
| [33] | 解开治, 徐培智, 严超, 张发宝, 陈建生, 唐拴虎, 黄旭, 顾文杰. 不同土壤改良剂对南方酸性土壤的改良效果研究. 中国农学通报, 2009, 25(20): 160-165. |
| [36] | 于宁, 关连珠, 娄翼来, 马莹, 颜丽. 施石灰对北方连作烟田土壤酸度调节及酶活性恢复研究. 土壤通报, 2008, 39(4): 849-851. |
| [37] | 柴仲平, 梁智, 王雪梅, 贾宏涛. 连作对棉田土壤物理性质的影响. 中国农业通报, 2008, 24(8): 192-195. |
| [38] | 马彦霞, 郁继华, 张国斌, 李雯琳, 曹刚. 谷胱甘肽对自毒作用下辣椒叶片光合特性的影响. 核农学报, 2012, 26(2): 396-402. |
 2014, Vol. 34
2014, Vol. 34




