文章信息
- 谭秋锦, 宋同清, 彭晚霞, 曾馥平, 杜虎, 张浩, 范夫静
- TAN Qiujin, SONG Tongqing, PENG Wanxia, ZENG Fuping, DU Hu, ZHANG Hao, FAN Fujing
- 峡谷型喀斯特不同生态系统的土壤微生物数量及生物量特征
- Characteristics of soil microbial populations and biomass under different ecosystems in a canyon karst region
- 生态学报, 2014, 34(12): 3302-3310
- Acta Ecologica Sinica, 2014, 34(12): 3302-3310
- http://dx.doi.org/10.5846/stxb201310252573
-
文章历史
- 收稿日期:2013-10-25
- 修订日期:2014-4-4
2. 广西大学林学院, 南宁 530004;
3. 中国科学院环江喀斯特生态系统观测研究站, 环江 547100;
4. 江西农业大学, 南昌 330045
2. Forestry College of Guangxi University, Nanning 530004, China;
3. Huanjiang Observation and Research Station of Karst Ecosystem, Huanjiang 547100, China;
4. Jiangxi Agricultural University, Nanchang 330045, China
土壤微生物是土壤的重要组成部分,主要通过分解动植物残体而参与土壤系统中的能量流动和物质循环,是土壤养分的储备库和植物生长可利用养分的一个重要来源,影响早期植被演替的分布格局及其后来的演替过程[1, 2]。土壤微生物量是土壤碳循环最为活跃的部分,是土壤生态系统中物质和能量流动的重要参数之一,可反映土壤同化和矿化能力的大小,是土壤活性大小的标志[3],一直被认为是土壤活性养分的暂时储存库。土壤微生物数量是研究和评价土壤微生物调控功能的重要参数[4, 5],土壤微生物数量不仅反映了土壤各因素对土壤微生物的影响,同时也反映了其对植物的生长发育、土壤肥力的影响[6, 7],对整个生态系统也有一定的调节作用。许多学者研究认为土壤微生物对土壤生态系统功能如养分运转、能量流动、土壤结构维持、温室气体产生、土壤安全调节发挥着重要作用,即土壤微生物群落在一定程度上调节着土壤乃至整个生态系统功能,甚至影响着全球生态系统的变化[8, 9, 10]。
贵州处于我国西南喀斯特地区的中心,因生态环境脆弱,植被破坏后很难恢复,形成了不同程度的“石漠化”,其恢复与重建已成为农业生产、环境改善、区域经济发展及人民脱贫致富的迫切需求。土壤微生物是地球生物演化进程中的先锋种类[11],被公认为土壤生态系统变化的预警及敏感指标[12],对喀斯特退化生态系统的恢复与重建作用重大。张利青等[13]发现石灰土土壤微生物生物量在坡面尺度范围内存在着明显的空间分布;宋敏等[14]认为不同土地利用方式通过改善地上植被种类和覆盖度影响了土壤微生物的群落特征;宋同清等[15]、龙健等[16]、魏媛等[17]发现喀斯特区域植被恢复影响土壤微生物活性,何寻阳等[18]、鹿士杨等[19]认为不同退耕还林还草措施能改善土壤微生物特性,提高土壤质量,且自然恢复方式优于人工恢复方式[16]。这些研究多针对于表层土,且局限在喀斯特峰丛洼地。涉及到土壤微生物与土层深度关系方面的研究极少,而对峡谷型喀斯特不同生态系统土壤微生物群落特征的研究未曾报道。本文以贵州省晴隆县孟寨小流域典型峡谷型喀斯特的6个生态系统为研究对象,研究不同深度土壤微生物数量、生物量的变化特征及分形关系,目的在于探明退化喀斯特恢复的土壤微生物机理,为该地区乃至整个喀斯特地区植被恢复与生态重建提供理论依据。
1 材料与方法 1.1 研究区概况研究区为贵州省晴隆县孟寨河小流域,位于25°33′—26°11′N、105°01′—105°25′E之间,最高海拔2025 m,属北亚热带湿润季风气候区,年平均气温14.0—15.9 ℃,年极端高温为33.4 ℃,最低气温为-6.2 ℃,日照时数1453 h,无霜期280 d。年降水量1500—1650 mm,集中在6—9月份,年蒸发量1800 mm,空气相对湿度在50%以下。地形起伏大,具有山高、谷深、坡陡的特点,属二迭纪岩层风化而成的石灰土。研究区人地矛盾突出,人为干扰强烈,植被退化严重,长年水土流失导致石漠化趋势明显,生态环境十分脆弱。该小流域与普定后寨(高原型)、印江朗溪(岩溶槽谷型)、 荔波板寨(峰丛洼地型)并称四大喀斯特地貌类型区的4个小流域。
1.2 试验设计与调查2012年5—6月,对研究区域进行实地踏查,选择具有代表性的水田(ST)、旱地(HD)、草地(CD)、灌丛(GC)、人工林(RGL)、次生林(CSL) 6个生态系统,在母质、土壤类型、坡度等立地条件基本一致的基础上各设置3个样地(表 1),样地面积为20 m×20 m,系统进行了植被、立地因子、人为干扰等因子调查,并用手持GPS(Global Positioning System)(GPSmap 60) 定位。
|
生态系统
Ecosystems | 地理位置
Graphical location | 坡向/坡度
Slope aspect/ Slope/(°) | 海拔高度
Altitude/m | 土壤类型
Soil type | 优势种
Dominant species | 平均年龄
Mean age/a | 平均高度
Mean height/m | 盖度
Coverage |
| ST:水田Paddy field;HD:旱地Dry land;CD:草地Grassland;GC:灌草Shrubbery;RGL:人工林Plantation forest;CSL:次生林Secondary forest | ||||||||
| ST | 25°52.755′N,
105°16.476′E | 西 / 0 | 962 | 棕色石灰土
Brown limy soil | 水稻(Oryza sativa)、小麦(Triticum aestivum) | |||
| HD | 25°52.018′N,
105°17.047′E | 西 / 8 | 1006 | 棕色石灰土
Brown limy soil | 玉米(Zea mays)、油菜(Brassica napus) | |||
| CD | 25°52.755′N,
105°17.410′E | 西 / 2 | 1097 | 棕色石灰土
Brown limy soil | 宽叶雀稗(Paspalum wettsteinii)、白三叶
(Trifolium repens) | 2 | 0.2 | 0.95 |
| GC | 25°54.041′N,
105°15.718′E | 西 / 17 | 1145 | 棕色石灰土
Brown limy soil | 车桑子
(Dodonaea viscosa) | 3 | 1.3 | 0.75 |
| RGL | 25°50.723′N,
105°15.540′E | 西 / 22 | 1284 | 棕色石灰土
Brown limy soil | 楸树(Catalpa bungei) | 12 | 7.0 | 0.50 |
| CSL | 25°51.445′N,
105°16.748′E | 西南 / 25 | 1279 | 棕色石灰土
Brown limy soil | 白栎(Quercus fabri)、
椿树(Toona sinensis) | 20 | 7.8 | 0.70 |
首先将每个生态系统的3个样地都划分为16个5 m×5 m的小样方,各样地获得25个网点,用土钻测定每个网格点的土壤厚度。在每个样地中挖取典型剖面,直至出现岩石层为止,用环刀分0—10 cm(Ⅰ层)、10—20 cm(Ⅱ层)、20—30 cm(Ⅲ层)、30—50 cm(Ⅳ层)、50—100 cm(Ⅴ层)5层测容重。在样地的4个角和中间按土壤机械分5层取样,5个点同层次的土样组成一个混合样,一个样地获取5个土样,每个生态系统共15个土样。土样充分混合后将待测样品分成两部分,一部分带回实验室风干测定土壤理化性质[20],结果见表 2。另一部分带回实验室置于4 °C恒温冰箱中,测定土壤微生物生物量碳(MBC)、氮(MBN)、磷(MBP),以及细菌、真菌、放线菌。土壤微生物生物量均采用氯仿熏蒸法:微生物碳(MBC)与氮(MBN)采用K2SO4浸提法,转换系数K为0.45,微生物磷(MBP )采用NaHCO3提取,外加Pi 校正,转换系数K为0.4。土壤微生物数量采用稀释平板涂抹法计:细菌用牛肉膏蛋白胨培养基,真菌用马丁氏培养基,放线菌用改良高氏1号培养基,以上分析方法参见文献[21],分形维数D值是在双对数坐标下对A、B 的一系列值进行线性回归,所得拟合直线的斜率,A=kBD(k为比例系数)[22]。
|
生态系统
Ecosystems | pH | 有机碳
Organic carbon SOC /(g/kg) | 全氮
Total nitrogen TN/(g/kg) | 全磷
Total phosphorus TP/(g/kg) | 全钾
Total potassium TK/(g/kg) | 碱解氮
Available nitrogen AN/(mg/kg) | 速效磷
Available phosphorus AP/(mg/kg) | 速效钾
Available potassium AK/(mg/kg) |
| 同列数据后不同大、小写字母分别表示差异达到极显著和显著水平 | ||||||||
| ST | 8.2±0.05Aa | 17.56±1.91Cc | 1.31±0.74Bb | 0.96±0.09Aa | 10.70±0.31Cc | 120±4.33Cc | 43.70±6.14Aa | 83.38±6.70Aa |
| HD | 8.1±0.08Aa | 16.70±3.39Cc | 1.12±0.23Bb | 0.70±0.10Bb | 10.43±1.80Cc | 110±15.6Cc | 39.31±17.07Aa | 59.93±9.04Bb |
| CD | 8.1±0.12Aa | 19.81±0.98Cc | 0.97±0.06Bb | 0.70±0.05Bb | 14.40±1.00Bb | 86±2.70Cc | 8.81±1.27Bb | 61.29±6.42Bb |
| GC | 8.1±0.51Aa | 21.50±0.81Cc | 1.14±0.20Bb | 0.37±0.04Cd | 5.36±0.83Dd | 130±2.07Cc | 3.45±0.54Bb | 57.46±11.75Bb |
| RGL | 7.8±0.49Bb | 29.39±8.54Bb | 1.76±0.38Aa | 0.63±0.14Bb | 18.93±3.51Aa | 200±4.73Bb | 9.52±1.14Bb | 91.28±5.61Aa |
| CSL | 6.4±0.37Cc | 44.11±10.81Aa | 1.81±0.06Aa | 0.88±0.26Aa | 7.57±0.62Cc | 280±8.64Aa | 11.24±4.15Bb | 62.77±2.72Bb |
所有数据处理和分形特征计算均在Excel 2007、SPSS 16. 0 软件中完成,多重比较分析采用单因子(one-way ANOVA),差异显著性检验采用LSD 检验(显著性水平设定为a=0.05,极显著水平设定为a=0. 01)。
2 结果与分析 2.1 不同生态系统土壤微生物数量的变化由表 3可以看出,峡谷型喀斯特不同生态系统土壤微生物数量及组成不同,随着退化喀斯特植被的恢复,土壤细菌、真菌、放线菌及微生物总数均呈上升趋势。不同生态系统的土壤微生物总数量依次为次生林>人工林>灌丛>草地>水田>旱地。次生林与人工林均为乔木群落,差异不显著,但极显著高于其他生态系统;灌丛显著高于草地,草地与水田差异不显著,水田显著高于旱地。细菌、放线菌、真菌的数量变化趋势除放线菌、真菌表现为旱地>水田外,其变化规律与总数一致,且均具有次生林和人工林差异不显著、但极显著高于其他生态系统的特征。不同生态系统微生物数量组成均呈细菌>放线菌>真 菌,细菌的比例为87.00%—95.50%,各生态系统差异不显著;放线菌与真菌的比例分别为4.21%—12.39%和0.24%—0.61%,旱地极显著高于其他生态系统,其他生态系统差异不显著。
|
生态系统
Ecosystems | 细菌
Bacteria/ (×105cfu/g) | 真菌
Fungi/ (×05cfu/g) | 放线菌
Actinomycetes/ (×105cfu/g) | 总数
Sum/ (×105cfu/g) | 细菌比例
Percentage of bacteria/% | 真菌比例
Percentage of fungi/% | 放线菌比例
Percentage of actinomycetes/% |
| ST | 26.66±1.70Cc | 0.07±0.00Bc | 1.45±0.15CDd | 28.18±1.78Cc | 94.61±0.46Aa | 0.24±0.03Bb | 5.15±0.46Bb |
| HD | 13.54±1.87Dd | 0.10±0.01Bbc | 1.93±0.09Cc | 15.56±1.85Dd | 87.00±1.83Aa | 0.61±0.17Aa | 12.39±1.69Aa |
| CD | 30.79±2.76Bbc | 0.11±0.00Bbc | 2.15±0.17Cc | 33.04±2.88Cc | 93.18±0.29Aa | 0.32±0.03Bb | 6.50±0.30Bb |
| GC | 44.53±1.20Bb | 0.13±0.01Bb | 2.58±0.35Bb | 47.24±1.54Bb | 94.26±0.52Aa | 0.28±0.02Bb | 5.46±0.54Bb |
| RGL | 67.57±0.58Aa | 0.21±0.02Aa | 2.98±0.14Bb | 70.76±0.62Aa | 95.50±0.21Aa | 0.30±0.01Bb | 4.21±0.19Bb |
| CSL | 71.64±7.37Aa | 0.23±0.05Aa | 3.78±0.18Aa | 75.65±4.41Aa | 94.70±0.18Aa | 0.31±0.02Bb | 4.99±0.20Bb |
由于土壤微生物量周转快,灵敏度高,可以反映土壤质量微小的变化,常被作为研究土壤健康的生物学指标。由表 4可以看出,峡谷型喀斯特不同生态系统的土壤微生物量碳(MBC)、氮(MBN)、磷(MBP)的含量不同,但均为MBC>MBN>MBP。MBC含量的大小顺序为次生林>人工林>水田>灌丛>草地>旱地,其中次生林极显著高于其他生态系统,人工林、水田和灌丛差异不显著,但显著高于草地和旱地,草地和旱地差异不显著。MBN含量的大小顺序为次生林>人工林>灌丛>水田>旱地>草地,次生林与人工林差异不显著,但极显著高于其他生态系统,其他生态系统差异不显著;MBP含量的大小顺序为人工林>次生林>灌丛>水田>旱地>草地,同样是次生林与人工林差异不显著,但极显著高于其他生态系统,其他生态系统差异不显著。进一步分析发现,不同生态系统的MBC/SOC、MBN/TN、MBP/TP分别为0.44%—0.97%、2.13%—3.13%、1.46%—2.13%之间,差异不显著;MBC/MBN在3.06—6.54,其中次生林极显著高于其他生态系统,其他生态系统差异不显著。
|
生态系统
Ecosystems | 微生物碳
Microbial biomass carbon MBC/(mg/kg) | 微生物氮MBN
Microbial biomass nitrogen/(mg/kg) | 微生物磷MBP
Microbial Biomass phosphorus/(mg/kg) | 微生物碳/有机碳
MBC/SOC/% | 微生物氮/全氮
MBN/TN/% | 微生物磷/全磷
MBP/TP/% | 微生物碳/
微生物氮 MBC/MBN |
| ST | 169.656±23.10Bb | 34.677±1.38Bb | 21.052±0.28Bb | 0.97±0.14Aa | 2.65±0.26Aa | 1.61±0.16Aa | 4.89±1.20Bb |
| HD | 78.522±13.34Cc | 25.624±0.95Bb | 18.834±0.42Bb | 0.47±0.19Aa | 2.29±0.52Aa | 1.68±0.32Aa | 3.06±0.77Bbc |
| CD | 86.414±8.01Cc | 20.705±2.22Bb | 20.648±1.63Bb | 0.44±0.06Aa | 2.13±0.17Aa | 2.13±0.93Aa | 4.17±0.59Bb |
| GC | 130.477±5.61Bb | 35.714±2.14Bb | 20.422±3.81Bb | 0.61±0.00Aa | 3.13±0.47Aa | 1.79±1.39Aa | 3.65±0.90Bbc |
| GRL | 170.080±15.24Bb | 46.472±2.86Aa | 31.055±0.80Aa | 0.58±0.27Aa | 2.64±0.49Aa | 1.76±1.19Aa | 3.66±0.50Bbc |
| CSL | 330.94±34.02Aa | 50.630±6.05Aa | 26.510±2.30Aa | 0.75±0.21Aa | 2.80±0.38Aa | 1.46±1.04Aa | 6.54±2.09Aa |
土壤微生物生物量可反映参与调控土壤中能量和养分循环以及有机质转化的微生物数量。由表 5可以看出,石灰土土壤微生物MBC、MBN、MBP与土壤细菌、真菌及放线菌都具有良好的分形关系,相关系数分别为0.4545,0.6708,0.7137;.3981,0.6692,0.7554和0.3444,0.6428,0.7296,均达到了极显著水平(P<0.01),分形维数D值分别为-2.970,-2.492,-4.508;-2.254,-2.110,-3.872和-1.591,-1.642,-3.084,具有统计学意义。
| 模型Models | R2 | F | P |
| yC:MBC;yN:MBN;yP:MBP;xB:细菌数量 Bacteria population; xF:真菌数量 Fungi population; xA: 放线菌数量 Actinomycetes population | |||
| logyC=-2.970+0.772logxB | 0.4545 | 23.3053 | <0.01 |
| logyC=-2.492+1.121logxF | 0.6708 | 57.0558 | <0.01 |
| logyC=-4.508+1.234logxA | 0.7137 | 69.8110 | <0.01 |
| logyN=-2.254+0.571logxB | 0.3981 | 18.5200 | <0.01 |
| logyN=-2.110+0.880logxF | 0.6692 | 55.0600 | <0.01 |
| logyN=-3.872+1.002logxA | 0.7554 | 86.4950 | <0.01 |
| logyP=-1.591+0.4444logxB | 0.3444 | 14.7117 | <0.01 |
| logyP=-1.642+0.724logxF | 0.6428 | 50.3800 | <0.01 |
| logyP=-3.084+0.823logxA | 0.7296 | 75.5400 | <0.01 |
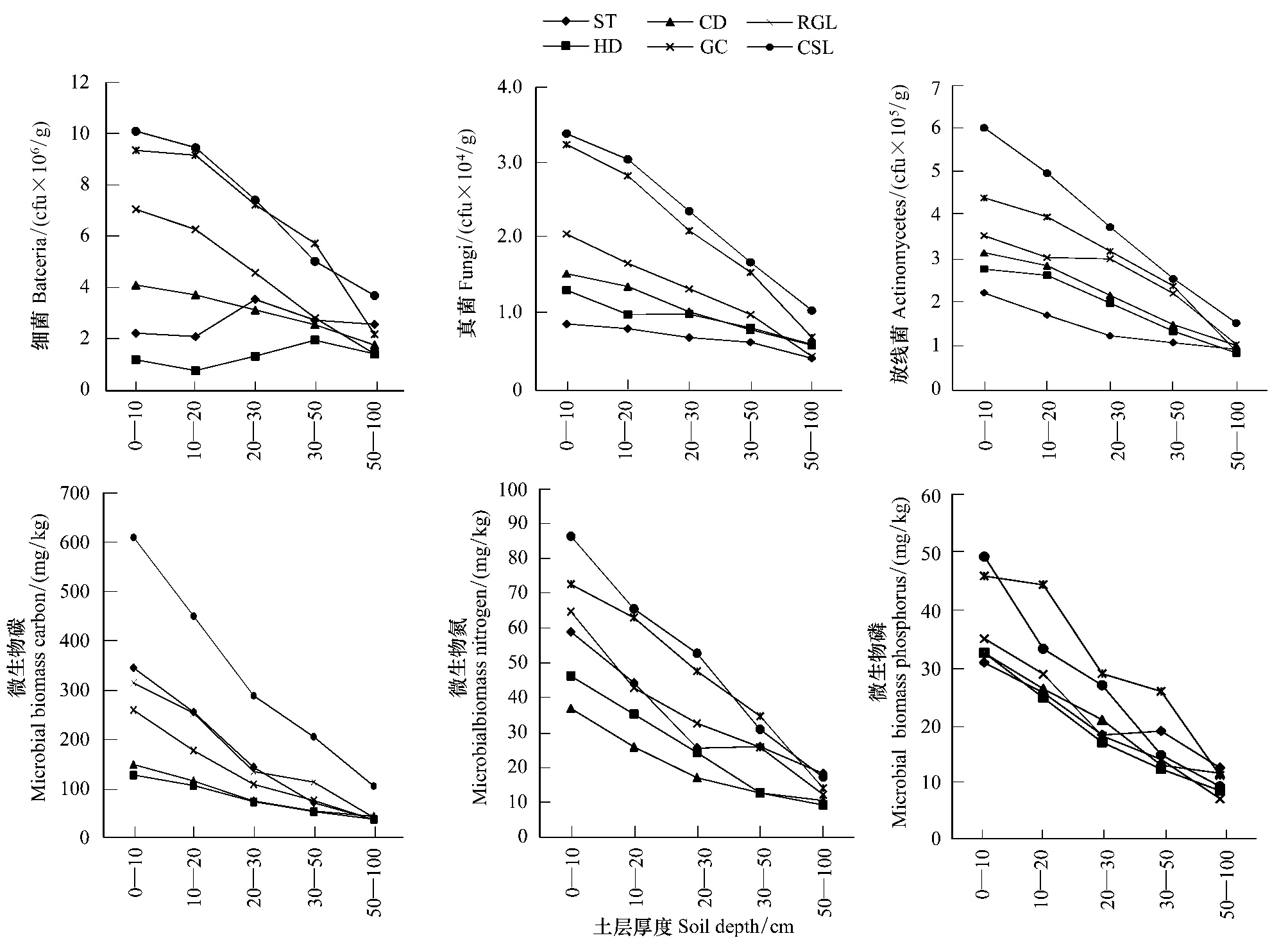
由图 1可以看出,不同生态系统的细菌、真菌及放线菌数量呈现随土层厚度加深而减少的趋势(除水田和旱地)。在表层土壤(0—10 cm)中,草地、灌丛、人工林和次生林的细菌数量为4.13×106,7.08×106,9.38×106和10.13×106 cfu/g,最深层的土壤(50—100 cm)为1.79×106,1.44×106,2.21×106和3.72×106 cfu/g,前者分别是后者的2.31,4.92,4.24和2.72倍。而水田和旱地的细菌数量随土层厚度加深波动不大,主要是由人为干扰太大、土壤翻耕频繁所致,真菌和放线菌的变化趋势相似;不同生态系统的土壤微生物MBC、MBN与MBP均呈现随土层厚度加深而减少的趋势。在表层土壤(0—10 cm)中,水田、旱地、草地、灌丛、人工林和次生林的MBC分别为344.16,126.38,147.84,258.32,313.19和609.09 mg/kg,而最深层土壤(50—100 cm)分别为36.45,36.71,42.74,35.64,40.12和104.24 mg/kg,前者是后者的9.44,3.44,3.46,7.25,7.81和5.84倍。土壤的MBN和MBP同样具有类似趋势。
|
| 图 1 不同生态系统的土壤微生物生物量与数量的垂直变化 Fig.1 Vertical variations in soil microbial biomass and populations for the ecosystems |
土壤微生物数量与组成很大程度上影响并决定着土壤的生物活性、有机质分解、腐殖质合成、土壤团聚体形成以及土壤养分的转化[4];同时土壤微生物深受土壤、植被、气候等因子的影响。不同生态系统植被组成和发育阶段不同,其分泌物的种类、数量和性质也不同,微生物数量和种类组成也不同。西南喀斯特属亚热带季风气候,雨热条件丰富,极有利于土壤微生物的繁衍和生长,土壤微生物的数量较高。张利青等[13]研究发现,高原型喀斯特处于北亚热带,温度较低、降雨量较少,典型坡耕地土壤微生物总数仅为1.75×105 cfu/g,三大菌类的组成与前人研究的结果不同,为放线菌>细菌>真菌[15]。宋敏等[14]对中亚热带喀斯特峰丛洼地坡耕地、草丛、灌丛、人工林、次生林5个不同生态系统土壤微生物的数量研究表明,其土壤微生物总数量为4.27×104—3.14×106 cfu/g,其中坡耕地、草丛、灌丛土壤三大菌类的组成也为放线菌>细菌>真菌,人工林和次生林则为细菌>放线菌>真菌,本研究区域为北亚热带典型的峡谷型喀斯特,温度较低,但降雨量大,土壤微生物的数量高达1.57×106—7.57×106 cfu/g,三大菌类的组成与其他土壤类型的研究结果一致[23, 24],均为细菌>放线菌>真菌,表明不同植被恢复模式对土壤微生物数量、分布存在重要影响。土壤微生物总数、细菌、放线菌和真菌数量均以次生林最高,水田和旱地较低,这是由于次生林枝落叶物的凋落、分解及根系分泌物死亡,为微生物的生长提供丰富的能源物质,且均随土壤厚度的加深而下降。
3.2 土壤微生物量碳、氮、磷不同生态系统及土壤类型条件下土壤微生物量的变化剧烈,受地上植被类型的影响很大[25]。峡谷型喀斯特土壤MBC的范围为78.52—330.94 mg/kg,与其他土壤类型相比比较适宜[26],但明显低于北亚热带高原型喀斯特(383.80 mg/kg)和中亚热带峰丛洼地型喀斯特(131.7—776.2 mg/kg)[13, 19],且变化相对平缓;MBN为20.71—50.63 mg/kg,明显低于温度森林土壤(130—216 mg/kg)[26]和高原型喀斯特(71.50 mg/kg)[13],高于峰丛洼地型喀斯特(16.67—46.13 mg/kg)[19],变异很小;MBP为18.834— 26.510 mg/kg,介于峰丛洼地型喀斯特(4.33—76.65 mg/kg)和高原型喀斯特(15.41 mg/kg)之间,变异非常小;MBC、MBN、MBP受植被恢复的影响较大,均以人工林和次生林最高,森林生态系统凋落物、根表脱落物和根系分泌物对土壤碳库、氮库、磷库的不断补充,增强了土壤微生物活性,导致土壤微生物量不断上升。与微生物数量一样,土壤微生物生物量随土壤深度的加深而下降,可能由于土壤中大多数微生物属于有机营养型,随着植物根系分泌物和脱落物的不断减少以及土层温度的降低,土壤中营养物质逐渐减少,减慢了微生物的自身合成代谢。
Vance等[27]认为,土壤微生物生物量绝对量并不能完全反映微生物的活性、结构和功能,应考虑微生物生物量碳、氮、磷在全碳、全氮和全磷中的比例,揭示峡谷型喀斯特不同生态系统土壤微生物质量的变异。Zeller等[28]报道MBC、MBN、MBP占有机碳、全氮和全磷的比例分别为0.3%—7.0%、2.0%—6.0%和0.5%—8.5%。本研究结果与其相似,分别为0.44%—0.95%、2.13%—3.13%、1.46%—2.13%,差异不显著,但MBC、MBN、MBP的比例均偏低,这是因为峡谷型喀斯特土壤虽少,但“窝窝土”现象严重,土壤周围分布的裸露岩石上的风化凋落物缓缓向土壤输入,土壤碳、氮、磷含量较高,但应提高土壤的微生物活性和微生物代谢能力,保证植物生长所需的营养物质。MBC/MBN的值是否恒定,不同学者其观点不同,Anderson等[29]认为MBC/MBN平均值为6.7,陈国潮等[30]认为红壤土壤MBCM/MBN平均值为6.2,峡谷型喀斯特不同生态系统中只有次生林生态系统的土壤与其接近,为6.54,其他生态系统的MBCM/BN显著低于次生林,为3.06—4.89,应提高土壤微生物生物量碳的固持能力[16]。
3.3 土壤微生物量与微生物数量的分形特征分形理论一般用于植物分布格局和土壤团聚体等方面的研究[31],而针对土壤微生物量与微生物数量关系的研究很少,涉及喀斯特不同生态系统的更少。本研究表明,土壤微生物MBC、MBN、MBP与土壤细菌、真菌及放线菌都具有良好的分形关系,经F检验,其分析模型精度及分形维数D值均达到显著水平。由分形模型拟合得到的D值是对MBC、MBN、MBP空间分布的维度特征的表征,D值越大,表明微生物量碳、氮、磷在土壤空间积累越多,分布空间越大[31]。喀斯特峰丛洼地不同土地利用方式中,MBC与土壤真菌数量、细菌数量及放线菌数量(P=0.01),MBN、MBP与细菌数量、真菌数量、放线菌数量不存在显著关系[14];喀斯特峰丛洼地不同退耕还林还草模式中,只有MBC与细菌数量、MBN与真菌数量(P=0.01)、MBC与放线菌数量(P=0.05)呈显著性关系[19]。峡谷型喀斯特土壤微生物量与土壤微生物数量的空间分布格局存在差异,其中MBC、MBN、MBP与放线菌数量相关(D=-4.508,-3.882,-3.084)最大,其次是MBC、MBN与细菌数量(D=-2.970,-2.254)及MBP与真菌数量(D=-1.642),MBC、MBN与真菌数量(D=-2.492,-2.110)及MBP与细菌数量(D= -1.591)的相关性较小。同时,土壤微生物数量与微生物量空间分布分形特征的存在,可以通过土壤微生物的数量变化来预测该地区微生物生物量的动态变化,从而为喀斯特植被恢复重建过程中的土壤健康保护、植被恢复模式选择提供基础数据。
| [1] | Zhang X J, Liu J H, Li L J, Wang Z G, Duan Y K, Su S H. Effects of different conservation tillage on soil microbes quantities and enzyme activities in dry cultivation. Chinese Journal of Soil Science, 2009, 40(3): 542-546. |
| [2] | Kardol P, Cornips N J, Van Kempen M M L, Bakx-Schotman J M T, Van der Putten W H. Microbe-mediated plant-soil feedback causes historical contingency effects in plant community assembly. Ecological Monographs, 2007, 77(2):147-162. |
| [3] | Liu M Q, Hu F, He Y Q, Li H X. Seasonal dynamics of soil microbial biomass and its significance to indicate soil quality under different vegetations restored on degraded red soils. Acta Pedologica Sinica, 2003, 40(6): 937-943. |
| [4] | Harris J A. Measurements of the soil microbial community for estimating the success of restoration. European Journal of Soil Science, 2003, 54(4): 801-808. |
| [5] | Xu H F, Liu X T, Bai J H. Dynamic change and environmental effects of soil microorganism in marsh soils from Carex Meyeriana Wetlands in Changbai Mountain. Journal of Soil and Water Conservation, 2004, 18(3): 115-117, 122. |
| [6] | Wu J F, Lin X G. Effects of soil microbes on plant growth. Soil, 2003, 35(1): 18-21. |
| [7] | Chen S M, Lin H P, Zhang L Q. Introduction to Microbial Ecology. Beijing: Higher Education Press, 2007. |
| [8] | Vitousek P M, Matson P A. Mechanisms of nitrogen retention in forest ecosystems: a field experiment. Science, 1984, 255(4657): 51-52. |
| [9] | Kennedy A C, Smith K L. Soil microbial diversity and the sustainability of agricultural soils. Plant and Soil, 1995, 170(1): 75-86. |
| [10] | Lamar R T, Dietrich D M. In situ depletion of pentachlorophenol from contaminated soil by Phanerochaete spp. Applied Environmental Microbiology, 1990, 56(10): 3093-3100. |
| [11] | Lin X G, Hu J L. Scientific connotation and ecological service function of soil microbial diversty. Acta Pedologica Sinica, 2008, 45(5): 892-900. |
| [12] | Ren T Z, Grego S. Soil bioindicators in sustainable agriculture. Scientia Agricultura Sinica, 2000, 33(1): 68-75. |
| [13] | Zhang L Q, Peng W X, Song T Q, Zou D S, Zeng F P, Song M, Yu Z, Liu Y. Spatial heterogeneity of soil microbial biomass carbon, nitrogen, and phosphorus in sloping farmland in a karst region on the Yunnan-Guizhou Plateau. Acta Ecologica Sinica, 2012, 32(7): 2056-2065. |
| [14] | Song M, Zou D S, Du H, Peng W X, Zeng F P, Tan Q J, Fan F J. Characteristics of soil microbial populations in depressions between karst hills under different land use patterns. Chinese Journal of Applied Ecology, 2013, 24(9): 2471-2478. |
| [15] | Song T Q, Peng W X, Zeng F P, Wang K L, Liu L, Lu S Y, Du H. Soil ecological effects of converting cropland to forest and grassland in depressions between karst hills. Acta Pedologica Sinica, 2011, 48(6): 1219-1225. |
| [16] | Long J, Li J, Jiang X R, Huang C Y. Soil microbial activies in Maolan karst forest, Guizhou Province. Acta Pedologica Sinica, 2004, 41(4): 597-602. |
| [17] | Wei Y, Yu L F, Zhang J C. Soil microbial characteristics during succession of degraded karst vegetation. Scientia Silvae Sinicae, 2008, 44(7): 6-10. |
| [18] | He X Y, Su Y R, Liang Y M, Yang S, Wang K L. Soil microbial diversity in typical Karst peak-cluster depression under effects of different de-farming patterns. Chinese Journal of Applied Ecology, 2010, 21(2): 317-324. |
| [19] | Lu S Y, Peng W X, Song T Q, Zeng F P, Du H, Wang K L. Soil microbial properties under different grain-for-green patterns in depressions between karst hills. Acta Ecologica Sinica, 2012, 32(8): 2390-2399. |
| [20] | Bao S D. Soil and Agricultural Chemistry Analysis. 3rd ed. Beijing: China Agriculture Press, 2000. |
| [21] | Wu J S, Lin Q M, Huang Q Y, Xiao H A. Soil Microbial Biomass-Methods and Application. Beijing: China Meteorological Press, 2006. |
| [22] | Liu Y, Zha T G, Wang Y K, Wang G M. Soil aggregate stability and soil organic carbon characteristics in Quercus variabilis and Pinus tabulaeformis plantations in Beijing area. Chinese Journal of Applied Ecology, 2013, 24(3): 607-613. |
| [23] | Institute of Soil Science, CAS. Analytical Method of Soil Physics and Chemistry of Chinese Soil System Classification. Beijing: Chinese Agriculture Science and Technology Press, 1992. |
| [24] | Liu S L, Xiao H A, Tong C L, Wu J S. Microbial biomass C, N and P and their responses to application of inorganic and organic fertilizers in subtropical paddy soils. Research of Agricultural Modernization, 2003, 24(4): 278-283. |
| [25] | Zhu Z J, Jiang P K, Xu Q F. Study on the active organic carbon in soil under different types of vegetation. Forest Research, 2006, 19(4): 523-526. |
| [26] | Liu S, Wang C K. Spatio-temporal patterns of soil microbial biomass carbon and nitrogen in five temperate forest ecosystems. Acta Ecologica Sinica, 2010, 30(12): 3135-3143. |
| [27] | Vance E D, Brookes P C, Jenkinson D C. An extraction method for measuring soil microbial biomass C. Soil Biology and Biochemistry, 1987, 19(6): 703-707. |
| [28] | Zeller V, Bardgett R D, Tappeiner U. Site and management effects on soil microbial properties of subalpine meadows: a study of land abandonment along a north-south gradient in the European Alps. Soil Biology and Biochemistry, 2001, 33(4/5): 639-649. |
| [29] | Anderson J P E, Domsch K H. Quantities of plant nutrients in the microbial biomass of selected soils. Soil Science, 1980, 130(4): 211-216. |
| [30] | Chen G C, He Z L. Study on microbial biomass in red soil under different land use types. Chinese Journal of Soil Science, 1998, 29(6): 276-278. |
| [31] | Yang P L, Luo Y P, Shi Y C. Using weight distribution of soil particle size to express soil fractal feature, 1993, 38(20): 1896-1899. |
| [1] | 张星杰, 刘景辉, 李立军, 段宇坤, 王智功, 苏顺和. 保护性耕作方式下土壤养分、微生物及酶活性研究. 土壤通报, 2009, 40(3): 542-546. |
| [3] | 刘满强, 胡峰, 何园球, 李辉信. 退化红壤不同植被恢复下土壤微生物量季节动态及其指示意义. 土壤学报, 2003, 40(6): 937-943. |
| [5] | 徐惠风, 刘兴土, 白军红. 长白山沟谷湿地乌拉苔草沼泽湿地土壤微生物动态及环境效应研究. 水土保持学报, 2004, 18(3): 115-117, 122-122. |
| [6] | 吴建峰, 林先贵. 土壤微生物在促进植物生长方面的作用. 土壤, 2003, 35(1): 18-21. |
| [7] | 陈声明, 林海萍, 张立钦. 微生物生态学导论. 北京: 高等教育出版社, 2007. |
| [11] | 林先贵, 胡君利. 土壤微生物多样性的科学内涵及其生态服务功能. 土壤学报, 2008, 45(5): 892-900. |
| [12] | 任天志, Grego S. 持续农业中的土壤生物指标研究. 中国农业科学, 2000, 33(1): 68-75. |
| [13] | 张利青, 彭晚霞, 宋同清, 邹冬生, 曾馥平, 宋敏, 俞孜, 刘艳. 云贵高原喀斯特坡耕地土壤微生物量 C、N、P空间分布. 生态学报, 2012, 32(7): 2056-2065. |
| [14] | 宋敏, 邹冬生, 杜虎, 彭晚霞, 曾馥平, 谭秋锦, 范夫静. 不同土地利用方式下喀斯特峰丛洼地土壤微生物群落特征. 应用生态学报, 2013, 24(9): 2471-2478. |
| [15] | 宋同清, 彭晚霞, 曾馥平, 王克林, 刘璐, 鹿士杨, 杜虎. 喀斯特峰丛洼地退耕还林还草的土壤生态效应. 土壤学报, 2011, 48(6): 1219-1225. |
| [16] | 龙健, 李娟, 江新荣, 黄昌勇. 贵州茂兰喀斯特森林土壤微生物活性的研究. 土壤学报, 2004, 41(4): 597-602. |
| [17] | 魏媛, 喻理飞, 张金池. 退化喀斯特植被恢复过程中土壤微生物学特性. 林业科学, 2008, 44(7): 6-10. |
| [18] | 何寻阳, 苏以荣, 梁月明, 杨珊, 王克林. 喀斯特峰丛洼地不同退耕模式土壤微生物多样性. 应用生态学报, 2010, 21(2): 317-324. |
| [19] | 鹿士杨, 彭晚霞, 宋同清, 曾馥平, 杜虎, 王克林. 喀斯特峰丛洼地不同退耕还林还草模式的土壤微生物特性. 生态学报, 2012,32(8): 2390-2399. |
| [20] | 鲍士旦. 土壤农化分析(第三版). 北京: 中国农业出版社, 2000. |
| [21] | 吴金水, 林启美, 黄巧云, 肖和艾. 土壤微生物生物量测定方法及其应用. 北京: 气象出版社, 2006. |
| [22] | 刘艳, 查同刚, 王伊琨, 王高敏. 北京地区栓皮栎和油松人工林土壤团聚体稳定性及有机碳特征. 应用生态学报, 2013, 24(3): 607-613. |
| [23] | 中国科学院南京土壤研究所编. 中国土壤系统分类土壤物理和化学分析方法. 北京: 中国农业科技出版社, 1992. |
| [24] | 刘守龙, 肖和艾, 童成立, 吴金水. 亚热带稻田土壤微生物生物量碳、氮、磷状况及其对施肥的反应特点. 农业现代化研究, 2003, 24(4): 278-283. |
| [25] | 朱志建, 姜培坤, 徐秋芳. 不同森林植被下土壤微生物量碳和易氧化态碳的比较. 林业科学研究, 2006, 19(4): 523-526. |
| [26] | 刘爽, 王传宽. 五种温带森林土壤微生物生物量碳氮的时空格局. 生态学报, 2010, 30(12): 3135-3143. |
| [30] | 陈国潮, 何振立. 红壤不同利用方式下微生物量的研究. 土壤通报, 1998, 29(6): 276-278 |
| [31] | 杨培岭, 罗远培, 石元春. 用粒径的重量分布表征的土壤分形特征. 科学通报, 1993, 38(20): 1896-1899. |
 2014, Vol. 34
2014, Vol. 34




