文章信息
- 黄秋斌, 张颖, 刘凤英, 王淼, 王刚
- HUANG Qiubin, ZHANG Ying, LIU Fengying, WANG Miao, WANG Gang
- 蜡样芽孢杆菌B3-7在大田小麦根部的定殖动态及其对小麦纹枯病的防治效果
- Colonization dynamics of Bacillus cereus B3-7 on wheat roots and control efficiency against sharp eyespot of wheat
- 生态学报, 2014, 34(10): 2559-2566
- Acta Ecologica Sinica, 2014, 34(10): 2559-2566
- 10.5846/stxb201307221929
-
文章历史
- 收稿日期:2013-7-22
- 网络出版日期:2014-2-20
2. 棉花生物学国家重点实验室, 开封 475004;
3. 河南大学生物工程研究所, 开封 475004
2. State Key Laboratory of Cotton Biology, Henan University, Kaifeng 475004, China;
3. Institute of Bioengineering, Henan University, Kaifeng 475004, China
小麦纹枯病(sharp eyespot of wheat)是由植物病原真菌禾谷丝核菌(Rhizoctonia cerealis)侵染引起一种分布广泛、危害严重的土壤传播病害。病菌以菌丝或菌核在土壤和病残体上越冬或越夏。播种后开始侵染为害[1]。在田间发病过程可分5个阶段即冬前发病期、越冬期、横向扩展期、严重度增长期及枯白穗发生期。一般使小麦减产10%—20%,严重地块减产50%左右,个别地块甚至绝收。由于目前尚缺乏高抗小麦纹枯病的小麦品种,生产上对于该病的防治主要通过施用化学农药如井冈霉素和粉锈宁等方法,不仅提高了小麦生产成本,而且容易导致抗药性菌株的出现,进一步降低化学药剂的防治效果[2]。因此,寻找一种有效的小麦纹枯病防治方法成为小麦生产上的当务之急。
植物根际细菌(rhizobacteria)作为一类存在于植物根际,对于植物生长发育具有重要作用的一类微生物[3]。大量的研究表明,根际细菌中存在包括荧光假单胞菌、枯草芽孢杆菌、和蜡样芽孢杆菌等多种能够控制植物病害发生的细菌类型[4, 5]。不同的微生物可以通过产生抗菌物质、生态位与营养竞争以及诱导植物产生抗性等多种机制发挥作用[6, 7]。利用根际细菌防治植物病害,对于替代或者减少化学农药的使用,促进农业的可持续发展具有重要价值。植物病害生物防治的本质是植物、病原菌以及生防微生物之间的相互作用,通过三者的互作,减少病原菌对于植物的危害。因此,利用根际微生物防治植物病害的前提是这些微生物能够在植物根部有效定殖并具有较好的环境适应性。研究生防细菌的环境适应性和在植物根部的定殖能力,有助于认识生防细菌的作用机制,提高生防细菌的防治效果。蜡样芽孢杆菌B3-7菌株是作者前期研究过程中从健康小麦根际分离得到的1株生防菌株[8, 9]。该菌株能够产生多种抗菌物质,可以在固体基质表面产生大量的有助于其存在的生物膜(biofilm),在温室测定中能够在小麦根部稳定定殖且对于小麦纹枯病和小麦全蚀病具有较好的生防效果。该生防菌株在大田条件下是否能够在小麦根部长期定殖以及是否对于病害具有防治效果,有待于进一步研究。因此,本研究通过利用绿色荧光蛋白(green fluorescent protein,GFP)标记菌株,利用标记菌株测定了其在大田小区中在小麦根部的定殖和对小麦纹枯病的生物防治。
1 材料与方法 1.1 供试材料 1.1.1 供试菌株、质粒和培养条件本研究供试植物病原真菌、生防细菌及其衍生菌株和和质粒的特征及来源见表1。大肠杆菌(Escherichia coli ) 和生防细菌蜡样芽孢杆菌 (Bacillus cereus ) 常规培养采用LB培养基,生物薄膜测定采用Standard succinate medium(SSM)培养基[6]。试验用抗生素浓度为氨苄青霉素(Ampicillin,Amp)100μg/mL、红霉素(Erythromycin,Erm) 10μg/mL、利福平(Rifampin,Rfp)100 μg/mL。凝胶回收试剂盒、内切酶、T4 DNA 连接酶,Taq酶等均购自 Fermentas 公司。
|
菌株和质粒 Strain and plasmid | 相关性状 Relevant characteristics | 来源 Source |
|
大肠杆菌 Escherichia coli GM2163 | 甲基化酶缺陷菌株,具有链霉素抗性。 | Fermentas 公司 |
|
蜡样芽孢杆菌 Bacillus cereus B3-7 B3-7 (Δamy::gfp) | 小麦纹枯病生防菌株,具有利福平抗性 。 amy基因缺失菌株,具有绿色荧光蛋白编码基因 | 本实验室保存 本研究 |
|
禾谷丝核菌 Rhizoctonia cerealis | 小麦纹枯病致病菌 | 本实验室保存 |
|
质粒 Plasmid pMAD pAD123 pMAD-ΔamY | 含有温度敏感复制子的穿梭载体. 不含gfp基因启动子的穿梭载体 gfp插入到amy基因的pMAD 质粒 | [10] [11] 本研究 |
选用的农田为河南省夏邑县太平村的麦田,种植制度为多年小麦-玉米轮作,土壤呈弱碱性(pH,7.7),有机质7—9 g/kg,全氮含量0.7—0.85g/kg,全磷含量0.5—0.6g/kg,全钾含量19.8—20.2g/kg,速效磷2 mg/kg,速效钾,137 mg/kg。小麦品种为当地大面积种植的矮抗58。
1.2 生防菌株B3-7绿色荧光蛋白(GFP)标记菌株的构建根据B3-7菌株α-淀粉酶编码基因amY的核苷酸序列设计设计引物,上游的一对引物分别是amY-up-S(CCCAGGATCCTTTAAAAGAATAACAATAGTC,划线部分为BamH I位点)和amY-up-A(CCAA AAGCTTCAAAATCAAGATCCGCATACA,划线部分为Hind III位点),下游的一对引物分别是amY-down-S(CCCAAAGCTTTGCGAATGAAATGAAAAAATG,划线部分为Hind III位点)和amY-down-A(CAAA GTCGACCTGCTGAACATATATGGAAAC,划线部分为Sal I位点)。利用引物amY-up-S和amY-up-A扩增出amY基因上游片段,利用amY-down-S和amY-down-A扩增出amY基因下游片段,然后用内切酶Hind III分别酶切后,与同样用Hind III酶切质粒pAD123得到的绿色荧光蛋白编码基因gfp片段等浓度混合,经T4连接酶连接后,用amY-up-S和amY-down-A扩增出插入gfp基因的amY基因片段,将此片段用BamH I和Sal I双酶切后,插入到穿梭载体pMAD的对应位点内,构建amY基因的敲除载体pMAD-ΔamY,将此敲除载体转化进入生防菌B3-7的电击转化感受态细胞,根据Maryvonne等[9]的方法获得产淀粉酶缺陷并在蓝光照射下发出绿色荧光的突变株。
1.3 生防菌株B3-7及其GFP标记突变株生物学性状比较 1.3.1 菌落形态和群体生长特性比较分别将野生型B3-7及其GFP标记突变株接种于液体LB培养基中,于30 ℃振荡(200 r/min)培养24 h后,离心收集细菌,加入新鲜的LB液体培养基中,调整浓度OD600=0.1,用移液器分别取2μL点接到LB平板上,于30℃培养箱中培养5 d,观察B3-7及其GFP标记突变株菌落形态是否存在差别。同时,分别取OD600=0.1的菌液300μL加入深孔培养板中,然后将培养板至全自动生长曲线分析仪(Bioscreen C),进行生长曲线测定(参数设置为:振荡温度,30℃;振荡时间,57 h;测定时间间隔,1 h;测定吸光度OD(530—580),比较B3-7及其GFP标记突变株群体生长曲线是否存在差别。
1.3.2 生物薄膜形成能力比较分别挑取野生型B3-7菌株及其GFP标记菌株,接种于液体LB培养基中,30℃、200 r/min的摇床中培养至对数期,用LB培养基分别稀释菌液至OD600=0.1,取20 μL菌液加入到含有2mL培养基的玻璃管中(直径D=0.8 cm),轻轻混匀后于22℃静止培养5 d,观察不同菌株在玻璃管内壁生物薄膜的形成情况。之后,轻轻吸去每个管中的菌液(注意不要触碰管壁),向玻璃管中加入1.5 mL的蒸馏水,轻轻晃动,再用枪头将蒸馏水吸出,反复清洗3次,去除管底菌体,加入2.5 mL 0.1%(w/v)的结晶紫溶液,室温染色20 min,吸去染色液,加入蒸馏水轻轻冲洗3次,直到水变为无色。加入2.5 mL 10% SDS,反复晃动试管溶解生物薄膜,用10% SDS稀释5倍,吸取2.5 mL至比色皿中,以2.5 mL 10% SDS作为对照,测定OD590的光吸收值。每个处理设置8个重复,试验重复3次。
1.3.3 室内条件下测定B3-7及其GFP标记菌株在小麦根部的定殖状况利用LB液体培养基培养B3-7及其GFP标记菌株,离心去除上清后,加入1%的羧甲基纤维素钠(carboxymethyl cellulose,CMC),调整浓度至OD600=1.5,将已经催芽的小麦种子(品种为中国春)浸入菌液中1 h,播种至盛有无菌土的一次性塑料杯中,每个杯子中央播种3粒种子。将各个处理随机放入22 ℃培养室内培养,待小麦出苗后,每隔5 d取样,轻轻抖掉麦苗所带的泥土并剪去地上部,分别称重后将根放入定量的0.1% Tween-20溶液中,剧烈振荡3 min后梯度稀释并涂布含有利福平的LB平板,30 ℃培养24 h后,统计平板菌落数,同时,在蓝光下观察GFP标记菌株的荧光菌落并计数,计算单位根重含有的菌落数(CFU/g根)。每个处理设置15个重复,试验重复3次。
1.4 GFP标记菌株在大田小麦根部的定殖情况及其对小麦纹枯病的防治效果利用上年小麦纹枯病严重发病的麦田,从中选取15 m×12 m(长×宽)的区域设置试验小区,共设9个试验小区(纵横各3个小区)。每个小区为6 m2(3m×2m,长×宽),小区与小区之间间隔2 m,用于保护行,小区的外侧设置1 m的距离用作保护行。试验设置B3-7、GFP标记菌株和阴性对照3个处理,每个处理设置3个重复,即每个小区为1个重复。播种时间为10月上旬,播种前,利用LB液体培养基培养细菌,经离心后,将细菌悬浮于1% CMC溶液中,调整细菌浓度约至109 CFU/mL,将麦种浸入菌液1h,捞出麦种晾干后进行播种,播种量为10 kg/666.7m2。阴性对照和保护行小麦处理时,仅在不含有细菌的1% CMC浸种。小麦出苗后,分别于冬前分蘖期、越冬期、拔节期、孕穗期和灌浆期取样调查。调查小麦发病情况时,每个小区随机调查100株小麦,根据Clarkson和Cook[12]的方法进行调查,统计病害的严重度。同时计算出不同时期的病害防治效果。
测定生防菌株的定殖数量时,从GFP标记菌株处理的小区五点取样(3个小区共15个取样点)。每个取样点取20株小麦,轻轻地连根挖出小麦植株,带土分别放入无菌牛皮纸袋中带回实验室,根据1.3.3 所述的方法统计小麦根部GFP菌株的数量。为了证实分离出的荧光菌株就是接种的GFP标记菌株,从分离得到的荧光菌落中随机挑取部分菌落,利用根据B3-7基因组序列设计的两对特异引物进行进行菌落PCR,根据扩增结果判断分离菌落的正确性。
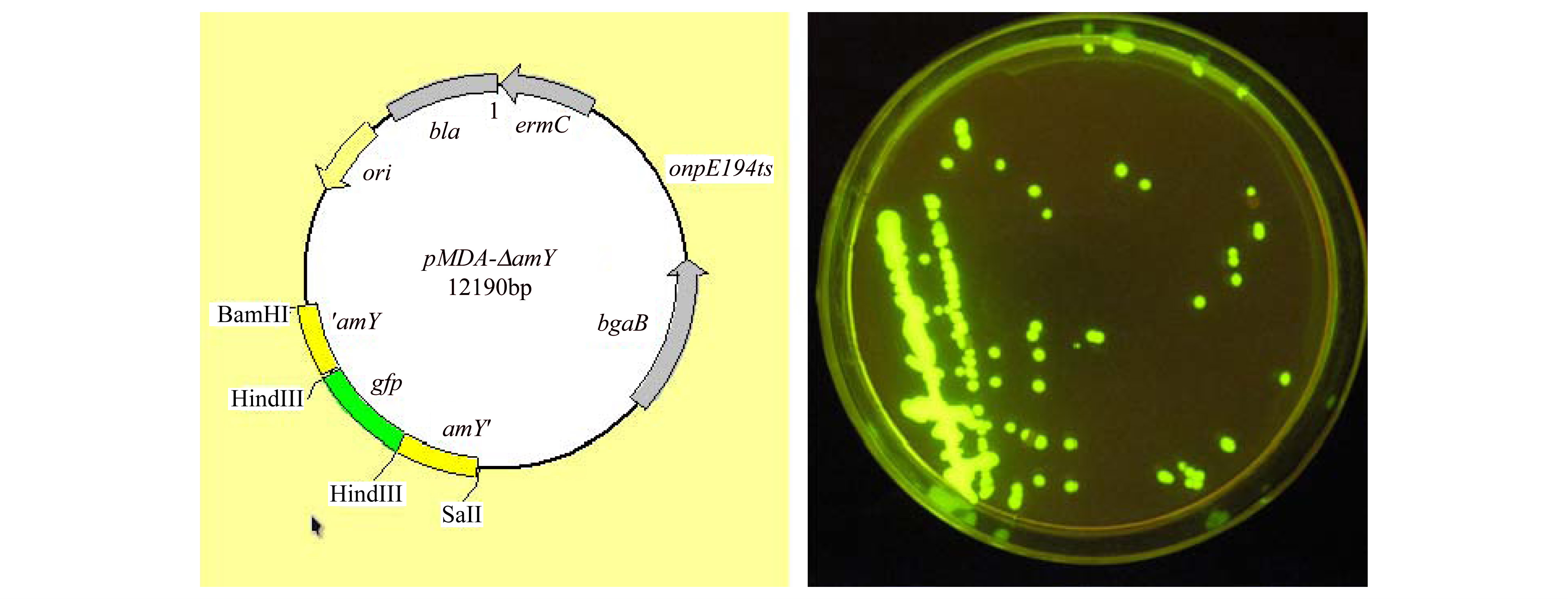
2 结果与分析 2.1 生防菌B3-7绿色荧光蛋白标记菌株的构建为了测定B3-7菌株在大田小麦根系的定殖动态,需要构建能够区分土著微生物的标记菌株。为此,将绿色荧光蛋白(GFP)的编码基因gfp插入到生防菌的基因组中。 利用PCR对α-淀粉酶编码基因amY阅读框内的上游和下游片段进行,成功扩增出上游711 bp的片段和下游840bp片段,经过序列测定正确后,分别利用Hind III酶切上述两个片段,然后与同样用Hind III酶切的gfp基因及其启动子片段混合,经T4连接酶连接后扩增出2.5 kb的片段,将此片段插入穿梭载体pMAD中,构建成功amY基因敲除载体pMAD-ΔamY(图1)。在此基础上,将敲除载体pMAD-ΔamY转化进入B3-7菌株,通过热处理和蓝白斑筛选等一系列步骤,获得基因双交换白色菌落,该菌落在蓝光下发绿色荧光,经过多次传代后菌落的荧光特性不发生改变,表明GFP标记菌株构建成功(图1)。
|
| 图 1 生防细菌B3-7绿色荧光蛋白(GFP)标记突变菌株的构建 Fig. 1 Construction of green flurescence protein (GFP) tagging mutant of biocontrol strain B3-7 |
通过测定生防菌株B3-7及其GFP标记菌株在LB培养基平板上菌落形态,发现两者之只是菌落颜色方面存在差别,GFP标记菌株呈现淡绿色,而野生型B3-7菌株为乳白色。只有由于标记菌株GFP表达的结果,其它形态特征如生长速度、菌落形态和菌落大小等方面没有明显差别。通过测定上述两个菌株在LB液体培养基内的群体生长,发现二者不存在差别,在生长过程中表现出相同的迟缓期,对数生长期和稳定期(图2)。上述结果表明GFP标记不影响该细菌在固体基质和液体基质内的生长。

|
| 图 2 生防细菌B3-7及其GFP标记突变株的群体生长曲线 Fig. 2 Growth curves of biocontrol bacteria B3-7 and its GFP tagging mutant |
采用定性和定量测定相结合的方法测定了B3-7及其GFP标记衍生菌株在固体基质表面(试管内壁)形成生物膜的能力,结果发现两者没有明显差异(图3)。生物膜作为自然状态下微生物存在的方式,微生物通过形成生物膜附着在固体基质表面,提高对于环境胁迫的抗性,上述两个菌株在生物膜形成方面不存在差异,表明GFP标记菌株可能与其野生型具有相似的定殖能力。

|
| 图 3 生防细菌B3-7及其GFP标记突变株的生物薄膜形成 Fig. 3 biofilm formation of biocontrol strain B3-7 and its GFP tagging mutants |
室内限菌条件下测定了生防菌B3-7及其GFP标记菌株在小麦根部的定殖能力,结果发现二者均能高效地在小麦根部定殖。在测定的30 d内,随着时间的延长,定殖数量总体呈现下降趋势,但是保持在每克根重105菌落形成单位(CFU)之上。测定的两个菌株之间无显著差异,表明GFP标记后至少在室内条件下不影响生防菌的定殖。综合上述GFP标记菌株的菌落形态、群体生长、生物膜形成以及在小麦根部的定殖动态测定结果,认为GFP标记不影响菌株的生物学特性。
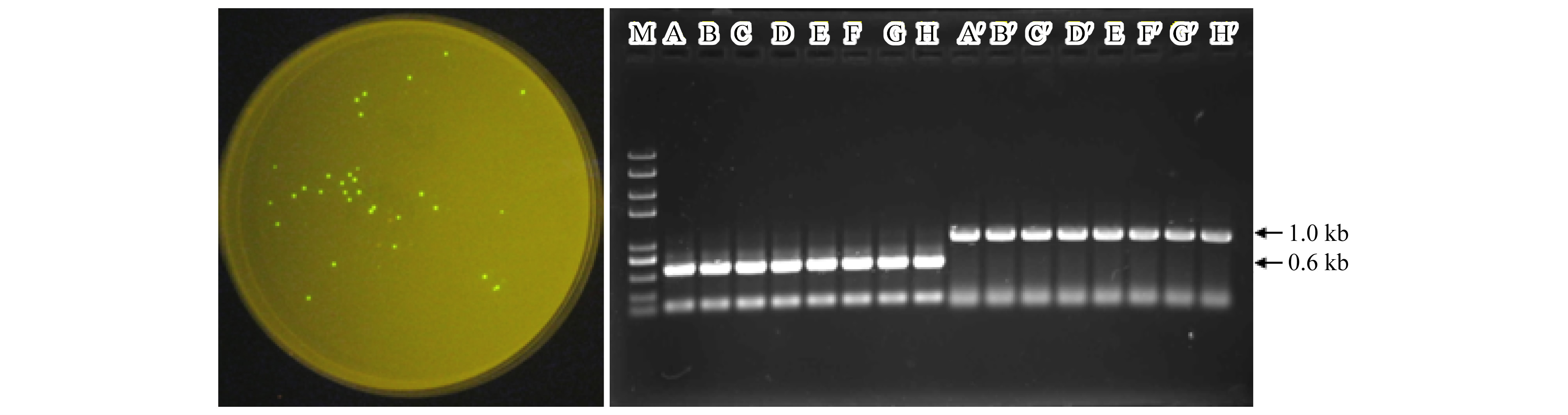
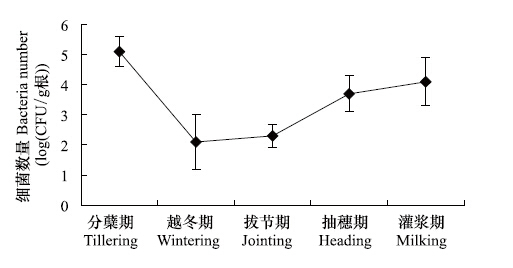
2.3 GFP标记菌株在大田小麦根部的定殖动态在室内测定生防菌B3-7菌株的GFP标记突变体基本生物学特性的基础上,于2002—2003年测定了该标记菌株在大田小区条件下在小麦根系的定殖能力和对小麦纹枯病的生物防治效果。结果发现,小麦的整个生育期均能在小麦根部分离出发绿色荧光的菌株,利用PCR方法对发光菌株进行特异性扩增,证明其为施用的GFP标记菌株(图4)。GFP标记菌株在小麦根部的定殖数量呈现明显的规律性,即冬前分蘖期最多,每克根重的细菌数量达到105 CFU,之后随着温度的降低,小麦进入越冬期,分离出的GFP菌株数量达到最低,仅为102 CFU,越冬后小麦进入拔节期时,细菌数量虽然有所增加,但是与越冬期没有明显的差别。之后,随着温度的进一步升高,小麦进入抽穗期和灌浆期,分离出的GFP标记细菌迅速增加,到灌浆期时单位根重(g)的细菌数量达到104 CFU(图5)。
|
| 图 4 大田小麦根部分离获得的GFP标记菌株及其PCR鉴定 Fig. 4 PCR identification to GFP tagging strains isolated from roots of wheat grown in field |
|
| 图 5 GFP标记菌株在不同生育期小麦根部的定殖动态 Fig. 5 Colonization dynamic of GFP tagging strain on roots of different growth stages wheat |
分别于小麦冬前分蘖期、拔节期、孕穗期和灌浆期调查大田不同小区施用生防菌B3-7及其GFP标记菌株后小麦纹枯病的发病率和严重度,结果发现,与不施用任何菌株的对照相比,施用B3-7及其GFP标记菌株后小麦纹枯病的发病率没有差别。病害的严重度除了在拔节期差别不明显外,在分蘖期、孕穗期和灌浆期差异显著。B3-7及其GFP标记菌株在分蘖期、孕穗期和灌浆期对于小麦纹枯病的防治效果分别为60%—62%、34%—39%和34%—38%,两个菌株之间防病效果无明显差异。病田通过施用生防菌能够提高产量,B3-7菌株及其GFP标记菌株能够提高产量13%—15%(表2)。
| 处理 Treatment |
严重度Severity | 产量 Yield/(kg/6m2) |
|||
| 分蘖期 Tillering period |
拔节期 Jointing stage |
抽穗期 Heading period |
灌浆期 Milking period |
||
| B3-7 | 7.9 a | 12.3 a | 15.2 a | 20.6 a | 4.05±0.22 |
| B3-7(GFP) | 7.5 a | 13.1 a | 16.7 a | 19.5 a | 4.11±0.41 |
| 对照Control | 19.8 b | 14.2 a | 25.2 b | 31.4 a | 3.56±0.20 |
| 数据后不同小写字母表示差异显著(P<0. 05),产量为3个试验小区产量的平均数±标准差 | |||||
上述结果表明,GFP标记后不改变生防菌B3-7对于小麦纹枯病的防病效果,B3-7通过降低病害的严重度,增加小麦的产量,具有一定的应用前景。
3 讨论植物在生长过程中,通过其根系向周围环境中分泌大量的有机物,营造了适于微生物生长繁殖的环境,导致大量微生物存活于于植物根部。其中某些根部细菌一方面利用根系分泌物获取营养,另一方面通过其本身的代谢活动促进植物生长,这些细菌被称为根际促生细菌(plant growth-promoting rhizobacteria,PGPR)。有研究表明,PGPR可以通过多种机制促进植物生长。这些机制主要包括:1)促生作用,某些种类的PGPR能够通过生物固氮、产生植物激素和解磷解钾等方式促进植物生长[6];2)抑制有害生物对于植物的危害,PGPR可以通过产生抗菌物质或者利用生态位和营养竞争作用减少包括植物病原真菌在内的有害生物对于植物的危害,间接促进植物生长[13];3)诱导植物产生对于逆境胁迫的抗性,有些PGPR本身的细胞成分或者细胞分泌物能够激发植物产生抗性,提高植物的对于逆境胁迫的抗性[14]。利用PGPR防治植物病害,尤其是土壤传播病害对于替代化学农药的使用、减少抗药性病原菌的产生、减少病害造成的损失和改善作物品质具有重要价值。国内外已有多种利用PGPR开发的生物农药实现商业化应用[15]。
自然状况下,植物根际是一个复杂的生态环境,不仅存在温度、湿度等环境因子的变化,而且不同微生物之间存在营养和生态位竞争。PGPR生防菌株 发挥作用的前提是能够在植物根际长期定殖并形成数量优势,这就需要生防菌株具有良好的生态适应性。芽孢杆菌作为一类在自然界中广泛存在的微生物类型,其可以分泌多种胞外水解酶和抗菌物质,有助于在竞争中获得优势[16]。尤其重要的是,芽孢杆菌可以在逆境胁迫下产生特殊的休眠结构芽孢,有助于该类细菌在低温、高温和干旱等逆境条件下环境中长期存在,待条件适宜时,芽孢萌发并快速分裂形成大量个体,形成优势种群,促进其生防作用的发挥。本研究利用的B3-7菌株是一株蜡样芽孢杆菌,前期研究中发现在室内对于小麦纹枯病和小麦全蚀病具有较好的生防效果。该菌株已经授权国家发明专利。为了进一步解析该菌株在大田中的作用效果,本研究利用广泛使用的标记蛋白GFP对其进行标记。通过比较标记菌株与B3-7的生物学特性,发现GFP标记不改变生防菌的生物学特性和对于小麦纹枯病的生防特性。大田小区实验不仅证明了生防菌株具有较强的适应性,而且证明了生防菌株B3-7在大田条件下也对病害具有防治效果,为进一步开发生防制剂奠定了基础。本研究仅仅是单点小区试验,对于B3-7在其它不同气候条件下的生态适应性和对病害的防治效果,有待进一步研究。
| [1] | Han Y P,Chen X L,He Z T,Wang J R,Yang H F. Progress, problem and prospect of wheat sharp eyespot research. Journal of Triteceae Crops,2001,21(1): 81-84. |
| [2] | Wen C Y,Wang K X,Wang M,Wang N,Wu Z. Colonization trends of endophytic bacteria EBS05 in wheat and its control effect on wheat sharp eyespot. Acta Phytophylacica Sinica,2011,38(6):481-486. |
| [3] | Jetiyanon K,Fowler W D, Kloepper J W. Broad-spectrum protection against several pathogens by PGPR mixtures under field conditions in Thailand. Plant Disease, 2003,87(11):1390-1394. |
| [4] | Raupach G S, Kloepper J W. Biocontrol of cucumber diseases in the field by plant growth-promoting rhizobacteria with and without methyl bromide fumigation. Plant Disease,2000,84(10):1073-1075. |
| [5] | Myoungsu P,Chungwoo K,Jinchul Y,Hyoungseok L,Wansik S,Seunghwan K,Tongmin S. Isolation and characterization of diazotrophic growth promoting bacteria from rhizosphere of agricultural crops of Korea. Microbiological Research,2005,160(4):127-133. |
| [6] | Jos M R,Maria V,Jorge T. Antibiotic production by bacterial biocontrol agents. Antonie van Leeuwenhoek,2002,81(1):537-547. |
| [7] | Niranjan R S,Chaluvaraju G,Amruthesh K N,Shetty H S,Reddy M S,Kloepper J W. Induction of growth promotion and resistance against downy mildew on pearl millet (Pennisetum glaucum) by rhizobacteria. Plant Disease,2003,87(4):380-384. |
| [8] | Wang G,Liu F Y,Wang M,Peng L. Motility of endophytic bacteria strain B3-7 involved in endophytic colonization of wheat roots and biological control of wheat take-all. Acta Phytopathologica Sinica,2011,41(5):526-533. |
| [9] | Sun Y N. Construction of transposon inserted mutant library with wheat endophytic bacillus and selection of mutants antagonism against Rhizoctonia cerealis[D]. Kai Feng:Henan University,2010. |
| [10] | Maryvonne A,Arnaud C,Michel D. New vector for efficient allelic replacement in naturally nontransformable, low-GC-content,gram-positive bacteria. Applied and Environmental Microbiology, 2004,70(11):6887-6891. |
| [11] | Dunn A K, Handelsman J. A vector for promoter trapping in Bacillus cereus.Gene, 1999,226(2): 297-305. |
| [12] | Clarkson J D,Cook R J. Effect of sharp eyespot (Rhizocionia cerealis) on yield loss in winter wheat. Plant Pathology,1983,32(4):421-428. |
| [13] | Handelsman J,Stabb E V. Biocontrol of soilborne plant pathogens.The Plant Cell, 1996,8(10):1855-1869. |
| [14] | Dutta S,Mishra A K,Kumar B S. Induction of systemic resistance against fusarial wilt in pigeon pea through interaction of plant growth promoting rhizobacteria and rhizobia. Soil Biology & Biochemistry,2008,40(2):452-461. |
| [15] | Borneman J,Becker J O. Identifying microorganisms involved in specific pathogen suppression in soil. Annual Review of Phytopathology,2007,45:153-172. |
| [16] | Viviana Y,Houda Z,Inmaculada V,Rosario T,Josep U,Antonio V,Alejandro P,Neus T. Biological control of peach brown rot (Monilinia spp.) by Bacillus subtilis CPA-8 is based on production of fengycin-like lipopeptides. European Journal of Plant Pathology,2012,132(11):609-619. |
| [1] | 韩月澎,秀兰,何震天,王锦荣,杨鹤峰. 小麦纹枯病研究现状, 问题与展望. 麦类作物学报,2001,21(1):81-84 |
| [2] | 文才艺,王凯旋,汪敏,王努,武哲. 内生细菌EBS05在小麦体内的定殖动态及其对小麦纹枯病的防治作用.植物保护学报,2011,38(6):481-486. |
| [8] | 王刚,刘凤英,王淼,彭玲. 内生细菌B3-7的运动性参与其在小麦根系的内生定殖和对小麦全蚀病的生物防治. 植物病理学报,2011,41(5):526-533. |
| [9] | 孙勇娜. 小麦内生芽孢杆菌插入突变体库的构建及其对禾谷丝核菌拮抗能力变异突变体的筛选 [D]. 开封:河南大学,2010. |
 2014, Vol. 34
2014, Vol. 34




