文章信息
- 李然然, 章光新, 张蕾
- LI Ranran, ZHANG Guangxin, ZHANG Lei
- 查干湖湿地浮游植物与环境因子关系的多元分析
- Multivariate analysis of the relations between phytoplankton assemblages and environmental factors in Chagan Lake Wetland
- 生态学报, 2014, 34(10): 2663-2673
- Acta Ecologica Sinica, 2014, 34(10): 2663-2673
- http://dx.doi.org/10.5846/stxb201306091545
-
文章历史
- 收稿日期:2013-6-9
- 修订日期:2014-4-17
2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
查干湖国家级自然保护区是由湖泊、沼泽、沼泽化草甸等不同生态系统复合而成的、以浅水型湖泊为核心的典型草原湖泊湿地生态系统,是吉林省西部重要的生态屏障,也是吉林省重要的渔业基地和旅游区,发挥着调节气候、保护区域生物多样性、发展生态产业、维护区域生态平衡的重要功能。在全球气候变化和人类活动影响下查干湖湿地水环境发生了深刻变化,已面临农业面源污染、盐碱化、有机污染等严峻的生态环境问题[1, 2]。目前,吉林省承担着增产百亿斤粮食的重任,主要途径之一开发盐碱荒地发展灌区,农田退水中的盐碱、N、P污染物势必会对查干湖湿地水环境安全带来潜在风险。
浮游植物是水域生态系统的初级生产者,其种类组成和分布对环境变化具有指示作用,其生物量及群落结构的动态变化能很好地反映水环境现状及变化,浮游植物因为其多样性的时间和空间分布特征而被视为水环境的重要指示生物之一,反过来环境条件也能直接影响浮游植物的群落结构[3, 4, 5]。浮游植物作为水环境特征的重要指示剂,已引起了世界范围内的研究和关注[6, 7],但查干湖湿地浮游植物与环境因子之间关系的研究还鲜有报道。本文首次较系统地调查分析了查干湖湿地浮游植物群落组成、丰度及其空间分布特征,应用冗余分析(RDA)探讨查干湖湿地浮游植物群落与环境因子间的关系,利用浮游植物生态指标评价其水质营养状态,为查干湖湿地水资源开发与水环境保护提供生物学依据。
1 实验设计及研究方法 1.1 研究区概况查干湖湿地位于吉林省西部松原市内(124°03′—24°34′E,45°05′—45°30′N),属半干旱温带大陆性季风气候,多年年均温4.5 ℃,多年年均降雨量为415.4 mm,其中6—9月降雨量占全年的80%左右,多年年均蒸发量为1400—2100 mm,平均水位1.5 m。自然状态下,7—9月为丰水期,10月—次年4月为枯水期,5—6月为平水期,生长季为5—10月。
1.2 样品采集于2012年平水期5月和丰水期9月对查干湖湿地设置了13个采样点 (图 1),由于新庙泡为芦苇沼泽,船无法驶入,故在引松灌渠进入新庙泡处-高家桥即点3和新庙泡与查干湖相连处-川头闸即点1设置取样点,另在庙东核心区即点2布设样点。在查干湖主湖区,沿新庙泡—查干湖—辛甸泡方向设定3条平行样带,间隔5 km,在每条样带每隔5 km设置一个样点。浮游植物定性样品以25号浮游生物网(孔径64 μm)在水面下0.3—0.5 m处缓慢地做“∞”状拖取3min后将生物网中的水浓缩至100 ml保存,用1—2 mL鲁哥试液固定;定量样品使用采水器在表层采取1 L加10—15 mL鲁哥试剂固定,于实验室中经48 h沉淀后浓缩至30 mL,加4%甲醛溶液保存以备镜检。

|
| 图 1 查干湖湿地采样点分布图 Fig. 1 Sampling sites in Chagan Lake wetland |
浮游植物种类鉴定依据联合国教科文组织推荐的《浮游植物手册》[8]和《中国淡水藻类——系统、分类及生态》[9],硅藻种类的鉴定主要是以硅藻壳的形态及壳表面上的花纹为依据,需加酸煮沸去除其内含物后用蒸馏水洗净烤干,用安息香酸钠封片制成永久玻片观察;藻类计数采用0.1 mL计数框,在显微镜(Olympus CX21,400x)下进行,每个样本重复计数2次,每次观察100个视野,取其平均值;藻类生物量采用细胞体积法推算,单细胞藻类的生物量主要根据藻类个体形状测量而得[10]。
在各采样点使用多参数水质分析测定仪(HI9828)现场测定溶解氧(DO)、pH值、水温(T)、总溶解性固体(TDS),并用采水器采集表层水样1 L,带回实验室后依据《地表水环境质量标准》(GB3838—2002)[11],总氮 (TN)采用碱性过硫酸钾消解紫外分光光度法、磷酸盐(PO3-4)采用磷钼蓝法、高锰酸钾指数 (CODMn)采用高锰酸钾法)、五日生化需氧量(BOD5)采用稀释与接种法测定。
1.3 数据处理和统计分析浮游植物群落多样性指数采用Shannon多样性指数(H′)、Margalef丰富度指数(D)、Pielou均匀度指数(J)和多样性阈值(Dv) (公式1—4)[12, 13]描述,通过优势度(公式5)确定样本的优势种群(Y)。
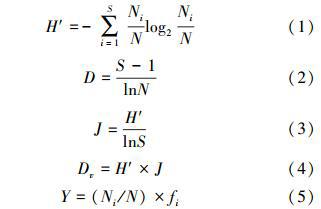
利用SPSS16.0软件进行Bray-Curtis相似性聚类分析,并采用多维排序尺度(MDS)分析相结合分析浮游植物群落的空间分布。用CANOCO4.5软件分析浮游植物分布与环境因子的关系:对平水期和丰水期种群信息进行去趋势对应分析(DCA),排序轴梯度长度(LGA)分别为0.867和1.651,均小于3,适合用基于线性的冗余分析(RDA),相关显著性用Monte Carlo法进行检验。为使浮游植物的个体数和环境因子的数据获得正态分布,除pH值外均进行lg(x+1)转换。由于环境因子之间可能存在较高的相关性,偏相关系数大于0.8和膨胀因子(VIF)大于20的环境因子都不进入RDA分析[15]。
按照优势度,本文用于排序的种群满足以下要求:Y≥0.02,且该种群不同时期出现的频率>2.5%,该种群至少在一个样点的相对丰度>1%[16, 17]。
2 结果与分析2012年查干湖湿地平水期和丰水期环境因子见表 1,平水期水温极显著低于丰水期,分别在15.8—18.6 ℃、19.8—22.4 ℃之间变化;pH值平水期显著高于丰水期,分别在7.8—8.8,7.1—8.0之间波动;平水期DO、BOD5含量极显著高于丰水期,而CODMn含量显著低于丰水期。营养盐中SiO3-Si含量丰水期显著高于平水期,TN、NO3-N、TP、PO4-P没有显著性差异。
| 参数Parameters | 平水期 Intermediate season | 丰水期 Rainy season | t检验t-testP值 P value | ||||
| 平均Mean | 最小Min | 最大Max | 平均Mean | 最小Min | 最大Max | ||
| **表示环境因子在0.01水平上存在极显著差异,*表示环境因子在0.05水平上存在显著差异 | |||||||
| 水温Temperature/ ℃ | 17.34 | 15.77 | 18.63 | 21.07 | 19.8 | 22.42 | -12.060** |
| 盐度Salinity / (mg/L) | 442 | 140 | 600 | 396 | 190 | 490 | 0.807 |
| pH | 8.2 | 7.8 | 8.8 | 7.6 | 7.1 | 8.0 | 6.336** |
| 溶解氧Dissolved oxygen/ (mg/L) | 10.5 | 6.4 | 12.5 | 6.6 | 4.6 | 7.9 | 7.836** |
| 高锰酸钾指数/ (mg/L)Chemical oxygen demand | 9.7 | 3.3 | 14.6 | 12.5 | 6.9 | 16.1 | -2.204* |
| 生化需氧量/ (mg/L) 5-day biochemical oxygen demand | 3.64 | 1.80 | 4.65 | 1.95 | 0.69 | 2.65 | 5.362** |
| 总氮Total nitrogen/ (mg/L) | 1.74 | 1.02 | 3.61 | 1.94 | 1.36 | 3.21 | -0.849 |
| NO-3-N/ (mg/L) | 0.05 | 0.02 | 0.15 | 0.05 | 0.01 | 0.18 | -0.148 |
| 总磷 Total phosphorus/ (mg/L) | 0.11 | 0.07 | 0.15 | 0.11 | 0.05 | 0.19 | 0.287 |
| PO3-4-P / (mg/L) | 0.02 | 0.01 | 0.05 | 0.01 | 0.01 | 0.02 | 0.878 |
| SiO2-3-Si / (mg/L) | 7.01 | 4.79 | 16.92 | 9.61 | 8.36 | 12.07 | -2.617* |
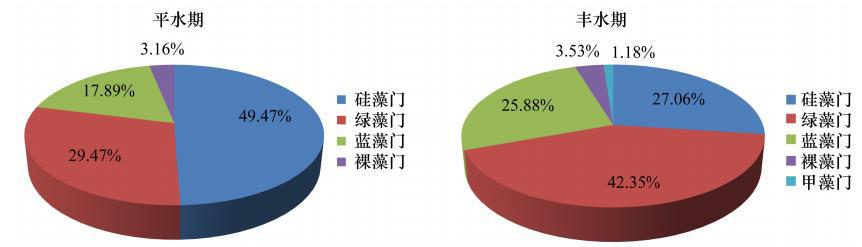
本次调查共鉴定出浮游藻类5门53属127种,其中硅藻门18属52种,占40.94%;绿藻门20属46种,占36.22%;蓝藻门13属25种,占19.69%;裸藻门1属3种,甲藻门1属1种。平水期物种较多,4门48属95种,丰水期略少,5门43属85种,藻类组成均以硅藻门和绿藻门为主(图 2)。根据优势度计算共发现浮游植物优势种群15个,其中平水期12个,丰水期11个,共有属8个(表 2)。
|
| 图 2 查干湖湿地浮游植物种类组成 Fig. 2 Phytoplankton composition in Chagan Lake wetland |
| 编号 Code | 门Phylum | 属Genus | 拉丁学名Latin names | 优势度 Dominance | |
| 平水期Intermediate season | 丰水期Rainy season | ||||
| n1 | 硅藻门 | 针杆藻 | Synedra | 0.140 | - |
| n2 | 硅藻门 | 舟形藻 | Navicula | 0.109 | - |
| n3 | 硅藻门 | 脆杆藻 | Fragilaria | 0.048 | - |
| n4 | 硅藻门 | 直链藻 | Melosira | 0.022 | 0.025 |
| n5 | 蓝藻门 | 束丝藻 | Aphanizomenon | 0.216 | 0.074 |
| n6 | 蓝藻门 | 席藻 | Phormidium | 0.132 | - |
| n7 | 蓝藻门 | 颤藻 | Oscillatoria | 0.023 | 0.045 |
| n8 | 蓝藻门 | 拟鱼腥藻 | Anabaenopsis | - | 0.020 |
| n9 | 绿藻门 | 栅列藻 | Scenedesmus | 0.140 | 0.354 |
| n10 | 绿藻门 | 十字藻 | Crucigenia | 0.020 | 0.050 |
| n11 | 绿藻门 | 纤维藻 | Ankistrodesmus | 0.021 | 0.020 |
| n12 | 绿藻门 | 盘星藻 | Pediastrum | 0.020 | 0.071 |
| n13 | 绿藻门 | 实球藻 | Pandorina | - | 0.050 |
| n14 | 绿藻门 | 空球藻 | Coelastum | - | 0.036 |
| n15 | 裸藻门 | 裸藻 | Euglena | 0.022 | 0.051 |
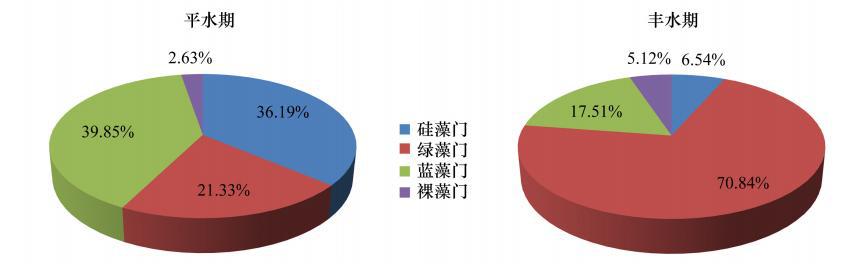
调查区平水期和丰水期浮游植物丰度分别介于34.27—1143.1×104 个/L、5.016—972×104 个/L,平均值分别为658.0×104 个/L、459.3×104 个/L。平水期蓝藻在丰度上占绝对优势,占浮游植物丰度的39.85%,丰度为0.92—494.1×104 个/L,平均为262.2×104 个/L,其次为硅藻,占36.19%,丰度为23.46—475.2×104 个/L,平均为238.2×104 个/L,再次为绿藻,占21.33%,丰度为6.5—287.7×104 个/L,平均为140.4×104 个/L;丰水期绿藻在丰度上占绝对优势,占浮游植物丰度的70.84%,丰度为0.132—811.3×104 个/L,平均为325.4×104 个/L,其次为蓝藻,占17.51%,丰度为0.083—215.0×104 个/L,平均为80.5×104 个/L,再次为硅藻,占6.547%,丰度为2.55—85.5×104 个/L,平均为27.3×104 个/L (图 3)。平水期和丰水期浮游植物生物量分别介于0.43—22.61 mg/L、0.20—20.69 mg/L,平均值分别为:11.86、8.24 mg/L。
|
| 图 3 查干湖湿地平水期和丰水期浮游植物相对丰度 Fig. 3 Relative abundance of phytoplankton in the intermediate and rainy season |
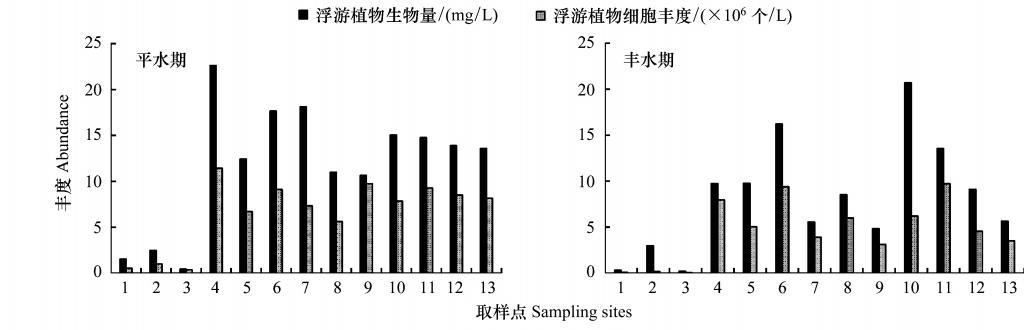
由查干湖湿地各站点浮游植物丰度和生物量分布图可以看出(图 4):新庙泡三点的浮游植物丰度和生物量明显低于主湖区,主湖区各点差异不显著,丰水期低于平水期。
|
| 图 4 查干湖湿地各站点浮游植物丰度和生物量分布图 Fig. 4 Density and biomass of phytoplankton in each site,Chagan Lake wetland |
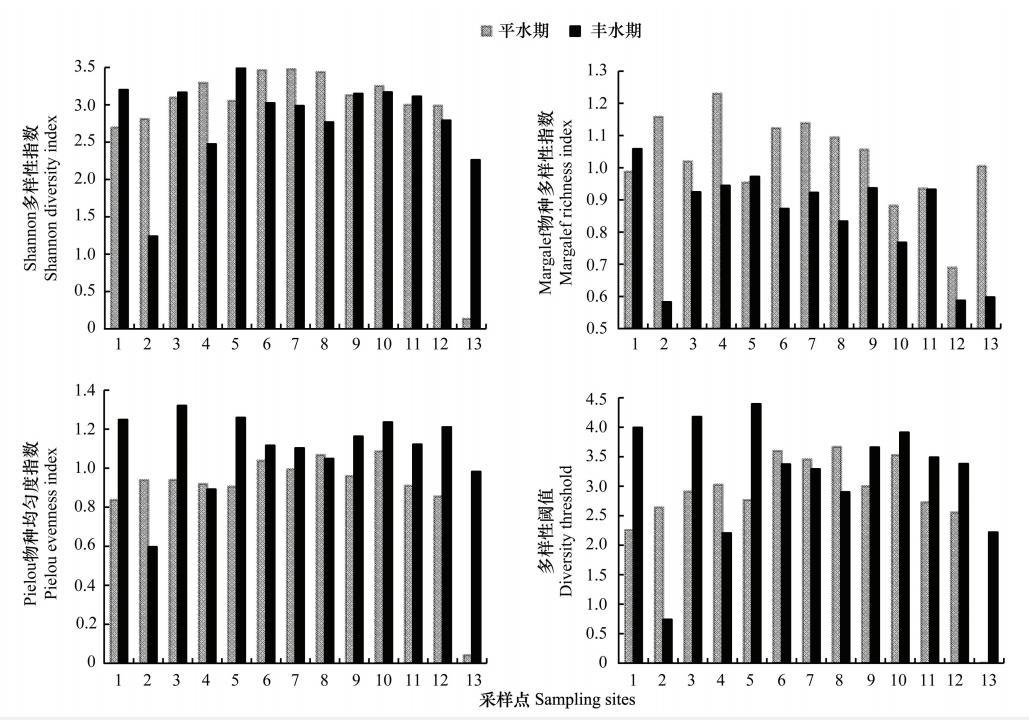
查干湖湿地平水期和丰水期的表层水域浮游植物群落Shannon多样性指数(H′)、Margalef指数(D)、Pielou均匀度指数(J)以及物种多样性阈值(DV)的平面分布如图 5所示。
|
| 图 5 查干湖湿地浮游植物多样性指数分布 Fig. 5 Distribution of diversity index of phytoplankton in Chagan Lake wetland |
平水期和丰水期浮游植物群落H′分别介于0.14—3.48、1.93—3.49,均值分别为2.91、2.83,D分别介于0.88—1.23、0.58—1.06,均值分别为1.02、0.80,J分别介于0.05—1.20、0.60—1.32,均值分别为1.04、1.1,DV分别介于0.01—4.10、0.74—4.39,均值分别为3.27、3.21。H′和J表现出一致的时空变化趋势。对比浮游植物丰度的平面分布(图 4),多样性指数的平面分布与浮游植物丰度呈镶嵌分布,表明:在丰度的高值区,浮游植物基本上是由高丰度的单一优势种群组成。
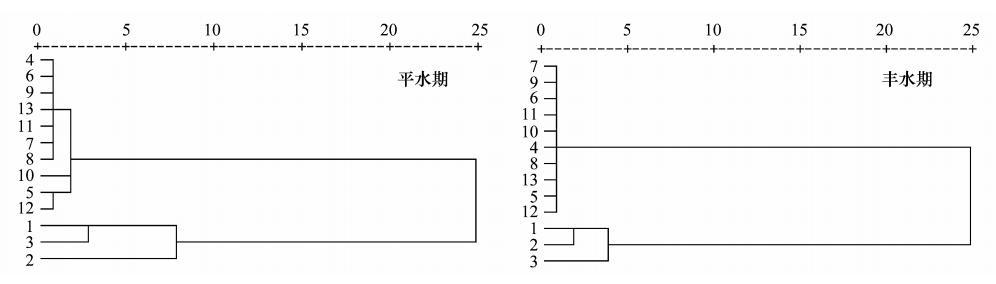
2.5 浮游植物优势种群空间分布特征在Bray-Curtis相似性测量基础上,采用组间平均聚类分析方法画出聚类树枝图(图 6)。可知,查干湖湿地平水期和丰水期浮游植物组成在10%处均可划分为两个聚类类型。各群聚类型包含站点和所处位置不同,类型Ⅰ(含调查点位1、2、3)分布于新庙泡,类型Ⅱ(含调查点位4—13)位于查干湖主湖区,与浮游植物群落多维排序尺度分析(图 7)一致。
|
| 图 6 查干湖湿地浮游植物群落聚类分析 Fig. 6 Cluster analysis of phytoplankton community in Chagan Lake wetland |
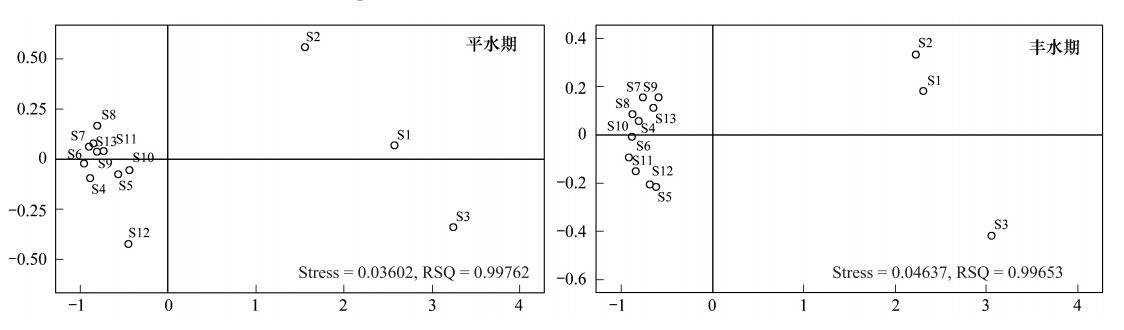
|
| 图 7 查干湖湿地浮游植物群落多维排序尺度分析 Fig. 7 MDS of phytoplankton community in Chagan Lake wetland |
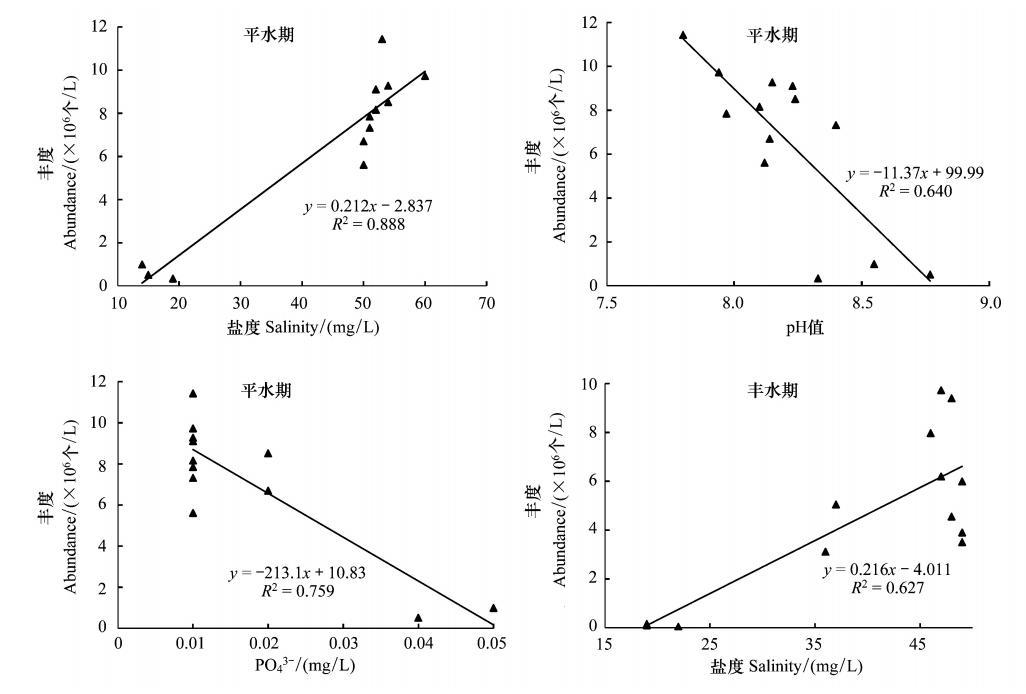
相关分析表明(图 8):平水期,查干湖湿地浮游植物丰度与盐度呈显著正相关,与pH值、PO3-4呈显著负相关;丰水期,浮游植物丰度与盐度呈显著正相关,与pH值、PO3-4、TN不存在统计学意义上的相关性。
|
| 图 8 查干湖湿地浮游植物丰度与环境因子的关系 Fig. 8 Correlation between phytoplankton abundance and environmental variables in Chagan Lake wetland |
查干湖湿地平水期和丰水期浮游植物群落与环境因子的RDA分析结果见表 3和图 9。由表 3知:在排序图中,平水期轴Ⅰ和轴Ⅱ的特征值分别为0.7、0.038,丰水期的分别为0.613和0.059;所选的环境因子共解释了平水期77.1%、丰水期71.1%的物种变化信息,前两轴累计解释了平水期73.8%、丰水期67.1%的物种变化信息和平水期95.7%、丰水期94.4%的物种-环境关系信息;两水文期的两个物种排序轴近似垂直,相关系数分别为-0.0524、0.0251,环境因子轴与物种排序轴之间的相关系数平水期为0.9714、0.8146,丰水期为0.9559、0.8442,两水文期两个环境排序轴的相关系数均为0(两水文期Monte Carlo置换检验所有排序轴均达到显著水平(P<0.05))说明排序结果可靠[15],排序轴与环境因子间线性结合的程度较好地反映了物种与环境之间的关系。
| 时间 Time | 轴 Axis | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 平水期 | 特征值 | 0.7 | 0.038 | 0.017 | 0.011 |
| Intermediate season | 浮游植物种属与环境因子相关关系 | 0.971 | 0.815 | 0.659 | 0.652 |
| 浮游植物种属的累积百分数/% | 70 | 73.8 | 75.5 | 76.6 | |
| 浮游植物与环境因子相关性的累积百分数/% | 90.8 | 95.7 | 97.9 | 99.3 | |
| 典型特征值总和 | 0.771 | ||||
| 丰水期 | 特征值 | 0.613 | 0.059 | 0.021 | 0.015 |
| Rainy season | 浮游植物种属与环境因子相关关系 | 0.956 | 0.844 | 0.626 | 0.676 |
| 浮游植物种属的累积百分数/% | 61.3 | 67.1 | 69.3 | 70.8 | |
| 浮游植物与环境因子相关性的累积百分数/% | 86.2 | 94.4 | 97.4 | 99.5 | |
| 典型特征值总和 | 0.711 |

|
| 图 9 浮游植物与环境因子RDA排序图 Fig. 9 Correlation plots of the redundancy analysis (RDA) on the relationship between the environment variables and phytoplankton taxa |
利用向前引入法对环境因子进行逐步筛选,Monte Carlo置换检验结果见图 9:平水期TN、BOD5、PO3-4、pH值主要在第Ⅰ轴影响浮游植物的分布,水温(T)主要在第Ⅱ轴影响浮游植物分布。平水期优势属与PO3-4、pH值呈反向相关,这与2.6分析结果一致;位于左下方的直链藻Melosira (n4)、纤维藻Ankistrodesmus (n11)与水温有正向相关;位于左上方的针杆藻Synedra (n1)、舟形藻Navicula (n2)、脆杆藻Fragilaria (n3)、颤藻Oscillatoria (n7)、裸藻Euglena(n15)与水温有反向关联;位于Ⅰ轴两侧的针杆藻Synedra (n1)、脆杆藻Fragilaria (n3)、束丝藻Aphanizomenon (n5)、席藻Phormidium (n6)、栅列藻Scenedesmus (n9)、十字藻Crucigenia (n10)、盘星藻Pediastrum (n12)、裸藻Euglena(n15)与TN、BOD5有正向关联,与pH、PO3-4负相关。而丰水期,盐度(sal.)、pH值、和BOD5主要在第一轴影响浮游植物分布,水温(T)和PO3-4主要在第Ⅱ轴影响浮游植物分布:丰水期优势属与盐度、pH值、PO3-4、BOD5有正向关联,位于左下方的拟鱼腥藻 Anabaenopsis (n8)、纤维藻Ankistrodesmus (n11)与水温呈正向相关。由RDA分析知:影响平水期浮游植物优势属分布的最主要环境因子是pH值、TN和BOD5,而盐度、PO3-4和BOD5则是影响丰水期浮游植物分布的最主要因子。
3 讨论 3.1 浮游植物群落结构特征调查期间,查干湖湿地浮游植物群落由平水期的硅藻型发展为丰水期的绿藻型,这与温度变化及水质状况密切相关。平水期,水温较低,适合硅藻生长,丰水期,随着温度升高,绿藻开始大量繁殖。这与杨富亿1994年9月对查干湖浮游植物的调查结果一致[18]。同南方浅水性湖泊相比,查干湖共检出浮游植物5门53属127种,在种类和数量上少于鄱阳湖(鄱阳湖1987—1993年浮游植物种类数为8门153属319种[19]),多于太湖(太湖1991—2002年检出浮游植物4门74种[20])。与中国东北镜泊湖(镜泊湖2007年浮游植物种数为8门103种[21])和小兴凯湖相近(小兴凯湖2011年浮游植物种数为7门121种[22])。
3.2 浮游植物群落结构与环境因子的关系水温是浮游植物水平分布的主要影响因素之一,浮游植物丰度、生物量均随水温的升高而增加[23]。但在查干湖湿地,虽然丰水期水温高于平水期,但其浮游植物物种数、丰度及生物量均低于平水期。原因在于:一方面,丰水期时降水量增加,来自前郭灌区的农田退水也汇入查干湖,致使水位升高了40 cm,对浮游植物丰度和生物量具稀释作用,且导致水力滞留时间减少,水流速度增加,而浮游植物的水平分布受水流的影响很大[24],较快的水流不利于浮游植物生物量的积累;另一方面,查干湖湿地浮游植物丰度与盐度呈显著正相关关系,而丰水期盐度低于平水期;第三,查干湖湿地作为吉林省重要的渔业基地,每年春秋两季都会投放鱼苗几十万斤,随着鱼类生长,其摄食量的增加也加剧了两水文期浮游植物丰度和生物量的时间差异。
浮游植物丰度和生物量的空间分布显示:新庙泡浮游植物的丰度、生物量均显著低于查干湖主湖区。同一水文期内,主湖区的丰度、生物量是新庙泡的8—10倍。这是由于:平水期浮游植物丰度与盐度呈正相关,与pH值及PO3-4呈显著负相关,而平水期查干湖主湖区的盐度(52.7 mg/L)是新庙泡(16.0 mg/L)的3.3倍,且新庙泡pH值(平均为8.6)、PO3-4含量(平均为0.045 mg/L)高于查干湖主湖区(pH值、PO3-4平均值分别为8.1、0.012 mg/L);而丰水期主湖区的盐度(45.6 mg/L)是新庙泡(20 mg/L)的 2.3倍,浮游植物丰度空间分布主要受盐度影响。此外,新庙泡内3号点高家桥和1号川头闸位于农田退水进出新庙泡处,较大的流速不利于浮游植物的富集,致使两处浮游植物丰度较低。
浮游植物群落的时间差异显示:平水期优势属纤维藻Ankistrodesmus (n11)喜欢水温高的生境,在丰水期仍为优势属;而硅藻门的针杆藻Synedra (n1)、舟形藻Navicula (n2)、脆杆藻Fragilaria (n3),蓝藻门的颤藻Oscillatoria (n7),裸藻门的裸藻Euglena(n15)等喜低温生境的优势属则为喜高温的绿藻取代,这也使得浮游植物群落结构由平水期的硅藻型演变为丰水期的绿藻型。平水期优势属喜低碱、低磷素、高氮素的生境,而丰水期优势属则喜微碱性、高盐度、高磷素、高BOD5的生境。本次调查发现的物种均为温带常见小型藻类,新陈代谢速度较快,属于能迅速吸收营养盐并进行繁殖生长的种类[25],因此,它们在较高营养盐条件下可以形成较高的相对丰度。
不同湖泊由于其自然条件和人类干扰不同,影响其浮游植物群落和分布的环境因子各不相同。Naselli-Flores等[26]研究Arancio湖表明:水体温度、电导率、库容对浮游植物的影响最大,而Arhonditisis等[27]研究了华盛顿湖发现透明度、总磷和捕食压力对浮游植物的影响最大;张怡等[28]应用冗余度分析研究南屏水库发现水力滞留时间、降雨量和正磷是影响南屏水库浮游植物功能类群演替的重要因子;吴卫菊等[29]通过冗余度分析渔洞水库浮游植物群落结构发现水温是影响渔洞水库浮游植物结构季节性变化的主要因素,而水文动力学对水库浮游植物多样性及优势种的形成有较大影响。查干湖湿地作为前郭灌区农田退水的承泄区,营养盐对浮游植物的分布有重要作用。
3.3 基于生物多样性的查干湖湿地水质生态学评价环境条件可以直接影响浮游植物的群落结构,浮游植物的优势种群及群落结构特征指数的变化也可以在一定程度上反映水环境现状及变化。物种多样性就是衡量群落中物种组成的稳定程度及其数量分布的均匀程度和群落结构特征的重要营养指标。在生物水质监测中H′>3为轻或无污染,3—2为β-中度污染(轻中污染),2—1为α-中度污染(重中污染),0—1为重度污染。本次研究H′结果表明查干湖湿地水体处于β-中度污染(轻中污染),平水期略严重。
4 结论(1)调查期间共鉴定出浮游植物5门53属127种,主要由硅藻和绿藻组成,浮游植物丰度变化明显,为平水期>丰水期,浮游植物群落结构的时间差异较大,平水期优势种群以硅藻为主,丰水期以绿藻为主。据浮游植物多样性结果判断查干湖湿地处于β-中度污染水平。
(2)根据Bray-Curtis相似性系数聚类和多维排序尺度分析查干湖湿地浮游植物群落结构,可以把查干湖湿地划为新庙泡和主湖区两个区域,受盐度、营养盐、流速影响,新庙泡丰度、生物量低于主湖区。影响浮游植物群落优势属分布的环境因子,平水期为pH值、TN和BOD5,丰水期为盐度、PO3-4和BOD5。平水期优势属喜低碱、低磷素、高氮素的生境,而丰水期优势属则喜欢微碱性、高盐度、高磷素、高BOD5的生境。两个水文期浮游植物优势种群多为温带小型藻类能迅速吸收营养盐并进行繁殖生长,在较高营养盐条件下可以形成较高的相对丰度。
(3)由于查干湖湿地在吉林西部特殊的生态地位及经济价值,应研究其浮游植物群落特征在不同季节、不同年份之间的长期变化特征,因此需要更多资料的积累,同时对于浮游植物各物种与环境之间关系的认识,还有待进一步的现场实验去验证和完善。
致谢: 本研究在浮游植物样品的采集、鉴定过程中得到东北师范大学环境学院宋传涛老师及其团队的大力协助,英文摘要得到了澳大利亚詹姆斯库克大学工程学院孙广智老师的修改润色,特此致谢。
| [1] | Dai X J, Tian W. Analysis and countermeasures on water pollution of lake Chagan. Journal of Arid Land Resources and Environment, 2011, 25(8):179-184. |
| [2] | Xiao H F, Xue B, Yao S C, Lv X G. Water quality of lakes evolution in Songnen Plain. Wetland Science, 2011, 9(2): 120-124. |
| [3] | Whitton B A. Use of Algae for monitoring rivers. Journal of Applied Phycology, 1991, 3(3): 287-287. |
| [4] | Whitton B A. Changing approaches to monitoring during the period of the 'Use of Algae for Monitoring Rivers’ symposia. Hydrobiologia, 2012, 695(1): 7-16. |
| [5] | Lepisto L, Holopainen A L, Vuoristo H. Type-specific and indicator taxa of phytoplankton as a quality criterion for assessing the ecological status of Finnish boreal lakes. Limnologica, 2004, 34(3): 236-248. |
| [6] | Beisner B E, Longhi M L. Spatial overlap in lake phytoplankton: Relations with environmental factors and consequences for diversity. Limnology and Oceanography, 2013, 58(4): 1419-1430. |
| [7] | Longhi M L, Beisner B E. Environmental factors controlling the vertical distribution of phytoplankton in lakes. Journal of Plankton Research, 2009, 31(10): 1195-1207. |
| [8] | Hasle G, Sournia A. Phytoplankton Manual, Monographs on Oceanographic Methodology. Paris: UNESCO, 1978. |
| [9] | Hu H J, Wei Y X. The freshwater algae of China: systematic, taxonomy and ecology, Beijing: Sciences Press, 2006. |
| [10] | Sun J, Liu D Y. Study on phytoplankton biomass: Ⅰ. Phytoplankton measurement biomass from cell volume or plasma volume. Acta Oceanologica Sinica, 1999, 21(2): 75-85. |
| [11] | Standardization Administration of China. GB3838-2002, National Standard of the People's Republic of China: Environmental Quality Standards for Surface Water. Beijing: Standards Press of China, 2002. |
| [12] | Jin X C, Tu Q Y. The Standard Methods in Lake Eutrophication Investigation. Beijing: China Environment Science Press, 1990. |
| [13] | Liu W Y, Gao R H, Zhang Q L, Chen Y H, Xing X J, Bai Z Y, Jia L Q, Yu X Z. The diversity of phytoplankton in salina-alkaline wetland on the Erdos Plateau. Journal of Arid Land Resources and Environment, 2009, 27(5): 143-148. |
| [14] | Xu Z L, Chen Y Q. Aggregated intensity of dominant species of zooplankton in autumn in the East China Sea and Yellow Sea. Journal of Ecology, 1989, 8(4): 13-15, 19. |
| [15] | Ter Braak C J, Prentice I C. A theory of gradient analysis. Advances in Ecological Research, 1988, 18: 277-315. |
| [16] | Lopes M R M, Bicudo C E M., Ferragut M C. Short term spatial and temporal variation of phytoplankton in a shallow tropical oligotrophic reservoir, southeast Brazil, Hydrobiologia, 2005, 542: 235-247. |
| [17] | Muylaert, K, Sabbe K, Vyverman W. Spatial and temporal dynamics of phytoplankton communities in a freshwater tidal estuary (Schelde, Belgium). Estuarine, Coastal and Shelf Science, 2000, 50(5): 673-687. |
| [18] | Yang F Y. Comprehensive exploitation and utilization of Chagan Lake. Resource Development &Marker, 1998, 14(6): 247-249, 254. |
| [19] | Xie Q M, Li C C, Peng C L. Primary studies on community ecology of floating algae in Poyang Lake. Jiangxi Sciecce, 2000, 18(3): 162-166. |
| [20] | Qian K M, Chen Y W, Song X L. Long-term development of phytoplankton dominant species related to eutrophicarion in Lake Taihu. Ecological Science, 2008, 27(2): 65-70. |
| [21] | Song C, Yu H X. Phytoplankton diversity in Jingpo Lake and water quality evaluation. Journal of Northeast Forestry University, 2009, 37(4): 39-42. |
| [22] | Yuan Y X, Yu H X, Jiang M. Phytoplankton community structure and diversity in Xiaoxingkai Lake. Wetland Science, 2013, 11(2): 151-157. |
| [23] | Lehman W. The influence of climate on phytoplankton community biomass in San Francisco Bay Estuary. Limnology and Oceanography, 2000, 45(3): 580-590. |
| [24] | Wu N C, Tang T, Zhou S C, Fu X C, Jiang W X, Li F Q, Cai Q H. Influence of cascaded exploitation of small hydropower on phytoplankton in Xiangxi River. Chinese Journal of Applied Ecology, 2007, 18(5): 1093-1098. |
| [25] | Sandgren C D. Growth and reproductivestrategies of freshwater phytoplankton. Cambridge: Cambridge University Press, 1992. |
| [26] | Nasell-iFlores L, Barone R. Phytoplankton dynamics in two reservoir with different trophic state(Lake Rosamarina and Lake Arancio, Sicily, Italy). Hydrobiologia, 1998, 369: 163-178. |
| [27] | Arhonditsis G B, Winder M, Brett M T, Schindler, D E. Patterns and mechanisms of phytoplankton variability in Lake Washington(USA). Water Research, 2004, 38: 4013-4027. |
| [28] | Zhang Y, Hu R, Xiao L J, Han B P. Comparative analysis of succession of the phytoplankton functional groups in two reservoirs with different hy drodynamics in Southern China. Ecology and Environmental Sciences, 2012, 21(1): 107-117 |
| [29] | Wu W J, Yang K, Wang Z C, Li G B, Liu B D. Community structure and seasonal succession of phytoplankton in Yundong Reservoir of Yungui-plateau. Journal of Hrdroecology, 2012, 33(2): 69-75. |
| [1] | 代雪静, 田卫. 查干湖水质污染分析及控制途径. 干旱区资源与环境, 2011, 25(8): 179-184. |
| [2] | 肖海丰, 薛滨, 姚书春, 吕宪国. 松嫩平原湖泊水质演化研究. 湿地科学, 2011, 9(2): 120-124. |
| [9] | 胡鸿钧, 魏印心. 中国淡水藻类——系统、分类及生态. 北京: 科学出版社, 2006. |
| [10] | 孙军, 刘东艳. 浮游植物生物量研究: Ⅰ. 浮游植物生物量细胞体积转化法. 海洋学报, 1999, 21(2): 75-85. |
| [11] | 中国国家标准化管理委员会. GB3838—2002, 中华人民共和国国家标准:地表水环境质量标准. 北京: 中国标准出版社, 2002. |
| [12] | 金相灿, 屠清瑛. 湖泊富营养化调查规范. 北京: 中国环境科学出版社, 1990. |
| [13] | 刘文盈, 高润宏, 张秋良, 陈玉海, 邢小军, 白兆勇, 贾丽琼, 于向芝. 鄂尔多斯高原盐沼湿地浮游植物的多样性与评价. 干旱区资源与环境, 2009, 27(5): 143-148. |
| [14] | 徐兆礼, 陈亚瞿. 东黄海秋季浮游动物优势种聚集强度与鲐鲹渔场的关系. 生态学杂志, 1989, 8(4): 13-15, 19. |
| [18] | 杨富亿. 查干湖的综合开发与利用. 资源开发与市, 1998, 14(6): 247-249, 254. |
| [19] | 谢钦铭, 李长春, 彭赐莲. 鄱阳湖浮游藻类群落生态的初步研究. 江西科学, 2000, 18(3): 162-166. |
| [20] | 钱奎梅, 陈宇炜, 宋晓兰. 太湖浮游植物优势种长期演化与富营养化进程的关系. 生态科学, 2008, 27(2): 65-70. |
| [21] | 宋辞, 于洪贤. 镜泊湖浮游植物多样性分析及水质评价.东北林业大学学报, 2009, 37(4): 39-42. |
| [22] | 袁宇翔, 于洪贤, 姜明. 小兴凯湖浮游植物群落结构及多样性. 湿地科学, 2013, 11(2): 151-157. |
| [24] | 吴乃成, 唐涛, 周淑婵, 傅小城, 蒋万祥, 李凤清, 蔡庆华. 香溪河小水电的梯级开发对浮游藻类的影响. 应用生态学报, 2007, 18(5): 1093-1098. |
| [28] | 张怡, 胡韧, 肖利娟, 韩博平. 南亚热带两座不同水文动态的水库浮游植物的功能类群演替比较. 生态环境学报, 2012, 21(1): 107-117. |
 2014, Vol. 34
2014, Vol. 34




