文章信息
- 杜照奎, 李钧敏, 钟章成, 董鸣
- DU Zhaokui, LI Junmin, ZHONG Zhangcheng, DONG Ming
- 花生叶片蛋白组对UV-B辐射增强的响应
- A proteomic analysis of Arachis hypogaea leaf in responses to enhanced ultraviolet-B radiation
- 生态学报, 2014, 34(10): 2589-2598
- Acta Ecologica Sinica, 2014, 34(10): 2589-2598
- http://dx.doi.org/10.5846/stxb201302030223
-
文章历史
- 收稿日期:2013-2-3
- 网络出版日期:2014-3-21
2. 台州学院生态研究所, 台州 318000;
3. 中国科学院植物研究所植被与环境变化国家重点实验室, 北京 100093;
4. 杭州师范大学生命与环境科学学院, 杭州 310036
2. Institute of Ecology, Taizhou University, Taizhou 318000, China;
3. State Key Laboratory of Vegetation and Environmental Change, Institute of Botany, Chinese Academy of Sciences, Beijing 100093, China;
4. College of Life and Environmental Sciences, Hangzhou Normal University, Hangzhou 310036, China
人类工业的快速发展使得大量氯氟烃类气体被释放到空气中,导致大气臭氧层变薄,从而提高到达地球表面的UV-B(ultraviolet-B,UV-B,280—320 nm)水平[1]。UV-B虽然只是太阳光谱中的一小部分,但是很容易被生物分子(例如:核酸、蛋白质和脂质等)大量吸收,从而引起高等植物中分子和细胞水平的生化反应历程发生改变[2]。目前,植物对UV-B辐射响应的研究报道较多,但大多集中在光合作用、形态变化和生理抗性等。总体而言,增强的UV-B辐射会使较多的植物净光合速率降低、株高变低、叶片变厚、生物量下降,并且伴随抗氧化酶活性升高或UV-B吸收物质含量增加等[3]。
当前,评价UV-B辐射增强对植物光合作用影响时通常是比较处理与对照间植物的净光合速率(Pn),如果Pn下降,则一般会从3个方面进行解释:一是透射电镜观察叶绿体超微结构遭到破坏[4],二是核酮糖-1,5-二磷酸羧化酶(Rubisco)羧化效率下降[5],三是电子传递效率降低[6],但深层原因的解释较少。此外,植物应对UV-B辐射方面,较多的研究将重点集中在一些常见的抗氧化酶、非酶抗氧化性物质[7]和UV-B吸收物质(如:类黄酮)等层面,其它方面研究鲜有报道。
植物在生长发育过程中,常常会受到某些非生物胁迫,引发蛋白质在表达量和种类上的显著改变,而以双向电泳与质谱技术为标志的蛋白质组学为从分子水平揭示植物对非生物胁迫(如:干旱、低温、盐、臭氧和重金属等)的响应机制提供了有力保障[8]。花生(Arachis hypogaea L.)是豆科落花生属一年生草本植物,富含脂肪和蛋白质,为重要的食用植物油来源。研究发现,UV-B辐射可导致花生产量下降[9],原因是因为净光合速率降低,株高变矮和叶片数目减少,但有关花生UV-B辐射对花生影响的分子机制尚未明确。本课题组在前期研究发现大田种植的花生在接受UV-B补增处理24 h后,净光合速率显著下降,本研究拟借助于蛋白质组学技术,分析花生幼苗在UV-B辐射增强下蛋白质表达的差异,旨在从蛋白质水平揭示:1)UV-B辐射增强处理降低花生光合速率的分子机理,2)花生抵御UV-B辐射增强的分子机制,从而为最终培育优良抗性品种提供理论依据。
1 材料与方法 1.1 供试材料供试花生(A. hypogaea L.)品种为小京生,该品种为浙江省优异花生,种子购自新昌县种子公司。
1.2 试验设计试验在浙江省临海市许市村旱地进行,土壤为沙性土,其基本理化性质为:pH 7.57、有机质26.21 g/kg、全氮1.08 g/kg、全磷1.55 g/kg、全钾15.20 g/kg、碱解氮36.15 mg/kg、有效磷112.26 mg/kg、速效钾为155.62 mg/kg。2012年5月1日挑选健康饱满、大小均匀的花生种子于25 ℃自来水中浸泡24 h,穴播,每穴2粒,行距40 cm,穴距20 cm。
花生萌发后,每穴保留2棵幼苗,待主茎4对真叶全部展开时开始进行补增UV-B辐射处理,UV-B光源采用北京电光源研究所生产的紫外灯管(发射波段280—320 nm,峰值308 nm)。将紫外灯具悬挂在试验组花生上方,维持UV-B辐射强度在54 μW/cm2左右(相当于试验地太阳光UV-B的20%,UV enhanced,UVE),每天辐射时间8 h,共处理3d;为保证两组接受太阳光照射条件尽可能一致,对照组(CK)花生上方也悬挂灯架,但不安装灯管。处理结束后,收获植株最顶端2张叶片,对照和处理各设8个重复,液氮速冻,并保存于-80 ℃冰箱中,用于蛋白质组学分析。
1.3 研究方法 1.3.1 花生蛋白质的提取与制备将5个重复的冷冻样品取出,称取1 g左右叶片,混合,液氮中充分研磨;按照1∶10的比例加入预冷的含10%三氯乙酸的丙酮,-20 ℃沉淀1h;4 ℃,15000 r/min离心15 min,取沉淀,加入预冷丙酮,-20 ℃沉淀1h;4℃,15000 g离心15 min,取沉淀,真空冷冻干燥;在20 mg干燥蛋白粉末中加入1 ml样品裂解液(9 mol/L尿素、4% CHAPS、1% IPG buffer、1% DTT),30 ℃恒温水浴溶解1h,使蛋白充分溶解;将溶液在室温下15000 r/min离心15 min,取上清,并再次离心取上清,充分去除不溶性杂质。上清液即为组织的总蛋白溶液,采用Bradford法测定提取的蛋白浓度并分装后储存于-80 ℃备用或直接用于双向电泳。
1.3.2 花生蛋白质的双向电泳第一向固相pH梯度等电聚焦电泳(Isoelectric focusing,IEF):采用GE Healthcare生产的 IPG胶条(24 cm,pH=3—10),上样蛋白量为200 μg(体积为450 μL)。水化和聚焦温度均为20 ℃,等电聚焦程序为:50 V聚焦12 h、500 V聚焦1h、1000 V聚焦1 h、1000—10000 V梯度升压聚焦1 h、10000 V聚焦10 h。
第二向SDS-PAGE电泳:聚焦完毕后,取出胶条,在10 ml平衡缓冲液Ⅰ[6 mol/L尿素、50 mmol/L Tris·HCl(pH=8.8)、30%甘油、2%SDS、1%DTT和0.05%溴酚兰]和10 ml平衡缓冲液Ⅱ[6 mol/L尿素、50 mmol/L Tris·HCl(pH=8.8)、30%甘油、2%SDS、2.5%碘乙酰胺和0.05%溴酚兰]的平衡管中缓慢水平摇晃15 min。在SDS-PAGE凝胶(12%)的上表面加入封胶液(25 mmol/L Tris、192 mmol/L甘氨酸、0.1%SDS和0.5%琼脂糖),将胶条放到第二向SDS-PAGE凝胶的上表面,使胶条与SDS-PAGE凝胶的胶面充分接触。待琼脂糖完全凝固后,将凝胶转移至电泳槽中,在15 ℃按如下参数进行电泳:100 V电泳45 min后将电压改为200V,电泳至溴酚兰前沿刚好跑出凝胶。
1.3.3 硝酸银染色电泳结束后,轻轻撬开两层玻璃板,取出凝胶按Shevchenko等[10]方法进行硝酸银染色,略有修改。具体操作如下:双蒸水洗5 min;固定液(30%乙醇、10%乙酸)固定30 min;10%乙醇洗两遍,每遍5 min;双蒸水洗两遍,每遍5 min;敏化液(0.02%硫代硫酸钠)敏化1 min;水洗两遍,每次1 min;银染液(0.1%硝酸银)染色20 min;双蒸水洗两次,每次30 s;显影液(0.25%碳酸钠,0.04%甲醛溶液)显影3 min;至图像满意;停显液(5%乙酸)终止显色;双蒸水洗3 次,每次5 min,保鲜膜密封。4 ℃保存备用。
1.3.4 双向电泳图谱分析银染后的凝胶应用Image Scanner(GE Healthcare)扫描仪进行扫描,扫描模式为灰度模式,光密度值为300 dpi。使用PDQuest 8.0软件(Bio-Rad)对处理和对照的双向电泳图像进行分析,按照软件说明进行凝胶蛋白点检测、图像背景扣除、蛋白点灰度值标准化和不同凝胶间蛋白点匹配,以变化倍数大于2.5倍或小于0.4倍为标准选择差异蛋白点用于质谱分析。
1.3.5 质谱鉴定与数据库检索从凝胶上切取差异蛋白质点,用胰蛋白酶于37 ℃酶解16 h,利用基质辅助激光解析电离飞行时间质谱(MALDI-TOF-TOF MS,质谱仪器型号:ABI 5800 Proteomics Analyzer)对蛋白质进行鉴定。将一级和二级质谱数据整合并使用GPS 3.6(Applied Biosystems)和Mascot2.1(Matrix Science)对质谱数据进行分析和蛋白鉴定,搜索参数如下:数据库为NCBInr 绿色植物数据库(Viridiplantae),酶为胰蛋白酶,允许最大漏切位点为1,质量允许误差范围为 0.3 Da,在Protein score C.I.%大于95为鉴定成功。
1.3.6 生物信息学分析依据UniProtKB数据库(http://www.uniprot.org/)提供的蛋白质注释信息对蛋白质进行功能分类[11]。
2 结果与分析 2.1 花生叶片蛋白质双向电泳图谱花生叶片总蛋白质经IEF/SDS-PAGE、银染和图像扫描,获得了双向电泳图谱(图1),可以看出,对照(自然光照)与处理(UV-B辐射增强)之间叶片蛋白质在2D胶上的分布基本一致。用PDQuest 8.0软件对其进行分析,经自动检测和人工去除杂点后,从对照和处理2D凝胶上分别得到757个和779个稳定且重复性较好的蛋白质点。

|
| 图 1 自然光照(CK)和UV-B辐射增强处理(UVE)下花生叶片蛋白双向电泳图谱 Fig.1 2-DE maps of total proteins from A. hypogaea leaves treated with ambient UV-B radiation (CK) and with UV-B radiation enhanced (UVE) |
利用PDQuest 8.0软件对2-DE图谱进行分析,发现一些蛋白质在对照与处理间的表达丰度存在明显的差异。以对照相对处理蛋白质丰度变化在2.5倍以上(或0.4倍以下)作为检测阈值,比较对照和处理的2-DE凝胶图谱,结果表明UV-B辐射增强处理24 h后的花生叶片中共有39个蛋白质差异表达,为便于蛋白点的比较及质谱鉴定,分别标记为1—39。在39个差异表达的蛋白质点中,UV-B辐射增强处理使得22种蛋白质表达下调(图1CK中箭头所指蛋白质点),17种蛋白表达上调(图1UVE中箭头所指蛋白质点),部分差异表达蛋白质点见图2。
2.3 花生叶片差异表达蛋白点的质谱鉴定经过胰蛋白酶酶解、MALDI-TOF-TOF质谱分析获得肽质量指纹图谱,将肽质量指纹图谱与多肽序列标签数据提交Mascot网站,选用NCBInr数据库进行检索,成功对27个差异表达蛋白质进行了鉴定,表1为各差异表达蛋白质点的质谱鉴定结果。
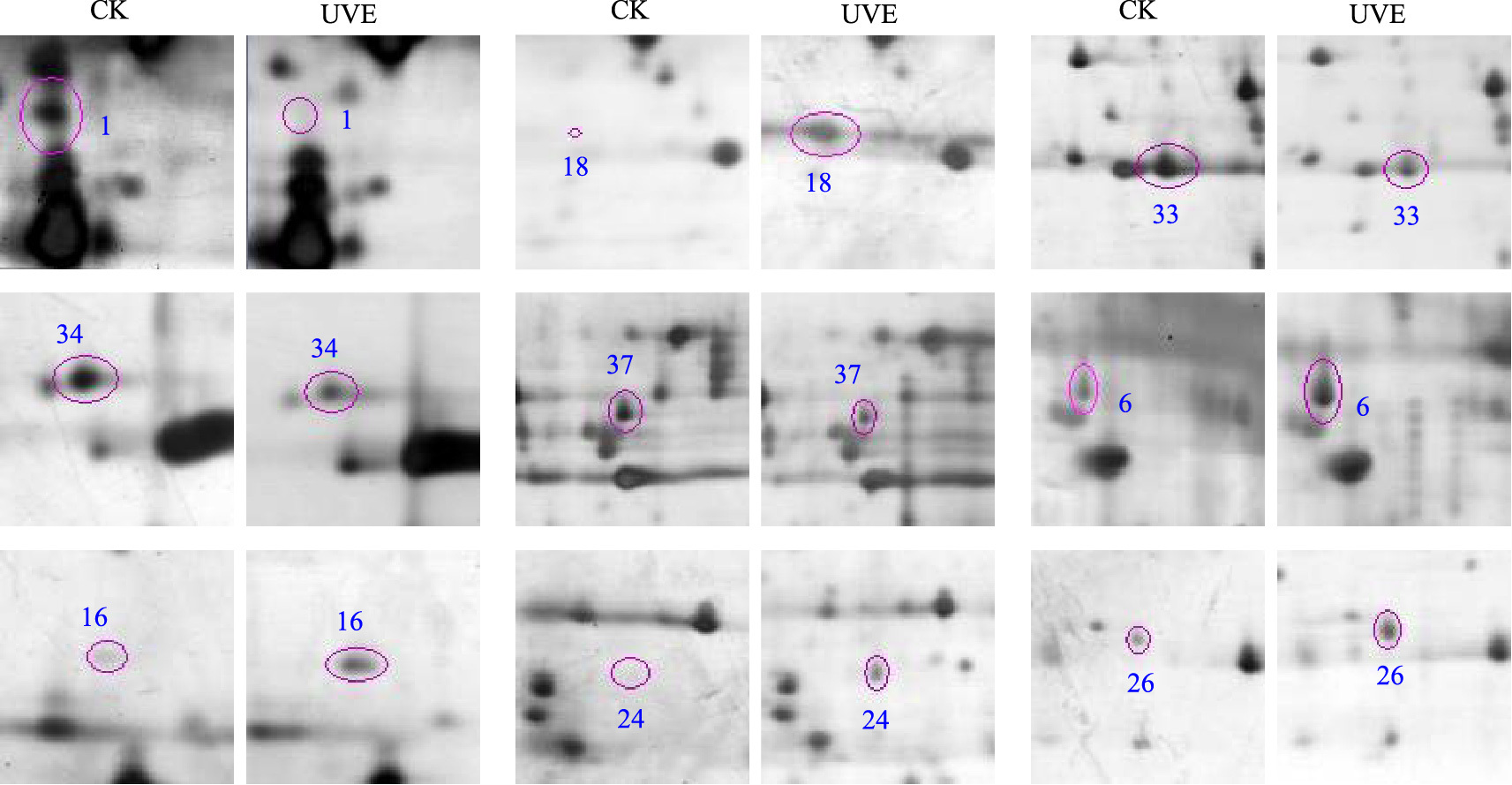
|
| 图 2 部分差异表达蛋白点的放大比较 Fig.2 Enlarged images of partial differentially expressed protein spots |
|
功能 Function | 蛋白点编号 Spot No. | 登录号 Accession number | 蛋白点名称 Protein name | 分子量 Molecular weight (Theo. / Exp.) (kD) | 等电点 Isoelectric point (Theo. / Exp.) | 得分 Score | 物种 Species | 表达调控 Regulation |
| ↑代表蛋白质表达量上调;↓代表蛋白质表达量下调 | ||||||||
| 光合作用 | 1 | gi|351727559 | 质体蓝素 | 16.55/16.40 | 4.82/3.24 | 177 | 大豆Glycine max | ↓ |
|
Photosynthesis | 3 | gi|1079736 | 核酮糖-1,5-二磷酸羧化酶小亚基前体 | 19.98/16.43 | 8.80/3.95 | 374 | 野大豆Glycine soja | ↓ |
| 7 | gi|1079736 | 核酮糖-1,5-二磷酸羧化酶小亚基前体 | 19.98/16.73 | 8.80/4.14 | 374 | 野大豆G. soja | ↓ | |
| 18 | gi|131386 | 放氧增强蛋白1 | 35.25/37.50 | 5.58/5.42 | 616 | 菠菜Spinacia oleracea | ↓ | |
| 22 | gi|356571888 | PsbP结构域蛋白6 | 28.51/29.91 | 5.73/6.33 | 409 | 大豆G. max | ↓ | |
| 37 | gi|351724481 | 果糖二磷酸醛缩酶 | 38.66/48.44 | 6.77/8.51 | 676 | 大豆G. max | ↓ | |
| 糖代谢 | 32 | gi|37725953 | 苹果酸脱氢酶 | 37.39/40.85 | 7.01/8.29 | 699 | 豌豆Pisum sativum | ↓ |
| Carbohydrate | 33 | gi|2827080 | 苹果酸脱氢酶前体 | 36.00/44.28 | 8.80/7.97 | 634 | 紫花苜蓿 Medicago sativa | ↓ |
| metabolism | 36 | gi|37725953 | 推测的苹果酸脱氢酶 | 37.39/39.35 | 7.01/8.51 | 699 | 豌豆P. sativum | ↓ |
| 能量生物合成 | 9 | gi|356512762 | ATP合成酶24kD亚基 | 29.98/32.23 | 8.87/5.16 | 300 | 大豆G. max | ↑ |
| Energy | 17 | gi|356563202 | ATP合成酶δ链 | 27.44/24.70 | 5.98/5.94 | 256 | 花生Arachis hypogaea | ↓ |
| biosynthesis | 21 | gi|224145221 | ATP合成酶δ链 | 26.94/25.14 | 6.02/6.52 | 378 | 毛果杨Populus trichocarpa | ↓ |
|
氨基酸生物合成 Amino acid biosynthesis | 23 | gi|255567778 | 半胱氨酸合成酶 | 43.38/43.39 | 7.60/6.54 | 696 | 蓖麻Ricinus communis | ↑ |
| 蛋白质加工 | 14 | gi|399940 | 70kD热激蛋白 | 72.72/78.86 | 5.95/5.57 | 1264 | 菜豆Phaseolus vulgaris | ↑ |
| Protein processing | 16 | gi|123556 | 18.2kD热激蛋白 | 18.15/22.86 | 5.81/5.93 | 266 | 紫花苜蓿M. sativa | ↑ |
|
蛋白质翻译 Protein translation | 38 | gi|356536011 | 核糖体循环因子 | 28.57/30.91 | 8.86/8.74 | 248 | 大豆G. max | ↓ |
| 防御蛋白 | 4 | gi|116330 | 酸性几丁质酶 | 31.70/33.09 | 4.90/3.49 | 587 | 赤豆Vigna angularis | ↑ |
| Defence protein | 31 | gi|1237027 | 几丁质酶(类型II) | 29.42/40.15 | 6.29/8.23 | 557 | 花生A. hypogaea | ↑ |
| 11 | gi|194466268 | 过氧化物酶 | 18.84/50.30 | 5.93/5.33 | 186 | 花生A. hypogaea | ↑ | |
| 12 | gi|194466268 | 过氧化物酶 | 18.84/48.96 | 5.93/5.33 | 186 | 花生A. hypogaea | ↑ | |
| 15 | gi|71040665 | Cu-Zn超氧化物歧化酶 | 15.20/18.05 | 5.27/5.42 | 284 | 花生A. hypogaea | ↓ | |
| 24 | gi|357470923 | 二羟肉桂酸 3-O-转甲基酶 | 29.34/51.39 | 5.59/6.45 | 328 | 蒺藜苜蓿 Medicago truncatula | ↑ | |
| 28 | gi|357513969 | 类萌发素蛋白 | 23.08/27.33 | 8.96/7.87 | 263 | 蒺藜苜蓿M. truncatula | ↓ | |
| 35 | gi|357513969 | 类萌发素蛋白 | 23.08/27.93 | 8.96/8.30 | 263 | 蒺藜苜蓿M. truncatula | ↓ | |
| 未知蛋白 | 6 | gi|359806300 | 非特征蛋白 | 37.88/55.00 | 4.53/3.41 | 664 | 大豆G. max | ↑ |
| Unkown protein | 30 | gi|255638833 | 未知蛋白 | 18.13/35.07 | 6.27/8.00 | 232 | 大豆G. max | ↓ |
| 34 | gi|351722815 | 非特征蛋白 | 21.17/21.49 | 8.74/8.69 | 280 | 大豆G. max | ↓ | |
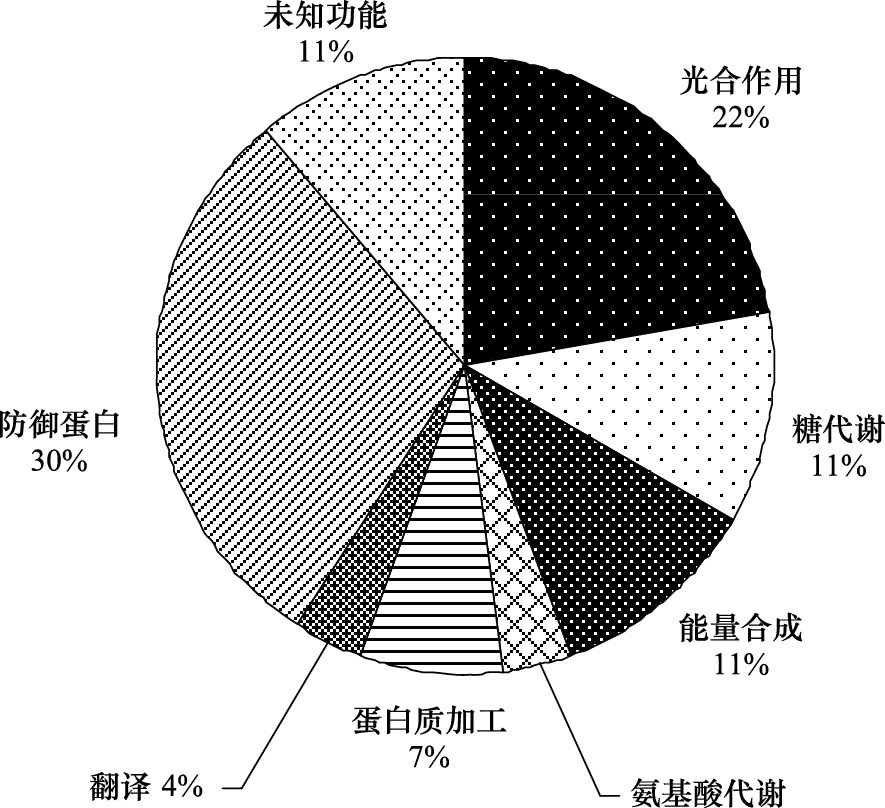
|
| 图 3 27个鉴定蛋白功能分类图 Fig.3 The distribution of the 27 identified proteins by functional category |
依据UniProtKB 数据库提供的蛋白质注释信息,所鉴定的27个叶片蛋白质按其功能可归为八类(图3)。第Ⅰ类:光合作用相关的蛋白质6种,包括质体蓝素(1号)、1,5-二磷酸核酮糖羧化酶小亚基(3号和7号)、放氧复合物增强子蛋白1(18号)、PsbP结构域蛋白6(22号)和果糖二磷酸醛缩酶(37号);第Ⅱ类:糖代谢相关蛋白质3种,包括苹果酸脱氢酶(32、33和36号);第Ⅲ类:能量合成相关蛋白质3种,包括ATP合酶(9、17和21号);第Ⅳ类:氨基酸代谢相关蛋白质1种,包括半胱氨酸合成酶(23号);第Ⅴ类:蛋白质加工相关蛋白质2种,包括热激蛋白(14和16号);第Ⅵ类:蛋白质翻译相关蛋白质1种,包括核糖体循环因子(38号);第Ⅶ类:防御相关蛋白质8种,包括酸性几丁质酶(4和31号)、过氧化物酶(11和12号)、Cu-Zn超氧化物歧化酶(15号)、二羟肉桂酸3-O-转甲基酶(24号)和类萌发素蛋白(28和35号);第Ⅷ类,未知功能蛋白质3种,包括6、30和34号。
3 讨论在质谱鉴定中,位置邻近的蛋白质点被鉴定为同一种蛋白质(3号和7号被鉴定为1,5-二磷酸核酮糖羧化酶小亚基、17号和21号均被鉴定为ATP合成酶δ链、28和35号被鉴定为类萌发素蛋白),类似的情况在小麦等作物中也存在,这可能是由于这些蛋白质表达丰度过高,在等电聚焦和二向分离时发生了位置偏移而造成的[12];当然也有可能是这些蛋白质发生局部降解或存在翻译后修饰现象。蛋白质翻译后修饰在植物体内可以参与植物生长发育、病理、非生物逆境应答等细胞信号转导过程,常见形式有磷酸化、糖基化、甲基化和乙酰化等[13]。
本研究以油料作物花生为材料,运用差异蛋白质组学技术试图从蛋白质表达水平揭示植物对UV-B辐射增强响应的分子机制。结果表明,室外补增UV-B处理改变了花生叶片中与光合作用、糖代谢、能量合成、氨基酸合成、蛋白质加工、蛋白质翻译和防御蛋白等代谢相关蛋白的表达。
3.1 UV-B辐射增强对光合作用相关蛋白质的影响光合作用光反应中光系统Ⅱ(PSⅡ)易受UV-B辐射损伤,尤其是反应中心的D1(psbA基因编码)和D2(psbD基因编码)蛋白,即使在非常低的UV-B辐射剂量下它们都能够被降解。UV-B辐射下PSⅡ活性与psbA基因转录产物及其翻译产物 D1蛋白的稳定性密切相关[14]。扫描电镜结果表明,UV-B辐射增强会破坏叶绿体的超微结构[4]、叶绿素荧光动力学研究表明遭受UV-B辐射的植物叶片PSⅡ活性和光合电子传递速率显著降低[15],从而降低其净光合速率[6],但UV-B如何破坏叶绿体和类囊体结构以及降低电子传递速率原因目前仍未明确。
PsbP为构成PSⅡ的亚基,大小约20.1kD,具有与Ca2+、Cl-和Mg2+相结合的能力,对光合放氧具有重要的作用[16]。Yi等[17]运用RNA干扰技术抑制拟南芥PsbP蛋白的表达后(PsbP的含量仅为对照的13%),结果发现叶绿体肿胀变圆,基粒类囊体内径变大且垛叠无序,据此推断PsbP对于稳定类囊体和叶绿体结构具有重要作用。本研究发现UV-B辐射后会引起花生叶片中PsbP结构域蛋白6表达量的下调(蛋白质点22),暗示UV-B或许通过下调PsbP的表达量进而破坏植物类囊体的结构,降低植物的光合能力。
核糖体循环因子(ribosome recycling factor,RRF)是蛋白质合成体系中核糖体循环再利用的关键因子,对菠菜[18]和水稻[19]的研究结果表明,RRF均由核基因编码,转录后被转运至线粒体或叶绿体中发挥作用。Wang等[20]最近报道,拟南芥RRF突变株hfp108-1叶绿体类囊体膜系统发育不成熟,基粒和基质类囊体模糊,免疫印迹发现:叶绿体蛋白,如D1、D2、CP43、CP47、PsbA和PsbB等蛋白表达量下降。本研究中,试验组花生RRF表达量下调,同时叶绿体蛋白PsbP表达量也出现下降,由此,我们推测可能是RRF量的不足影响PsbP的表达量降低,这需要试验进一步验证。
质体蓝素(plastocyanin,PC)于类囊体膜内表面,是高等植物中为Cytb6/f与光系统Ⅰ(PSⅠ)之间传递电子的一种含铜离子的蛋白质,为光合电子传递链中的重要成员[21]。研究显示,PC(蛋白质点1)在UV-B辐射增强下表达下调,PC含量的减少会影响到类囊体膜上电子传递的效率,使植物同化作用减弱。
核酮糖-1,5-二磷酸羧化酶(Ribulose 1,5-bisphosphate carboxylase,Rubisco)催化卡尔文循环中的羧化反应,UV-B对Rubisco含量的影响较大,Jordan等[22]用UV-B处理豌豆3d后,发现可溶性蛋白质下降了33%,其中Rubisco小亚基含量下降了56%,定量PCR检测发现Rubisco小亚基mRNA在处理4小时后下调量高于20%,时间更长甚至检测不出。果糖-1,6-二磷酸醛缩酶(fructose-1,6-bisphosphate aldolase,FBA)也是控制光合碳同化速率的重要酶之一。Uematsu等[23]将拟南芥FBA基因转入烟草后,促进了RuBP的生成并提高了光合速率,Hatano-Iwasaki和Ogawa[24]研究表明,转化FBA基因的拟南芥也能显著提高CO2同化速率。本研究表明,UV-B辐射降低了花生卡尔文循环中Rubisco(蛋白质点3和7)和FBA(蛋白质点37)两种酶的含量,这或许是对光合作用碳循环影响的主要因素。
3.2 防御相关蛋白质对UV-B辐射增强的响应大多数学者认为,紫外吸收物质(如:类黄酮、花色素苷和类胡萝卜素等)含量的诱导增加是植物应对UV-B辐射的重要防御机制,它们在植物应对 UV-B辐射方面的重要性逐渐被证实。但也有研究表明[25],UV-B辐射拟南芥使得叶片中芥子酰葡萄糖和芥子酰苹果酸含量提高,说明芥子酸酯在植物响应UV-B 辐射过程中起重要作用。二羟肉桂酸3-O-转甲基酶(caffeic acid 3-O-methyltransferase,COMT)可催化5-羟基阿魏酸甲基化生成芥子酸[26],本研究表明,花生也有可能通过COMT(蛋白质点24)的上调来提高芥子酸的生成,进而大量合成芥子酸酯达到保护植株的目的,这与Meiner等[27]认为芥子酰苹果酸只是在植物受到UV-B辐射初期能及时地起到保护作用较为相似。此外,COMT也可催化5-羟基松柏醇甲基化生成芥子醇,芥子醇是构成木质素的重要成分,因而COMT对木质素的合成具有调控作用。紫外线照射梁平柚(Citrus grandis L.)后,柚皮中COMT基因转录水平显著提高[28],且Yamasaki等[29]研究表明植物在接受UV-B辐射增强处理后,叶片中木质素含量较对照显著提高。本研究发现试验组花生叶片中COMT表达量上调,可能会加速叶片中木质素的合成,木质素或许对于抵御紫外线的辐射具有一定的作用。
UV-B对植物的伤害,其中重要的一条途径就是产生活性氧(如:O·-2,H2O2和·OH),对膜系统的过氧化损伤[30]。为抵御活性氧对植物产生的毒害作用,植物可通过抗氧化酶类或非酶抗氧化系统对活性氧进行清除。超氧化物歧化酶(SOD)和过氧化物酶(POD)能有效清除植物体内的O·-2和H2O2,抗坏血酸-谷胱甘肽(AsA-GSH)也是消除H2O2的重要成分。本研究发现,试验组花生叶片中POD(蛋白质点11和12)含量上升,半胱氨酸合成酶(蛋白质点23)表达量上调,使得半胱氨酸和GSH的含量可能增加,表明花生清除H2O2的能力得到了提高;但Cu/Zn-SOD(蛋白点质15)含量下降,说明清除O·-2的能力遭到破坏,花生膜系统可能受到较为严重O·-2胁迫。
类萌发素蛋白(GLPs)以糖蛋白的形式结合存在于细胞外基质中,可以催化草酸氧化产生过氧化氢。过氧化氢能够使植物初生壁中木聚糖交联,令细胞壁更为致密;同时还可诱导与抗性有关的基因表达,从而使植物对不良环境胁迫产生抗性[31]。将辣椒(Capsicum chinense Jacq.)GLPs基因转入烟草(Nicotiana tabacum Xanthi nc)后,提高了烟草对双生病毒的抗性[32],过表达GLPs基因也可让甘蓝型油菜阻止核盘菌(Sclerotinia sclerotiorum)的感染[33],沉默烟草中的GLP基因后,则提高了烟草天蛾(Manduca sexta)的取食偏好性[34]。本研究发现试验组中GLP(蛋白质点28和35)表达下调,这暗示着随着环境中UV-B辐射增强,花生抵抗病毒、细菌感染或采食天敌等方面的能力可能会下降。
病程相关蛋白(PR)是植物受到病原菌侵染或环境因素刺激时会产生多种抗性蛋白,在增强植物抗性方面发挥重要作用,其中,几丁质酶和β-1,3-葡聚糖酶是两类重要的PR蛋白[35]。几丁质酶(Chitinase)是一类水解几丁质单体N-乙酰-D-葡糖胺之间糖苷键的酶[36],花生易遭受锈病、叶斑病和茎腐病等病害的侵袭,这些病的病原菌均为真菌,由于其细胞壁中存在着丰富的几丁质,UV-B辐射增强处理后,花生叶片中几丁质酶(蛋白质点4和31)表达上调,意味着花生抵御真菌侵染的能力可能会得到提高。
此外,本研究中,试验组热激蛋白HSP18.2(蛋白质点16)和HSP70(蛋白质点14)表达上调,推测花生可能通过上调表达HSP来促进细胞质或细胞核内新生蛋白质的折叠、组装及跨膜运输等,以此应对UV-B对植株的不利影响,与本研究类似,Du等[37]用UV处理水稻后,也发现HSP70表达上调,而Murakami等[38]将来自水稻的HSP17.1转入水稻中后发现其抵抗UV-B的能力较对照组显著提高。
综上所述,UV-B辐射增强引起花生叶片光合作用下降的原因主要有三方面:首先可能是由于UV-B引起叶片核糖体循环因子表达量下调,导致PSⅡ的亚基PsbP表达量下降,从而破坏植物类囊体的结构;其次可能是质体蓝素含量下降引起光合电子传递效率降低;第三则可能是由于核酮糖-1,5-二磷酸羧化酶和果糖-1,6-二磷酸醛缩酶表达量降低导致碳同化能力下降。同时,花生也可能通过提高抗氧化酶或非酶抗氧化物质、类萌发素蛋白、病程相关蛋白和热激蛋白等的表达量来抵御UV-B胁迫。在后续的研究中,将对某些感兴趣差异表达的蛋白质的编码基因进行克隆,构建表达载体转化花生,进一步明确其在抵御UV-B过程中的具体作用及分子机制,为今后培育抗UV-B辐射的花生品种提供理论依据。
| [1] | Lu B R, Xia H. Environmental biosafety of transgenic plants: research and assessment of transgene escape and its potential ecological impacts. Chinese Bulletin of Life Sciences,2011,23(2):186-194. |
| [2] | Zhang F L, Liu Y, Tong H J, Yin Q, Tao L, Wang D, Zhou X Q, Chang L J, Song J, Liu W J, Lei S R, Guo L A. Differences in ecological fitness between Bt transgenic rice and regular rice under different insect-infestation pressures. Chinese Journal of Applied and Environmental Biology,2012,18(1):035-041. |
| [3] | Fredshavn J R, Poulsen G S, Huybrechts I, Rudelsheim P. Competitiveness of transgenic oilseed rape. Transgenic Research, 1995,4:142-148. |
| [4] | Hall L, Topinka K, Huffman J, Davis L, Good A. Pollen flow between herbicide-resistant Brassica napus is the cause of multiple-resistant B. napus volunteers. Weed Science,2000,48:688-694. |
| [5] | Åhman I, Lehrman A, Ekbom B. Impact of herbivory and pollination on performance and competitive ability of oilseed rape transformed for pollen beetle resistance.Arthropod-Plant Interactions,2009,3(2):105-113. |
| [6] | Zhou J Y, Wang C Y, Xu W L. Comparison between transgenic soybean and non-transgenic soybean in resistance to stresses. Journal of Ecology and Rural Environment,2006,22:26-30. |
| [7] | Song X L, Qiang S, Peng Y F. An experimental case of safety assessment of weediness of transgenic glyphosate-resistant soybean (Glycine mac (L.) Merri). Scientia Agricultura Sinica, 2009,42(1):145-153. |
| [8] | Liu W J, Liu Y, Zhou X Q, Xong J, Yin Q, Wang D, Zhang F L, Lei S R. Impact of competitive environment on growth and yield component of glyphosate tolerant soybean. Soybean Science,2012,31(1):64-72. |
| [9] | Lian L J, Li Y, Wang J, Guo N, Zhang K W. Investigations on survival competitiveness and gene flow of transgenic cotton with betA/Pals gene in the field. Journal of Shandong University(Natural Science),2009,44(5):20-27. |
| [10] | Zhang X H, Tian S L, Zhang T Y, Li J, Qiao Y Y. Studies on the competitive ability of transgenic cry1Ac+cry2Ab cotton and transgenic crylAc+EPSPS cotton in wasteland. Journal of Biosafety,2012,21(2):119-124. |
| [11] | Chen L Y, Snow A A, Wang F, Lu B R. Effects of insect-resistance transgenes on fecundity in rice (Oryza sativa, Poaceae): a test for underlying costs. American Journal of Botany,2006,93(1): 94-101. |
| [12] | Cui R R,Wei Y, Meng P P, Ma Y L, Jin Y, Li Q R, Qiang S, Dai W M, Song X L. Assessment on potential weediness of transgenic glufosinate-resistant rice Minghui86B. Chinese Journal of Rice Science,2012,26(4):467-475. |
| [13] | Zhou J, Wang C Y, Chen J Q. Indexes for assessment of genetically modified plants invasiveness. Rural Eco-environment,2003,19(2):61-64. |
| [14] | Zhang B, Rui W Y, Zheng J C, Zhou B, Yang F, Zhang W J. Responses of pollen activity and seed setting of rice to high temperature of heading period. Acta Agronomica Sinica, 2007,33(7):1177-1181. |
| [15] | Cellini F,Chesson A,Colquhoun I,Constable A,Davies H V,Engel K H,Gatehouse A M R,Kärenlampi S, Kok E J,Leguay J J,Lehesranta S,Noteborn H P J M,Pedersen J,Smith M. Unintended effects and their detection in genetically modified crops. Food and Chemical Toxicology,2004,42:1089-1125. |
| [16] | Pilson D, Prendeville H R. Ecological effects of transgenic crops and the escape of transgenes into wild populations. Annual Review of Ecology, Evolution, and Systematics, 2004, 35:149-174. |
| [17] | Ferry N, Edwards M G, Gatehouse J, Capell T, Christou P, Gatehouse A M R. Transgenic plants for insect pest control: a forward looking scientific perspective. Transgenic Research,2006,15:13-19. |
| [18] | Ceasar S A, Ignacimuthu S. Genetic engineering of crop plants for fungal resistance: role of antifungal genes. Biotechnology Letters,2012,34:995-1002. |
| [19] | Shu Q Y, Cui H R, Ye G Y, Wu D X, Xia Y W, Gao M W, Altosaar I. Agronomic and morphological characterization of Agrobacterium-transformed Bt rice plants. Euphytica, 2002,127:345-352. |
| [20] | Bashir K, Husnain T, Fatima T, Latif Z, Mehdi S A, Riazuddin S. Field evaluation and risk assessment of transgenic indica basmati rice.Molecular Breeding, 2004,13: 301-312. |
| [21] | Liu D M, Wu Z X, Liu C L, Li C W, Li F G. Variations of main agronomic traits in transgenenic cotton(Gossypium hirsutum L.)lines transformed by pollen-tube pathway method.Cotton Science, 2007,19(6):450-454. |
| [22] | Cuo Y S, Zhu Y M, Li J, Bai X, Cai H. Investigation and analysis of the main agronomic traits of transgenic soybean with two anti-fungal protein genes. Journal of Northeast Agricultural University,2008,29(1):10-12. |
| [23] | Wei X H, Yuan X P, Yu H Y, Wang Y P, Tang S X, Liao X Y. Effects of Transgenes insertion on pollen vigor and hybrid seed set of rice. Chinese Journal of Applied Ecology, 2005,16(1):115-118. |
| [24] | Xie X B, Cui H R, Shen S Q, Wu D X, Xia Y W, Shu Q Y. Studies on the distorted segregation of foreign genes in transgenic rice progenies.Acta Genetica Sinica, 2002, 29(11):1005-1011. |
| [25] | Guo J F,Huang Y X,Peng X L,Yuan H X,Jiang S H,Xu X P,Zhang J Z. Variation of non-target agronomic traits in the offspring of transgenic rice line E32 by particle bombardmen. Journal of Tropical and Subtropical Botany,2007,15(4):284-289. |
| [4] | 吴能表, 马红群, 胡丽涛, 洪鸿, 孙金春, 张扬欢, 戴大临. 增强 UV-B 辐射对胡椒薄荷叶片光合机构和光合特性的影响. 中国中药杂志, 2009, 34(23): 2995-2998. |
| [8] | 喻娟娟, 戴绍军. 植物蛋白质组学研究若干重要进展. 植物学报, 2009, 44(4): 410-425. |
| [12] | 邵彩虹, 钱银飞, 唐秀英, 刘光荣, 谢金水, 彭春瑞, 邱才飞. 养分胁迫对水稻籽粒灌浆充实影响的蛋白质组学研究. 中国水稻科学, 2012, 26(3): 267-274. |
| [19] | 胡欣, 胡昊, 洪国藩, 韩斌. 水稻两个frr基因的结构,转录特性及同源性分析. 植物生理与分子生物学学报, 2004, 30(1): 105-114. |
| [25] | 李敏, 王垠, 牟晓飞, 王洋, 阎秀峰. 拟南芥芥子酸酯对UV-B辐射的响应. 生态学报, 2012, 32(7): 1987-1994. |
| [28] | 程春振, 朱世平, 吴波, 阳佳位, 贝学军, 马岩岩, 钟广炎. 紫外线照射对梁平柚果皮基因表达的影响. 园艺学报, 2011, 38(5): 859-866. |
 2014, Vol. 34
2014, Vol. 34




